胰岛素泵治疗对不同 BMI初发 2型糖尿病患者胰岛功能的影响
2011-05-23井庆平孙爱东
井庆平,孙爱东
(淄博市第一医院,山东淄博 255200)
近年来,胰岛素泵作为糖尿病胰岛素强化治疗的一种方式在临床上获得了广泛应用,但强化治疗后糖尿病的缓解率文献报道略有差别。有报道预测影响患者缓解率的因素为年龄、糖尿病病程、餐后血糖、BMI等。本研究以 BMI为分类依据,对不同BMI患者胰岛素泵强化治疗后胰岛功能改善情况及缓解率进行了观察。
1 资料与方法
1.1 临床资料 选取 2007年 1~12月在我院住院的 2型糖尿病患者 42例,男 24例、女 18例,年龄(30~50)岁,诊断糖尿病病程 12~24个月。BMI 22.3~29.9 kg/m2,空腹血糖(FPG)10.3 ~ 15.4 mmol/L,糖化血红蛋白(HbA1c)8.4%~10.2%。胰岛素相关抗体检查阴性,心电图和心脏、颅脑彩超检查无明显心脑血管缺血病变,肾脏检查 24 h尿微量白蛋白 <150 mg,眼底无特征性微血管瘤及出血、渗出病变。排除甲状腺功能亢进症、皮质醇增多症等引起继发血糖升高的内分泌疾病及胰腺炎或胰腺肿瘤等外分泌腺疾病。以 BMI 25 kg/m2为界线,将受试者分为消瘦组16例和肥胖组 26例,其 BMI分别为(22.1±3.3)、(26.4 ±2.8)kg/m2。
1.2 方法 两组停服影响胰岛素分泌的药物 3 d后、在本次治疗前从肘静脉抽血,采用北京倍爱康生物技术有限公司生产的磁酶免分析仪及试剂,检测患者空腹和口服 75 g葡萄糖负荷后 0.5、2 h胰岛素水平,同时应用拜安易血糖仪检测各时间点血糖水平。患者均给予胰岛素泵强化治疗 2周。胰岛素泵应用美敦力 507型,模拟人体自身胰岛素脉冲分泌,通过连接导管及皮下埋植针头昼夜不停输注胰岛素,进餐时由胰岛素泵增加追加值。胰岛素采用通化东宝的重组人胰岛素甘舒霖 R。根据空腹和三餐前血糖水平调整胰岛素基础量和餐前大剂量泵入量。要求胰岛素泵治疗 3 d内血糖即控制在 6.0 mmol/L以下,此后使空腹和三餐前血糖尽可能在5.0 mmol/L左右。停用胰岛素 1周后,再进行相应的葡萄糖刺激下胰岛素分泌测定。住院期间患者均进行糖尿病教育、饮食及运动指导。用稳态模型计算 β细胞功能(HOMA-B)=20×空腹胰岛素/(空腹血糖 -3.5);早期胰岛素分泌指数为糖负荷后 30 min胰岛素增量与葡萄糖增量的比值,即 ΔI30/ΔG30;并计算胰岛素抵抗指数(HOMA-IR)。
1.3 统计学方法 采用 SPSS10.0软件,计量资料以±s表示,非正态分布资料经自然对数转化为正态分布后进行分析,治疗前后结果比较采用 t检验;胰岛功能与 BMI变化关系采用直线相关分析。P≤0.05为差异有统计学意义。
2 结果
2.1 两组治疗前后各检测指标比较 治疗前两组HOMA-B、HOMA-IR、ΔI30/ΔG30比较无统计学差异(P均 >0.05)。治疗后与治疗前比较,肥胖组 HOMA-B、HOMA-IR、ΔI30/ΔG30明显改善 (P均 <0.05),消瘦组 HOMA-B、ΔI30/ΔG30明显改善 (P均<0.05)。治疗后肥胖组 HOMA-B、HOMA-IR、ΔI30/ΔG30较消瘦组改善更明显(P均 <0.05)。见表1。
表1 两组治疗前后各检测指标比较(±s)
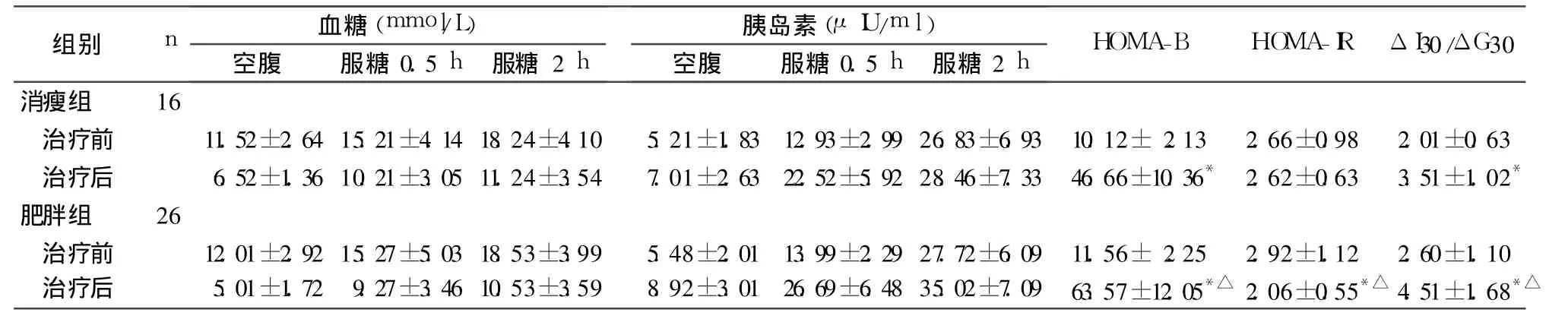
表1 两组治疗前后各检测指标比较(±s)
注:与本组治疗前比较,*P<0.05;与消瘦组治疗后比较,△P<0.05
消瘦组 16治疗前 11.52±2.64 15.21±4.14 18.24±4.10 5.21±1.83 12.93±2.99 26.83±6.93 10.12± 2.13 2.66±0.98 2.01±0.63治疗后 6.52±1.36 10.21±3.05 11.24±3.54 7.01±2.63 22.52±5.92 28.46±7.33 46.66±10.36* 2.62±0.63 3.51±1.02*肥胖组 26治疗前 12.01±2.92 15.27±5.03 18.53±3.99 5.48±2.01 13.99±2.29 27.72±6.09 11.56± 2.25 2.92±1.12 2.60±1.10治疗后 5.01±1.72 9.27±3.46 10.53±3.59 8.92±3.01 26.69±6.48 35.02±7.09 63.57±12.05*△ 2.06±0.55*△ 4.51±1.68*△
2.2 BMI与 ΔI30/ΔG30、HOMA-B的关系 治疗后以 BMI为因变量,ΔI30/ΔG30和 HOMA-B为应变量进行直线回归分析,结果显示,患者 BMI越高,经过胰岛素泵强化治疗后 ΔI30/ΔG30、HOMA-B改善越明显,BMI与 ΔI30/ΔG30、HOMA-B呈正相关 (r分别为0.688、0.746,P均 <0.05)。
3 讨论
3.1 高血糖对糖尿病患者胰岛功能的影响 有研究显示,部分新诊断的 2型糖尿病患者经短期胰岛素治疗可诱导出长期血糖控制良好而不需服用任何降血糖药物的“蜜月期”,患者胰岛 β细胞对葡萄糖敏感性的缺陷在血糖水平正常 20 h后可得到改善[1]。许多学者将糖尿病的长期缓解归因于胰岛素治疗纠正了高血糖的毒性,明显改善机体的胰岛素分泌功能和胰岛素敏感性,其改善的程度取决于血糖水平控制的严格程度。若血糖水平控制得不够低,则胰岛素治疗虽纠正了高血糖,但并不能改善胰岛素敏感性、葡萄糖敏感性和葡萄糖负荷后的急性胰岛素反应。近期研究显示,高血糖既是胰岛 β细功能受损和胰岛素抵抗的后果,也是其诱因[2],即使是轻度高血糖也可以削弱胰岛 β细葡萄糖刺激的胰岛素分泌反应并损害胰岛素介导的葡萄糖转运。长期暴露于严重高血糖环境中,会影响胰岛素基因的转录或表达,导致不可逆的 β细功能损害和细胞凋亡。而较短期高血糖仅影响 β细胰岛素的胞吐功能或胰岛素储存,所导致的 β细对葡萄糖的感知能力受损是暂时的、生理性的和可逆的[3,4]。初发 2型糖尿病患者经过短期胰岛素泵强化治疗快速稳定控制血糖后,可以防止发生被称为“葡萄糖毒性”的不可逆的 β细功能改变,逆转葡萄糖低感知现象[5,6]。使糖尿病患者的胰岛功能有不同程度的恢复。
3.2 胰岛素泵治疗对不同 BMI糖尿病患者胰岛功能的影响 胰岛素泵治疗能模拟生理性胰岛素分泌,可以准确释放极小剂量胰岛素(0.1 U),既可持续 24 h基础胰岛素输注,抑制肝糖生成,使夜间和两餐之间的血糖平稳下降,又可每餐给予追加释放量胰岛素以控制餐后血糖高峰,因而更易获得稳定的血糖控制,血糖变异性小。本研究根据患者 BMI的不同将糖尿病患者分为消瘦组和肥胖组。显示在治疗前两组 HOMA-B、HOMA-IR、ΔI30/ΔG30均相似的情况下,治疗后两组胰岛 β细功能、胰岛素早期分泌指数均有明显改善,但肥胖组改善较消瘦组更明显。患者 BMI越高,经胰岛素泵治疗后 ΔI30/ΔG30和 HOMA-B恢复越好。这提示胰岛素泵治疗在迅速纠正高血糖毒性之后,减轻了高血糖对 β细造成持续性刺激,减少了胰岛储备功能的消耗,使基础胰岛素分泌水平增加。同时,胰岛素泵泵入胰岛素的方式模拟正常人的胰岛素分泌呈脉冲的方式分泌,有助于防止靶组织中胰岛素受体水平的下调,维持胰岛素的敏感性,减少胰岛素用量,避免引起高胰岛素血症及其导致胰岛素受体水平下调,引发胰岛素抵抗,有效恢复 2型糖尿病患者胰岛素的分泌紊乱[7]。BMI较高的 2型糖尿病患者胰岛功能及胰岛素抵抗改善更明显,考虑肥胖患者常伴有胰岛 β细数量增加,存在更明显的胰岛素抵抗及更强的胰岛功能代偿,有较明显的胰岛 β细代偿增生,胰岛素的分泌上升更明显。
总之,胰岛素泵治疗可从胰岛素分泌缺陷和胰岛素抵抗这两方面改善了糖尿病的代谢紊乱,使糖尿病患者的胰岛充分休息,减少胰岛 β细凋亡,成为目前治疗初发 2型糖尿病较为理想的方式,尤其将对肥胖 2型糖尿病患者带来更大的益处。
[1]Vague P,Moulin JP.The defective glucose sensitivity of theβ-cell in non insulin dependent diabetes.Improvement after twenty hours of normoglycaemia[J].Metabolism,1982,31(3):139-142.
[2]Unger RH,Grundy S.Hyperglycaemia as an inducer as well as a consequence of impaired islet cell function and insulin resistance:implications for the management of diabetes[J].Diabetologia,1985,28(1):119-121.
[3]Toschi E,Camastra S,Sironi AM,et al.Effect of acrte hyperglycemia on insulin secretion in humans[J].Diabetes, 2002,51(Supp1):S130-S133.
[4]Hsieh CH,Hung YJ,He CT,et al.The capability of glucose toxicity on severe type 2 diabetes[J].Endocr Res,2005,31(7):149-158.
[5]翁建平,李延兵,许雯,等.短期持续胰岛素输注治疗对初诊 2型糖尿病患者胰岛 β细功能的影响[J].中国糖尿病杂志,2003,11(1):10-15.
[6]Unger RH.Lipotoxicity in the pathogenesis of obesity dependent NIDDM genetic and implications[J].Diabetes,1995,44(8):863-870.
[7]许曼因,陆广华,陈明道.糖尿病学[M].上海:上海科学技术出版社,2003:88-89.
