新型富勒烯-吖啶二酮衍生物的合成*
2010-11-26杨海涛阮小娇缪春宝
杨海涛, 阮小娇, 缪春宝
(江苏工业学院 精细化工重点实验室,江苏 常州 213164)
富勒烯(C60)在光学材料、超导和半导体材料、生物医药等领域都具有广泛的应用前景[1~6]。吖啶二酮作为激光染料[7]具有双重发色结构,在基态和激发态都既可以作为电子接受体也可作为电子给予体[8~10];在光聚合反应中作光敏剂和光引发剂也具有潜在的应用价值[11]。
本文将吖啶二酮结构引入富勒烯以期获得具有独特光学性能的新化合物。富勒烯经环加成、水解、酯化三步反应成功地合成了新的富勒烯-吖啶二酮衍生物(5, Scheme 1),其结构经UV,1H NMR,13C NMR, IR和MS表征。
1 实验部分
1.1 仪器与试剂
Bruker公司AVANCE 500 MHz型核磁共振仪(CS2/CDCl3为溶剂,TMS为内标);Nicolet FT-IR型红外光谱仪(KBr压片);Micromass TOF型质谱仪(2,5-二甲基苯甲酸做基质)。
C60,纯度≥99%,河南濮阳永新科技有限公司;其余所用试剂均为分析纯。
1.2 合成
(1) 富勒烯乙酸叔丁酯(2)的合成[12]
在圆底烧瓶中加入C6072 mg(0.1 mmol),硫盐(1) 38.6 mg(0.15 mmol),甲苯35 mL,超声溶解,搅拌下于室温反应3 h。过硅胶柱(3 cm,洗脱剂:甲苯),旋除溶剂,残余物经柱色谱层析(洗脱剂:CS2)分离得棕黄色固体250.1 mg,收率60%(回收C6020.2 mg)。
(2) 富勒烯乙酸(3)的合成
在圆底瓶中加入241.7 mg(0.05 mmol),一水合对甲苯磺酸4.8 mg(0.025 mmol),甲苯15 mL,搅拌使其完全溶解后回流反应2 h(TLC跟踪)。冷却至室温,离心分离,沉淀分别用甲苯、丙酮洗涤两次,干燥得褐色固体336.9 mg ,收率95%。
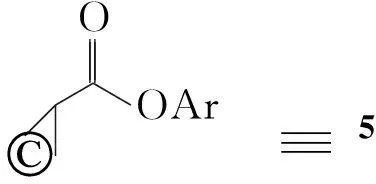
1 2 3

Scheme 1
(3)5的合成
在圆底烧瓶中加入31.1 mg(0.04 mmol),DCC(二环己基碳酰亚胺)24.7 mg(0.12 mmol), DMAP(4-二甲基氨基吡啶)2.5 mg(0.02 mmol), BtOH·H2O(1-羟基苯并三氮唑)6.8 mg(0.05 mmol)和甲苯/二氧六(等体积比)30 mL,超声使其分散均匀后再加入3,3,6,6-四甲基-9-(4-氯苯基)-10-羟乙基十氢吖啶-1,8-二酮(4) 21.4 mg(0.05 mmol),搅拌下于70 ℃(油浴)反应6 h。冷却,旋除溶剂,残余物经柱层析[V(CS2) ∶V(乙酸乙酯)=7 ∶1]分离,收集液旋干,残余物在离心管中用丙酮洗涤三次,干燥得棕黄色固体530.9 mg,收率65%; UVλ: 258, 327, 427 nm;1H NMRδ: 7.22(d,J=8.7 Hz, 2H, ArH), 7.16(d,J=8.7 Hz, 2H, ArH), 5.21(s, 1H, CH), 4.52(t,J=7.2 Hz, 2H, OCH2), 4.44(s, 1H, CH), 4.19(t,J=7.2 Hz, 2H, NCH2), 2.72(d,J=16.8 Hz, 2H, CH2), 2.45(d,J=16.3 Hz, 2H, CH2), 2.24(s, 4H, CH2), 1.12(s, 6H, CH3), 1.07(s, 6H, CH3);13C NMRδ: 194.81(C=O), 165.65(COO), 149.44(C=CN), 147.42, 145.38, 145.35(4C), 145.32, 145.23, 144.94, 144.84, 144.81, 144.80, 144.77, 144.73, 144.65, 144.60(1C), 144.55(1C), 143.99, 143.94, 143.80, 143.29, 143.19(1C), 143.13, 143.10, 143.06(1C), 142.97, 142.45, 142.23, 142.16, 141.95, 141.32, 141.10, 140.53, 136.60, 132.05(C of Ar), 129.09(C of Ar), 128.32(C of Ar), 116.18(C=CCO), 69.97(C sp3of C60), 64.58(OC H2), 49.91(COCH2), 42.73(NCH2), 40.72(CH2), 37.97(CH), 32.62(CMe2), 31.53, 29.24(CH3), 28.30(CH3);IRν: 2 927, 2 851, 1 743, 1 629, 1 575, 1 370, 1 239, 1 208,1 239, 1 089, 571, 525 cm-1; MSm/z: 1 187(M+)。
2 结果与讨论
合成2时改进了文献[12]方法,直接用硫盐与C60反应,并用弱碱K2CO3代替NaH;成功地避免了先分离硫叶立德再与C60反应的无水操作。
5的13C NMR谱图在69.97处出现了富勒烯上的C sp3信号峰;128.32~147.22共出现富勒烯骨架和苯环的34组信号峰,其中144.60, 144.55, 143.19和143.06四组峰对应C60的四个单碳,表明5具有C2对称性。
所有表征数据确认5与Scheme 1预期吻合。
[1] Martin N, Sanchez L, Llescas B,etal. C60-based electroactive organofullerenes[J].Chem Rev,1998,98(7):2527-2548.
[2] Prato M, Maggini M. Fulleropyrrolidines:A family of full-fledged fullerene derivatives[J].Acc Chem Res,1998,31(9):519-526.
[3] Nakamura E, Isobe H, Tomita N,etal. Functionalized fullerenes as an artificial vector for transfection[J].Angew Chem Int Ed,2000,39(23):4254-4257.
[4] Nakamura E, Isobe H. Functionalized fullerenes in water.The first 10 years of their chemistry,biology,and nanoscience[J].Acc Chem Res,2003,36(11):807-815.
[5] Guldi D M, Zerbetto F, Prato M,etal. Ordering ullerene materials at nanometer dimensions[J].Acc Chem Res,2005,38(1):38-43.
[6] Cremer J, Bauerle P, Wienk M M,etal. High open-circuit voltage poly(ethynylene bithienylene):Fullerene solar cells[J].J Chem Mater,2006,18(25):5832-5834.
[7] Shanmugasundaram P, Murugan P, Ramakrishnan V T. Synthesis of acridinedione derivatives as laser dyes[J].Heteroatom Chem,1996,6(1):17-22.
[8] Timpe H J, Ulrich S, Fouassier J P. Photochemistry and use of decahydroacridine-1,8-diones as photosensitizers for onium salt decomposition[J].J Photochem Photobiol A:Chem,1993,73(2):139-150.
[9] Ulrich S, Timpe H J, Fouassier J P,etal. Photoreduction of decahydroacridine-1,8-diones by amines[J].J Photochem Photobiol A:Chem,1993,74(2-3):165-170.
[10] Mohan H, Srividya N, Ramamurthy P,etal. One-electron reduction of acridine-1,8-dione in aqueous solution:A pulse radiolysis study[J].J Phys Chem A,1997,101(16):2931-2935.
[11] Timpe H J, Ulrich S, Decker C,etal. Photoinitiated polymerization of acrylates and methacrylates with decahydroacridine-1,8-dione/onium salt initiator systems[J].Macromolecules,1993,26:4560-4566.
[12] Wang Y, Cao J, Wilson S R,etal. A superior synthesis of [6,6]-methanofullerenes:The reaction of sulfonium ylides with C60[J].Tetrahedron Lett,1995,36(38):6843-6846.
