硅胶柱层析法分离提纯双基药中的硝化甘油
2010-09-18郑文芳潘仁明蔺向阳李生有
郑文芳,熊 鹰,潘仁明,蔺向阳,李生有
(1.南京理工大学化工学院 ,江苏 南京 210094;2.重庆水利电力职业技术学院,重庆 402160)
引 言
硝化甘油(NG)是一般双基药中的主要能量成分之一。NG的机械感度高,危险性大,为了安全,单质NG不允许厂外运输[1-4]。但在一些科研工作中常会用到少量NG。
有关NG的分离提纯方法,国内外进行了大量研究[5-8]。贾林等[6]在对某双基球形药定量分析时,首先用快速溶剂萃取法(ASE)使硝化纤维素(NC)与NG、叠氮硝胺(DIANP)等其他小分子分离,然后用高效液相色谱法(HPLC)将萃取的混合有机组分分离和定量,但是,由于气相或液相色谱法分析仪器的进样量水平都是微量的,难以达到小批量 NG的分离提纯要求。 Hewitt等[9]采用柱层析法从土壤中分离出双基药燃烧残渣中毫克级的NG和二硝基甲苯等物质,其分离原理与气相或液相色谱法原理相同,所不同的是柱层析法可以简便地通过增大层析装置的尺度来提高上样量水平,实现较大量混合物质的分离提纯[10-13]。目前,采用柱层析法克量级地分离提纯双基药中 NG的研究尚未见相关报道。本实验以某双基药为原料,采用柱层析法,研究从双基药中少量分离提纯NG的工艺方法。
1 实 验
1.1 材 料
待分离双基药配方(质量分数)为:硝化纤维素(NC),62.0%;硝化甘油(NG),28.0%;二苯胺(DPA),1.0%;邻苯二甲酸二丁酯(DBP),9.0%。
硅胶板:型号为GF254,尺寸 200mm×200mm,青岛海洋化工厂;硅胶:孔径 45~75μm,青岛海洋化工厂,110℃活化 1h后使用;石油醚、苯、二氯甲烷、乙醚、乙酸乙酯等试剂均为分析纯。
1.2 实验装置与仪器
提取与分离装置示意图如图 1所示,其中提取器为150mL的索氏提取器,层析柱为5.0cm×84cm的玻璃柱。
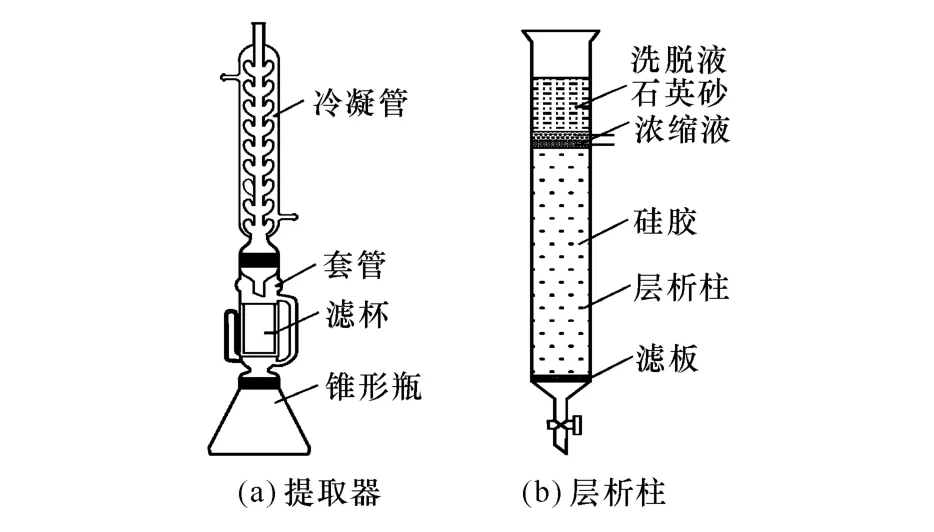
图1 提取与层析柱分离装置示意图Fig.1 Equipments of extraction and purification
Agilent 6890N-5975气质联用仪,美国 Agilent公司。色谱分析条件:使用DB-5型毛细管柱(30m×0.25mm× 0.25μm);柱温:初始温度 50℃ ,以 10℃ /min升温速率升至 150℃,然后以 3℃ /min升温速率升至 230℃后恒温;载气为氦气。质谱分析条件:EI电离源;电子能量为 70eV;离子源温度 200℃;质荷比(m/z)扫描范围为 20~ 550。
Agilent 1100型液相色谱仪,美国 Agilent公司。色谱分析条件:使用Zobax Ecilipse XDB-C18柱(4.6mm×150mm,5μm);流动相:甲醇和水体积比为 70∶ 30;柱温 30℃;进样量 0.1~ 10μL;检测器为DAD检测器,检测波长 223nm。
DRX 500MHz核磁共振仪,德国Brucker公司,以 TMS为内标,CDCl3为溶剂。
1.3 双基药的提取与NG的分离提纯工艺
由于双基药组分中 NC为高分子物质,将双基药溶解后,直接进行层析柱分离时易堵塞层析柱,从而导致分离失败。为此在分离前,用溶剂提取双基药中包括 NG在内的有机小分子组分,然后对提取得到的有机小分子混合物用柱层析法进行分离提纯,从而获取高纯度 NG。提取与分离工艺流程见图 2。
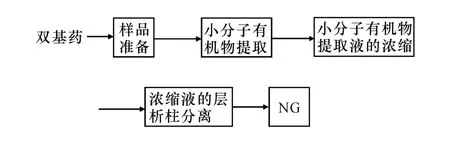
图 2 双基药提取与分离流程示意图Fig.2 Process of extraction and purification
1.3.1 双基药中有机小分子物质的提取与浓缩
将双基药试样用刀片切成粉状,过筛,取 850μm标准筛筛下物,备用。
准确称取3g备用双基药料,置于提取器滤杯内(见图 1),盖上滤纸片,稍稍压紧。接通冷凝水,将装有物料的滤杯放入提取器中,向提取器接收瓶(锥形瓶)内加入约100mL提取溶剂,连接提取器各部分,浸入水浴中(温度为 55~ 60℃),使提取器中溶剂回流速度不少于8次 /h;提取完成后,将提取液置于40~ 45℃水浴烘箱内,使溶剂挥发浓缩。滤杯置于110℃烘箱干燥0.5h,准确称量提取后的剩余物,按照式(1)计算提取率[14-15]。

式中:W为双基火药有机小分子的提取率,%;m为待提取双基火药质量,g;m1为提取后不溶物质量,g。
1.3.2 浓缩液的层析柱分离
(1)薄层色谱定性分析条件
层析柱分离过程中的定性分析采用薄层色谱分析。取活化后的硅胶 GF254板,用提取液或洗脱液点样,于流动相中上行展开,晾干后用碘蒸气显色。
(2)层析柱分离
取经活化的硅胶,加入流动相制成浆状,湿法装柱,然后用流动相平衡层析柱。将浓缩好的提取样品缓缓倒入柱中,进样完毕后加入流动相洗脱。控制空塔流速约为0.764cm/min,分步收集洗脱液,点样定性分析,合并富含各组分的洗脱液,于40~45℃水浴烘箱浓缩纯化至无溶剂气味备用。
2 结果与讨论
2.1 提取溶剂的选择
在常见双基药中,NC及各种无机物不溶于乙醚、二氯甲烷等有机溶剂,而NG、安定剂、DBP、二硝基甲苯(DNT)等有机小分子组分易溶于这些溶剂。因此,在双基药分析时常选用乙醚或二氯甲烷作为提取溶剂,将NG等有机小分子混合组分与NC等物质分离[14-15]。本研究采用这两种溶剂作为提取溶剂,分别进行双基药的提取,结果如表1所示。
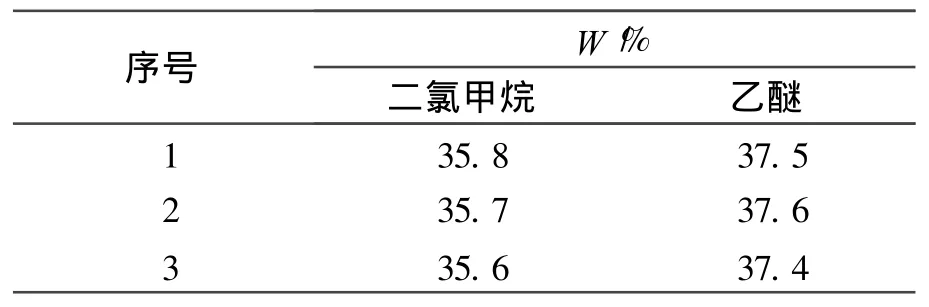
表 1 两种溶剂对双基药提取率的影响Table 1 Effects of two solvents on the extraction rate of double-base propellant
由表1可看出,用二氯甲烷作为提取溶剂,提取率的平均值为35.7%,而用乙醚作提取溶剂时,提取率的平均值为37.4%。显然,用乙醚作提取溶剂的提取率要高于二氯甲烷。这可能是因为乙醚在分子结构上与提取溶质更为接近所引起的。为此选择乙醚作为提取溶剂,得到的提取液经浓缩后,作为层析柱分离的上样原料。
2.2 流动相的选择
由双基药配方可知,经提取后,提取液中包含的有机小分子组分为NG、DPA、DBP。由于NG分子结构中有3个-ONO2基团,NG分子的极性较大。与NG相比,DPA与 DBP的极性相对较低,因此,选择极性适宜的溶剂作层析流动相可实现 NG的分离[12-13]。为此,按极性由低到高的顺序选择石油醚、苯、二氯甲烷和乙酸乙酯等 4种溶剂作为展开剂,对提取液进行薄层分离试验,选择适宜的流动相。
用提取液在 GF254硅胶板上点样,分别在选取的4种溶剂中展开,显色。图3是使用不同展开溶剂点样得到的提取液展开示意图。

图3 提取液在不同溶剂中的展开效果示意图Fig.3 Analysis results of thin-layer chromatography in different solvents
由图3可以看出,石油醚极性偏低,3种组分分离困难;乙酸乙酯极性偏高,薄层硅胶板前沿两组分分离困难;苯和二氯甲烷均能有效地将 3种组分展开,预计层析柱分离时能有效将3种组分分离。由于苯的沸点较高(苯的沸点为80.1℃,二氯甲烷沸点为39.8℃),不利于浓缩,故选择二氯甲烷作为层析柱分离的流动相。
2.3 层析分离组分的鉴别
用二氯甲烷为流动相进行层析柱分离,按出柱先后顺序分别收集组分。为确定收集得到的 3种组分,将洗脱液加热浓缩,然后用 GC/MS法和核磁共振法分别进行检测。
图4为3种组分的质谱图。其中洗脱出柱的第1组分与NG的匹配度为 64%,第 2组分与DPA的匹配度为81%,第3组分与DBP的匹配度为92%。因此可初步确定第 1组分应为 NG。
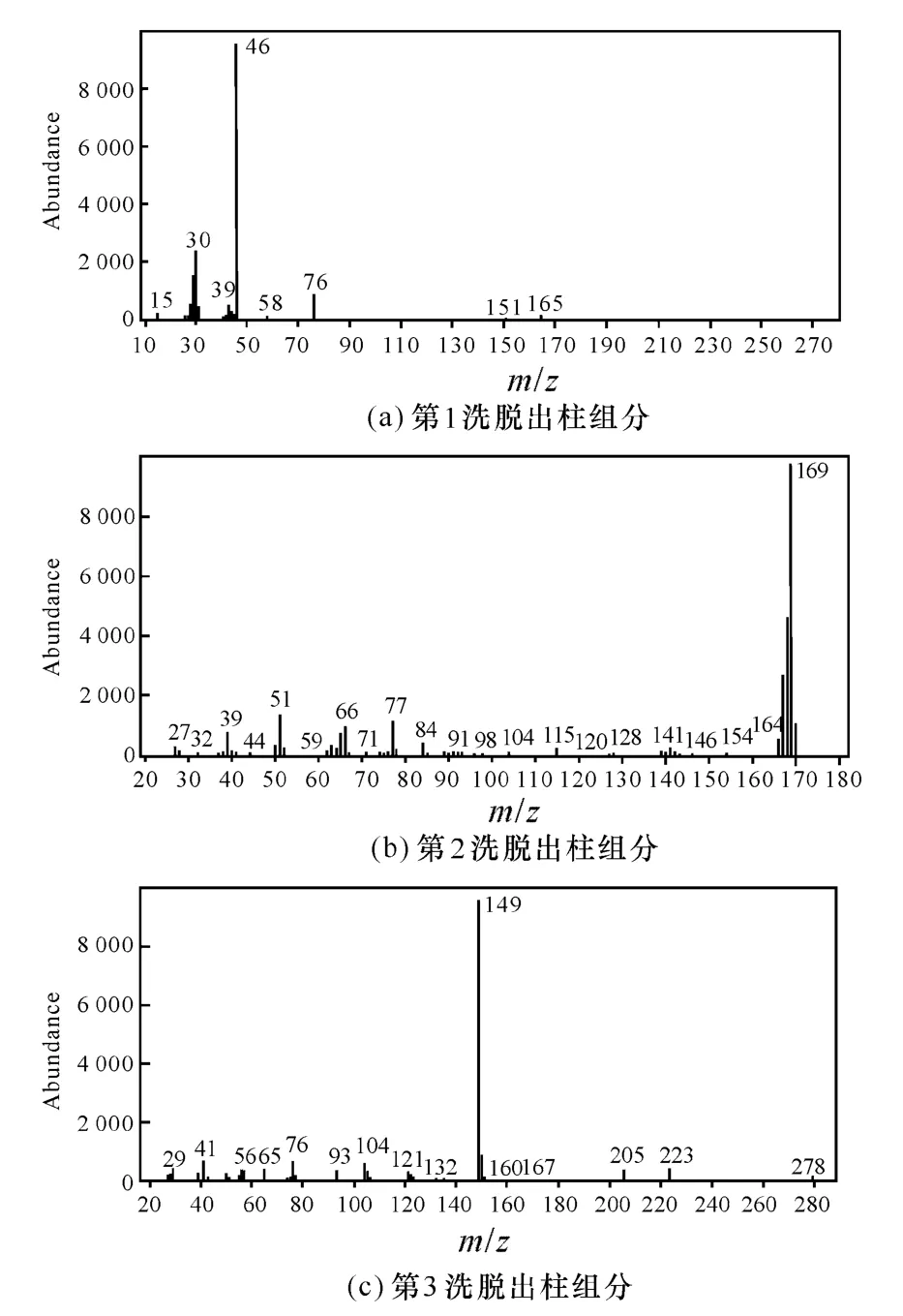
图4 层析柱分离洗脱出柱3种组分的质谱图Fig.4 GC-MS analysis results of the separate products
1HNMR(CDCL3),W:5.51~5.55(m,1H,-CH-);4.81~ 4.85(q,2H,-CH2-);4.65~ 4.69(q,2H,-CH2-)。结合 GC-MS分析结果,可知洗脱出柱第 1组分即为目标物硝化甘油。
2.4 分离提纯后NG的纯度
第1组分的核磁共振结果为:将收集的第1组分的洗脱液,在40~ 45℃水浴烘箱中浓缩去除溶剂二氯甲烷,然后进行高效液相色谱分析,结果见图 5。由图5(b)可知,谱图中只有一个 NG峰,未见任何杂峰,可见用柱层析法从双基药中分离的NG纯度很高。

图5 层析柱分离前后成分变化的 HPLC谱图Fig.5 HPLCanalysis results of the samples before and after purification
2.5 最大上样量的选择
上样量少,一次提取的 NG少;但过高的上样量又会使色谱柱负担过重,分离效果变差[10,13]。因此,在层析柱法提取NG时,需寻找适宜的上样量。
图6为实验得到的上样量与NG回收率间的关系曲线。由图6可知,上样量在5g附近时样品回收率较高。由此可见,如果采用层析法工艺提取NG,需根据实际使用的层析柱,通过实验来确定最大上样量。
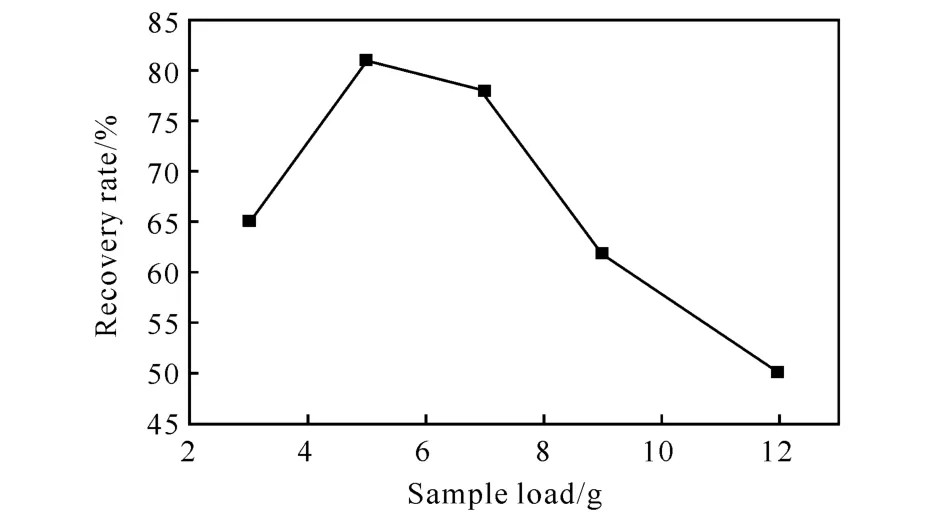
图6 上样量对NG回收率的影响Fig.6 Effect of loadbility on recovery rate of NG
3 结 论
(1)通过对双基药经溶剂提取浓缩液的层析柱分离与纯化,可以获得克量级纯度很高的 NG,经HPLC分析未见杂峰。
(2)本实验的提取与分离条件为:提取溶剂选用乙醚;层析柱分离时流动相选用二氯甲烷,固定相为 45~ 75μm层析用粗孔硅胶,空塔流速约为0.764cm/min,适宜上样量为 5g,但不同层析柱分离条件时,应通过实验来确定最大上样量。
[1] Nakahama M,Katoh K,Kawaguchi S,et al.Study on the thermal behavior of nitroglycerine[J].Science and Technology of Energetic Materials,2007,68(1):21-24.
[2] Naminosuke K.Propellants and Explosives[M].Weinheim:WILEY-VCH Verlag Gmb H& Co.KGaA,2007.
[3] Marshakov VN.Study on the structure of the combustion wave of nitroglycerine-based propellants[J].Russian Journal of Physical Chemistry B,2009,3(6):971-975.
[4] Lu Kai-tai,Lin Peng-chu.Study on the stability of nitroglycerine spent acid[J]. Process Safety and Environmental Protection,2009,87(2):87-93.
[5] Akrill P,Cocker J.Determination of nitr-oglycerin and its dinitrate metabolites in urine by gas chromatography-mass spectrometry as potential biomarkers for occupational exposure[J].Journal of Chromatography B,2002,778(1-2):193-198.
[6] 贾林,张皋,胡玲,等.ASE-HPLC检测某型号球形发射药中的叠氮硝胺、硝化甘油、Ⅱ号中定剂含量的研究 [J].分析测试技术与仪器,2008,14(4):222-225.JIA Lin,ZHANG Gao,HU Ling,et al.Determination of thecomponents in the globule gun-propellant using accelerated solvent extraction(ASE)followed by HPLC[J].Analysis and Testing Technology and Instruments,2008,14(4):222-225.
[7] 罗运军,严晓虎 ,吕桂琴.定量体积排除色谱用于火药成分分析的研究[J].火炸药学报,1998,21(1):28-29.LUO Yun-jun, YAN Xiao-hu, Lǜ Gui-qin.Investigation on the composition analysis of propellant by SEC[J]. Chinese Journal of Explosives and Propellants,1998,21(1):21,28-29.
[8] Martel R,Bellavance-Godin A,Lévesque R,et al.Determination of nitroglycerin and its degradation products by solid-phase extraction and LC-UV[J].Chromatographia,2010,71(3-4):285-289.
[9] Hewitt A D,Bigl S R.Elution of energetic compounds from propellant and composition B residues,ADA452664[R].Springfield:NTIS,2005.
[10]张颖颖,杨亦文,任其龙,等.硅胶柱层析法提纯大豆磷脂酰胆碱的研究[J].高校化学工程学报 2006,20(5):685-690.ZHANG Ying-ying,YANG Yi-wen,REN Qi-long,et al.Purification of soybean phosphatidylcholine by silica gel column chromatography[J]. Journal of Chemical Engineering of Chinese Universities,2006,20(5):685-690.
[11]周婕,杜斌,张振中,等.硅胶柱层析法纯化全苯异氰酸酯基-U-环糊精[J].应用化学,2008,25(5):548-551.ZHOU Jie,DU Bin,ZHANG Zhen-zhong.Separation of mono-6-N-allylam ino-perphenylcarbamoylated U-cyclodextrin with silica gel[J].Chinese Journal of Applied Chemistry,2008,25(5):548-551.
[12]尹芳华,钟王景.现代分离技术 [M].北京:化学工业出版社,2009.
[13]丁明玉.现代分离方法与技术 [M].北京:化学工业出版社,2006.
[14]王泽山,韩盘铭,张续柱.火药实验方法 [M].北京:兵器工业部教材编审室,1986.
[15]《发射药理化分析》编写组.发射药理化分析(下册 )[M].北京:国防工业出版社,1985.
