吉西他滨治疗非小细胞肺癌的时辰药理学研究Δ
2010-09-11赵文艳吴福林江苏无锡市第二人民医院无锡市214002
钟 皎,赵文艳,吴福林(江苏无锡市第二人民医院,无锡市 214002)
时辰药理学是研究药理作用节律问题的一门边缘学科,其依据生物学上的时间特性,研究药物作用的规律。这门学科近年来逐渐受到人们的重视并广泛开展了对药理效应、药动学和不良反应与时间周期性变化规律(生物节律)关系的研究,并获得了快速发展。目前,国内、外对心血管药物、非甾体抗炎药、平喘药等药物的时辰药理学已经有了深入研究,并找到了最佳给药时间。吉西他滨作为新一代抗肿瘤药[1~3],目前应用相当广泛,但是国、内外甚少有其关于时辰药理学这方面的文献报道。因此,本文旨在通过选择不同时间给药,观察吉西他滨的血药浓度、毒性以及药物的疗效,研究它们在不同时间内给药后的昼夜节律变化,最终选择临床最佳给药时间,获得最佳疗效。
1 仪器与材料
1.1 仪器
1100型高效液相色谱仪及其工作站(美国Agilent公司);XW-80A旋涡混合器(上海医科大学仪器厂);TGL-16G台式离心机(上海安亭科学仪器厂);AB-256-S电子分析天平(瑞士梅特勒-托利多公司)。
1.2 药品与试剂
吉西他滨标准品(江苏豪森药业股份有限公司,批号:070105,含量:98.6%);内标去氧氟尿苷(浙江国邦药业有限公司,批号:070427-1,含量:98.5%);注射用吉西他滨(江苏豪森药业股份有限公司,批号:060906、070404、071001、080503);顺铂注射液(江苏豪森药业股份有限公司,批号:060803、070302、070801、080402);空白血浆为无锡市第二人民医院检验科提供;乙腈为色谱纯(美国Merk公司);其它试剂均为市售分析纯;水为超纯水。
2 方法
2.1 病例选择
(1)患者需签署知情同意书;(2)年龄18~75岁;(3)有组织学或细胞学证实的局部或系统的非小细胞支气管癌(腺癌或未分类的非小细胞肺癌),细胞标本可以通过支气管镜刷检或活检获得,若有可测量或可评价病灶,胸膜积液的细胞样本也可以;(4)患者肺部应有X线或CT可测量或可评估病灶;(5)体力状况ECOG评分0~2;(6)预计生存期>12周;(7)血液学、肝肾功能正常。中性粒细胞计数>1 500·mm-3,血小板>100 000·mm-3,血红蛋白>8 g·mm-3,转氨酶<3倍正常值上限,胆红素<1.5倍正常值上限,肌酐<1.5 mg·dL-1。
2.2 给药时间
我院2006年~2008年病理或针吸细胞学确诊不能手术的NSCLC患者60例,随机分成3组,A组(n=20)在8∶00给药,B组(n=20)在14∶00给药,C组(n=20)在20∶00给药。吉西他滨1 g·m-2,ivgtt,第1、8天;顺铂75 mg·m-2,ivgtt,第1天,第21天重复。
2.3 血药浓度测定
患者停止静脉滴注吉西他滨后,于0.5、1.5、3 h各取静脉血4 mL(肝素抗凝),血浆样品经提取处理后用高效液相色谱法测定其血药浓度。
2.4 疗效及毒副反应评价
按世界卫生组织(WHO)实体瘤疗效通用标准,分为完全缓解(CR)、部分缓解(PR)、无变化(NC)和进展(PD),CR与PR合计为有效。毒副反应评价按WHO抗癌药物毒性反应分级标准(0~Ⅳ级)进行评定[4]。
3组均在化疗2周期后作首次疗效评价,无肿瘤进展者继续化疗;以后每2周期评价疗效1次;发现肿瘤进展,终止观察。
2.5 统计学方法
数据采用SPSS11.0统计软件进行分析处理,P<0.05为差异有统计学意义。
3 结果与分析
3.1 血药浓度
给药后3个时间点的浓度见表1。
表1 3组不同时间点给药后的血药浓度比较(±s)Tab 1 Serum concentrations of gemcitabine at 0.5 h,1.5 h and 3 h in 3 groups(±s)
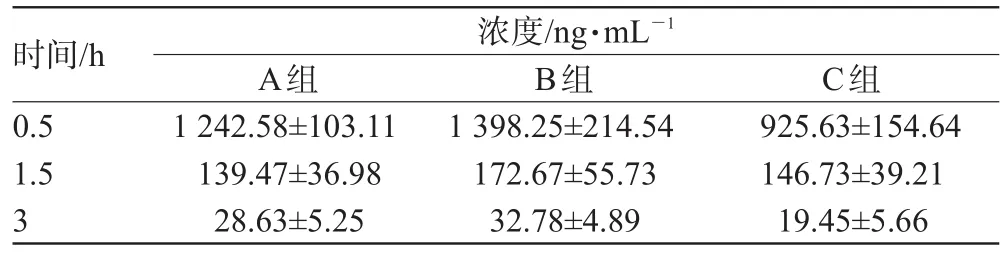
表1 3组不同时间点给药后的血药浓度比较(±s)Tab 1 Serum concentrations of gemcitabine at 0.5 h,1.5 h and 3 h in 3 groups(±s)
浓度/ng·mL-1时间/h 0.5 1.5 3 A组1 242.58±103.11 139.47±36.98 28.63±5.25 B组1 398.25±214.54 172.67±55.73 32.78±4.89 C组925.63±154.64 146.73±39.21 19.45±5.66
从表1可以看出,B组整体的血药浓度较A、C组偏高,但3个时间点组间差异无统计学意义(P>0.05),即3个时间点给药后的血药浓度无时辰节律变化。
3.2 近期疗效
有53例患者完成2周期以上化疗,可评价疗效。3组有效率差异无统计学意义(P>0.05),具体见表2。
3.3 毒副反应
3组毒副反应发生情况见表3。
3组患者给药后的血液系统、胃肠道、脱发毒性反应相对而言较为严重,肝肾功能、神经方面均无Ⅲ~Ⅳ级毒性反应发生。其中,与B组比较,A、C组毒性反应的严重程度明显降低,重度反应发生较少,无一例Ⅳ级毒副反应发生,患者容易接受,耐受性良好。
4 讨论
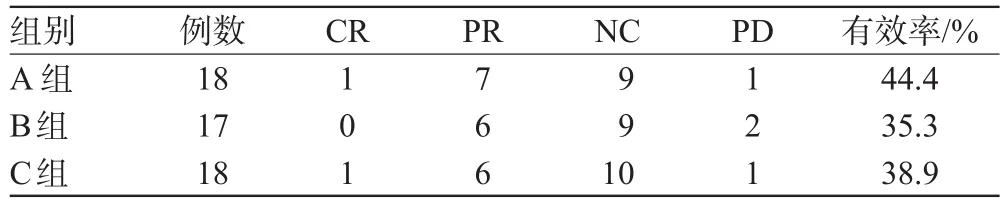
表2 3组有效率比较(n)Tab 2 Comparison of effective rate among 3 groups(n)
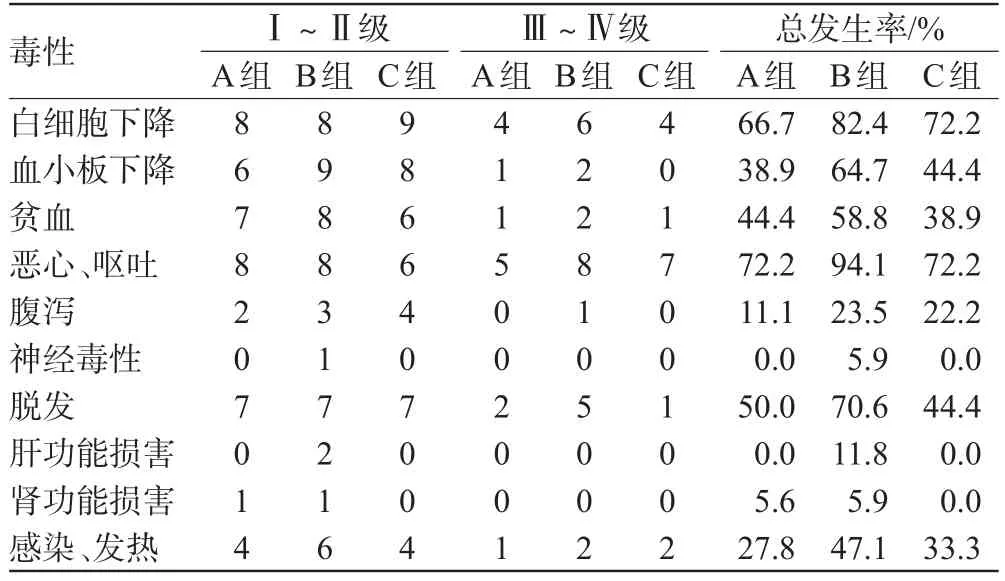
表3 3组毒副反应比较(n)Tab 3 Comparison of toxicity among 3 groups(n)
本试验在不同时间点给予患者吉西他滨后,其血药浓度、疗效在组间的差异无统计学意义,说明吉西他滨在不同时间点给药后血药浓度和疗效不存在时辰节律变化,但是14∶00给药组总的和Ⅲ~Ⅳ级的毒副反应发生率明显高于其他两组,尤其是血液毒性、胃肠道毒性。文献报道[5,6],肿瘤细胞与正常细胞具有不同的生物钟,癌细胞一般在上午生长较快,而正常细胞在下午生长较快。吉西他滨在抑制和杀伤肿瘤细胞的同时,也影响到正常细胞的快速分裂和生长,这可能是本试验14∶00给药后毒副反应大的原因之一。血药浓度一般与毒副反应存在一定的正相关关系[7~9]。14∶00给药组的血药浓度较其他两组偏高、这可能也是导致化疗效果较差、毒副反应发生率高、患者不易耐受的又一原因。在8∶00和20∶00给药组的患者都能较好地耐受化疗的毒副发应,疗效也较好,但是20∶00给药不符合患者的给药规律,影响患者的正常作息时间,因此8∶00给药时间最佳。为了进一步确定最佳给药时间点,有待扩大病例数作深入研究。
通过时辰节律变化选择最佳给药时间点,可使同等剂量的药物,发挥最大治疗作用的同时,毒副反应降至最低。
[1]Kosmas C,Tsavaris N,Mylonakis N,et al.An overview of current results with the gemcitabine and docetaxel combination as initial and salvage chemotherapy regimen in advanced non-small-cell lung cancer[J].Crit Rew Oncol Hemaol,2003,45(3):265.
[2]Heinemarm V.Role of gemcitabine in the treatment of advanced and metastatic breast cancer[J].Oncology,2003,64(3):191.
[3]陆方阳,黄贵佳,赵莉莉,等.吉西他滨联合顺铂序贯与同期放化疗治疗局部晚期非小细胞肺癌临床比较[J].中国药房,2008,19(20):1 572.
[4](美)罗兰T.斯基尔(Roland T.Skeel).癌症化疗手册[M].第6版.北京:科学出版社,2005:721~722.
[5]陈充抒,梁 燕.依据时辰药理正确择时给药[J].武警医学,2006,17(8):618.
[6]Morris K.New day danwns for research on circadian rh-ythms[J].Lancet,1999,353(9 157):990.
[7]Wang LR,Huang MZ,Xu N,et al.Pharmacokinetics of gemcitabine in Chinese patients with non-small-cell lung cancer[J].J Zhejiang Univ Sci B,2005,6(2):446.
[8]王临润,张国兵,黄明珠.吉西他滨固定速率输注的峰浓度与血液学毒性的相关性研究[J].浙江大学学报(医学版),2007,36(4):391.
[9]Kroep JR,Giaccone G,Voorn DA,et al.Gemcitabine and Paclitaxel:pharmacokinetic and pharmacodynamic interactions in patients with non-small-cell lung cancer[J].J CIin Oncol,1999,17(7):2 190.
