LC-MS法测定人血浆中尼美舒利的浓度
2010-09-11刘炜李晓晔程维明北京世纪坛医院药剂科北京市100038沈阳药科大学药学院沈阳市110016
刘炜,李晓晔,程维明#(1.北京世纪坛医院药剂科,北京市100038;.沈阳药科大学药学院,沈阳市110016)
尼美舒利(Nimesulide)属于非甾体类解热镇痛药,是第1个选择性环氧化酶-2(Eyclooxygenase-2,COX-2)抑制剂,用于治疗慢性关节炎、手术及急性创伤后疼痛和炎症、耳鼻咽部炎症所致的疼痛、上呼吸道感染引起的发热、头痛等,临床研究表明,其有着良好的抗炎、镇痛和退热作用[1~3]。同时,尼美舒利还可用于其他慢性疼痛与炎症的治疗,并可作为癌症三阶梯止痛疗法的第一阶梯首选药[4]。国内、外虽有关于尼美舒利血浆浓度测定方法的研究报道,但均是采用高效液相色谱法[5~7],灵敏度和时效性不能满足现代临床药学研究的要求。鉴于此,笔者首次建立了以缬沙坦为内标的测定人血浆中尼美舒利浓度的液-质联用(LC-MS)法。结果表明,本方法灵敏、简便、结果准确可靠,重复性好,可用于尼美舒利的临床血药浓度监测和药动学研究。
1 材料
1.1 仪器
1200系列高效液相色谱系统,包括G1376A高效液相泵、G1367B自动进样器、G1316A柱温箱、G1365B多波长紫外检测器、Hystar色谱工作站(美国Agilent公司);micrOTOFQ 125质谱系统(美国Bruker公司)。
1.2 试药
尼美舒利对照品(苏州俞氏药业有限公司,批号:050512);内标:缬沙坦对照品(北京法玛泰医药技术开发有限公司,批号:050789562);乙腈为质谱纯,其它试剂均为分析纯,水为双重蒸馏水。
2 方法与结果
2.1 色谱及质谱条件
色谱柱:Agilent Zorbox SB-Cl8(50 mm×2.1 mm,5 μm);流动相:乙腈-0.1%甲酸(65∶35);流速:1.0 mL·min-1;柱温:35℃;进样量:10µL。
高分辨质谱数据在正离子状态下采集,选择m/z309(尼美舒利,[M+H]+)和m/z436(缬沙坦,[M+H]+)进行监测;毛细管电压:4 500 V;干燥气:氮气;流速:4 L·min-1;干燥气温度:250℃;喷雾气:氮气;流速:0.8 L·min-1;离子扫描范围:50~1 000m/z;质谱缓冲气体:氩气;流速:30 bar。
典型提取离子流色谱见图1;质谱见图2。
2.2 试验溶液的制备
2.2.1 尼美舒利对照品溶液:准确称取105℃干燥至恒重的尼美舒利对照品适量,置于5 mL容量瓶中,加甲醇溶解并稀释至刻度,得浓度为1 μg·mL-1的对照品溶液,摇匀,备用。
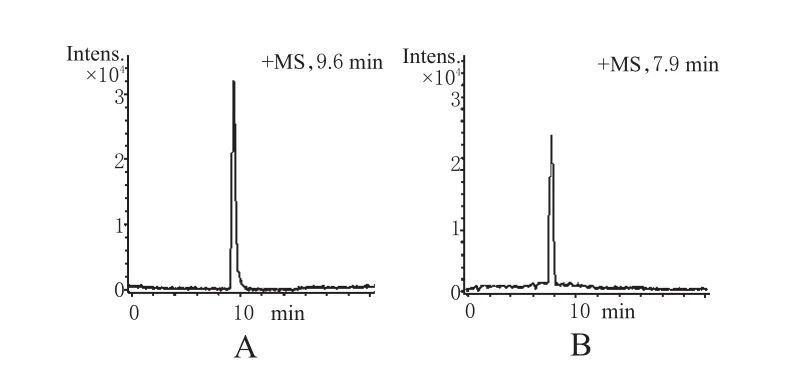
图1 典型提取离子流色谱Fig 1 Typical EIC

图2 质谱Fig 2 Mass Spectra
2.2.2 内标溶液:准确称取105℃干燥至恒重的缬沙坦对照品适量,置于1 mL容量瓶中,加甲醇溶解并稀释至刻度,得浓度为5 μg·mL-1的内标溶液,摇匀,备用。
2.3 样品处理
取血浆1.0 mL,置于具塞离心管中,加入内标溶液20 μL,涡旋混合30 s。加入提取溶剂乙醚3 mL,涡旋混合30 s后,15 000 r·min-1离心10 min,吸取有机层,置于5 mL离心管中,氮气吹干。进样前以乙腈-水(1∶1)100 μL复溶,吸取10 μL进样。
2.4 灵敏度试验
取空白血浆,加入尼美舒利对照品溶液适量,梯度稀释,使血浆最终药物质量浓度相当于1 ng·mL-1,进样10 μL ,记录m/z309的提取离子流的峰面积。以该峰面积对空白血浆中m/z309的提取离子流的峰面积进行比较,其S/N=3.5,故尼美舒利的灵敏度为1 ng·mL-1。
2.5 标准曲线的制备
取空白血浆,分别加入尼美舒利对照品溶液及内标溶液适量,使血浆中尼美舒利药物质量浓度相当于5、10、15、20、25、50 ng·mL-1,并且血浆中缬沙坦质量浓度为50 ng·mL-1,处理血样并各进样10 μL,记录m/z309和m/z436的提取离子流的峰面积。以m/z309与m/z436的峰面积比值(Y)对尼美舒利血药浓度(X)作图,绘制标准曲线,得回归方程为:Y=104.16X±6.99(r=0.998 9)。结果表明,尼美舒利血药浓度在5~50 ng·mL-1范围内线性关系良好。
2.6 方法回收率及精密度试验
用空白血浆将尼美舒利对照品溶液稀释成不同质量浓度的标准含药血浆样品,按“2.3”项下方法处理并测定,各浓度日内重复测定3次,并连续测定3 d。计算方法回收率及日内、日间精密度,结果均符合生物等效性研究的方法学要求。回收率及精密度试验结果见表1。
2.7 重复性试验
制备低、中、高(5、10、30 ng·mL-1)3种浓度的提取前和提取后的2组样品,每组样品重复进样5次,测定m/z309的提取离子流的峰面积,结果RSD=5.89%,表明试验重复性良好。
表1 回收率及精密度试验结果(±s,n=3)Tab 1 Results of recovery and precision(±s,n=3)
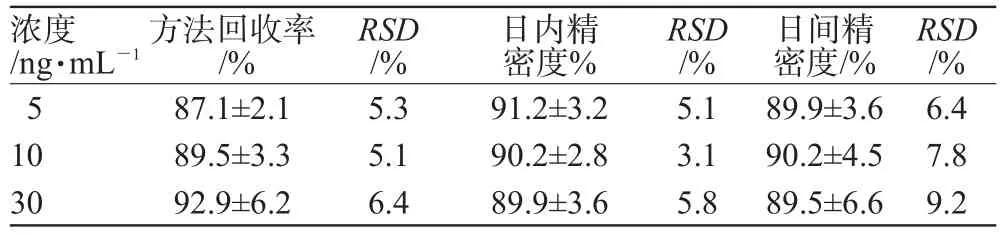
表1 回收率及精密度试验结果(±s,n=3)Tab 1 Results of recovery and precision(±s,n=3)
浓度/ng·mL-1 5 10 30方法回收率/%87.1±2.1 89.5±3.3 92.9±6.2 RSD/%5.3 5.1 6.4日内精密度%91.2±3.2 90.2±2.8 89.9±3.6 RSD/%5.1 3.1 5.8日间精密度/%89.9±3.6 90.2±4.5 89.5±6.6 RSD/%6.4 7.8 9.2
2.8 稳定性试验
按“2.3”项下方法分别制备并处理低、中、高(5、10、30 ng·mL-1)3种浓度的3组血浆样品,各组分别在室温放置(6、12、24 h)、长期冻存(-20℃冻存1、2、3周)和冻融(1、2、3次)条件下进行测定以考察稳定性,结果见表2。
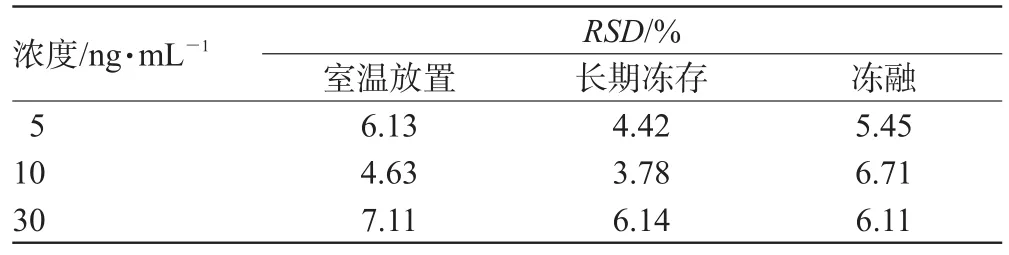
表2 稳定性考察结果Tab2 Stability of escitalopram
3 讨论
笔者曾考查乙腈沉淀蛋白法和有机溶剂提取法对于尼美舒利提取率的影响,发现乙腈沉淀蛋白法的尼美舒利回收率较低,推测为蛋白对尼美舒利的结合作用造成损失,故采用乙醚提取法,提取效率高,操作简便。
采用高效液相色谱法进行生物等效性试验时,由于紫外叠加原理,内标与药物、药物与杂质之间均需要有一定的分离度才可以定量准确。采用LC-MS法,由于采取了选择性离子监测,所以保证了目标物质的定性隔离,不再要求具有很高分离度的高效液相色谱条件,较常规的高效液相色谱法更具优势。
[1]苏玉永,杜江涛,张汉萍.尼美舒利片治疗骨关节炎的临床疗效和安全性[J].中国医院药学杂志,2002,22(4):228.
[2]吴抽浪,许胜敏,仇灵江,等.尼美舒利在烧伤换药中的镇痛作用[J].安徽医药,2007,11(5):401.
[3]罗利飞,韩子华.尼美舒利联合表阿霉素对人膀胱癌EJ细胞的体外作用[J].实用医学杂志,2009,25(2):182.
[4]张莉静.尼美舒利的镇痛与抗痛觉过敏作用的中枢成分[J].国外医学-药学分册,2004,31(1):24.
[5]霍 强,李见春,马 涛,等.HPLC测定血浆中尼美舒利浓度[J].淮海医药,2009,27(1):22.
[6]王丽萍,温 实,胡宝生.尼美舒利缓释微丸在家兔体内吸收与体外溶出相关性实验[J].中国药师,2005,8(1):10.
[7]Piera DM,Roberta C,Christine B,et al.Characterization and compaction behaviour of nimesulide crystal forms[J].International Journal of Pharmaceutics,2007,342(1):137.
