竹炭对溶液中二价锰离子的吸附特性研究
2010-08-21王伟刘神燕张启伟
王伟 刘神燕 张启伟
(丽水学院 化学化工系 浙江 丽水 323000)
竹炭对溶液中二价锰离子的吸附特性研究
王伟 刘神燕 张启伟*
(丽水学院 化学化工系 浙江 丽水 323000)
研究了竹炭对溶液中二价锰离子的吸附行为。试验结果表明:竹炭对锰2+吸附的最佳酸度为pH=4.4;温度在298K时,竹炭对锰2+的吸附平衡时间为6 h,且竹炭粒径对吸附平衡时间基本不产生影响;锰2+的初始浓度越大,一定量竹炭的吸附量越大;一定浓度、体积的溶液中,竹炭的投放量越大,去除率越大;在298~318 K的温度范围内,吸附量呈现先增后减的趋势。
竹炭;锰2+;吸附;影响因素
锰是环境水质污染物的重要重金属监测指标之一, 国家明文规定工厂排污口含锰及其化合物的最高排放质量浓度为2. 0 mg/L。因此,减少工业废水中二价锰离子的含量有着重要的意义[1-3]。竹炭是竹材热解得到的主要产品,是一种多孔性物质,具有较大的比表面积,因而它具有强吸附性。竹炭作为一种新型吸附材料,在环境保护、医学和食品等领域具有广泛的应用前景。竹炭作为吸附剂特点是吸附性广,表现在对许多重金属及有机物均有较好的吸附性[4-7],价格便宜,原料易得,吸附速度相对较快,操作简单。
本文研究了在最佳吸附酸度条件下,竹炭对锰2+的吸附特性,为了解竹炭对锰2+的吸附机理以及含锰废水的深度处理提供有效的理论依据。
1 试验材料与方法
1.1 主要仪器及试剂
722型分光光度计、THZ-82A型水浴恒温振荡器(±0.5 ℃)、pHS-3C型酸度计。
实验所用的条状机制竹炭由浙江富来森有限公司提供。竹炭经粉碎、过筛,选出20~30目、30~40目和70~80目的竹炭,平均粒径为0.90~0.60 mm、0.60~0.45 mm和0.22~0.18 mm。吸附前经去离子浸泡24h,并洗涤数次后,250℃烘干,待用。
2.0 mg/mL锰2+标准贮备溶液按常规配制;其它实验所用试剂均为分析纯。
1.2 分析方法
取适量二价锰离子样品溶液于250ml锥形瓶中,加水至50mL,加硝酸磷酸混合液2mL和玻璃珠3粒,煮沸3min,取下稍冷,加过硫酸铵和高碘酸钾固体各0.5g,保持微沸1min,冷却后,移入100mL容量瓶中,定容,以未加显色剂的样品溶液作空白,于530nm波长处测定吸光度[8]。
1.3 吸附平衡试验
称取经处理的一定量的竹炭于碘量瓶中,加入一定量的缓冲溶液及一定量的Mn2+标准溶液。于恒温振荡器中振荡至平衡,振荡速率控制在 80 次/min。按1.2 法分析水相中Mn2+的平衡浓度,按下式计算吸附量Q(mg/g)及去除率E%。
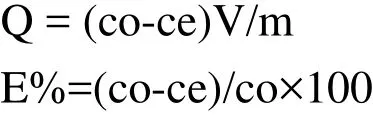
式中co为锰的原始浓度(mg/mL),ce为锰的平衡浓度(mg/mL);V为吸附质溶液体积(mL);m为吸附剂质量(g)。
2 结果与讨论
2.1 溶液酸碱度对吸附量的影响
准确称取50.0 mg竹炭(0.22~0.18 mm)于碘量瓶中,准确移入不同pH的NaAc-HAc缓冲溶液20.0 mL,加入一定量的锰2+标准贮备溶液,使Mn2+的初始浓度co=3.0 mg/mL,溶液总体积为100 mL,在T=298K条件下间隙振荡,每隔一定时间取样,分析溶液中Mn2+的浓度,直至平衡。计算竹炭对体系中Mn2+的吸附量与pH之间的关系。
在NaAc-HAc缓冲体系中,竹炭对锰2+的吸附量与酸度的关系见图1。根据图可知,在T=298 K条件下,竹炭对二价锰离子的最佳吸附酸度为pH=4.4,其吸附量为41.54 mg/g。以下实验均选用在pH=4.4的NaAc-HAcl缓冲溶液中进行。
2.2 吸附平衡时间
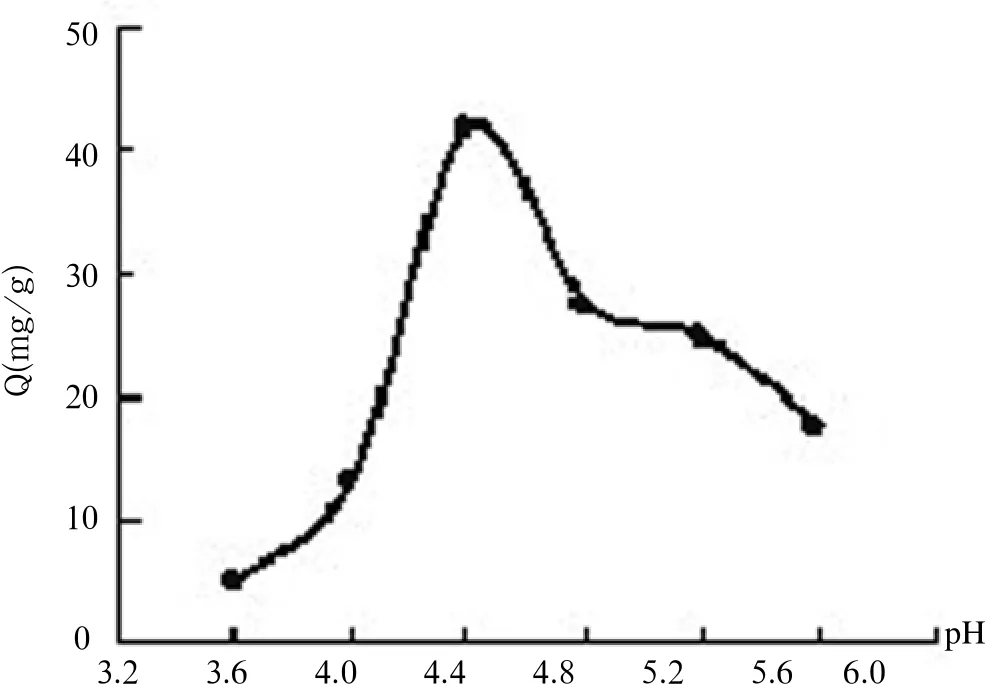
图1 ph对吸附量的影响
准确称取50.0 mg 竹炭(0.22~0.18 mm)于碘量瓶中,在pH=4.4的NaAc-HAc缓冲体系中,使Mn2+的初始浓度c0=3.0 mg/mL,溶液总体积为100 mL,置于恒温振荡器上,在T=298K条件下振荡,每隔一定时间取上层轻清液分析溶液中的Mn2+的残余浓度,直至达到平衡。将一系列数据经体积校正换算成每克竹炭对Mn2+吸附量Qt,实验数据见表1。
从表4可知:吸附量随时间的延长而增大,但在6h后吸附量基本趋于不变,即达到吸附平衡,所以确定竹炭吸附二价锰离子的平衡时间为6小时。
同样方法及条件也试验了不同粒径竹炭(0.90~0.60 mm和0.60~0.45 mm)对Mn2+的吸附平衡时间及平衡吸附量,其吸附平衡时间均为6.5h,吸附量分别为31.59 mg/g和39.15 mg/g。试验表明,不同粒径竹炭吸附平衡时间基本相同,但吸附量不同,粒径小吸附量大,平均吸附速率快。另外,大颗粒竹炭大多数沉于溶液底部,易分离。

表1 竹炭吸附平衡时间
2.3 竹炭用量对吸附效果的影响
分别准确称取30.0mg、50.0mg、70.0 mg、90.0mg、110.0mg、竹炭(0.22~0.18 mm)于碘量瓶中,在pH=4.4的NaAc-HAc缓冲体系中,使Mn2+的初始浓度c0=3.0 mg/mL,溶液总体积为100 mL,置于恒温振荡器上,在T=298K条件下振荡,直至平衡。测得吸附平衡时Mn2+的浓度ce mg/mL,换算成相应的吸附量Q mg/g,及计算吸附率E%。吸附量 Q(mg/g)或E%与竹炭量(mg)的关系见图2。
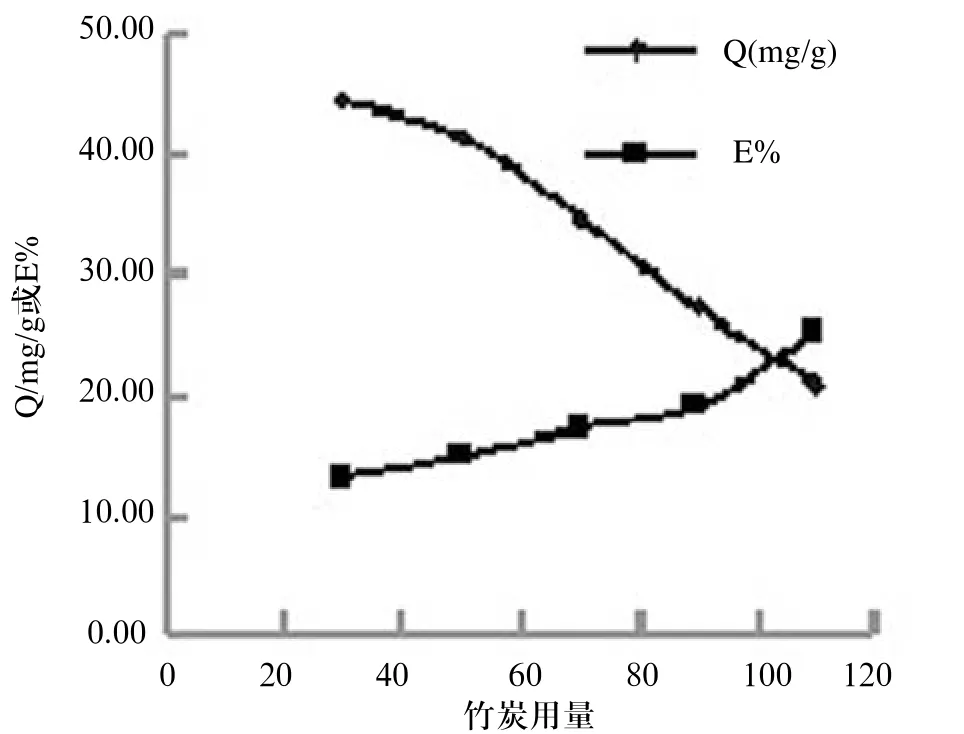
图2 竹炭的用量对吸附的影响
从图中不难看出在一定体积一定浓度的吸附质溶液中,竹炭的投放量越小其比吸附量越大,每克竹炭吸附越充分;而随着吸附剂用量的增大,吸附量减小,但吸附率是增大的,为了保证出水合格,应根据吸附剂的优劣,颗粒大小,适当地选择吸附剂用量[9]。
2.4 吸附质浓度对吸附效果的影响
分别准确称取50.0 mg的竹炭(0.22~0.18 mm)5份于碘量瓶中,加入不同量的二价锰离子标准溶液、20mL、pH=4.4的NaAc-HAc缓冲溶液和蒸馏水,溶液总体积均为100.0 mL,在T=298K条件下振荡,直至平衡。以未加竹炭的溶液作空白,置于水浴恒温振荡器上,振荡速率控制在150 r/min,在T=298 K条件下振荡,直至趋于平衡,测得吸附平衡时Mn2+的浓度ce mg/mL,换算成相应的吸附量Q mg/g,及计算吸附率E%。试验结果见图3。
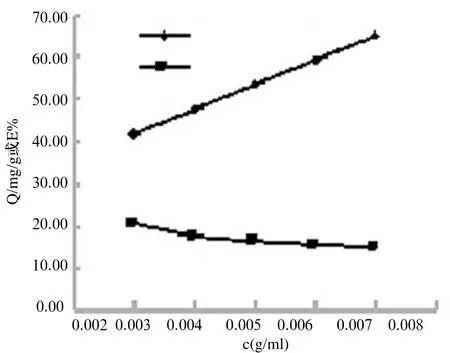
图3 吸附质浓度对吸附的影响
可以看出,吸附剂的吸附量与溶液中二价锰离子浓度有关,随着二价锰离子浓度的增大,吸附剂的吸附量增大,但吸附率减小。
2.5 温度对吸附量的影响
分别准确称取50.0 mg的竹炭(0.22~0.18 mm)3份于碘量瓶中,在pH=4.4的NaAc-HAc缓冲体系中,使Mn2+的初始浓度c0=3.0 mg/mL,溶液总体积为100 mL,置于恒温振荡器上,分别在T=298 K、308 K、318 K条件下恒温振荡,直至平衡,测得吸附平衡时Mn2+的浓度ce mg/mL,换算成相应的吸附量Q mg/g,及计算吸附率E%。结果见表2。

表8 温度对吸附量的影响
结果表明:在298~318 K的温度范围内,吸附量先增后减,说明在适当的温度范围内,升高温度可促进吸附;但当温度超过某值时,温度升高反而减小吸附量,即抑制吸附[10]。
3 小结
竹炭对锰2+吸附的最佳酸度为pH=4.4;温度在298K时,竹炭对锰2+的吸附平衡时间为6 h,且竹炭粒径对吸附平衡时间基本不产生影响;锰2+的初始浓度越大,一定量竹炭的吸附量越大;一定浓度、体积的溶液中,竹炭的投放量越大,去除率越大。在298~318 K的温度范围内,吸附量呈现先增后减的趋势。
1 于少亭,陈金镖.固定床吸附过程浓度分布方程在离子交换法去除酒中二价锰离子的应用[J].天津化工,19 93(1):20-22.
2 荆立坤,王银叶,王强.纳米分子筛和硅藻土吸附去除水中二价锰离子的研究[J].天津城市建设学院报,2008,14(3):207-209.
3 詹旭,罗泽娇,马腾.高岭土吸附剂去除含锰废水中二价锰离子的实验研究[J].地质科技情报,2005,24(1):95-98.
4 张启伟,王桂仙竹炭对溶液中汞(Ⅱ)离子的吸附行为研究.林业科学,2006,42(9):102-105.
5 王桂仙,张启伟竹炭对溶液中Zn2+的吸附行为研究[J].生物质化学工程,2006,40(3):17-20.
6 张启伟,王桂仙竹炭对溶液中铅(Ⅱ)离子的吸附行为研究[J].丽水学院学报,2005,27(5):60-63.
7 Wang Guixian, Wang Muhua, Zhang Qiwei Adsorption property of aniline on bamboocharcoal[J]林业科学,2008,44(3):135-139.
8 常文保,李克安.简明分析化学手册[M].北京:北京大学出版社,1981,10-132.
9 张启伟,王桂仙.竹炭对饮用水中氟离子的吸附条件的研究[J].广东微量元素科学,2005,12(3):63-66.
10 王娟,廖水姣,朱端卫,等.不同氧化物硼负载体吸附二价锰离子的特性研究[J].土壤学报,2005,43(5):749-755.
Adsorption Behavior of Bamboo Charcoal for Divalent Manganese Ion
Wang Wei, Liu Shenyan, Zhang Qiwei
(Department of Chemistry, Lishui University, Lishui, 323000)
The adsorption of divalent manganese ion by bamboo charcoal from the solution was studied. The results revealed that the optimal acidity for bamboo charcoal to adsorb Mg2+was 4.4, when the temperature was 298 K, the adsorption equilibrium time of bamboo charcoal for divalent manganese ion was 6 h, and the particle size of bamboo charcoal basically had no impact on the adsorption equilibrium time, the higher the initial concentration of divalent management ion, the more the adsorption volume of the bamboo charcoal with certain amount in the solution with certain concentration and volume, the more the bamboo charcoal, the higher the adsorption rate, and within the temperature range from 298 K to 318 K, the adsorption volume rose fi rst and then declined.
bamboo charcoal, divalent manganese ion, adsorption, inf l uencing factor
浙江省大学生科技创新项目(2009R004),丽水学院开放实验室项目(2010005)
王伟,男,浙江湖州人,丽水学院化学本科在读学生,主要研究方向为环境化学。
张启伟,副教授,E-mail:lsxyzqw@126.com
