HPLC 法测定大鼠肝微粒体中睾酮的含量
2010-08-06夏宗玲陈荣邹素兰王明丽江苏常州市第一人民医院药剂科常州市213000
夏宗玲,陈荣,邹素兰,王明丽(江苏常州市第一人民医院药剂科,常州市213000)
目前已发现与药物代谢密切相关的细胞色素P450酶(CYP450)主要有CYP1~4[1],其中以CYP3A亚族最为重要,占人肝脏CYP450总量的30%,主要成员包括CYP3A3、CYP3A4、CYP3A5和CYP3A7,成人肝脏中以CYP3A4为主[2]。CYP3A4的底物较多,据统计大约38个类别共150多种药物是其底物[3],约占全部药物的50%,因此能够准确地评价CYP3A4的酶活性对药物相互作用研究以及临床合理用药都是十分重要的。目前国内、外多采用睾酮作为CYP3A4的探针底物[4,5],通过测定肝微粒体体外代谢反应过程中睾酮的减少量或其代谢产物6-羟基睾酮的生成量来评价该酶的活性。文献[6,7]报道的高效液相色谱(HPLC)法多采用外标法测定,由于操作过程复杂,从而影响了睾酮的定量,较难准确评价CYP3A4的活性。本研究在借鉴前人研究的基础上,简化了样品处理方法,采用内标法建立了一种快速、高效、稳定的测定大鼠肝微粒体温孵体系中睾酮含量的HPLC法。
1 材料
1.1 仪器
HPLC系统,包括2996紫外检测器、1525双元梯度泵、717自动进样器、Empower色谱工作站(美国Waters公司);电子分析天平(赛多利斯科学仪器(北京)有限公司,精密度:1×10-5g);5417R高速台式离心机(德国Effendorf公司);低温冰箱(日本Sanyo公司);旋涡混合器(上海医科大学仪器厂);恒温振荡水槽(上海精宏仪器设备有限公司);雪花制冰机(北京长流科学仪器公司)。
1.2 试药
睾酮对照品(常州佳尔科药业集团有限公司提供,批号:090301,纯度:99.3%);地西泮标准品(中国药品生物制品检定所,批号:230-9601,供含量测定用);乙腈为色谱级;枸橼酸三钠盐、枸橼酸脱氢酶、氧化/还原型辅酶Ⅱ均购于Sigma-Aldrich(上海)试剂公司。
1.3 动物
Sprague-Dawley(SD)大鼠,♂,体质量200~250 g,月龄1.5个月,合格证号:SCXK(沪)2003-0003,购于上海斯莱克实验动物有限责任公司。
2 方法与结果
2.1 色谱条件
色谱柱为Ultimate-XB C18(250 mm×4.6 mm,4 μm),流动相为水-乙腈(50∶50,V/V),内标为地西泮,流速为1.0 mL·min-1,检测波长为245 nm,柱温为30 ℃,进样量为20 μL。取空白微粒体、空白微粒体+睾酮+内标、37℃下睾酮代谢15 min后的微粒体样品(含地西泮)进样测定,记录色谱,结果详见图1。
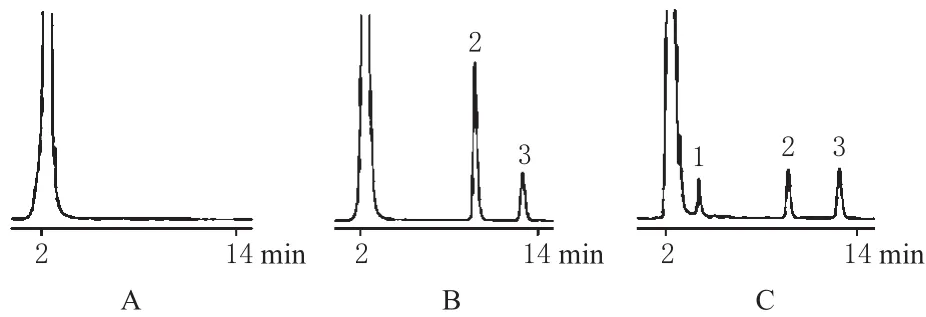
图1 高效液相色谱图A.空白微粒体;B.空白微粒体+睾酮+地西泮;C.微粒体样品;1.代谢产物;2.睾酮;3.地西泮Fig 1 HPLC chromatogramsA.blank microsome;B.blank microsome+testosterone+diazepam;C.microsomes sample;1.metabolite;2.testosterone;3.diazepam
2.2 溶液的制备
2.2.1 对照品溶液:精密称取睾酮对照品约28.836 mg,置于10 mL容量瓶中,加甲醇溶解并稀释至刻度,混匀得浓度为10 mmol·L-1的对照品溶液,待用。
2.2.2 内标溶液:精密称取地西泮标准品5.4 mg,置于25 mL容量瓶中,加甲醇溶解并稀释至刻度,混匀得浓度为200 μg·mL-1的内标溶液,待用。
2.2.3 再生系统溶液:枸橼酸三钠盐2.8 mg,枸橼酸脱氢酶0.5 mg(相当于10 u),0.15 mol·L-1氯化镁0.1 mL,0.1 mol·L-1三羟甲基甲烷-盐酸(Tris-HCl)缓冲液(pH 7.4)0.9 mL,混合,可根据需要按比例制备一定量,临用新配。
2.3 微粒体的制备
取SD大鼠,断头后打开腹腔暴露出肝脏,用冰浴冷却的生理盐水经胸动脉或门静脉注入肝脏,直至肝脏颜色变黄后取出肝脏浸入冰冷的生理盐水中,洗去血水(均在4℃以下操作)。滤纸吸干水分,称重后加入4倍于肝重的0.25 mol·L-1蔗糖溶液,制成匀浆,于9 000 r·min-1离心20 min,取上清液于19 000 r·min-1离心20 min,分取上清液,加入1/10体积的88 mol·L-1氯化钙溶液,置于冰浴中5 min,不时搅拌,于27 000 r·min-1离心20 min,除去上清液,在沉淀物中加入pH 7.4的0.1 mol·L-1Tris-KCl缓冲液(含0.15 mol·L-1KCl)混匀,27 000 r·min-1离心30 min,取沉淀物加pH 7.4的50 mmol·L-1Tris-蔗糖缓冲液制成微粒体悬浮液,于-80℃下保存备用。以BCA(Bicinchoninic aicd)法测定微粒体中的蛋白浓度。
2.4 生物样品处理
取大鼠肝微粒体适量,用新鲜制备的枸橼酸-枸橼酸脱氢酶再生系统溶液稀释成蛋白浓度为1.0 mg·mL-1的混合悬液,充氧气2 min,取此混悬液0.2 mL,加对照品溶液2 μL,混匀,预孵5 min后,加氧化/还原型辅酶Ⅱ的0.1%NaHCO3溶液(临用新配,置于冰浴中,终浓度为0.25 mmol·L-1/0.1 mmol·L-1)启动反应,并开始记时,孵育一定时间后加冰冷的乙腈0.2 mL(含20 μL地西泮,终浓度为10 μg·mL-1)终止反应,涡旋1 min,15 000 r·min-1离心10 min,取上清液20 μL进样,测定代谢反应完成后剩余CYP3A4底物睾酮浓度。
2.5 标准曲线的制备
取对照品溶液制备成不同浓度的溶液,依次取2 μL加入经60℃加热失活的大鼠肝微粒体中至200 μL,分别制备成浓度为10.0、25.0、50.0、75.0、200 μmol·L-1的生物标准品(每个浓度平行3份,同时做空白对照),加20 μL的内标溶液,180 μL乙腈沉淀蛋白,旋涡振摇1 min,15 000 r·min-1离心10 min,取上清液20 μL进样,进行色谱分析。以睾酮峰面积与地西泮峰面积的比值(R)对浓度(X)进行线性回归,得回归方程:R=0.025 7X+0.035 3(r=0.999 5)。结果表明,睾酮在10.0~200.0 μmol·L-1浓度范围内与R有良好的线性关系。本实验睾酮最低检测浓度为0.76 ng。
2.6 回收率试验
取对照品溶液制备成不同浓度的溶液,依次取2 μL加入经60℃加热失活的大鼠肝微粒体中至200 μL,分别制备成浓度为15.0、50.0、100.0 μmol·L-1的生物标准品(每个浓度平行5份,同时做空白对照),按“2.5”项下方法处理,进行色谱分析,计算方法回收率(即将所得信号值代入回归方程,求得测定值,与加入量比较)及相对回收率(即测得睾酮和内标峰面积的比值与相同浓度的睾酮和内标的纯溶液的峰面积比值比较),结果见表1。

表1 回收率试验结果(n=5)Tab 1 Results of recovery tes(tn=5)
2.7 精密度试验
取“2.6”项下低、中、高(15.0、50.0、100.0 μmol·L-1)浓度的生物标准品(每个浓度平行5份,同时做空白对照),按“2.5”项下方法处理,分别在同日内测定5次(每隔1 h测定1次)和连续测定5 d(每天同一时间每个浓度平行测定5份),计算日内、日间RSD,结果见表2。

表2 精密度试验结果(n=5)Tab 2 Results of precision test(n=5)
2.8 CYP3A4活性测定
分别取大鼠肝微粒体适量,加入2 μL一定浓度的睾酮溶液,使其终浓度为25 μmol·L-1,加入枸橼酸-枸橼酸脱氢酶适量,预孵5 min后,加氧化/还原型辅酶Ⅱ的0.1%NaHCO3溶液5 μL(临用新配,置于冰浴中,终浓度为0.25 mmol·L-1/0.1 mmol·L-1)启动反应,并开始记时,37 ℃下分别孵育5、10、15 min后,按“2.4”项下方法加冰冷的乙腈处理后,取上清液20 μL进样,根据以下公式依次计算出代谢量、反应率及反应速度,结果见表3。

表3 不同反应时间下大鼠肝微粒体中CYP3A4活性测定结果(n=3)Tab 3 Determination results of CYP3A4 activity in mice liver microsomes at different reaction time(n=3)
W=W0-Wt(W:代谢量;W0:初始加入睾酮的量;Wt:反应t时间后剩余睾酮的量)

由表3可见,随着反应时间的延长反应率直线增加,反应速度略有增加但无显著性差异(P>0.05),表明所制备的大鼠肝微粒体中CYP3A4活性稳定可靠,可用于药物体外代谢研究。
3 讨论
近年来新药上市后因发生代谢性相互作用原因而退出市场的情况时有发生[8],因此了解药物代谢性相互作用已成为医务人员及患者的迫切要求。为了避免因药物代谢性相互作用而引起的严重不良反应的发生,药物代谢的研究越来越引起广大科研人员的重视,目前美国食品与药品管理局(FDA)已规定新药在上市前必须做其代谢研究。由于大部分药物都是通过CYP450酶催化代谢的,因此通过探针底物测定CYP450酶的活性尤其重要。
CYP3A亚族催化大部分药物的氧化代谢,而其中也有较多是用于体内外分析酶活性的探针底物,如用N-甲基14C标记的红霉素测定CYP3A4[9],但这种方法对仪器设备要求较高,一般实验室较难达到,故本论文采用睾酮作为探针底物,建立了一种快速、灵敏、准确测定睾酮含量的高效液相色谱法,此法可用于CYP3A4活性的测定。
在内标物的选择上,笔者考察了地塞米松、甲睾酮、氢化可的松、可的松、胺碘酮、卡马西平、米达唑仑、茶碱、苯妥英钠等,最终发现地西泮无论在出峰时间、峰形,还是分离度方面都是最佳选择。
在反相液相色谱条件下,乙腈洗脱能力优于甲醇,可以得到相对较高柱效的睾酮峰,且使睾酮与内标得到很好分离,故选择乙腈-水=50∶50的比例作为流动相。
[1]Nelson DR,Kamataki T,Waxman DJ,et al.The P450superfamily:update on new sequences,gene mapping,accession numbers,early trivial names of enzymes,and nomenclature[J].DNA Cell Biol,1993,12(1):1.
[2]Imaoka ST,Yamada T,Hiroi K,et al.Muitiple forms of human P450expressed in saccharomyces cerevisiae,systematic characterization and comparison with those of the rat[J].Biochem Pharmacol,1996,51(8)∶1 041.
[3]Yamano S,Tatsuno J,Gonzale FJ.The CYP2A3 gene product catalyzes coumarin 7-hydroxylation in human liver microsomes[J].Biochemistry,1990,29(5)∶1 322.
[4]Caroline AL,Sue HK,Thomas AK,et al.CYP3A4 expressed by insect cells infected with a recombinant baculovirus bontaining both CYP3A4 and human NADPH-cytochrome P450reductase is catalytically similar to human liver microsomal CYP3A4[J].Archives of Biochemistry and Biophysics,1995,319(1):157.
[5]Arthur GR,William MA.Energetics of heterotropic cooperativity between a-naphthoflavone and testosterone binding to CYP3A4[J].Archives of Biochemistry and Biophysics,2007,463(1):89.
[6]张 荣,刘昌辉,王宁生,等.以睾酮为探针采用高效液相色谱法测定细胞色素CYP4503A4的酶活性[J].色谱,2008,26(1):80.
[7]Jessica LF,David MP,Barbara JR,et al.A novel testosterone 6b-hydroxylase activity assay for the study of CYP3A-mediated metabolism,inhibition,and induction in vitro[J].J Pharmacol Toxicol Methods,2002,46(2):117.
[8]张石革.若干处方药撤出市场的回顾与思考[J].药物不良反应杂志,2002,4(1):14.
[9]Rile RJ,Howbrook D.In vitro analysis of the activity of the major human hepatic CYP enzyme(CYP3A4)using[N-methyl-14C]-erythromycin[J].J Pharmacol Toxicol Methods,1997,38(4):189.
