可变剂量帕利哌酮缓释剂治疗急性期精神分裂症的疗效、耐受性及安全性
2010-07-18余一旻李华芳杨甫德胡建赵振环董继承陈红辉许秀峰李鸣王刚王晓萍0谢世平唐济生张晋碚关念红丁瑛谭庆荣李惠春钟华张鸿燕谢光荣孙学礼0顾牛范
余一旻李华芳杨甫德胡 建赵振环董继承陈红辉许秀峰李 鸣王 刚王晓萍0谢世平唐济生张晋碚关念红丁 瑛谭庆荣李惠春钟 华张鸿燕谢光荣孙学礼0顾牛范
可变剂量帕利哌酮缓释剂治疗急性期精神分裂症的疗效、耐受性及安全性
余一旻1李华芳1杨甫德2胡 建3赵振环4董继承5陈红辉6许秀峰7李 鸣8王 刚9王晓萍10谢世平11唐济生12张晋碚13关念红13丁 瑛14谭庆荣15李惠春16钟 华17张鸿燕18谢光荣19孙学礼20顾牛范1
目的 研究可变剂量的帕利哌酮缓释剂治疗急性期精神分裂症患者的有效性、耐受性与安全性。方法 采用开放性、单组、多中心研究,使用可变剂量的帕利哌酮缓释剂(3~12 mg/d)治疗急性期精神分裂症患者608例,观察期8周,通过阳性和阴性综合征量表(PANSS)评价有效性。通过体检、实验室检查、心电图检查及其他不良事件的报告评价安全性。结果 治疗有效率(PANSS减分率≥30%)随治疗时间而增加,治疗8周末有效率为82.6%。研究终点PANSS总分与基线相比,差异具有统计学意义(P<0.01)。终点平均剂量为(7.9±2.2)mg/d。治疗8周时40.11%患者的治疗剂量保持6 mg/d的水平,4.44%患者的治疗剂量下调至3 mg/d。常见的不良事件为锥体外系反应、便秘、肝功能异常、睡眠障碍、嗜睡、疲乏及恶心。结论 可变剂量帕利哌酮缓释剂(3~12 mg/d)治疗急性期精神分裂症有效,且耐受性、安全性良好。
帕利哌酮缓释剂 精神分裂症 有效性 耐受性 安全性
帕利哌酮(paliperidone,9-羟利培酮)是一种新型的非典型抗精神病药,它是利培酮的主要活性代谢产物,主要拮抗多巴胺D2受体和5-羟色胺2A受体(5HT2A)。帕利哌酮缓释剂由强生药物研发公司(J&JPRD)开发,已作为治疗精神分裂症的一种新药[1,2]。
迄今关于帕利哌酮治疗精神分裂症疗效的信息大多来自随机、对照的临床试验[3-5]。在这些研究中将固定目标剂量的帕利哌酮缓释剂(3、6、9、12或15 mg/d)随机分配给患者。众所周知,不同患者对药物的敏感性存在很大差别,临床上更应关注患者个体,优化个体的治疗方案。因此,可变剂量的研究更符合临床实际情况。
本研究是一项为期8周的开放性、单组多中心研究,目的是评估可变剂量的帕利哌酮缓释剂治疗急性期精神分裂症住院患者的耐受性、安全性与有效性。由上海市精神卫生中心负责,国内20家精神卫生中心共同完成。
1 对象与方法
1.1 研究对象
1.1.1 入组标准 符合美国精神障碍诊断与统计手册第4版(DSM-IV)精神分裂症的诊断标准;性别不限,年龄≥18岁;住院患者;受试者必须处于精神分裂症急性发作阶段,基线期的PANSS总分≥70分。
1.1.2 排除标准 筛查前3个月使用了氯氮平或长效的注射类抗精神病药;有重大或不稳定的躯体疾病,包括最近或目前存在有临床意义的实验室检查异常(血、尿常规和血生化检测);曾经或目前存在迟发性运动障碍症状的患者;曾有抗精神病药所致恶性综合征病史的患者;存在暴力或者自伤行为或倾向者;怀孕或者哺乳的女性患者;胃肠道狭窄或梗阻;过去的6个月有物质依赖史。
1.1.3 受试者 本次研究于2008年4—12月共入组病例608例,其中男性289例,女性313例,平均年龄为(32±11)岁,总病程0~44年,中位数为4.9年,使用抗精神病药物0~44年,中位数为3.5年。
1.2 方法
1.2.1 用药方法 研究过程中,剂量可在3~12 mg/d范围内调整。起始剂量为缓释胶囊6 mg/d,如能耐受可根据病情由研究者决定是否加量或保持6 mg/d。如果根据病情需要增加剂量,每隔14 d可增加3 mg/d,直到最高达12 mg/d。为了保证患者安全,在研究过程的任何时间,可因耐受性下调剂量,最低3 mg/d,如果下调到3 mg后耐受但疗效不佳可以调回6 mg。治疗观察期为8周。
1.2.2 合并用药 任何先前使用的抗精神病药逐渐减量,并在研究的最初2周内停用;在入选前已经接受稳定剂量苯二氮卓艹类药物的患者,可使用苯二氮卓艹类药物治疗兴奋、焦虑或者睡眠困难,允许合并劳拉西泮(最高剂量6 mg/d)或地西泮(最高剂量30 mg/d),连续使用不超过10 d;可用抗胆碱药苯扎托品、双环哌丙醇(最高剂量4 mg/d)或苯海索治疗锥体外系反应(EPS),苯二氮卓艹药物可用来治疗静坐不能,治疗前必须评定异常不自主运动量表(AIMS)、Barnes静坐不能分级量表(BARS)和Simpson-Angus分级量表(SAS)。
1.2.3 有效性评价 主要疗效评价指标为研究结束时(第8周末)阳性与阴性综合征量表(PANSS)总分较基线的变化,研究终点的PANSS总分比基线期至少降低30%为有效[减分率公式:100%×(PANSS基线总分-PANSS终点总分)/(PANSS基线-30)]。次要疗效评价指标为PANSS总分、分量表评分和因子评分。各项指标在治疗前和治疗第1、2、4、8周末分别进行评定。
1.2.4 安全性评价 记录患者自接受研究药物开始至研究结束期间发生的所有不良事件;在基线、第4周和第8周进行实验室检查与心电图检查;在治疗前和治疗第1、2、4、8周末测量生命体征、体重,进行体格检查,用AIMS、BARS和SAS评定EPS。
1.2.5 统计分析方法 全部资料采用SAS 8.0统计分析软件进行数据处理比较。采用意向性分析对全部接受了至少1次帕利哌酮缓释剂治疗的受试者进行人口统计学以及基线特征性数据分析,对全部接受了至少1次帕利哌酮缓释剂治疗和提供了≥1次基线后疗效测定数据的受试者进行有效性数据分析。使用Wilcoxon符号秩和检验(有序/连续的数据)和符号检验(名义变量)分析每次随访和基线值的变化。
2 结果
2.1 病例入选与完成情况(分析集)
本次研究共入组病例608例,其中6例病例无基线后疗效数据,不纳入全分析集(FAS),FAS共602例,占入组病例的99.01%。
研究期间服用其他抗精神病药物病例共24例,脱落54例,脱落原因包括不良事件(11例)、撤回知情同意(9例)、服药依从性差(7例)、违背研究方案(1例)以及失访(21例)及其他(5例),不纳入符合方案集(PPS)。PPS共524例,占入组病例的86.18%。
2.2 耐受性
研究开始2周时,97.46%患者可耐受6 mg/d,2.03%(12例)患者因不能耐受下调至3 mg/d,0.51%(3例)的患者违反方案加量至9 mg/d(研究结束后统计时发现违反方案);治疗8周时,44.18%患者的剂量为9 mg/d,11.28%为12 mg/d,仍有40.11%患者的剂量保持6 mg/d,不能耐受而下调至3 mg/d的患者比例为4.44%,平均剂量为(7.9 ±2.2)mg/d。
2.3 合并用药
608名受试者中,93.42%(568例)的患者合并用药,63.16%(384例)的患者在研究中使用其他抗精神病药物,绝大多数(360例)在研究开始前就使用,但按照方案于研究开始后2周内停用。64.8%的患者合并使用苯二氮卓艹类药物(劳拉西泮或地西泮),连续使用未超过10 d。52.14%的患者合并使用治疗EPS的药物。
2.4 有效性评价
2.4.1 PANSS总分 各个访视点PANSS评分与基线相比逐渐减少。经配对t检验,基线与各个访视点PANSS评分的差异均有统计学意义(P<0.01),
见表1。
表1 602例患者PANSS总分变化,分

表1 602例患者PANSS总分变化,分
访视点PANSS总分与基线差值t值P值基线89.9±13.6第1周75.3±15.2-(14.6±12.5)28.48<0.01第2周67.9±16.2-(22.0±15.3)35.21<0.01第4周60.4±16.8-(29.5±17.5)41.34<0.01第8周54.3±18.9-(35.6±20.6)42.35<0.01
2.4.2 PANSS分量表评分和因子评分 PANSS分量表评分(阳性症状、阴性症状、一般精神病理症状)和因子评分(阳性症状、阴性症状、思维紊乱、难以控制的敌意/兴奋、焦虑/抑郁)随着研究治疗时间延长均显著下降,见表2、表3。
表2 602例患者PANSS分量表评分变化,分

表2 602例患者PANSS分量表评分变化,分
访视点阳性症状t值P值阴性症状t值P值一般精神病理症状t值P值基线23.7±5.8 22.5±7.5 43.7±7.8第1周18.8±5.9 26.14<0.01 19.6±7.2 19.24<0.01 36.9±8.1 25.41<0.01第2周16.4±5.8 33.26<0.01 17.9±7.2 23.64<0.01 33.6±8.2 31.33<0.01第4周13.9±5.6 38.80<0.01 16.2±6.8 27.45<0.01 30.3±8.3 36.23<0.01第8周12.3±6.1 37.63<0.01 14.6±6.8 30.48<0.01 27.3±9.0 38.10<0.01
表3 602例患者PANSS因子评分变化,分
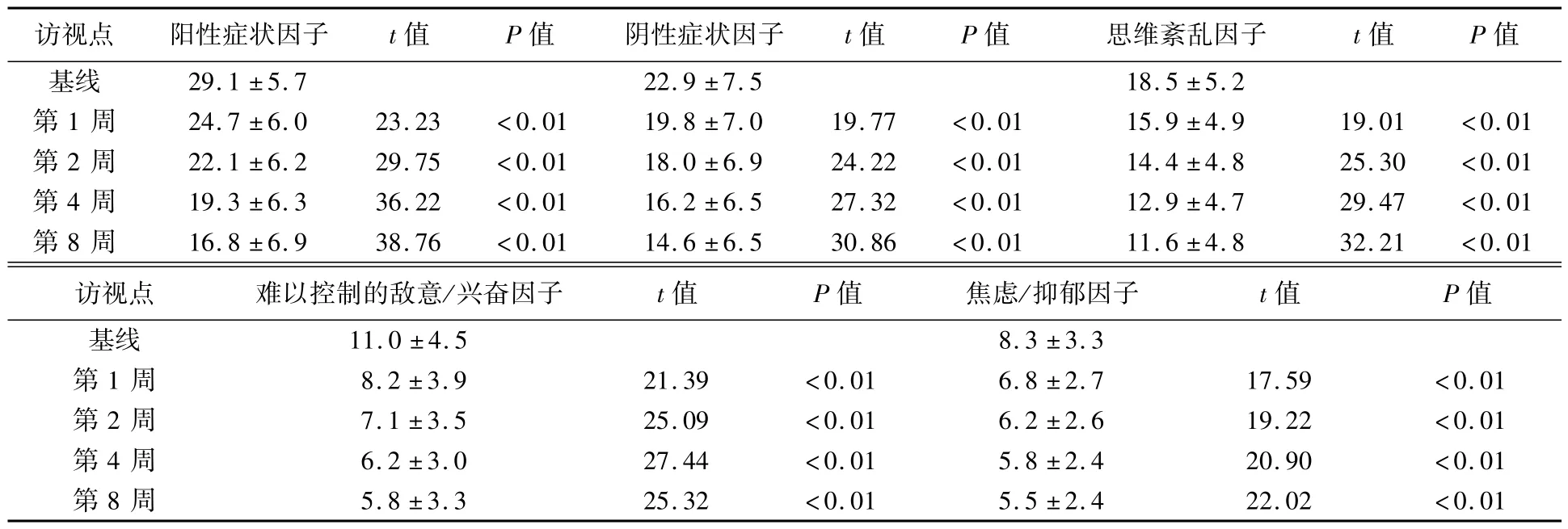
表3 602例患者PANSS因子评分变化,分
访视点阳性症状因子t值P值阴性症状因子t值P值思维紊乱因子t值P值基线29.1±5.7 22.9±7.5 18.5±5.2第1周24.7±6.0 23.23<0.01 19.8±7.0 19.77<0.01 15.9±4.9 19.01<0.01第2周22.1±6.2 29.75<0.01 18.0±6.9 24.22<0.01 14.4±4.8 25.30<0.01第4周19.3±6.3 36.22<0.01 16.2±6.5 27.32<0.01 12.9±4.7 29.47<0.01第8周16.8±6.9 38.76<0.01 14.6±6.5 30.86<0.01 11.6±4.8 32.21<0.01访视点难以控制的敌意/兴奋因子t值P值焦虑/抑郁因子t值P值基线11.0±4.5 8.3±3.3第1周 8.2±3.9 21.39<0.01 6.8±2.7 17.59<0.01第2周 7.1±3.5 25.09<0.01 6.2±2.6 19.22<0.01第4周 6.2±3.0 27.44<0.01 5.8±2.4 20.90<0.01第8周 5.8±3.3 25.32<0.01 5.5±2.4 22.02<0.01
2.4.3 有效率 第1周末治疗有效208例,有效率34.55%,第2周末治疗有效355例,有效率58.97%,第4周末治疗有效460例,有效率76.41%,到治疗终点治疗有效497例,有效率达到82.56%。
2.5 安全性评价
全体患者被纳入安全性分析。608名受试者中有413名(67.9%)报告发生不良事件,报告不同的不良事件例数达524例(同一个受试者可以报告多例不良事件)。至少可能与药物有关的不良事件包括8大系统47项,发生率为57.2%(348/608)。较常见的不良事件(发生率≥3%)为8项,分别是EPS(41.8%)、上呼吸道感染(9.0%)、便秘(7.7%)、肝功能异常(5.1%)、睡眠障碍(4.1%)、嗜睡(4.1%)、疲乏(3.9%)、恶心(3.6%)。
严重不良事件发生率为0.86%(共计5例),分别是复发住院2例,顿服研究药物5片再住院1例,左锁骨骨折1例,体温升高、血压下降、意识不清1例。仅前3例与研究药物可能有关或有关。严重不良事件占不良事件比例为1.2%,无一例发生死亡。
2.5.1 生命体征及实验室检查 受试者的心率、收缩压和舒张压都有统计学意义地轻微下降,但无临床意义。体重由基线(61.0±12.5)kg增加到治疗终点时的(62.8±12.3)kg,差异有统计学意义,体重增加范围-9.0~18.0 kg,中位数为1.0 kg。15.22%(84/608)的患者治疗终点时体重增加≥7%。
总体实验室各项指标终点与基线水平相当。血糖基线(4.7±0.9)mmol/L,终点(4.8±0.8) mmol/L,差异基本不具有临床意义,有8例(1.3%)血脂升高,均为轻度。
共有67例次基线心电图正常但终点心电图异常,其中仅9例的心电图异常判定为有临床意义(9/608,1.5%),4例出现心动过缓伴或不伴心律不齐(4/608,0.7%),其余包括T波改变、心肌损伤和偶发房性早搏。
2.5.2 锥体外系反应 EPS不良事件报告率为41.8%,被判断与药物有关的EPS发生率为37.2%。AIMS量表评分(面部、四肢、躯干)基线时0~13分,中位数0分,治疗终点0~7分,中位数0分,差异无统计学意义(t=1.74,P=0.08)。SAS量表评分由基线0~16分,中位数0分,终点0~15分,中位数0分,组内比较差异有统计学意义(t= 2.19,P=0.03),但数值改变化极轻微,无临床意义。BARS量表客观评价、主观-对多动不安的知觉、主观-与不安相关的痛苦、对静坐不能的总体评价等评分基线与终点变化差异均无统计学意义(P>0.05)。
2.5.3 泌乳素水平 本研究共发生9例(1.48%)可能与泌乳素水平升高相关的不良事件,分别是泌乳4例(0.66%),闭经2例(0.33%),月经紊乱3例(0.49%),不良事件对应的剂量为(6.7±1.3) mg/d,平均服药(22.0±9.1)d发生。但是本研究未测定泌乳素水平。
3 讨论
帕利哌酮是一种新型单胺能拮抗剂,主要拮抗D2和5HT2A受体。一般抗精神病药推荐小剂量起始,逐渐滴定到靶剂量。由于帕利哌酮缓释剂采用分子结合渗透泵式控制释放技术,可在24小时内以一个相对受控制的速度释放,首次服用后血药浓度平缓升高,并且血药浓度峰谷波动维持在幅度较小的范围内[1,6]。研究发现,帕利哌酮的这种药代动力学特征使大部分受试者可以从抗精神病药的有效剂量直接作为起始剂量服用,而不需要剂量滴定[7]。本研究结果同样支持本结论,研究开始2周时,97.46%患者可耐受6 mg/d,仅2.0%患者不能耐受而下调至3 mg/d,治疗8周时不能耐受6 mg/d而下调至3 mg/d的患者比例也仅为4.44%,多数受试者治疗剂量为6 mg/d或9 mg/d。终点平均剂量为(7.9±2.2)mg/d。本研究结果表明精神分裂症患者对可变剂量帕利哌酮缓释剂(3~12 mg/d)的耐受性良好,以帕利哌酮缓释剂治疗精神分裂症可从有效剂量6 mg/d开始。
本研究结果还显示,在治疗剂量范围内应用帕利哌酮缓释剂是安全的,常见的不良事件为EPS、便秘、肝功能异常、睡眠障碍、嗜睡、疲乏、恶心等。对血糖、血脂、心电图几乎无影响,体重增加轻微,与国外同类研究报道的增重1~2 kg相似[4]。与泌乳素水平升高有关的不良事件发生率为1.48%,与国外报道的1%相似[4]。虽然主观报告EPS发生率较高,但研究者评定发生的EPS的程度与基线相比差异无统计学意义。EPS发生率较高的原因可能与在住院环境下8周急性期治疗药物剂量递增较快有关。国外多个研究均发现帕利哌酮缓释剂EPS发生率与安慰剂相当[4,5,8]。
本研究根据PANSS总分下降情况,观察到帕利哌酮缓释剂有效率达到82.6%。其他次要有效性评价指标与该观察结果一致。PANSS各因子评分持续显著下降表示帕利哌酮缓释剂急性期治疗可以全面控制症状。该结果表明,精神分裂症急性期治疗中,大多数患者可通过6~9 mg/d的帕利哌酮缓释剂获得病情改善。
上述结果与国外相关研究基本一致,国外研究结果同样显示帕利哌酮缓释剂对精神分裂症阳性症状、阴性症状、情感症状和认知症状等均有治疗作用,疗效优于安慰剂[4,5,8]。
本研究具有一定局限性。第一,本研究为开放性、单组研究,缺乏随机对照组;第二,本研究量表评分未使用盲态评分员,评分者了解患者所使用的药物剂量;第三,本研究允许研究开始后2周内使用其他抗精神病药物,未能对其加以清洗。上述因素都可能导致偏倚,在一定程度上影响研究结果的真实性与可靠性。
声明:本研究得到杨森制药研发公司资助。
1 Owen RT.Extended-release paliperidone:efficacy,safety and tolerability profile of a new atypical antipsychotic.Drugs Today(Barc),2007,43(4):249-258.
2 Yang LP,Plosker GL.Paliperidone extended release.CNS Drugs,2007,21(5):417-425.
3 Meltzer HY,Bobo WV,Nuamah IF,et al.Efficacy and tolerability of oral paliperidone extended-release tablets in the treatment of acute schizophrenia:pooled data from three 6-week,placebo-controlled studies.J Clin Psychiat,2008,69(5):817-829.
4 Marder SR,Kramer M,Ford L,et al.Efficacy and safety of paliperidone extended-release tablets:results of a 6-week,randomized,placebo-controlled study.Biol Psychiat,2007,62(12):1363-1370.
5 Kane J,Canas F,Kramer M,et al.Treatment of schizophrenia with paliperidone extended-release tablets:a 6-week placebocontrolled trial.Schizophr Res,2007,90(1-3):147-161.
6 Pani L,Marchese G.Expected clinical benefits of paliperidone extended-release formulation when compared with risperidone immediate-release.Expert Opin Drug Deliv,2009,6(3):319-331.
7 Boom S,Talluri K,Janssens L,et al.Single-and multiple-dose pharmacokinetics and dose proportionality of the psychotropic agent paliperidone extended release.J Clin Pharmacol,2009,49(11):1318-1330.
8 Davidson M,Emsley R,Kramer M,et al.Efficacy,safety and early response of paliperidone extended-release tablets(paliperidone ER):results of a 6-week,randomized,placebo-controlled study. Schizophr Res,2007,93(1-3):117-130.
Effectiveness,tolerability and safety of flexible-dose treatment w ith oral extended release paliperidone in acute schizophrenia
Yu Yimin1,Li Huafang1,Yang Pude2,et al.1.Shanghai Mental Health Center,Shanghai Jiaotong University School of Medicine,Shanghai 200030;2.Beijing HuiLongGuan Hospital,Beijing 100096
Objective:Evaluate flexible-dose treatment with paliperidone extended release tablets in acute schizophrenia.M ethods:Patients with acute schizophrenia(N=608)participated in an open label,8-week,one-arm,multicenter trial of flexible dose treatment with paliperidone extended release tablets(3-12 mg/d).The Positive and Negative Syndrome Scale(PANSS)was used to evaluate effectiveness.Safety was assessed.The results of a physical examination,lab tests,an electrocardiogram and an adverse events scale were used to evaluate safety.Results:The response rate(that is,the proportion of subjects with at least 30% drop from the baseline PANSS total score)increased with the duration of treatment and was 82.6%at week 8. The baseline and 8-week PANSS total scores were significantly different(P<0.01).The average dosage was(7.9±2.2)mg/d at week 8.The dose of paliperidone in 40.11%patients remained 6 mg/d and 4.44% down to 3 mg/d at endpoint.Common adverse events included extrapyramidal symptoms,constipation,hepatic dysfunction,sleeping disorder,drowsiness,fatigue,and nausea.Conclusion:Flexible dosing(3~12 mg/d) treatment with paliperidone extended release tablets is safe,well-tolerated and effective for patients with acute schizophrenia.
Extended release paliperidone Schizophrenia Effectiveness Tolerability Safety
2010-08-14)
(本文编辑:张红霞)
国家“重大新药创制”科技重大专项创新药物研究开发技术平台建设——精神药物新药临床评价研究技术平台(2008ZX09312-003)
1.上海交通大学医学院附属精神卫生中心 200030;2.北京回龙观医院 100096;3.哈尔滨医科大学第一临床医学院150036;4.广州脑科医院 510370;5.青岛市精神卫生中心 266042;6.武汉市精神卫生中心 430022;7.昆明医学院第一附属医院650032;8.苏州市广济医院 215008;9.首都医科大学附属北京安定医院 100088;10.武汉大学人民医院 430060;11.南京脑科医院210029;12.山东省精神卫生中心 250014;13.中山大学附属第三医院 510630;14.杭州市第七人民医院 310013;15.第四军医大学西京医院 710032;16.浙江大学医学院附属第二医院 310009;17.湖州市第三人民医院 313000;18.北京大学第六医院 100083;19.中南大学湘雅二院 410013;20.四川大学华西医院 610041。通信作者:李华芳,电子信箱lhlh5@yahoo.com.cn
