药品不良反应报告分析
2010-06-11陈廷霞潘海涛
陈廷霞 潘海涛
我院2009年共收集106例药品不良反应(ADR),笔者拟通过对这些报告的统计、分析,以引起临床医药工作者对ADR的重视,进一步推进ADR检测和报告工作在我院的开展,并为临床安全用药提供参考。
1 资料与方法
1.1 一般资料 本院2009年通过网络系统向国家ADR数据库上报的ADR报表106份。
1.2 方法 按患者性别、年龄、涉及药物、给药途径、临床表现等进行统计、分析。
2 结果
2.1 性别与年龄分布 106例ADR的病例中,男53例(占50.00%),女53例(占50.00%);年龄1~79岁,19~60岁成人的ADR例数最多,达57.54%。发生ADR患者的性别与年龄分布见表1。
2.2 ADR涉及的药物类型及构成比 106例ADR涉及的药品有34种,其中抗菌药物发生率最高,达84例,占ADR总数的79.24%。ADR涉及的药物类型及构成比见表2。
2.3 引发ADR的给药途径 各种给药途径中,静脉给药引起的ADR最多,共99例,占93.40%;口服7例,占6.60%。
2.4 ADR涉及的抗菌药物类别、种类及ADR例数 在106例抗菌药物引发的ADR中,氟喹诺酮类为22例(占20.74%)居首位,其次是头孢菌素类21例(占19.81%),β-内酰胺酶抑制剂10例(占9.43%),克林霉素类10例(占9.43%)。ADR涉及的抗感染药类别、品种数及ADR例数见表3。
2.5 ADR涉及的器官或系统及主要临床表现 106例ADR中,涉及皮肤及其附件62例(占43.36%),其次为消化系统26例(占18.18%),神经系统16例(占11.18%)。ADR涉及的器官或系统及主要临床表现见表4(其中,有些ADR涉及多个器官和系统,故总计数为143例,大于106例患者)。
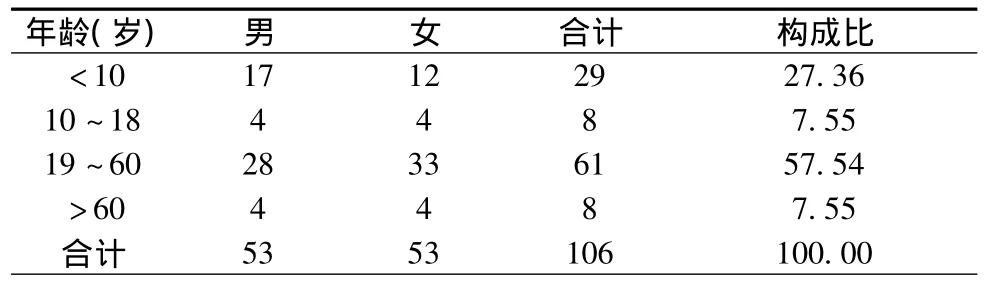
表1 发生ADR的年龄与性别分布(例,%)
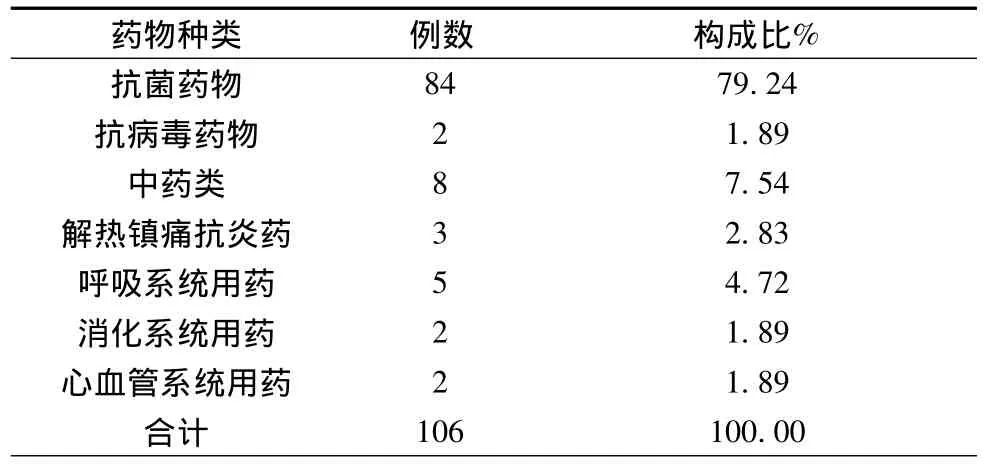
表2 ADR涉及的药物类型及构成比(例,%)
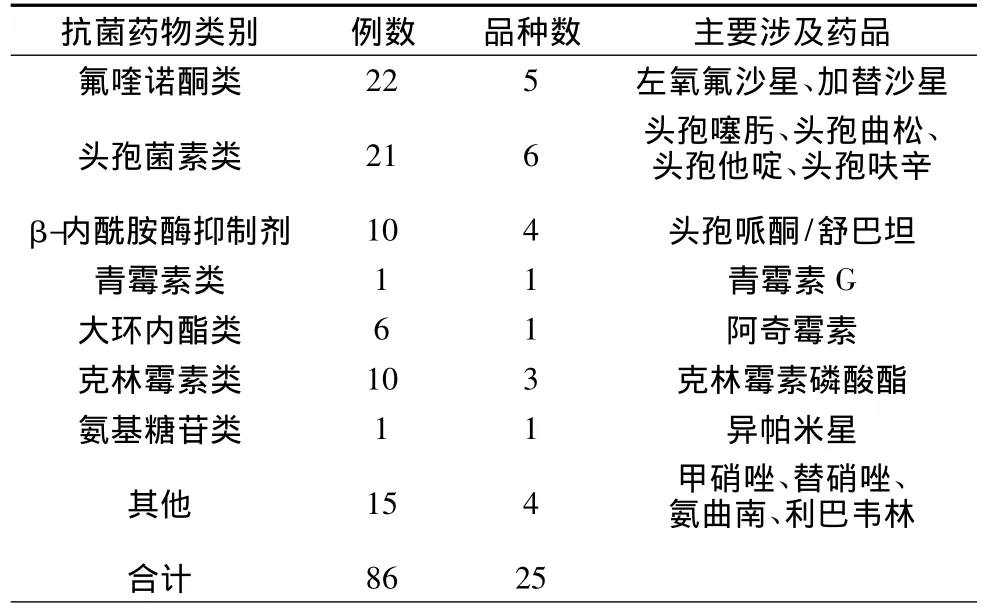
表3 ADR涉及的抗菌抗菌药物类别、品种及ADR例数(例,%)
2.6 ADR发生时间的分布 分析收集的ADR报表发现,用药后24 h之内ADR发生率最高,ADR发生时间的分布见表5。
2.7 ADR报表来源 106例ADR报表来源于医师的有33份(占31.13%),来源于护士的有60份(占56.60%),来源于药师的有13份(占12.27%)。上报科室以儿科、急诊科、妇产科、消化科较多。

表4 ADR涉及的器官或系统及主要临床表现(例,%)

表5 ADR发生时间的分布(例,%)
3 讨论
统计结果显示,ADR的发生率男女统计学差异无统计学意义。在年龄方面,19~60岁成人所占的比例居首位,这与该年龄段人群的免疫应答能力较强,使用药物频率过高有关;10岁以下婴幼儿患者占总例数的27.36%,提示婴幼儿患者是ADR的重要监测对象之一。婴幼儿由于各器官正在发育,功能尚未齐全,因此,婴幼儿用药,应当适当调整剂量,并加强用药监测。
从106例ADR报表人身份分布情况看,护士报告的占大多数,药师、医生报告的较少。这由于医务人员与患者接触密切,最易发现问题,医生日常工作十分繁忙,对上报ADR不够重视,好多事情都是让护士代劳,我院之前缺乏专职的临床药师,与临床接触的机会少,发现ADR的机会少有关。
由表2、表3可知,ADR涉及的药物以抗菌药物居多,这可能与抗菌药物种类多、应用范围广、用药频率高有关。此外,抗菌药物的合理应用存在一定问题,如无指征盲目使用、预防用药过长、医师用药起点偏高等也是导致ADR发生的重要因素。表3显示,氟喹诺酮类在抗菌药物品种及报告例数中均居首位,这与随着氟喹诺酮类大量使用,ADR发生率逐步提高的报告一致[2]。这与此类药具有抗菌谱广,杀菌力强有关。氟喹诺酮在临床上的广泛、大量使用,使得细菌对喹诺酮类药物的耐药成蔓延趋势,耐药细菌种类不断增多,耐药程度也趋于加重,故应尽量短期使用,不宜采取大剂量、长疗程使用。
ADR涉及的临床表现主要为皮肤及其附件的损害(占43.36%),其次是心血管系统、消化系统、神经系统等损害。大多数的ADR的程度较轻,危害较小,但个别较严重,如关节损伤、过敏性休克、急性播散性脑脊膜炎等,如救治不当则可对机体造成严重的或永久性的损伤,应引起足够的重视。建议医师使用药物前要详细询问患者的过敏史和家族史,加强用药过程的监测,以减少ADR的发生。
本次分析表明,静脉途径给药ADR的发生率最高,这是由于静脉给药起效快,而被临床广泛采用。但由于同时存在配伍、给药速度、热源反应等因素,使得ADR更容易发生。建议医师应根据患者的情况,合理选择给药途径,提高用药的安全性。
ADR监测工作不能给医院带来直接的经济利益,但这项工作是一项非常重要的事业,是医务工作者的义务和责任。应强化知识,不断提高我院ADR的数量和质量。
[1]何伟珍,吴丽兰,应小飞,等.浙江丽水市2004年501例药品不良反应报告分析.中国药房,2005,16(10):774.
[2]贺密会,周践,周筱青.1534例ADR报告分析.药物不良反应杂志,2004,6(3):189.
[3]胡广卉,尹玉雷.药品不良反应报告分析.中国医院用药评价与分析,2008,8(4):316.
