改良法白内障囊外摘除术的临床效果观察
2010-05-25马立威陆博刘冰阳张劲松
马立威,陆博,刘冰阳,张劲松
(1.中国医科大学 附属第四医院眼科中心,中国医科大学眼科医院 辽宁省晶状体学重点实验室,沈阳 110005;2.中国医科大学 第93期临床医学7年制,沈阳 110001)
随着我国医疗保险体制的日渐完善,农村合作医疗覆盖人口大幅度增加,越来越多的基层医院开始开展白内障复明手术。一方面,就近手术为广大参合患者提供方便;另一方面,较高的报销比例(50%~70%)大大减轻了患者的经济负担。但是由于技术水平及现有设备条件的限制,大多数县镇级医院的白内障手术仍停留在传统的大切口囊外摘除术阶段。虽然在现代化的大、中型医院里传统的大切口囊外摘除术已经很少应用,取而代之的是白内障超声乳化摘除术或是非超声乳化小切口白内障摘除术(非超小),但非超小术中的手法碎核对于术者手术手技要求较高,而超声乳化手术除了对手术手技有更高的要求外,还必须有一定的设备投入。因此直接开展这两种术式对于基础薄弱的基层医院眼科医生是有难度的。为了使基层手术医生提高技术水平、尽快与现代技术接轨,我们设计了一种改良的大切口白内障囊外摘除术式,即将隧道式自闭切口、连续环形撕囊(continuouscurvicular capsulorhexis,CCC)与水分离等现代超声乳化白内障摘除术中的关键技术应用于大切口囊外摘除手术[1~3]。通过这种术式,术者可以尽快完成技术过渡,实现技术转型,从而提高临床实践水平,造福于广大患者。以下是该技术在我院应用的临床报告。
1 资料与方法
1.1 一般资料
所有患者均为2005年6月至2006年10月中国医科大学附属第四医院眼科中心收治的年龄相关性白内障患者,共96例(128眼)。随机分为3组,其中传统白内障囊外摘除(extracapsular cataract extraction,ECCE)加人工晶状体植入术组28例(40眼)(ECCE组);改良组白内障囊外摘除加人工晶状体植入术组32例(42眼)(改良ECCE组);超声乳化白内障囊外摘除术加人工晶状体植入术组36例(46眼)(超乳组)。所有患者均为成熟期或过熟期皮质性白内障,或Emery-LittleⅤ级核性白内障。3组患者在年龄、性别、白内障类型等方面无统计学差异(表 1)。
1.2 手术方法

表1 3组患者的组间资料对比Tab.1 Comparison of the characteristics of patients in 3 groups
1.2.1 术前检查:全面眼部检查,包括视力、矫正视力、裂隙灯检查、非接触式眼压、角膜内皮细胞计数、A、B型超声检查、角膜地形图等。患者入组标准:角膜内皮细胞计数>1 000个/mm2,眼压<30 mmHg,排除其他眼病及全身病变。
1.2.2 手术方法:所有手术均由同一名经验丰富的白内障医生完成。
1.2.2.1 传统白内障囊外摘除加人工晶状体植入术:表面麻醉加结膜下麻醉后,沿角膜缘剪开上方球结膜,上方角膜处120°~180°垂直板层切口,穿刺后开罐式截囊,沿角膜缘扩大切口,挽核,双管针头冲洗皮质,植入一片式聚甲基丙烯酸甲酯(polymethyl methacrylate,PMMA)人工晶状体(直径 5.5 mm,OII,USA)于睫状沟,10-0尼龙线结节缝合切口4~5针,再次前房冲洗。妥布霉素地塞米松眼膏涂眼,术毕。
1.2.2.2 改良式白内障囊外摘除加人工晶状体植入术:表面麻醉加结膜下麻醉后,上方球结膜切开后电凝止血,于角膜缘后1.0 mm使用3.2 mm一次性钢刀制作直线型巩膜隧道切口,隧道深度1/2巩膜厚度,隧道长度2.0 mm,确保隧道内切口位于角膜缘内1.0 mm透明角膜处;前房内注入黏弹剂,用撕囊镊或自制截囊针行连续环形撕囊,前囊撕开窗直径为6~7 mm;再行水分离及水层分离,使晶状体皮质与囊膜分离、晶状体核与核上皮质分离并脱出于囊袋上;若晶状体核过大,不能自行脱出,则用调位钩旋转晶状体核使之脱出于囊袋外;核上及核下注入黏弹剂保护角膜内皮及后囊膜,扩大隧道切口至晶状体核直径大小,一般约5~6 mm;将晶状体圈套器伸入晶状体核下,将其娩出眼外;双管针头冲洗残留皮质,前房及囊袋内注入黏弹剂,植入一片式PMMA 人工晶状体(直径 5.5 mm,OII,USA)于囊袋内,10-0尼龙线结节缝合隧道切口1~2针,双管针头再次冲洗前房及囊袋内残留皮质及黏弹剂。妥布霉素地塞米松眼膏涂眼,术毕。
1.2.2.3 超声乳化白内障摘除加人工晶状体植入术:隧道切口制作、连续环形撕囊及水分离步骤同改良ECCE组,前囊撕开窗约5~6 mm。用超声乳化机(Infiniti ALCON)进行乳化碎核,参数设计为:连续超声模式下摆动振幅100%、超声能量15%,流量36 ml/min,负压 400 mmHg,灌注瓶高 90 cm。灌注/抽吸(I/A)手柄清除残留皮质后前房及囊袋内注入黏弹剂,扩大隧道切口至5.5 mm,植入一片式PMMA人工晶状体(直径 5.5 mm,OII,USA)于囊袋内,I/A 手柄再次冲洗前房及囊袋内残留皮质及黏弹剂,检查前房水密性,必要时缝合巩膜隧道切口一针。妥布霉素地塞米松眼膏涂眼,术毕。
1.2.3 观察指标:平均手术时间,指从制作结膜切口开始计时,到切口关闭、前房形成计时停止。术中并发症(后囊膜破裂)发生率,术后1个月时角膜内皮细胞计数及最佳矫正视力(BCVA),术后1年时的后发性白内障发生率。其中后发性白内障诊断标准为术后最佳矫正视力下降2行或以上(国际标准视力表),需行YAG激光后囊膜切开。
1.3 统计学方法
应用Shapiro-Wilk检验检查数据的正态分布,组间差异采用Kruskal-Walls检验及χ2检验(SPSS 11.0),P<0.05表示差异具有统计学意义。
2 结果
2.1 平均手术时间
传统ECCE组的平均手术时间为(15.0±6.32)min、改良 ECCE 组为(8.0±4.71)min、超乳组为(6.0±3.46)min,组间差异有统计学意义(P<0.01)。
2.2 术中并发症
晶状体后囊膜破裂在ECCE组有2例(2/40),玻璃体脱出,经前段玻切处理后其中1例人工晶状体放置在残留后囊膜上,1例人工晶状体经睫状沟缝合固定;改良ECCE组有1例(1/42),人工晶状体置于环形撕开的前囊膜上。超乳组有2例(2/46),破裂口较小1例经前段玻切处理后,人工晶状体仍能植入囊袋内。另1例因破裂口较大,有较大碎核块残留,扩大切口取出核块后将人工晶状体置于环形撕开的前囊膜上。
切口处后弹力层脱离在3组中均有发生,发生率无显著性差异,经前房内无菌空气泡顶压后均复位良好。
所有病例均未见其他术中并发症。
2.3 术后结果
患者分别于手术后1周、1个月、3个月、6个月及1年复诊。我们分别记录了手术后1个月时角膜内皮细胞计数、最佳矫正视力以及手术后1年时后发性白内障发生率(表2)。
手术后1年时ECCE组失访8人(12只眼),改良组失访13人(15只眼),超乳组失访10人(13只眼)。
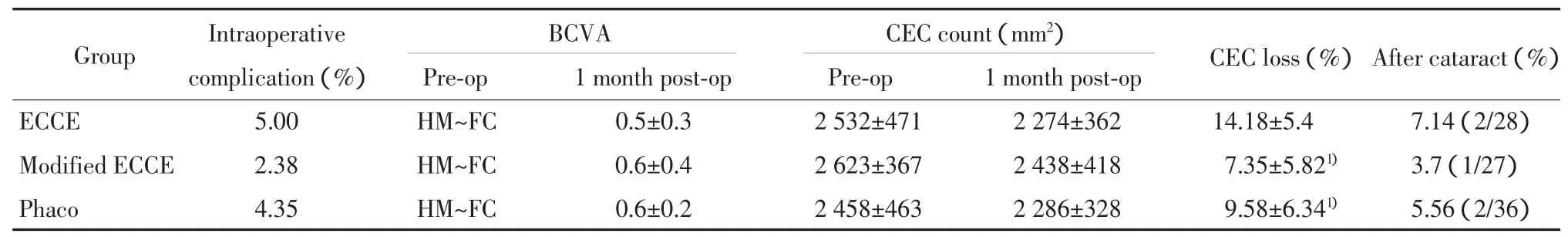
表2 3组患者手术结果比较Tab.2 Comparison of surgical outcomes of patients in 3 groups
3 讨论
白内障是第一位的治盲眼病,手术是目前唯一有效的治疗方法。我国积存的急需手术治疗的白内障致盲人口逾300万,每年新增病例40万,我国的白内障手术率(每百万人群中所做的白内障手术例数,cataract surgical rate,CSR)仅为 500,而发达国家为3 000~5 000。为改善我国的防盲治盲工作水平,亟需开展大规模的白内障复明手术[4~6]。虽然白内障超声乳化摘除及折叠式人工晶状体植入是目前白内障手术的金标准,但由于我国的地区经济及技术差异,很难在全国范围内普及。因此一段时期内大切口白内障囊外摘除加人工晶状体植入术将仍是我国白内障复明的主要手段。本研究中采用的改良的白内障囊外摘除术是在传统的大切口囊外摘除术的基础上应用了现代超声乳化手术的关键技术,即隧道式切口、连续环形撕囊及水分离。这种术式既保留了传统术式所需器械简单、手术费用少的优点,又实现了现代技术带来的安全与高效。
3.1 改良法白内障囊外摘除术的技术要点
(1)虽然切口仍为大切口,但其结构为隧道式。外切口应位于角膜缘后1 mm处的巩膜上,可为直线型或反眉弓型。内切口位于角膜缘内1 mm的透明角膜处,保证隧道长度至少为2 mm。内切口可根据晶状体核的大小适当扩大,大于外切口,即隧道可为矩形或梯形。这样的切口结构使晶状体核在挽出过程中由于隧道上下壁的挤压尽可能地去除核上皮质,只有最硬的核心部分通过外切口娩出。因此外切口通常只须5~6 mm即可。另外,由于内切口位于虹膜平面上方,避免传统术式中挽核及前房冲洗时常出现的虹膜脱出现象;而且手术结束时,外切口仅缝合1~2针即可保证前房的水密性。(2)前囊的撕开方式为连续环形撕开,直径应为6~8 mm,大于超声乳化手术中常用的5~6 mm左右。较大的前囊撕开窗便于晶状体核脱出于囊袋外。囊袋的相对完整,使囊袋内手术成为可能,减少术中角膜内皮及虹膜的损伤。并且提高了手术成功率,即便发生后囊膜破裂,人工晶状体仍可在保留的环形前囊膜上很好的固定。(3)水分离及水层分离务必完全彻底,使囊膜与晶状体皮质、晶状体皮质与晶状体核之间充分分离,使晶状体核可以通过较小的切口挽出,晶状体皮质的清除更彻底、更容易,减少后发性白内障的发生。另外水分离时要注意向下压切口下唇,保证隧道而切口开放,防止眼压急剧升高以致后囊膜破裂。一些术者建议不做水分离,通过手法旋转使晶状体核脱出囊袋[5]。笔者认为成熟期的白内障多合并囊膜及晶状体悬韧带的变性,机械旋转大而硬的晶状体核增加了囊袋和悬韧带破坏的风险,而水分离产生的力量比较均匀,比较适合初学者掌握。当然水分离必须在连续环形撕囊顺利完成的条件下进行。
3.2 改良法白内障囊外摘除术的临床效果
本组病例中,与传统白内障囊外摘除手术比较,改良术式组的平均手术时间、术中并发症、术后1月时角膜内皮细胞丢失率及1年时的后发性白内障发生率均较低。手术时间缩短主要在于减少了切口的缝合以及残留皮质清除比较容易。传统术式的垂直全层切口缝合需要4~5针,而改良术式的隧道切口仅需1~2针即可,有的报告甚至不进行切口缝合[2]。因此大大的缩短了手术时间,熟练的术者所需时间与超乳手术相差无几[6]。残留皮质清除在传统术式中受到开罐式截囊产生的不规则前囊膜片影响比较费时,而改良术式中由于采用了环形撕囊及水分离,前囊膜边缘光滑整齐、皮质与囊膜分离完全,所以残留皮质清除起来比较容易、彻底,这可能也是改良术式组后发性白内障发生率低的原因之一。传统术式中要靠障匙在角膜外下方挤压使晶状体核抬头后由张开的角膜缘切口挽出晶状体核,在此过程中眼压波动明显,若患者配合度差或后房压力高则容易出现后囊膜破裂,同时由于晶体核直接与角膜内皮摩擦,因此角膜内皮损伤也较重。而改良术式中,通过水分离及旋转晶状体核使之脱出于囊袋外,再用圈套器托住晶状体核将其由隧道切口挽出,整个过程中眼球处于相对密闭状态,眼压波动不大,后囊膜破裂发生的几率较小,且晶体核仅通过隧道切口娩出眼外,未与角膜内皮直接接触,因此角膜内皮的损伤较轻[2,7,8]。本组病例的结果也证实了这一点。与超声乳化白内障囊外摘除手术比较,改良术式组的平均手术时间略长、但术中并发症、及1年时的后发性白内障发生率均接近或较低。在植入硬性人工晶状体的情况下,二者手术效果差别无几。这些结果与其他文献报道相近[6~10]。在3组患者中均有数例出现切口附近后弹力膜脱离,可能与手术器械反复进出切口造成机械损伤有关,在冲洗皮质时仔细观察可以及时发现。本研究中的8例患者经前房无菌空气泡顶压后均复位良好,未造成不良后果。
总之,与传统的大切口白内障囊外摘除术相比,改良术式具有手术时间短、术中、术后并发症少的优点。我科多年来承担各级别的白内障手术培训班,特别自2007年以来开始承担农村适宜技术的推广、教学工作。基层医院的手术医生只要具有囊外摘除手术经验,经过培训期间的动物眼实习及30~50例白内障手术的实践操作,均比较顺利地掌握了隧道切口、环形撕囊及水分离技术,在未增加设备及特殊手术器械的情况下,大大地提高了他们的临床实践水平。熟练掌握隧道切口、环形撕囊及水分离这些关键技术后,术者可以进一步尝试小切口非超声乳化白内障摘除术。对于已熟练掌握超乳手术的医生,改良法白内障囊外摘除术也是有其实用价值的。例如,患者年龄较大的黑核白内障或过熟期的皮质性白内障,由于晶状体悬韧带松弛、囊膜变性、角膜内皮细胞功能不良等原因,超声乳化手术容易出现并发症,这时改良的囊外摘除术就是不错的选择,在降低手术风险的同时实现恢复视力的目的。
[1]Müller-Jensen K,Barlinn B,Zimmerman H.Astigmatism reduction:no-stitch 4.0 mm versus sutured 12.0 mm clear corneal incisions[J].JCataract Refract Surg,1996,22(8):1108-1112.
[2]Hennig A,Kumar J,Yorston D,et al.Suturelesscataract surgery with nucleusextraction:outcomeof aprospectivestudy in Nepal[J].Br J Ophthalmol,2003,87(3):266-270.
[3]Gogate PM,Wormald RP,Deshpande M,et al.Extracapsular cataract surgery compared with manual small incision cataract surgery in community eye care setting in Western India:A randomized controlled trial[J].Br JOphthalmol,2003,87(6):667-672.
[4]Li Z,Cui H,Liu P,et al.Prevalenceand causesof blindnessand visual impairment among the elderly in ruralsouthern Harbin,China[J].Ophthalmic Epidemiol,2008,15(5):334-338.
[5]Gogate M.Small incision cataract surgery:Complications and minireview[J].Indian JOphthalmol,2009,57(1):45-49.
[6]Gogate PM,Deshpande MD,Nirmalan P.Why do phacoemulsification?Manual small incision cataract surgery isalmost aseffectiveand moreeconomical[J].Ophthalmology,2007,114(5):965-968.
[7]George R,Rupauliha P,Sripriya AV,et al.Comparison of endothelial cell loss and surgically induced astigmatism following conventional extracapsular cataract surgery,manual small-incision surgery and phacoemulsification[J].Ophthalmic Epidemiol,2005,12(5):293-297.
[8]Walkow T,Anders N,Klebe S.Endothelial cell loss after phacoemulsification:relation to preoperative and intraoperative parameters[J].JCataract Refract Surg,2000,26(5):727-732.
[9]Gogate PM,Kulkarni SR,Krishnaiah S,et al.Safety and efficacy of phacoemulsification compared with manual small incision cataract surgery by a randomized controlled clinical trial:Six weeks results[J].Ophthalmology,2005,112(5):869-874.
[10]Venkatesh R,Muralikrishnan R,Balent LC,et al.Outcomes of high volumecataract surgeriesin adevelopingcountry[J].Br JOphthalmol,2005,89(9):1079-1083.
