地榆升白片对非小细胞肺癌化疗患者骨髓抑制、细胞因子的影响
2025-02-07林学英周凯董陶明



【摘要】 目的:探讨地榆升白片对非小细胞肺癌(NSCLC)化疗患者骨髓抑制及细胞因子的影响。方法:回顾性选取2022年11月—2023年11月在景德镇市第二人民医院就诊的82例NSCLC化疗患者的临床资料,根据治疗方法分为对照组(n=48)和治疗组(n=34)。对照组采用TP方案化疗,治疗组采用TP方案+地榆升白片治疗。比较两组疗效,治疗前后骨髓抑制[血小板计数(PLT)、白细胞计数(WBC)及血红蛋白(Hb)]、细胞因子[肿瘤坏死因子-α(TNF-α)、白细胞介素-6(IL-6)及C反应蛋白(CRP)],治疗后骨髓抑制程度,以及治疗期间安全性情况。结果:两组治疗总有效率比较,差异无统计学意义(字2=0.088,P=0.767);治疗后,两组PLT、WBC及Hb水平均下降,与对照组比较,治疗组均高(Plt;0.05);治疗后,两组TNF-α、IL-6及CRP水平均下降,与对照组比较,治疗组均低(Plt;0.05);与对照组比较,治疗组骨髓抑制程度轻(Plt;0.05);两组副作用发生率比较,差异无统计学意义(Pgt;0.05)。结论:地榆升白片治疗NSCLC化疗患者,可以调节骨髓抑制,减轻炎症反应和骨髓抑制程度,且安全性好。
【关键词】 地榆升白片 非小细胞肺癌 化疗 骨髓抑制 细胞因子
Effects of Diyu Shengbai Tablets on Bone Marrow Suppression and Cytokin in Patients with Non-small Cell Lung Cancer Undergoing Chemotherapy/LIN Xueying, ZHOU Kai, DONG Taoming. //Medical Innovation of China, 2025, 22(02): 0-103
[Abstract] Objective: To explore the effects of Diyu Shengbai Tablets on bone marrow suppression and cytokin in patients with non-small cell lung cancer (NSCLC) undergoing chemotherapy. Method: Clinical data of 82 patients with NSCLC treated with chemotherapy in the Second People's Hospital of Jingdezhen from November 2022 to November 2023 were retrospectively selected, and divided into control group (n=48) and treatment group (n=34) according to treatment methods. The control group was treated with TP regimen chemotherapy, and the treatment group was treated with TP regimen + Diyu Shengbai Tablets. The efficacy, peripheral blood indexes [platelet count (PLT), white blood cell count (WBC) and hemoglobin (Hb)] and cytokin [tumor necrosis factor-α (TNF-α), interleukin-6 (IL-6) and C reactive protein (CRP)] before and after treatment, the degree of bone marrow suppression after treatment, and safety during treatment were compared between the two groups. Result: There was no significant difference in total effective rate between the two groups (字2=0.088, P=0.767). After treatment, the levels of PLT, WBC and Hb in both groups were decreased, which were higher in the treatment group than those in the control group (Plt;0.05). After treatment, the levels of TNF-α, IL-6 and CRP in both groups were decreased, which were lower in treatment group than those in control group (Plt;0.05). Compared with the control group, the degree of bone marrow suppression in the treatment group was lighter (Plt;0.05). There was no significant difference in the incidence of side effect between the two groups (Pgt;0.05). Conclusion: Diyu Shengbai Tablets in the treatment of patients with NSCLC can regulate peripheral blood indexes, reduce inflammatory reaction and bone marrow suppression, and it is safe.
[Key words] Diyu Shengbai Tablets Non-small cell lung cancer Chemotherapy Bone marrow suppression Cytokin
First-author's address: Department of Oncology, the Second People's Hospital of Jingdezhen, Jingdezhen 333000, China
doi:10.3969/j.issn.1674-4985.2025.02.023
肺癌(LC)属于全球性恶性肿瘤,发病率和病死率均较高,其中,约有80%的LC为非小细胞肺癌(NSCLC)[1]。早期NSCLC临床症状不明显,患者在确诊时往往已处于中晚期,失去了手术根治的最佳时机[2-3]。临床治疗NSCLC以延长生存期为主,主要通过含铂化疗方案治疗,但是该方法在清除肿瘤细胞的同时也会带来不良反应,其中,最常见和最严重的为骨髓抑制,导致白细胞水平降低,患者出现精神倦怠、睡眠障碍、食欲不振等症状,还易增加感染风险[4-5]。临床常用重组人粒细胞集落刺激因子(rhG-CSF)来缓解骨髓抑制,效果确切,但也会引起肌肉酸痛等不适症状[6]。地榆升白片为中药制剂,含有多种有效成分,在恢复癌症患者白细胞水平方面具有较好作用[7]。本研究探讨地榆升白片在NSCLC化疗患者中的应用效果,旨在为NSCLC化疗患者的治疗提供参考。
1 资料与方法
1.1 一般资料
回顾性选取2022年11月—2023年11月于景德镇市第二人民医院就诊的82例NSCLC化疗患者。纳入标准:(1)符合NSCLC诊断标准[8],且经病理学检查确诊;(2)年龄18~75周岁;(3)临床分期Ⅲ、Ⅳ期;(4)行化疗。排除标准:(1)精神疾病;(2)造血、凝血、免疫系统疾病;(3)心、肝、肾功能不全;(4)放化疗史;(5)入院前3周服用治疗骨髓抑制药物;(6)合并其他恶性肿瘤;(7)感染性疾病。根据治疗方法不同将患者分为对照组(n=48)和治疗组(n=34)。本研究已经本院医学伦理委员会批准。
1.2 方法
(1)对照组:采用TP方案化疗。21 d为1个周期,于第1天静脉滴注紫杉醇(生产厂家:江苏九旭药业有限公司,批注文号:国药准字H20067715,规格:5 mL︰30 mg)135 mg/m2,第1~3天静脉滴注顺铂(生产厂家:南京制药厂有限公司,批注文号:国药准字H20030675,规格:20 mL︰20 mg)25 mg/m2,共治疗4个周期。(2)治疗组:在TP方案基础上口服地榆升白片(生产厂家:成都地奥集团天府药业股份有限公司,批注文号:国药准字Z20026497,规格:每片重0.1 g),3次/d,3片/次,21 d为1个周期,治疗4个周期。
1.3 观察指标及判定标准
(1)于治疗后评估疗效,完全缓解:肿瘤病灶全部清除,且持续≥4周;部分缓解:病灶直径之和缩小≥30%,且持续≥4周;疾病稳定:病灶直径之和缩小lt;30%或增加≤20%;疾病进展:发现新病灶,或病灶直径之和增加gt;20%[9]。总有效率=(完全缓解+部分缓解)例数/总例数×100%。(2)于治疗前后采集患者肘静脉血,血小板计数(PLT)、白细胞计数(WBC)及血红蛋白(Hb)均使用全自动血液细胞分析仪(Beckman Coulter,Inc.)测定。(3)于治疗前后采集患者肘静脉血,分离血清,肿瘤坏死因子-α(TNF-α)、白细胞介素-6(IL-6)及C反应蛋白(CRP)均通过酶联免疫吸附试验测定。(4)于治疗后评估患者的骨髓抑制程度,0级:PLT≥100×109/L,WBC≥4.0×109/L,Hb≥110 g/L;Ⅰ级:PLT(75~99)×109/L,WBC(3.0~3.9)×109/L,Hb(95~109)g/L;Ⅱ级:PLT(50~74)×109/L,WBC(2.0~2.9)×109/L,Hb(80~94)g/L;Ⅲ级:PLT(25~49)×109/L,WBC(1.0~1.9)×109/L,Hb(65~79)g/L;Ⅳ级:PLTlt;25×109/L,WBClt;1.0×109/L,Hblt;65 g/L[10]。(5)安全性分析。记录治疗期间肌肉酸痛、乏力、胸闷等副作用发生情况。
1.4 统计学处理
使用SPSS 24.0统计软件处理数据。计量资料以(x±s)表示,组间比较进行独立样本t检验,组内比较进行配对t检验;计数资料以率(%)表示,进行字2检验。Plt;0.05表示差异有统计学意义。
2 结果
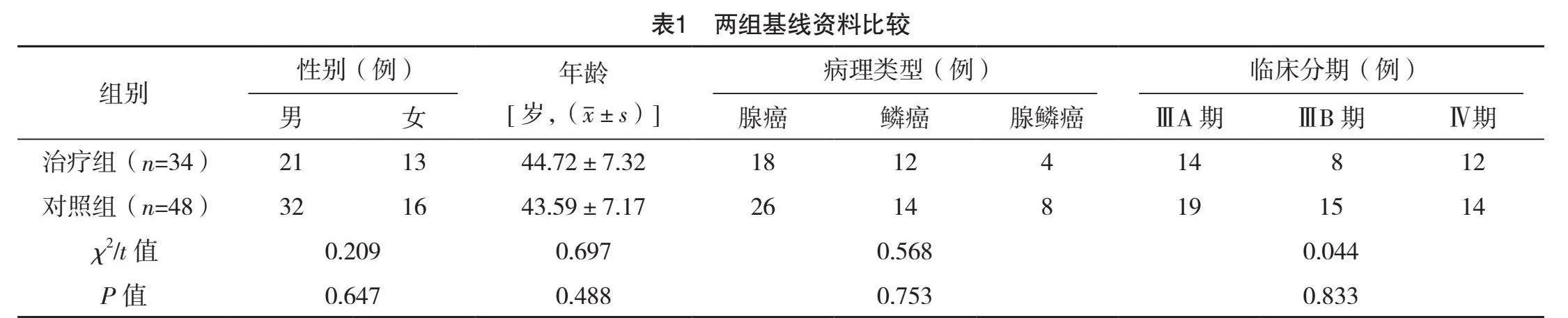
2.1 两组基线资料比较
两组患者的基线资料比较,差异均无统计学意义(Pgt;0.05),具有可比性,见表1。
2.2 两组治疗效果比较
两组治疗总有效率比较,差异无统计学意义(字2=0.088,P=0.767),见表2。
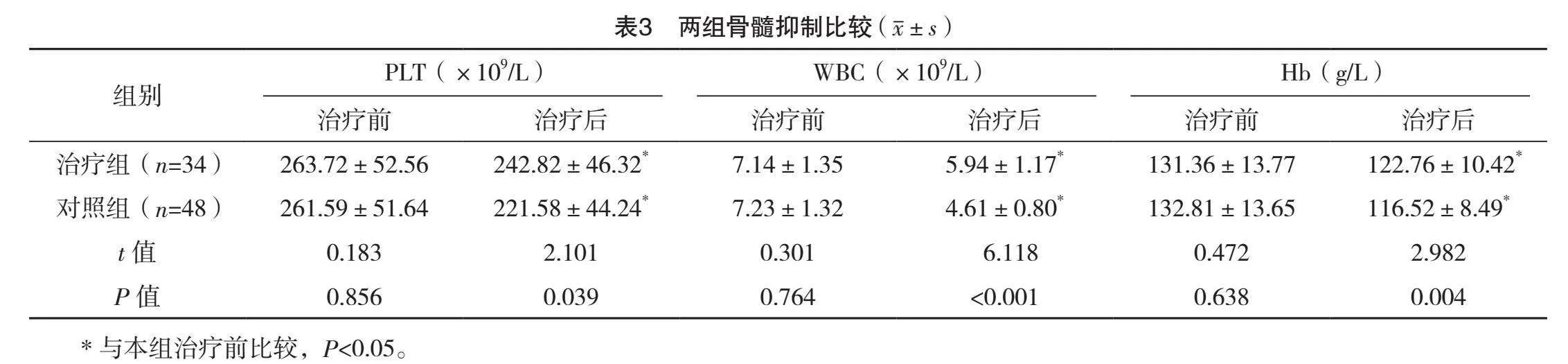
2.3 两组骨髓抑制比较
治疗前,两组PLT、WBC及Hb水平比较,差异均无统计学意义(Pgt;0.05);治疗后,两组PLT、WBC及Hb水平均下降,与对照组比较,治疗组以上指标均高(Plt;0.05)。见表3。
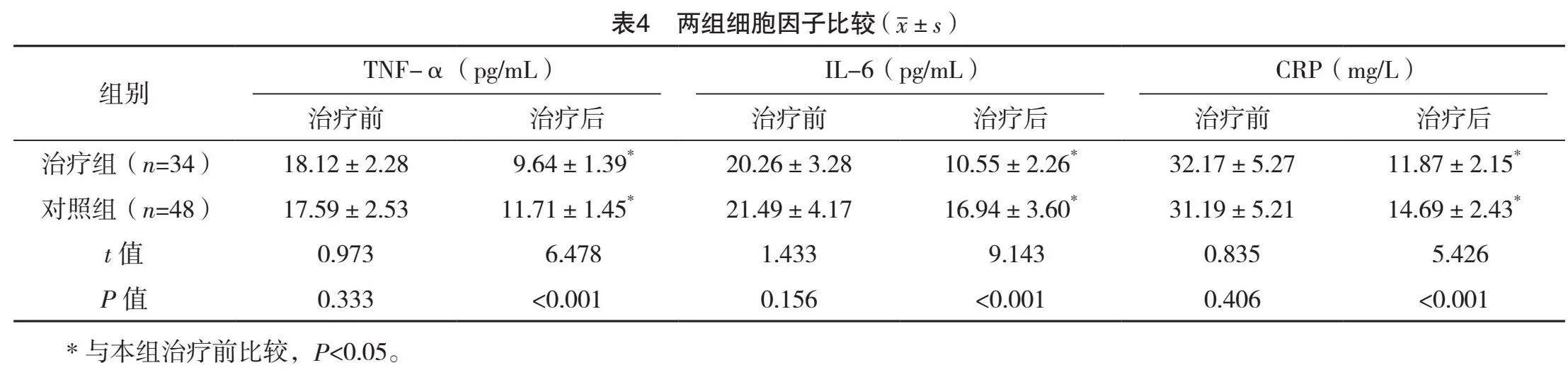
2.4 两组细胞因子比较
治疗前,两组TNF-α、IL-6及CRP水平比较,差异均无统计学意义(Pgt;0.05);治疗后,两组TNF-α、IL-6及CRP水平均下降,与对照组比较,治疗组以上指标均低(Plt;0.05)。见表4。
2.5 两组骨髓抑制程度比较
与对照组比较,治疗组骨髓抑制程度轻(Z=3.971,P=0.046),见表5。
2.6 两组副作用比较
两组副作用发生率比较,差异无统计学意义(字2=1.640,P=0.200),见表6。
3 讨论
大部分NSCLC患者确诊时已为中晚期,错过了最佳手术治疗时机。伴随临床对LC研究的加深,靶向治疗和免疫治疗等精准治疗应用于临床,但是,由于需要进行基因检测,加上患者本身高龄、基础疾病等原因,难以大量应用[11-13]。中晚期NSCLC的治疗仍以化疗为主,其中,TP化疗方案应用较多,但是该方案在保持对肿瘤细胞杀伤力的同时,也会不分敌我,会对骨髓干细胞等正常细胞产生毒副作用,影响患者化疗依从性[14-16]。中医理论指出,化疗药物属于邪毒,会损伤脾肾,而脾可以生化气血,肾主骨生髓,化疗的毒副作用会导致脾肾亏虚,因此,治疗以健脾益肾为治疗原则[17-18]。
地榆升白片为健脾补肾良药,在治疗乳腺癌、胃癌、子宫颈癌等癌症化疗患者中具有较好的拮抗骨髓抑制效果[19]。本研究发现,两组总有效率比较差异无统计学意义,提示地榆升白片治疗并不会显著改善临床效果。分析认为,地榆升白片活性成分地榆皂苷Ⅱ可以作用于细胞凋亡通路,促进肿瘤细胞凋亡,另一种成分鞣花酸,具有抗菌、降压、抗氧化等多种生理作用,同时还可以抑制肿瘤血管生成,延缓肿瘤生长和扩散,发挥抗肿瘤作用[20-21]。地榆升白片可能会在一定程度上增加患者化疗获益效果,但对NSCLC患者而言,发挥主要作用的仍然是化疗方案本身,且地榆升白片增加化疗获益主要是通过提高患者化疗耐受性实现,故在疗效方面,治疗组稍高,但无显著差异。本研究发现,治疗后,与对照组比较,治疗组TNF-α、IL-6及CRP水平均低,提示地榆升白片可以缓解炎症反应,这可能是由于地榆升白片中的黄酮类成分可以激活巨噬细胞等免疫细胞功能,发挥抗炎作用。本研究中,治疗后,与对照组比较,治疗组PLT、WBC及Hb水平均高,且骨髓抑制程度轻,说明地榆升白片治疗可以减轻骨髓抑制紊乱和骨髓抑制程度。地榆升白片可以诱导造血干细胞增殖分化,增加PLT、WBC及Hb等细胞数量,改善骨髓微循环,而且,该药物含有的地榆皂苷成分,可以促进骨髓粒单系祖细胞增殖,从而有效抑制骨髓抑制[22-23]。治疗期间,两组副作用发生率比较,差异无统计学意义,提示地榆升白片不会增加药物副作用,安全性好。
综上所述,对于NSCLC化疗患者,增用地榆升白片能够调节骨髓抑制,缓解炎症反应,减轻骨髓抑制程度,且安全性好。
参考文献
[1] ZHUANG Q Y,HUANG Y J,HONG Y P,et al.Vinpocetine enhances cisplatin sensitivity of non-small cell lung cancer cells by reducing the nuclear factor erythroid 2-related factor 2 signaling[J].J Investig Med,2022,70(6):1358-1364.
[2] KLARENBEEK S E,AARTS M J,VAN DEN HEUVEL M M,et al.Impact of time-to-treatment on survival for advanced non-small cell lung cancer patients in the Netherlands:a nationwide observational cohort study[J].Thorax,2023,78(5):467-475.
[3] CHENG Y,CHEN Z Y,HUANG J J,et al.Efficacy evaluation of neoadjuvant immunotherapy plus chemotherapy for non-small-cell lung cancer:comparison of PET/CT with postoperative pathology[J].Eur Radiol,2023,33(10):6625-6635.
[4] LOMBARD A,MISTRY H,AARONS L,et al.Dose individualisation in oncology using chemotherapy-induced neutropenia:example of Docetaxel in non-small cell lung cancer patients[J].Br J Clin Pharmacol,2021,87(4):2053-2063.
[5] LEE C K,NOVELLO S,RYDÉN A,et al.Patient-reported symptoms and impact of treatment with Osimertinib versus chemotherapy in advanced non-small-cell lung cancer:the AURA3 trial[J].J Clin Oncol,2018,36(18):1853-1860.
[6] DÓMINE GÓMEZ M,CSŐSZI T,JAAL J,et al.Exploratory composite endpoint demonstrates benefit of Trilaciclib across multiple clinically meaningful components of myeloprotection in patients with small cell lung cancer[J].Int J Cancer,2021,149(7):1463-1472.
[7]张熙祎.地榆升白片治疗白细胞减少疗效观察及体会[J].陕西中医,2016,37(4):470.
[8]中华医学会肿瘤学分会,中华医学会杂志社.中华医学会肿瘤学分会肺癌临床诊疗指南(2021版)[J].中华肿瘤杂志,2021,43(6):591-621.
[9] EISENHAUER E A,THERASSE P,BOGAERTS J,et al.New response evaluation criteria in solid tumours:revised RECIST guideline(version 1.1)[J].Eur J Cancer,2009,45(2):228-247.
[10]祝亚男,汪永坚,陈晓洁,等.足三里穴位注射地塞米松在提高乳腺癌化疗耐受性中的应用效果[J].中华现代护理杂志,2014,20(2):158-161.
[11] BORGHAEI H,LANGER C J,PAZ-ARES L,et al.
Pembrolizumab plus chemotherapy versus chemotherapy alone in patients with advanced non-small cell lung cancer without tumor PD-L1 expression:a pooled analysis of 3 randomized controlled trials[J].Cancer,2020,126(22):4867-4877.
[12] HOU H L,WANG Y J,SUN D T,et al.Neoadjuvant Toripalimab plus Platinum-paclitaxel chemotherapy in stage Ⅱ-Ⅲ non-small cell lung cancer:a single-center, single-arm,phase Ⅰ study in China[J].Invest New Drugs,2023,41(1):86-92.
[13] GARGIULO P,ARENARE L,GRIDELLI C,et al.
Chemotherapy-induced neutropenia and treatment efficacy in advanced non-small-cell lung cancer:a pooled analysis of 6 randomized trials[J].BMC Cancer,2021,21(1):549.
[14] LU S,FANG J,WANG Z P,et al.Results from the IMpower132 China cohort:Atezolizumab plus platinum-based chemotherapy in advanced non-small cell lung cancer[J].Cancer Med,2023,12(3):2666-2676.
[15] BENJAMIN D J,CHEN S,ELDREDGE J B,et al.The role of chemotherapy plus immune checkpoint inhibitors in oncogenic-driven NSCLC:a university of California lung cancer consortium retrospective study[J].JTO Clin Res Rep,2022,3(12):100427.
[16] XU Z Y,LI T,HU X S,et al.Efficacy and safety profile of combining programmed cell death-1 (PD-1) inhibitors and antiangiogenic targeting agents as subsequent therapy for advanced or metastatic non-small cell lung cancer(NSCLC)[J].Thorac Cancer,2021,12(17):2360-2368.
[17]陈姣红,古红莉,员建中,等.参术扶正抗癌汤联合化疗及三维适形放疗对晚期非小细胞肺癌患者血清T细胞亚群水平及生存质量的影响[J].陕西中医,2019,40(5):564-567.
[18]向薇,谢雨洮,张惠.益气升白汤治疗非小细胞肺癌化疗后白细胞减少症的临床疗效[J].现代肿瘤医学,2019,27(12):2117-2121.
[19]张敏,帅晋豪.地榆升白片联合聚乙二醇化重组人粒细胞刺激因子治疗乳腺癌化疗后粒细胞减少价值研究[J].中华中医药学刊,2019,37(5):1201-1204.
[20]邓波,易峰涛,谢俊杰,等.地榆升白片对宫颈癌患者辅助放疗期间免疫功能的影响[J].医药导报,2018,37(2):193-195.
[21]杜子伟,戎成婷,侯环,等.地榆升白片同步化疗对胃癌患者增效减毒效果及免疫机制调节作用的研究[J].广州中医药大学学报,2022,39(6):1241-1247.
[22] ZHONG W Z,CHEN K N,CHEN C,et al.Erlotinib versus Gemcitabine plus Cisplatin as neoadjuvant treatment of stage ⅢA-N2 EGFR-mutant non-small-cell lung cancer (EMERGING-CTONG 1103):a randomized phase Ⅱ study[J].
J Clin Oncol,2019,37(25):2235-2245.
[23] LI M,CHEN R,JI B Y,et al.Role of ERCC5 polymorphisms in non-small cell lung cancer risk and responsiveness/toxicity to Cisplatin-based chemotherapy in the Chinese population[J].Oncol Rep,2021,45(3):1295-1305.
(收稿日期:2024-05-20) (本文编辑:陈韵)
