QuEChERS结合高效液相色谱串联质谱法检测猪肉中16种兽药残留量
2024-12-11陈楠楠陈秀明詹清揭小玲周阿容方东升




摘要:建立了一种QuEChERS前处理与高效液相色谱串联质谱法(HPLC-MS/MS)相结合同时检测猪肉中16种兽药残留的方法。样品采用水-0.1%甲酸乙腈经QuEChERS技术提取和净化后,在正离子多反应监测模式(multiple reaction monitoring,MRM)下进行分析测定。结果表明:16种兽药在2.0~100.0μg·kg¹的范围内有良好的线性关系(相关系数r>0.9970);检出限(LOD,S/N=3)和定量限(LOQ,S/N=10)的范围分别为0.01~0.25μg·kg¹、0.03~0.82μg kg-¹;在猪肉样品中进行了2、4、20μg-kg¹3个不同浓度水平的加标试验,相对标准偏差RSD为1.1%~9.0%,加标回收率在70.4%~118.1%。该方法的重复性和回收率满足试验要求,灵敏度高,适用于猪肉中多种类兽药残留的分析检测。
关键词:兽药残留;猪肉;高效液相色谱-串联质谱(HPLC-MS/MS);QuEChERS
中图分类号:S859.84文献标志码:A文章编号:0253-2301(2024)09-0051-08
DOI:10.13651/j.cnki.fjnykj.2024.09.009
Determination of 16 Kinds of Veterinary Drug Residues in Pork by QuEChERS Coupled with HPLC-MS/MS
CHEN Nan-nan,CHEN Xiu-ming,ZHANQing,JIE Xiao-ling,ZHOU A-rong,FANG Dong-sheng*
(Fujian Institute of Microbiology,Fuzhou,Fujian 350007,China)
Abstract:A method for the simultaneous determination of 16 veterinary drug residues in pork by using QuEChERS pretreatment combined withhigh performance liquid chromatography-tandem mass spectrometry(HPLC-MS/MS)was established.The samples were extracted and purified by using the QuEChERS technology with water-0.1%formic acid acetonitrile,and then analyzed and determined in the positive ion multiple reaction monitoring(MRM)model.The results showed that:there was a good linear relationship among the 16 veterinary drugs in the range of 2.0-100.0μg-kg¹(the correlation coefficient r>0.9970).The limits of determination(LOD,S/N=3)and limits of quantitation(LOQ,S/N=10)ranged from 0.01 to 0.25μg-kg¹and from 0.03 to 0.82μg-kg¹,respectively.The spiked experiments at three different concentration levels of 2,4 and 20μg-kg¹were carried out in the pork samples.The relative standard deviation(RSD)ranged from 1.1%to 9.0%,and the recovery rate ranged from 70.4%to 118.1%.The repeatability and recovery rate of the method met the test requirements,and the sensitivity was high,which was suitable for the analysis and detection ofvarious veterinary drug residues in pork.
Key words:Veterinary drug residues;Pork;High performance liquid chromatography-tandem mass spectrometry(HPLC-MS/MS);QuEChERS
作为世界上主要的猪肉生产和消费国,兽药在畜牧业中扮演着至关重要的角色,在预防动物疫病,确保食品产量方面发挥着关键作用。然而,部分养殖户为了经济利益,可能会滥用兽药或不遵守用药规范,造成猪肉中兽药残留超过规定限度,从而引起食品安全的问题1-2]。如果人们长期摄入这些兽残超标的动物源性食品,体内药物的累积可能会诱发毒性反应,危害健康3。因此,确保市售猪肉符合质量和安全标准,加强对猪肉中兽药残留的检测和研究显得尤为关键。现行国家标准GB 31650-2019《食品中兽药最大残留限量》[4和GB 31650.1-2022《食品中41种兽药最大残留限量》5等标准和法规已经为肉类、蛋类、乳制品等动物源食品的兽药残留量设定了明确的限制标准。为了保护消费者的健康和确保动物源食品的质量安全,开发出快捷、高效且能同时准确检测多种兽药残留的分析方法具有重要意义。
动物源食品由于其基质的复杂性,潜在干扰物多,这给兽药残留的检测带来了挑战。由于兽药残留在样品中含量很低,仪器的高选择性和高灵敏度成为了推动兽药残留检测技术发展的关键因素。高效液相色谱串联质谱技术(HPLC-MS/MS)结合了液相色谱的高效分离能力和质谱检测器的高灵敏度与选择性的优点,使其成为兽药残留检测的首选方法[6-9]。现行国家标准GB 31658.17-2021《动物性食品中四环素类,磺胺类和喹诺酮类药物残留量的测定液相色谱-串联质谱法》[10已提供一种用于检测猪肉中36种兽药残留的检测分析方法。然而,该标准中的样品前处理过程较为繁琐,处理效率不高,溶剂使用量大,成本也相对较高,无法很好地满足兽药残留快速检测的需求。因此,开发更为高效的样品前处理方法成为了当前兽药残留分析领域的重点。
QuEChERS技术是通过提取剂、吸水剂和净化剂对样品进行前处理。常用的净化剂包括N-丙基乙二胺(PSA)、C18和GCB,能够有效吸附并去除大部分杂质,达到净化样品的目的。QuEChERS技术因其高效省时、操作便捷、成本低、稳定性强和安全性佳等优势[1,在兽药残留分析领域被广泛应用[¹²-15]。因此,本研究采用QuEChERS前处理结合LC-MS/MS技术,对前处理条件、色谱、质谱条件等参数进行优化,构建了简单高效且具有高灵敏度的检测方法,能够同时检测猪肉中常见的16种残留兽药(包括磺胺类、喹诺酮类、大环内酯类等),以期为今后兽药残留检测提供借鉴。
1材料与方法
1.1供试材料
供试样品猪肉为市售产品。
1.2仪器和试剂
1.2.1主要试剂甲醇、乙腈均为色谱纯试剂(德国Merck公司);无水乙醇为分析纯试剂(西陇科学股份有限公司);甲酸为色谱纯试剂(德国CNW公司);PSA粉、C18粉、无水硫酸镁购自月旭科技(上海)股份有限公司;氯化钠、无水硫酸钠等其他试剂均为分析纯;陶瓷均质子(长2 cm×直径1 cm);尼龙微孔滤膜(13 mm,0.22μm);试验所用超纯水为Milli-Q超纯水仪制备。
标准品磺胺甲恶唑、磺胺甲基嘧啶、磺胺二甲基嘧啶、磺胺喹恶啉、磺胺嘧啶、磺胺氯哒嗪、盐酸林可霉素(一水物)均购自德国Dr.Ehrenstorfer公司;标准品磺胺间甲氧嘧啶、罗红霉素、替米考星、盐酸金刚乙胺、左旋咪唑、甲氧氯普胺、洛美沙星、氧氟沙星、沙拉沙星均购自北京坛墨质检科技有限公司。
1.2.2仪器与设备Agilent 6470三重四极杆质谱仪(Agilent公司);KQ-5200DE数控型超声仪(昆山市超声仪器有限公司);绞肉机(美的);超纯水仪Milli-Q(Millipore公司);XSE105分析天平(Mettler Toledo公司);BC-1000数显型多管式旋涡振荡仪(深圳逗点生物技术有限公司);Eppendorf 5810R冷冻离心机(Eppendorf公司);HSC-4B水浴氮吹仪(天津市恒奥科技发展有限公司)。
1.3试验方法
1.3.1样品前处理取猪肉适量,经绞肉机绞碎后,准确称量5.00 g的样品放入50 mL的离心管内,随后添加3.0 mL的超纯水和陶瓷均质子,通过涡旋混合1 min以确保肉质均匀分散。再加入20.0 mL含0.1%(v/v)甲酸的乙腈溶液,盖紧瓶盖充分振摇1 min,涡旋振荡提取5 min,使样品充分分散,再加入4.0 g硫酸钠和1.0 g氯化钠,涡旋5 min后,在低温下以5500 r min¹转速离心10min。将上清液转移到1个装有50 mg PSA粉末、200 mg C18粉末、1.0 g无水硫酸钠的15 mL塑料离心管中,涡旋振荡2 min,以6000 r·min¹的转速离心10 min。定量移取5mL净化后的上清液,于40℃下氮吹至干,然后加入1.0 mL的25%乙腈/水(体积比1:3)溶液溶解后再加入1.0 mL乙腈饱和的正已烷,涡旋混匀,5000 r·min¹离心5 min,将下层溶液通过0.22μm孔径的微孔滤膜进行过滤,然后进行上机测定。
1.3.2溶液配制(1)兽药标准储备液的配制:分别准确称取适量的兽药标准品,用甲醇溶解,获得浓度为1.0 mgmL¹的标准储备液,避光保存在-18℃的条件下。(2)混合标准中间溶液的配制:分别准确吸取适量上述各种兽药标准储备液,用甲醇稀释,配成浓度为10μg:mL¹的混合标准中间溶液,避光保存在4℃的条件下。(3)混合标准工作液的配制:准确量取适量兽药混合标准中间溶液,并用甲醇稀释,配成浓度为1μgmL¹的混合标准工作液,现配现用。
1.3.3仪器检测条件
(1)色谱条件
色谱柱:Agilent Eclipse Plus C18色谱柱(2.1 mm×50 mm,1.8μm);流速:0.4 mL.min¹;进样量:2μL;柱温:40℃。流动相A:含0.1%(体积分数)甲酸水溶液;流动相B:乙腈;梯度洗脱程序:0~3.60 min,5%B;3.60~3.80 min,5%~12%B;3.80~7.00 min,12%B;7.00~7.10 min,12%~26%B;7.10~9.00 min,26%~55%B;9.00~9.10 min,55%~100%B;9.10~11.50 min,100%B;11.50~11.60 min,100%~5%B;11.60~14.00 min,5%B。
(2)质谱条件
电喷雾离子源正离子模式(ESI),鞘气温度设定为250℃;鞘气流速调节至11.0 L·min-¹;雾化气压力设置为45 psi;毛细管电压调整至3.5 kV;干燥气温度升至300℃;干燥气流速设定为8.0 L·min¹;扫描方式:多反应离子监测,优化后的各种兽药的质谱检测参数见表1。
1.3.4提取溶剂的选择与其他有机溶剂相比,乙腈的优势在于它能有效减少脂肪和色素等杂质的提取,同时还能沉淀蛋白16,提取效果好17,因此适合用于动物源性食品中大部分偏极性兽药的提取18]。考虑到磺胺类和喹诺酮类兽药可呈酸碱两性,在酸性条件下更易于萃取,因此本试验中加入了一定量的甲酸。分别利用含有0.1%甲酸的乙腈溶液以及含有1%甲酸的乙腈溶液对猪肉样品进行提取,观察提取效果。在提取过程中,由于乙腈具有沉淀蛋白质的作用,直接添加会导致肉质结块。为避免出现以上问题,可以先加入适量的水使样品充分分散,然后再进行有机溶剂的提取。随后,通过添加无水硫酸钠和氯化钠,并在低温环境下进行快速离心,以实现水相和有机相的有效分离,从而在有机相中高效地富集目标化合物。这种方法能够有效防止水分和水溶性杂质混进提取液中,从而达到脱水和盐析的目的,同时提高提取效率。以阴性猪肉样品加标量10μg·kg-¹为试验样品,对比该样品在未加水分散情况下直接用有机溶剂提取和先加水分散后再用有机溶剂提取的16种兽药的上机响应值。
1.3.5净化条件优化在经过盐析处理后,猪肉提取液中仍然存在脂肪、蛋白质、甾醇、脂肪酸和色素等杂质。在QuEChERS净化技术中,常用的吸附剂包括N-丙基乙二胺(PSA)、C18和GCB。PSA通常用于吸附脂肪酸、色素和糖类等极性物质;C18能高效吸附甾醇、脂质化合物以及其他非极性成分;GCB的平面结构不仅能够吸附色素,还能吸附含有苯环结构的物质[1。由于本试验中的大部分兽药具有苯环结构,为了能有效去除基质提取液中大部分干扰物的影响,因而确定了PSA+C18这个净化剂组合。按照1.2.1样品前处理方法,利用加标量为20μg.kg¹的猪肉样品来评估净化效果,考察在脱水剂无水硫酸钠用量为1.0 g时,比较PSA与C18不同使用量的净化效果和加标回收率。1.3.6检测方法评估将阴性猪肉样品按1.2.1方法进行前处理,配制6个梯度水平(2、5、10、20、50、100μg·kg-¹)的基质匹配标准工作溶液,上机测定。以定量离子峰面积作为纵坐标,浓度作为横坐标,做定量工作曲线,考察方法的线性范围、灵敏度。通过对阴性猪肉样品进行加标回收试验,添加水平:2.0、4.0、20.0μg·kg-¹,按前述方法进行前处理和检测,每组浓度平行6次试验,计算实验的加标平均回收率和RSD,考察方法的准确度与精密度。
2结果与分析
2.1前处理条件优化
2.1.1提取溶剂的选择由图1可知,使用含有1%(v/v)甲酸的乙腈溶液作为提取溶剂时,猪肉样品出现了一定程度的结块现象,这不利于样品的均匀分散和兽药的彻底提取。因此,选择含有0.1%(v/v)甲酸的乙腈溶液作为提取溶剂。
由图2可知,以阴性猪肉样品加标量10μg-kg-1为试验样品,加水分散后再用有机溶剂提取的样品中的兽药在仪器上的响应较高说明该方法的提取效率比直接加入有机溶剂的要好。因此,本研究采用0.1%甲酸乙腈/水混合溶剂进行提取,并通过盐析离心分离技术来实现分层。
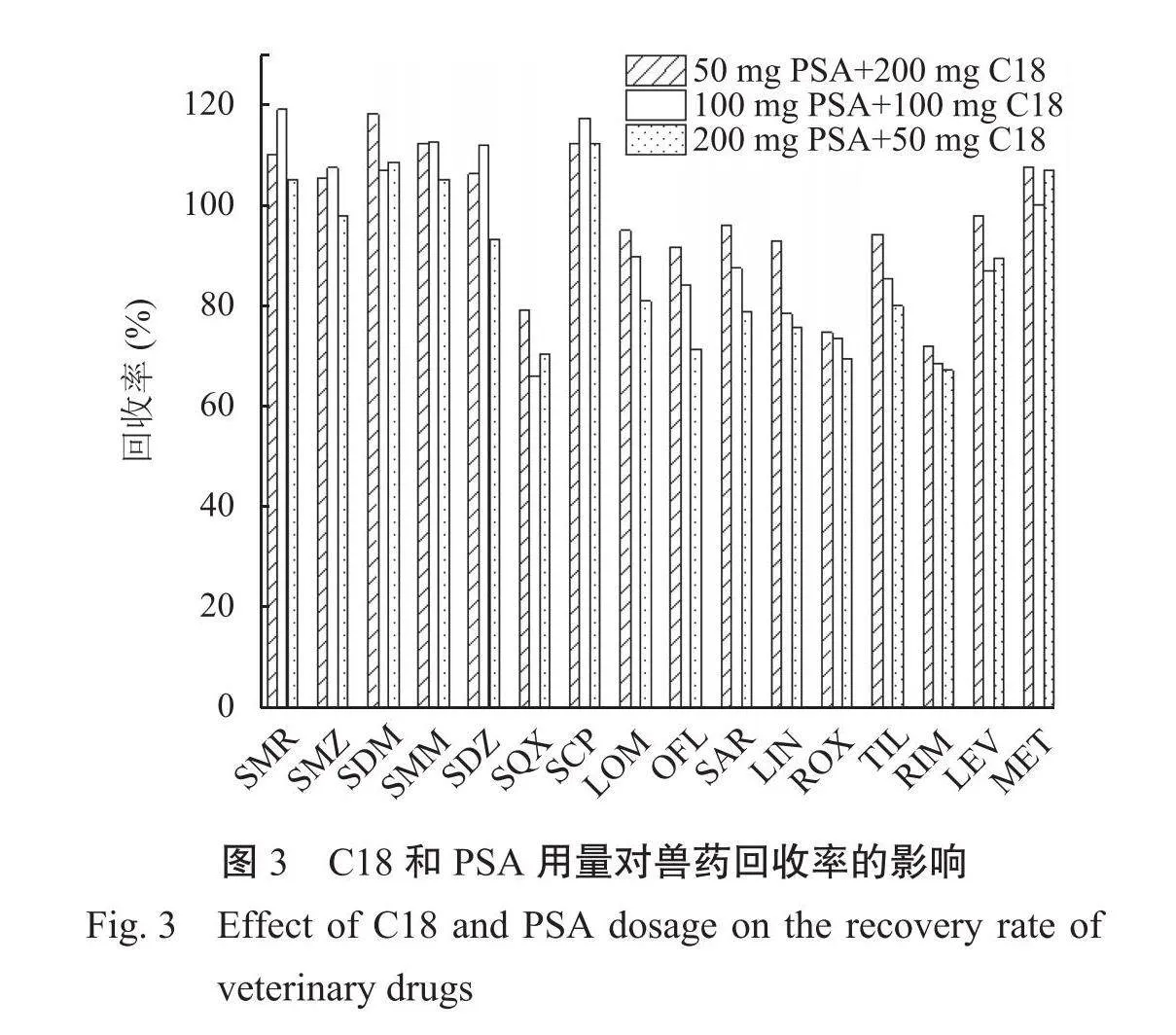
2.1.2净化条件优化由图3可知,通过比较3种吸附剂组合的回收率,可以发现50 mg PSA+200 mg C18这种吸附剂组合的回收率总体优于其他组合。因此,采用1.0 g无水硫酸钠、50 mg PSA和200 mg C18为净化剂组合对样品进行前处理。
2.2仪器条件的优化
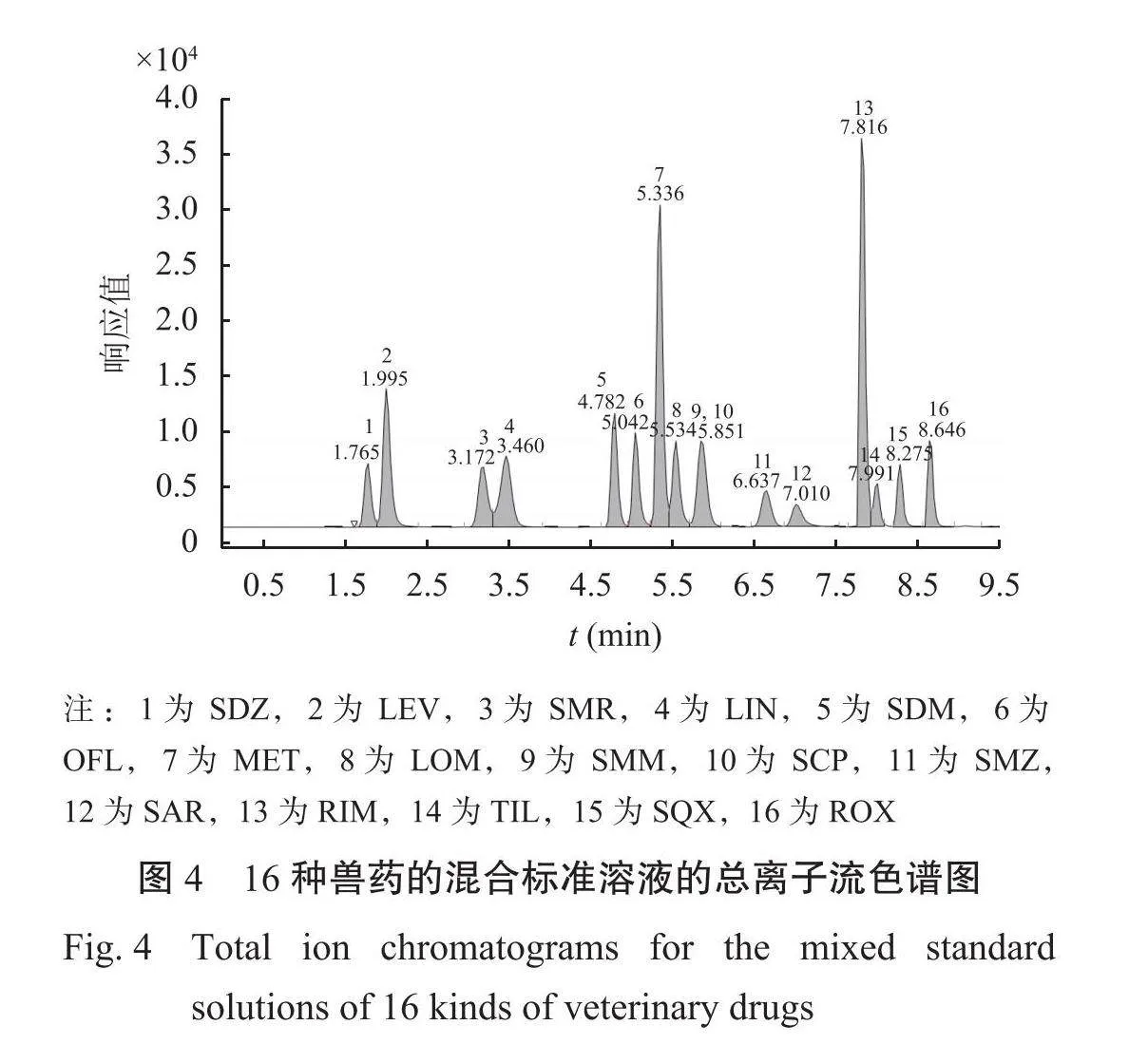
2.2.1色谱分离条件的选择本研究选用Agilent Eclipse Plus C18色谱柱来进行分离,考察了不同流动相条件对16种化合物的分离效果、峰形和信号响应产生的影响。结果表明,在采用乙腈-水作为流动相的条件下,这些兽药能在较短的时间内得到有效的分离,且分离效果较甲醇-水流动相体系更佳。此外,添加甲酸可较好提高目标化合物的信号响应。因此本研究使用乙腈和含0.1%体积分数甲酸的水溶液作为流动相。通过进一步优化梯度洗脱程序,基本实现本试验中16种兽药能在9 min内分离,且16种兽药均可取得较好的响应值,有利于后续的质谱检测分析。16种兽药混合标准溶液的总离子流色谱图见图4。
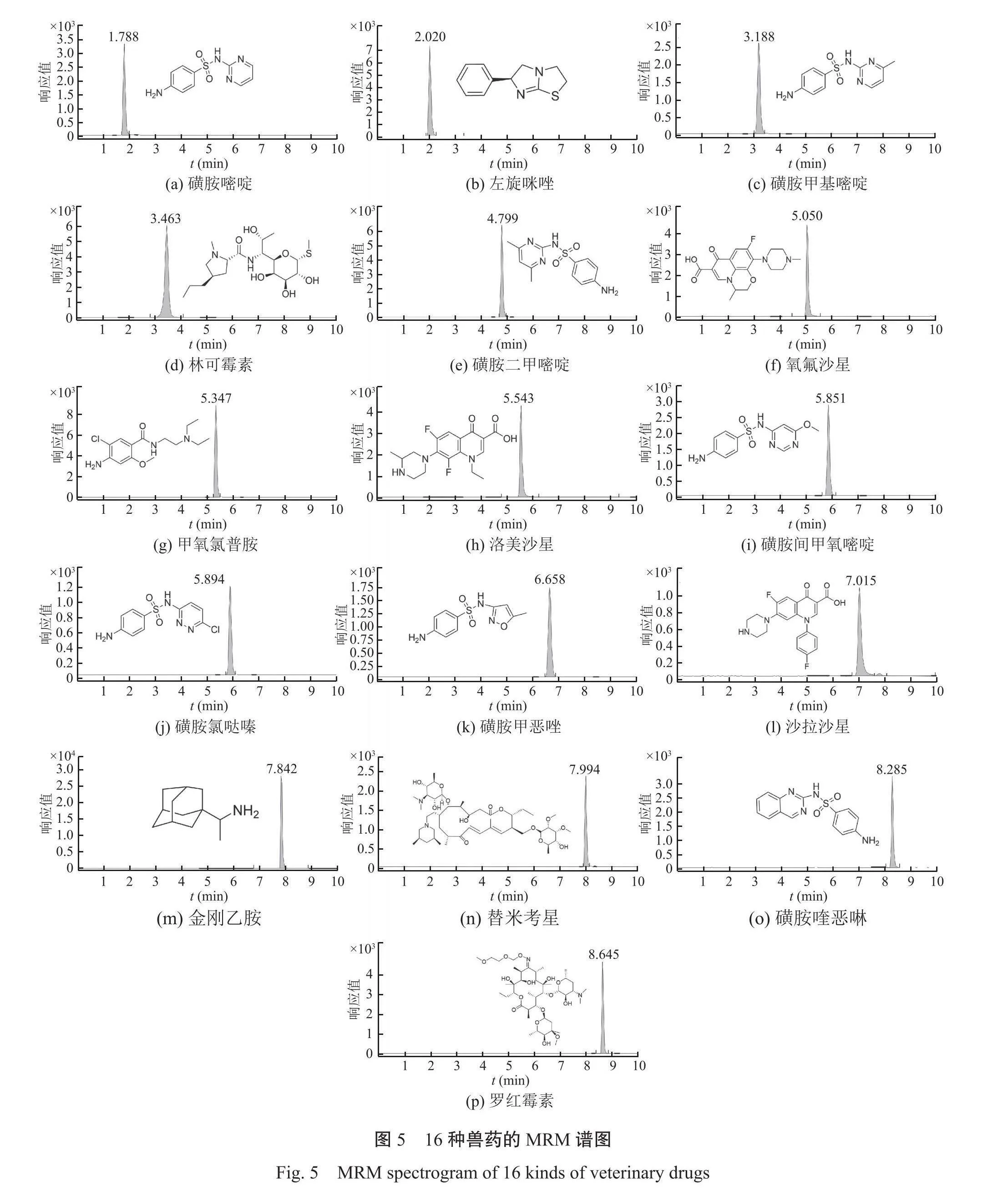
2.2.2质谱检测参数的优化本试验16种兽药化合物均易于进行离子化,因此适合采用电喷雾离子源。在正离子模式(ESI+)下,通过全扫描确定各化合物的母离子。在最优碎裂电压下,对母离子进行二级Product Ion质谱扫描,确定出定量与定性的离子对,进行多反应监测MRM参数优化,建立MRM采集方法。获得的最佳质谱参数见表1,各目标物的MRM色谱图见图5。
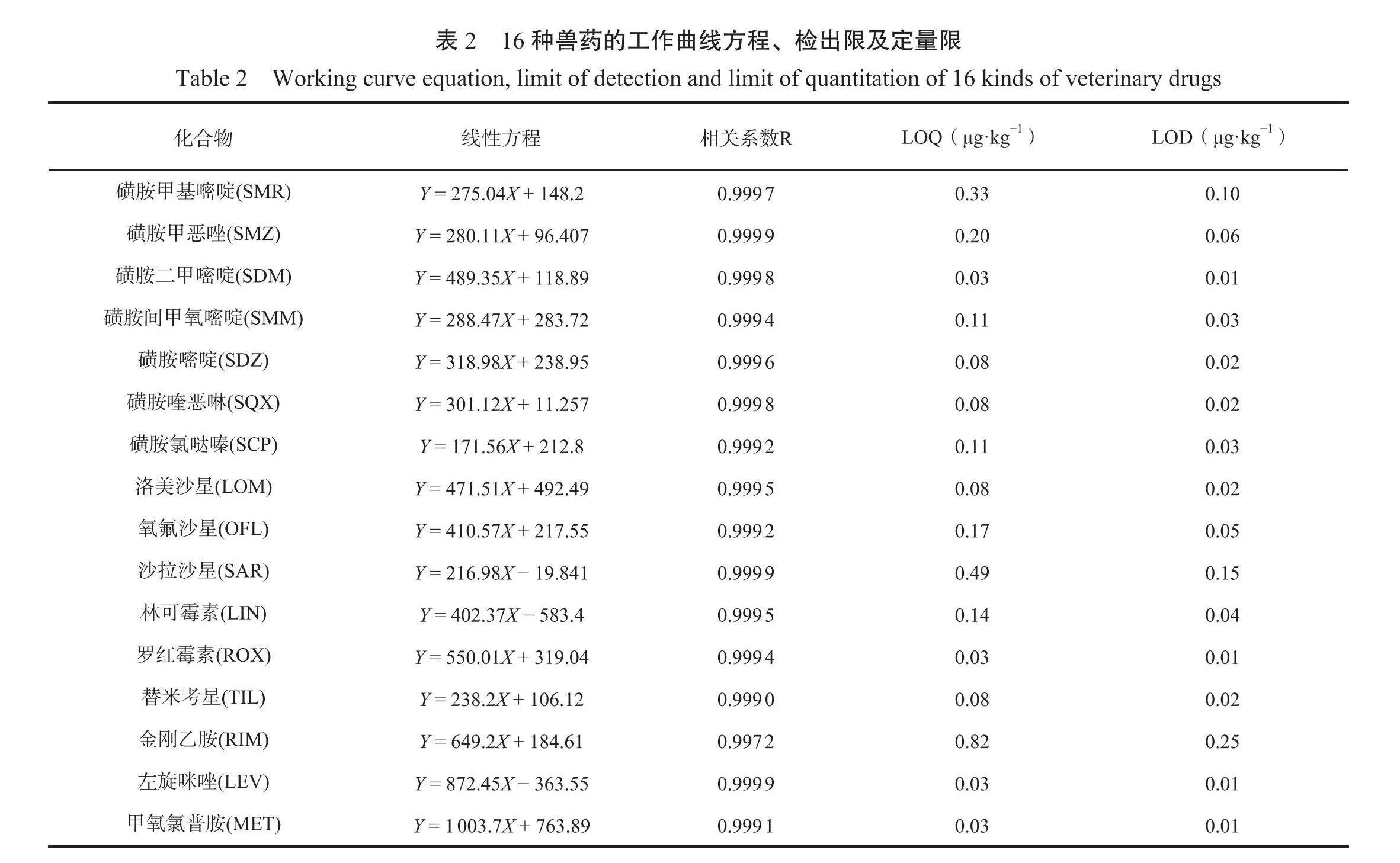
2.3方法的标准曲线及检出限与定量限
由表2可知,16种兽药在2.0~100.0μg-kg-的范围内有良好的线性关系(r>0.9970)。检出限(LOD)通过3倍信噪比(S/N)来确定,其对应的浓度范围为0.01~0.25μg-kg-¹。定量限(LOQ)则是基于10倍信噪比计算得出,对应的浓度范围为0.03~0.82μg-kg-¹。这些结果表明,该分析方法具有较高的灵敏度,能够满足GB 31650-2019《食品中兽药最大残留限量》4和GB 31650.1-2022《食品中41种兽药最大残留限量》⁵对这16种化合物最大残留限量的检测标准。
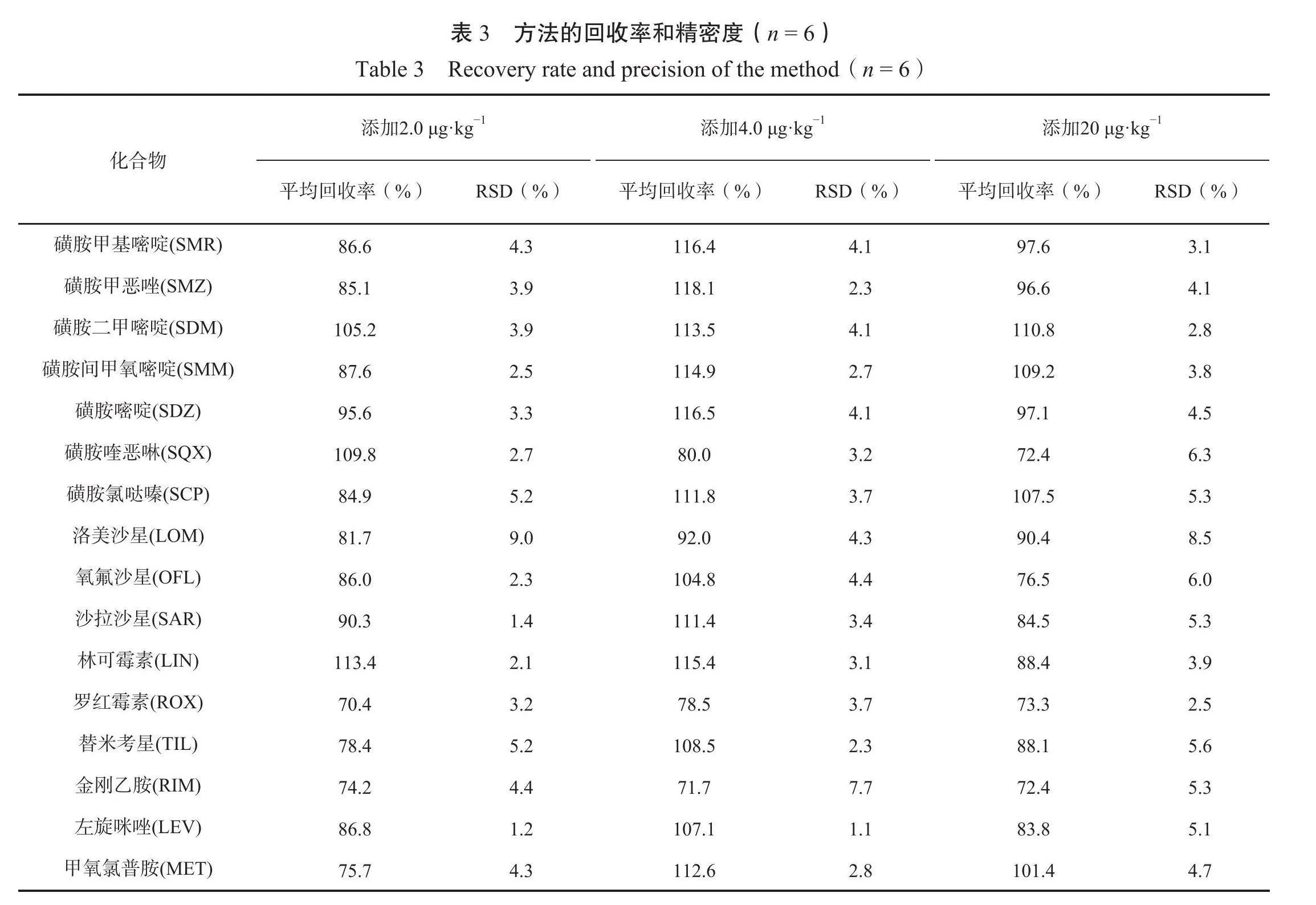
2.4方法的回收率和精密度
由表3可知,各兽药加标回收率范围在70.4%~118.1%内,相对标准偏差RSD为1.1%~9.0%,符合GB/T 27404-2008《食品理化检测》[20对回收率和精密度的要求。
2.5实际样品测试
为了验证本方法在实际样本中的检测效果,对市场上购买的12批次不同品种的猪肉进行测定。结果显示其中1份猪肉样品(图6)同时检出氧氟沙星、磺胺间甲氧嘧啶和磺胺甲恶唑,浓度分别为16.1、1.9、2.1μg-kg-¹,其余样品均未检出。国标GB 31650.1-2022《食品中41种兽药最大残留限量》s规定了磺胺类合成抗菌药在所有食品动物的肌肉中的最大残留限量为100μg·kg-¹,氧氟沙星在所有食品动物的肌肉中的最大残留限量为2μg-kg-¹,因此在此次样品检测试验中有1份实际样品存在兽药残留超标现象。
3结论与讨论
本研究采用QuEChERS前处理方式与高效液相色谱串联质谱法相结合的方法,用于同时检测猪肉中的16种兽药残留。对前处理条件、色谱、质谱条件等参数进行优化,有效地减少猪肉样品中复杂基质对分析结果的干扰。样品先用水分散后再用0.1%甲酸乙腈进行提取,经过吸附剂组合50 mg PSA和200 mg C18净化后,通过Agilent Eclipse Plus C18色谱柱分离,在HPLC-MS/MS系统的正离子多反应监测模式下进行分析。检测方法评估试验结果表明,16种兽药在2.0~100.0μg-kg-¹的范围内有良好的线性关系(相关系数r>0.9970);检出限(LOD,S/N=3)和定量限(LOQ,S/N=10)的范围分别为0.01~0.25μg·kg-¹、0.03~0.82μg-kg¹;在猪肉样品中进行了2、4、2 0μg·kg¹3个不同浓度水平的加标试验,相对标准偏差RSD为1.1%~9.0%,加标回收率在70.4%~118.1%。经本方法测试的各项兽残检出限均低于现有国家标准,同时具有良好的回收率和精密度。该方法检测分析结果灵敏度高,准确度好,且操作简便快速,能够满足猪肉中兽药残留相关安全检测要求,为动物源食品兽药残留检测提供方法参考,也为食品安全提供了技术支持。
参考文献:
[1]叶妮,孙雷,张骊,等.生鲜禽蛋中兽药使用现状及药物残留有关规定的概述[J].中国兽药杂志,2023,57(5):69-76.
[2]史艳艳,王俊菊.畜禽养殖业兽药使用现状及建议[J].畜牧兽医科学(电子版),2021(5):185-186.
[3]杜军,曾晓,贾荣玲.畜禽饲养中兽药残留的原因、危害及防控措施[J].山西农经,2020(16):134-135.
[4]中华人民共和国国家卫生健康委员会,中华人民共和国农业农村部,国家市场监督管理总局.食品中兽药最大残留限量:GB 31650-2019[s].北京:中国农业出版社,2019.
[5]中华人民共和国国家卫生健康委员会,中华人民共和国农业农村部,国家市场监督管理总局,食品中41种兽药最大残留限量:GB 31650.1-2022[s].北京:中国农业出版社,2022.
[6]裴斐,韩萍,王杰,等.基于UHPLC-Q-TOF/MS法同时检测猪肉中主要抗生素类兽药残留[J].食品工业科技,2022,43(10):298-304.
[7]李增明,解玉龙,马春光.QuEChERS-超高效液相色谱-串联质谱法测定牦牛肉中多种抗生素残留c4a99fcf62bde02933a857b3f75e3c548906caa03ee7a980c39236e4994f8189[J].化学试剂,2024,46(6):99-106.
[8]张朋杰,卢俊文,张宪臣,等.基于超高效液相色谱-四级杆-静电场轨道阱高分辨质谱建立鸡肉中双酰胺类和双酰肼类农药残留分析方法[J].食品与发酵工业,2024,50(4):302-307.
[9]KIM YR,PARK S,KIM JY,etal.Simultaneous determination of 31 Sulfonamide residues in variouslivestock matrices using liquid chromatography-tandem mass spectrometry[J].Applied Biological Chemistry,2024,67(1):DOI:10.1186/s13765-024-00864-z
[10]中华人民共和国国家卫生健康委员会,中华人民共和国农业农村部,国家市场监督管理总局.动物性食品中四环素类,磺胺类和喹诺酮类药物残留量的测定液相色谱-串联质谱法GB 31658.17-2021[s].北京:中国农业出版社,2021.
[11]LIS,LIU Y,JIANG D,etal.Simultaneous Quantification of39 Pesticides and Veterinary Drug Residues in Aquaculture Products Using Ultra Performance Liquid Chromatography Tandem Mass Spectrometry with Modified QuEChERS[J].Food Analbytical Methods,2024,17(6):797-811.
[12]陈容,刘育形,王泽林,等.QuEChERS/超高效液相色谱-串联质谱法测定禽蛋中90种禁用药物残留[J].分析测试学报,2023,42(10):1291-1300.
[13]黄梅花.QuEChERS结合液相色谱串联质谱法同时测定鸡蛋中氟虫腈与氯霉素等7种农兽药残留[J].食品安全质量检测学报,2020,11(6):1821-1826.
[14]李丹妮,严凤,周悦榕,等.QuEChERS-超高效液相色谱法-串联质谱法同时检测猪组织中赛庚啶及可乐定残留量[J].中国兽药杂志,2017,51(2):29-34.
[15]王小乔,李坚,许晓辉,等.超滤型高脂基质净化柱结合超高效液相色谱-三重四极杆液质联用法测定鱼肉中七种镇静剂[J].食品与发酵工业,2023,49(24):267-274.
[16]朱礼,邓航,袁列江,等.QuEChERS净化结合超高效液相色谱串联质谱法快速测定动物源性食品中溴虫氟苯双酰胺残留[J].食品与发酵工业,2024,50(17):336-342.
[17]肖泳,邓航,潘照,等.QuEChERS-超高效液相色谱-串联质谱法快速测定动物源性食品中矮壮素残留[J].食品与发酵工业,2022,48(10):272-277.
[18]郭添荣,吴文林,万渝平,等.HLB净化/高分辨液质联用法快速筛查动物肝脏中45种兽药残留[J].中国食品学报,2022,22(7):287-299.
[19]陈祥奕,姚奋增.QuEChERS-高效液相色谱-串联质谱法检测莲子中8种农药残留[J].食品安全质量检测学报,2021,12(12):4903-4908.
[20]中国国家标准化管理委员会,中华人民共和国国家质量监督检验检疫总局.实验室质量控制规范食品理化检测GB/T 27404-2008[s].北京:中国标准出版社,2008.
(责任编辑:林玲娜)
