心脏磁共振下早期矛盾运动可多角度评估急性心肌梗死患者术后心功能状态
2024-11-20丁斌王钧宋禧龙李尧丁丝雨王月燕宋宏伟李妙男王洪巨




摘要:目的 "探讨心脏磁共振(CMR)早期矛盾运动与急性心肌梗死(AMI)患者临床特征、危险分层和临床预后的相关性。方法 "连续纳入2022年6月~2024年4月在我科住院并确诊的首发AMI患者77例,其中男性53例,女性24例,年龄61.75±11.92岁。所有患者均在入院后行罪犯血管血运重建术,并在术后平均1周内行CMR检查。根据心肌应变是否出现矛盾运动,将其分为矛盾运动组(n=47)和非矛盾运动组(n=30)。所有患者平均随访7月,统计主要不良心血管事件(MACEs)的发生。结果 "矛盾运动组患者的脑钠肽、中性粒细胞/淋巴细胞比值高于非矛盾运动组,淋巴细胞计数低于非矛盾运动组(Plt;0.05)。两组病变支数、罪犯血管、Gensini评分的差异无统计学意义(Pgt;0.05)。CMR结果显示,矛盾运动组患者的梗死面积、左室收缩末期容积指数、微循环障碍容积高于非矛盾运动组(Plt;0.05),而左房射血分数、左室射血分数、梗死节段径向应变、梗死节段周向应变、梗死节段纵向应变、整体径向应变、整体周向应变、整体纵向应变均低于非矛盾运动组(Plt;0.05)。二元Logistic回归显示,中性粒细胞/淋巴细胞比值、梗死节段周向应变、整体纵向应变可以独立预测患者是否出现心肌矛盾运动。在矛盾运动组患者中,MACEs事件发生率高于非矛盾运动组(Plt;0.05),其中矛盾运动是AMI患者在接受成功血运重建后发生MACEs事件的独立危险因素(HR=2.551)。结论 "CMR可以多角度评估AMI术后心功能状态,为患者个体化治疗、改善临床预后提供了重要的参考依据。
关键词:急性心肌梗死;心脏磁共振;早期矛盾运动;心功能状态;不良心血管事件
Early paradoxical motion under cardiac magnetic resonance can be used to evaluate postoperative cardiac function in patients with acute myocardial infarction from multiple angles
DING Bin1, WANG Jun1, SONG Xilong1, LI Yao1, DING Siyu1, WANG Yueyan2, SONG Hongwei2, LI Miaonan1, WANG Hongju1
1Department of Cardiovascular Medicine, 2Department of Radiology, The First Affiliated Hospital of Bengbu Medical College, Bengbu 233004, China
Abstract: Objective To explore correlations of early contradictory movements with clinical characteristics, risk stratification, and clinical prognosis in patients with acute myocardial infarction (AMI). Methods This study consecutively enrolled 77 first-onset AMI patients who were hospitalized and diagnosed in our department from June 2022 to April 2024, including 53 males and 24 females, with a mean age of 61.75±11.92 years. All patients underwent culprit-only revascularization after admission and received cardiac magnetic resonance (CMR) imaging within an average of one week after surgery. According to whether there were contradictory movements in myocardial strain, the included patients were divided into contradictory movement group (n=47) and non-contradictory movement group (n=30). All patients were followed up for an average of 7 months to record the occurrence of major adverse cardiovascular events (MACEs). Results Patients in the contradictory movement group had significantly increased brain natriuretic peptide levels and neutrophil/lymphocyte ratio, but decreased lymphocyte counts than those in the non-contradictory movement group (Plt;0.05). There was no significant difference in the number of diseased vessels, culprit vessels, and Gensini score between the contradictory movement group and the non-contradictory movement group (Pgt;0.05). CMR results showed that patients in the contradictory movement group had significantly larger infarct areas visualized by LGE, higher left ventricular end-systolic volume index and microcirculation dysfunction volume than those in the non-contradictory movement group (Plt;0.05); while the former group had obviously lower left atrial ejection fraction, left ventricular ejection fraction, radial strain of the infarcted segment, circumferential strain of the infarcted segment, longitudinal strain of the infarcted segment, global radial strain, global circumferential strain, and global longitudinal strain than those in the latter group (Plt;0.05). Furthermore, binary logistic regression analysis showed that neutrophil/lymphocyte ratio, circumferential strain of the infarcted segment, and global longitudinal strain could predict whether patients had contradictory movements independently. In addition, the incidence of MACEs was significantly higher in the contradictory movement group than in the non-contradictory movement group (Plt;0.05), with contradictory movement being an independent risk
factor for MACEs in AMI patients after successful revascularization (HR=2.551). Conclusion CMR can facilitate the evaluation of the postoperative cardiac function status of AMI patients from multiple perspectives, which may provide a valuable reference for applying personalized treatment and improving the clinical prognosis of patients.
Keywords: acute myocardial infarction; cardiac magnetic resonance imaging; early contradictory movements; cardiac function status; major adverse cardiovascular events
急性心肌梗死(AMI)发病急骤、病死率高[1]。胸痛中心的建设及时有效地挽救了多数患者生命。但部分患者在经皮冠状动脉介入治疗(PCI)术后仍然发生不良心血管事件[2]。早期评估梗死后心脏及心肌功能、梗死范围、存活心肌、微循环障碍等,对临床进行个体化治疗和预后判断至关重要。但是现有的心脏超声等检查手段不能够为临床提供精准的判断[3]。心脏磁共振(CMR)技术弥补了既往检查的不足。近年来,通过延迟增强成像(LGE)及组织追踪技术精确量化心肌梗死区域,评估心肌应变功能及微循环障碍(MVO),从而提高了患者的风险分层和术后预后预测的准确性[4, 5];量化左心室的应变和不协调程度,从而有效预测心功能恢复及不良心血管事件[6]。但是心脏核磁下的早期矛盾运动与AMI的相关研究鲜有报道。本研究旨在探讨AMI患者早期心肌矛盾运动与临床特征、风险分层及预后之间的相关性,以期为AMI患者术后进行个体化治疗、改善临床预后提供参考依据。
1 "资料与方法
1.1 "一般资料
本研究连续纳入2022年6月~2024年4月蚌埠医科大学第一附属医院收治的77例因AMI行PCI的患者,其中男性53例,女性24例,年龄33~83(61.75±11.92)岁,PCI术后平均1周内接受CMR检查,将获得的CMR影像导入CVI42绘测软件进行组织追踪技术后处理,按左心室部分节段心肌应变是否同整体心肌应变一致将患者分为矛盾运动组(n=47)和非矛盾运动组(n=30)。所有患者平均随访7月,统计主要不良心血管事件(MACEs)的发生。纳入标准:符合AMI的临床诊断标准[7];首次发作心肌梗死,入院后急诊行PCI;直接PCI术后平均1周内完成CMR检查。排除标准:罪犯血管开通失败;心源性休克等血流动力学不稳定状况;既往有陈旧性心肌梗死或合并活动性心肌炎、心肌病(扩张型心肌病、肥厚型心肌病、限制型心肌病等);严重肝功能衰竭或肾功能不全;预期寿命小于半年;存在CMR检查禁忌(如幽闭恐惧症等);CMR图像质量差或扫描序列不完整。本研究获蚌埠医科大学第一附属医院伦理委员会审批(审批号:2023YJS248)。
1.2 "研究方法
1.2.1 "冠状动脉造影 " 由心内科专业医师采用Judkins法行冠状动脉造影,根据美国心脏病学会/美国心脏协会(AHA)经皮冠状动脉介入治疗指南[8]行结果判读,获取介入手术相关资料,详细记录手术过程。期间由2位熟练的心脏科医师采用Gensini评分系统[9]独立评估并计算均值。
1.2.2 "CMR检查及分析 nbsp; 采用1.5T场强超导磁共振扫描仪(MAGNETOM Avanto,西门子),通过短轴平衡稳态自由进动电影成像和LGE序列进行图像采集:患者取仰卧位,通过心电、呼吸门控监测,于呼气末屏气时采集左室短轴、左室两腔及四腔长轴方位的CINE电影序列。延迟强化采用反转恢复快速梯度回波序列,使用高压MR注射器(Spectris Solaris EP)静脉注射剂钆喷酸葡胺对比剂(规格为469 mg/mL×20 mL,剂量0.2 mmol/kg,注射速率4.0 mL/s)进行强化,10~15 min后扫描短轴位、两腔心、四腔心及左室流入流出道层面获得LGE图像。参数如下:层厚8 mm;回波时间1.1 ms;重复时间117.53 ms;视野400 mm×400 mm,翻转角50°。
使用AHA的17节段分法[10],于短轴层面上将左室心肌分为17段分析,经CVI42软件分析,生成16段牛眼图(因心尖帽测量误差较大,本研究剔除第17段)。图像上传至CVi42软件(Version 5.9, Circle Cardiovascular Imaging Inc. Calgary, Alberta, Canada)进行分析,将电影序列图像导入Strain模块,软件于3个长轴平面(二腔心、三腔心和四腔心)及1个短轴平面上特征追踪左心室心内、外膜轮廓,必要时手动调整初始轮廓,完成对全心动周期的轮廓追踪并进行整体及各节段应变分析。
1.2.3 "随访 " 所有患者出院后通过门诊和电话随访平均7月,统计MACEs事件的发生。MACEs事件包括:再发心绞痛、再发心肌梗死、心力衰竭、支架内血栓/再狭窄、再次血运重建、心源性死亡、全因死亡和脑卒中。
1.3 "统计学分析
采用SPSS 26.0统计软件进行统计学分析,采用GraphPad Prism 9.5.1绘图。符合正态分布的计量资料以均数±标准差表示,组间比较采用两独立样本t检验;非正态分布的计量资料以中位数(上下四分位数)表示,组间比较采用Mann-Whitney U检验;分类变量以n(%)表示,组间比较采用卡方检验。采用单因素和多因素Logistic回归分析矛盾运动的预测因素,并用ROC评估其诊断效能。采用Cox回归模型分析矛盾运动与MACEs事件发生之间的关系,并用Kaplan-Meier生存曲线分析矛盾运动对患者远期生存的影响。以Plt;0.05为差异有统计学意义。
2 "结果
2.1 "两组AMI患者基线特征的比较
矛盾运动组患者的脑钠肽(BNP)、中性粒细胞/淋巴细胞比值(NLR)高于非矛盾运动组,淋巴细胞计数低于非矛盾运动组(Plt;0.05),其余参数的差异无统计学意义(Pgt;0.05,表1)。
2.2 "两组AMI患者冠脉造影结果的比较
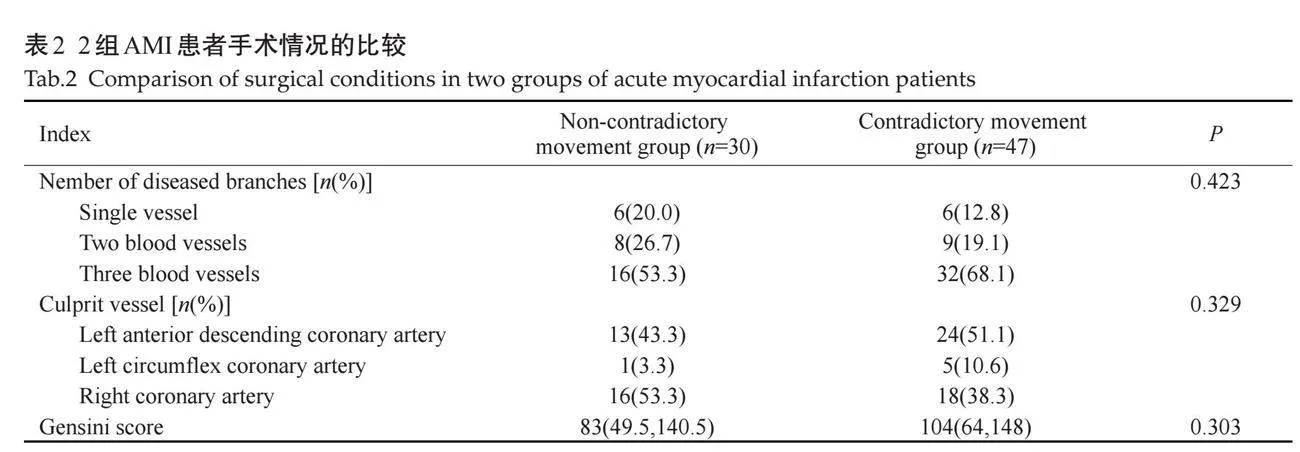
两组病变支数、犯罪血管及Gensini评分的差异均无统计学意义(Pgt;0.05,表2)。
2.3 "两组AMI患者CMR参数的比较
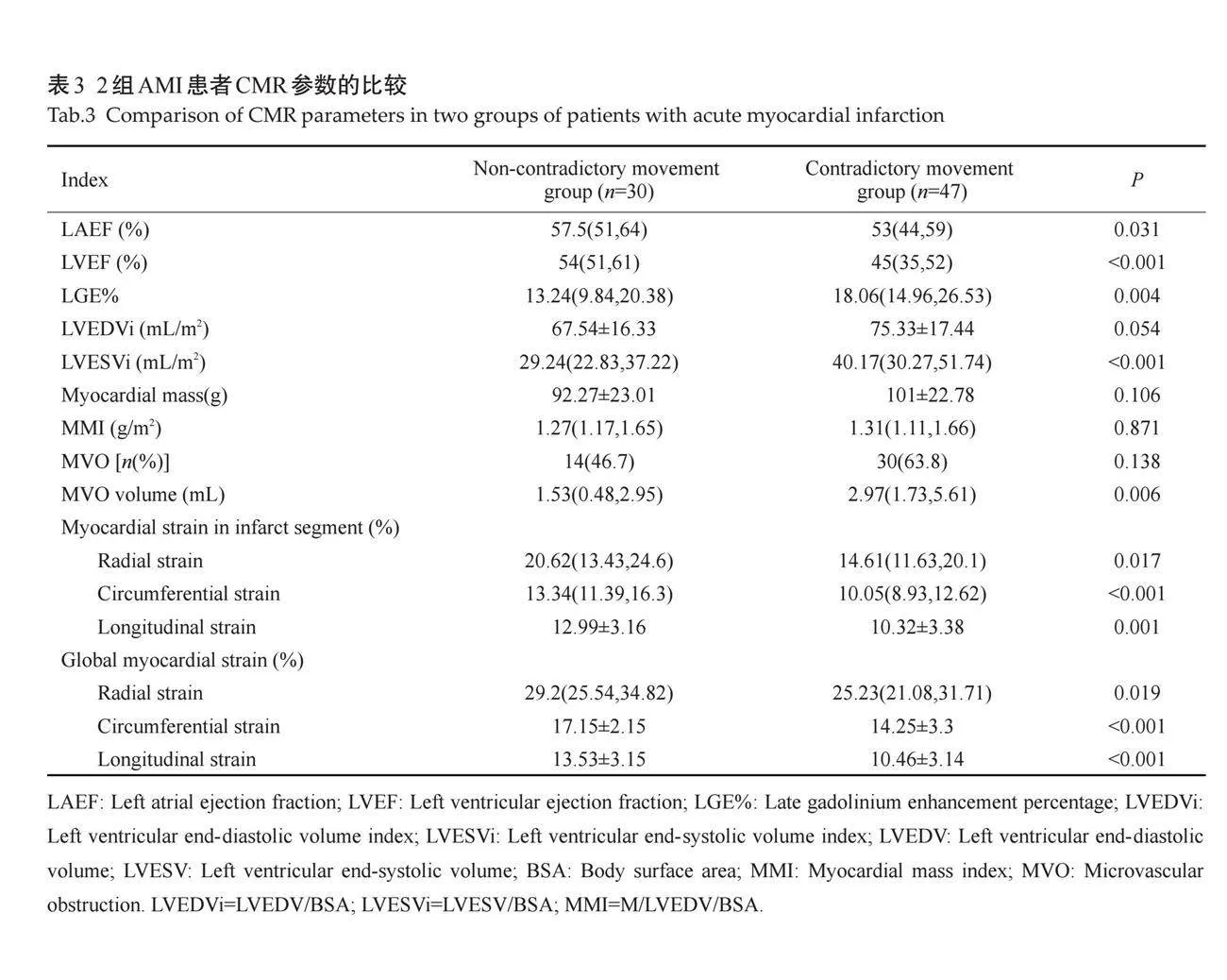
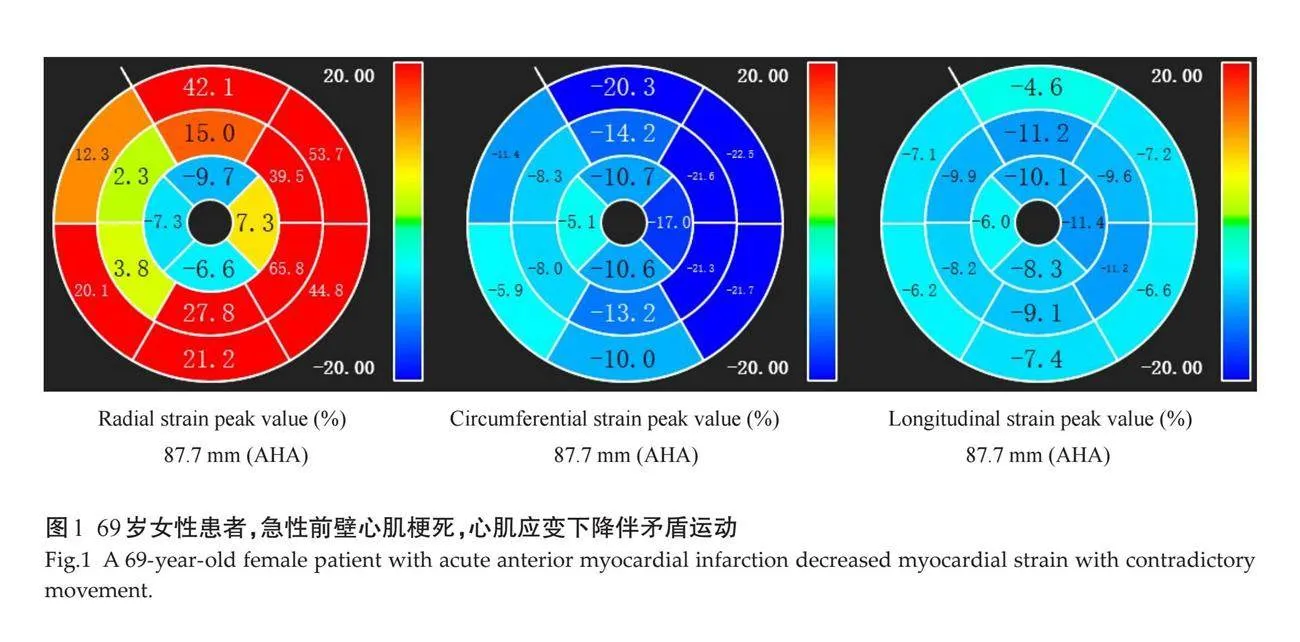
矛盾运动组患者的梗死面积(LGE%)、左室收缩末期容积指数(LVESVi)、微循环障碍容积高于非矛盾运动组,左房射血分数(LAEF)、左室射血分数(LVEF)、梗死节段径向应变、梗死节段周向应变、梗死节段纵向应变、整体径向应变、整体周向应变、整体纵向应变均低于非矛盾运动组(Plt;0.05),其余CMR参数的差异无统计学意义(Pgt;0.05,表3、图1、2)。
2.4 "矛盾运动的单因素与多因素Logistic回归分析
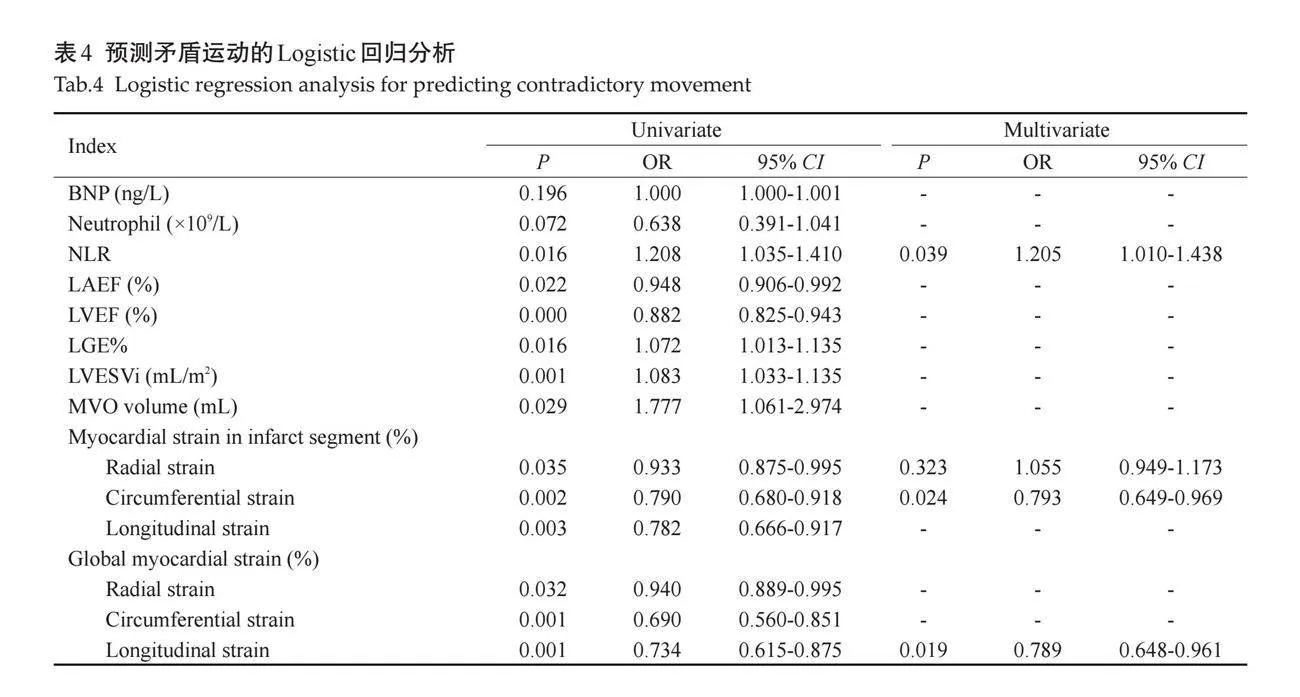
将差异有统计学意义的指标纳入单因素Logistic回归分析,再将分析结果中有统计学意义的参数纳入多因素Logistic回归分析。结果显示NLR、梗死节段周向应变、整体纵向应变是矛盾运动的独立预测因素(表4)。
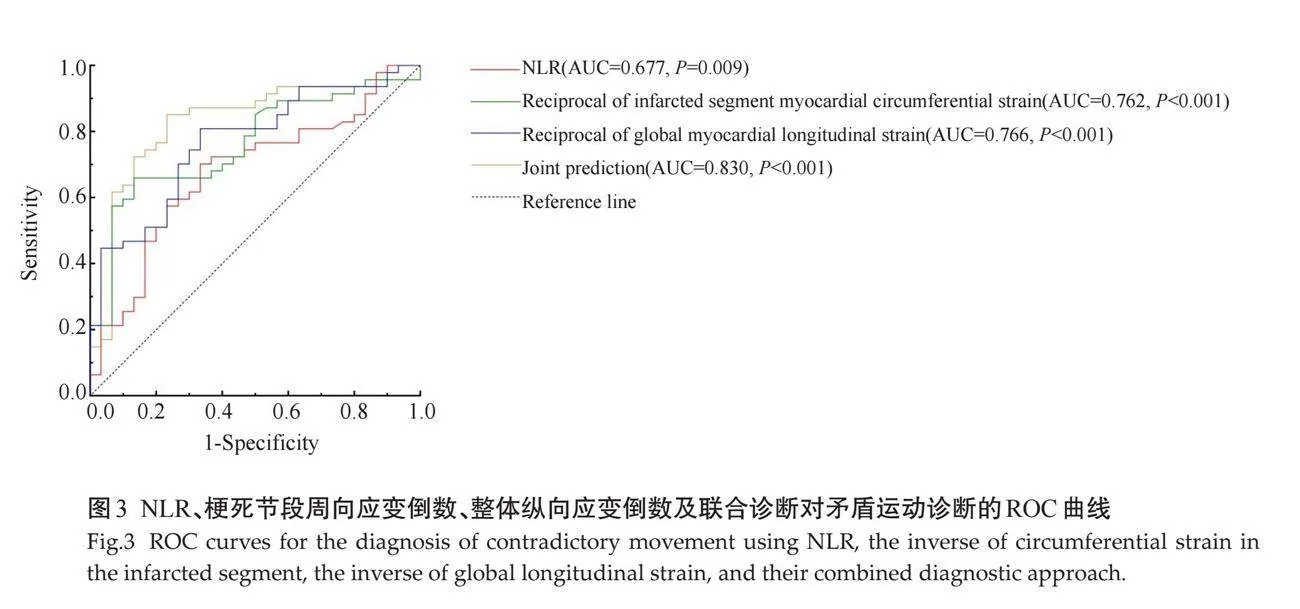
2.5 "NLR、梗死节段周向应变倒数、整体纵向应变倒数、联合诊断对矛盾运动的诊断价值分析
ROC曲线分析结果显示:NLR可以辅助对于矛盾运动的诊断,梗死节段周向应变倒数、整体纵向应变倒数对于矛盾运动的发生具有诊断价值。将以上3个预测因素同时纳入进行ROC诊断分析,其对矛盾运动诊断的AUC、敏感度较单独预测时上升,AUC为0.830(0.732~0.929),特异度为76.70%,敏感度为85.10%
(Plt;0.01,表5、图3)。
2.6 "随访
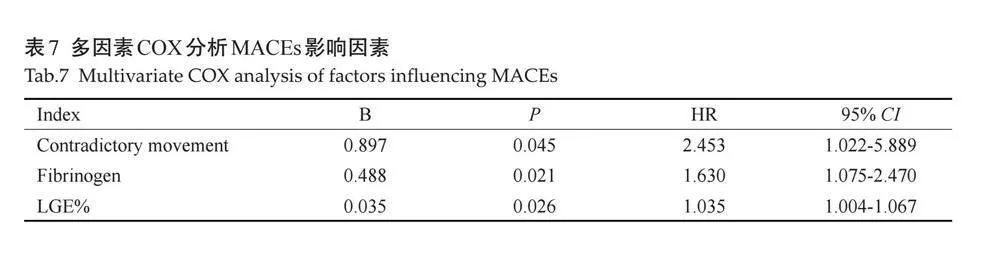
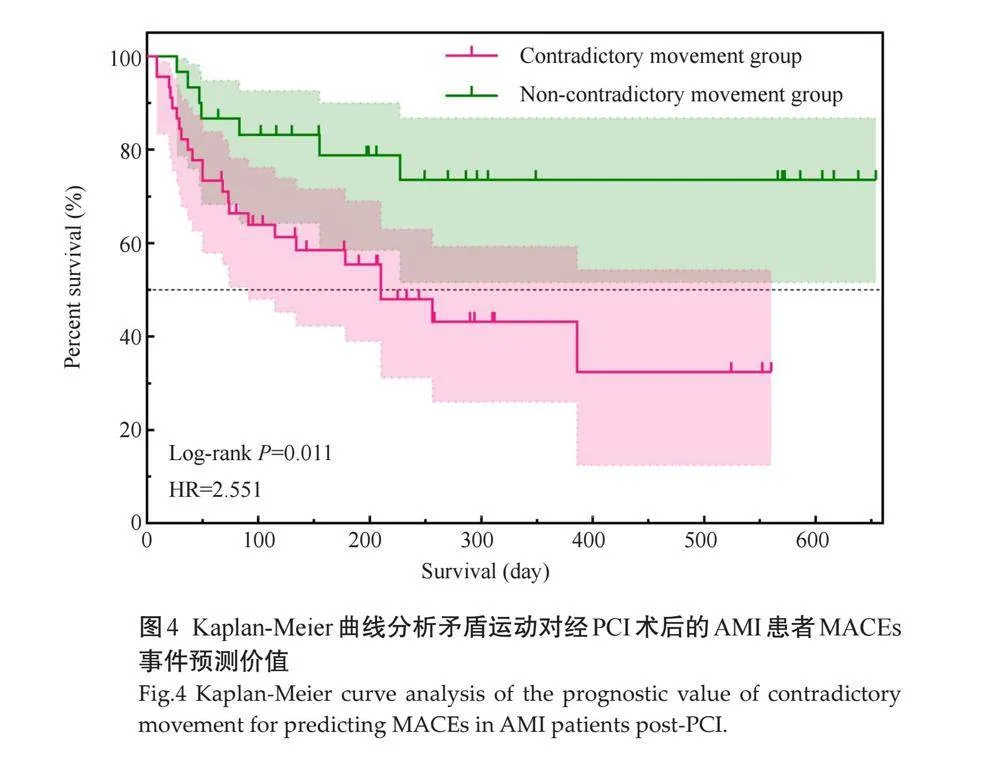
随访期间失访2人,总计MACEs事件发生率为40.00%。矛盾运动组MACEs事件发生率高于非矛盾运动组,其中心力衰竭发生率亦高于非矛盾运动组(Plt;0.05,表6)。多因素COX回归分析显示矛盾运动、纤维蛋白原、LGE%是AMI患者在接受罪犯血管血运重建后发生MACEs事件的独立危险因素(Plt;0.05,表7),K-M曲线显示,矛盾运动组患者较非矛盾运动组患者MACEs事件发生风险更高,是非矛盾运动组MACEs事件发生风险的2.551倍(P=0.011,图4)。
3 "讨论
AMI以其较高的死亡率和致残率备受医学界关注[11],难以早期识别AMI患者PCI术后并发症并及时予以针对性治疗是导致不良预后的一个重要因素[12]。CMR技术超越了传统的心脏彩超技术,受操作者主观影响较少,可重复性高,可通过无创检查完成对心脏结构、功能的检查与评价,是心脏疾病的诊断和评估的金标准之一,其搭载的组织追踪技术能够精确评估心肌的变形,检测疾病早期和治疗后心肌功能的变化,从而指导进一步的治疗[6]。
心肌应变作为心肌阶段位移的分数,可沿纵向、周向、径向3轴测量,精确量化心肌的局部运动异常,较传统指标LVEF更能敏感地反映心肌功能变化[13-15]。心肌纤维多层次、多方向分布于心内膜下层、心肌中层和心外膜下层,对应主导纵向应变、周向应变及径向应变,使心脏各个方向上协调收缩[16, 17]。通过CMR组织追踪测量心脏整体与梗死区域的应变,多层面评估心肌及心脏功能,对于识别术后不良结局的高风险患者具有重要价值。心肌应变与左室容积参数之间存在关联[18, 19],其中整体纵向应变是预测AMI患者MACEs事件的独立危险因素[20, 21]。既往研究主要通过应变成像技术,从径向、环向和纵向角度定量评估心肌应变功能,以识别和评估心肌病变的严重程度。然而,心肌应变不良包括应变降低和应变不协调两方面:应变降低反映心肌收缩力减弱或纤维化等直接损伤,而应变不协调则与电传导障碍或局部病变相关,表现为心肌收缩的时间差异。早期矛盾运动是应变不协调的极端形式,指受损心肌在收缩期反常扩张。本研究以此为切入点,探讨其与AMI患者PCI术后临床特征、风险分层及预后的相关性。
AMI患者心肌缺血坏死可致局部心肌应变受损,严重时引起心肌矛盾运动[22]。心肌的局部运动减弱、无运动或矛盾运动等现象,均可导致相应节段的心肌应变值出现下降,甚至产生反向应变,这反映了心肌功能受损的严重程度。左心室不同步性作为AMI后的一种重要并发症,研究表明其与梗死后心力衰竭和死亡发生独立相关[23],但心脏核磁下发现的早期矛盾运动现象与AMI患者临床特征及临床预后之间的关系鲜有研究。区别于通过不同步指数间接反映心脏部分节段相反运动的机械不同步性,本研究采用方向性应变量化法,量化左室心肌在不同方向上的形变,直接呈现收缩与舒张过程中应变的正负值,从而更直观地判断早期矛盾运动现象。在心功能方面,本研究中早期矛盾运动组左LVESVi高于非矛盾运动组,而LAEF、LVEF低于非矛盾运动组;在心肌应变评估上,早期矛盾运动组整体径向应变、整体周向应变、整体纵向应变、梗死节段径向应变、梗死节段周向应变、梗死节段纵向应变均低于非矛盾运动组;从预后预测的角度,较之非矛盾运动组,矛盾运动组MACEs事件发生率,尤其是心力衰竭发生率明显增高;再发心绞痛、心源性死亡及全因死亡亦有增高趋势,但差异无统计学意义,考虑可能与观察例数较少,随访时间较短等因素有关。伴随CMR的逐渐推广,通过CMR组织追踪检测到的早期矛盾运动现象为临床医生及早识别经PCI术后的AMI患者不良预后高危人群提供了新的参考依据,利于展开个性化治疗,从而降低不良心血管事件的发生率。
AMI患者即使在心外膜大血管成功开通后,由于前小动脉和微小血管的变化,约半数AMI患者仍会遭受MVO[24]。CMR晚期延迟强化技术能够直接检测AMI患者的梗死心肌位置、范围及透壁程度,从而反映心肌功能[25]。既往研究表明MVO亦有较高的预测MACEs事件的价值[26]。本研究发现矛盾运动组LGE%、MVO容积高于非矛盾运动组,其中单因素逻辑回归提示MVO容积为矛盾运动的危险因素。尽管本研究在MVO方面的结果与既往研究部分相符,但通过早期矛盾运动现象,本研究从另一个角度为MVO与AMI患者PCI术后不良预后的相关性提供了新的见解:早期矛盾运动和MVO可能共同影响此类患者预后。这一观点在既往研究中尚未得到充分探讨,有待未来通过构建评分模型进行进一步分析。
冠心病发病机制尚未完全清晰,炎症机制在其中扮演关键角色。既往研究表明,NLR、PLR可评估AMI患者不良预后[27-29]。本研究发现矛盾运动组的NLR高于非矛盾运动组,淋巴细胞计数低于非矛盾运动组,多因素逻辑回归及多因素COX回归分析进一步发现在PCI术后AMI患者中,NLR是出现早期矛盾运动的独立危险因素之一,且合并早期矛盾运动患者预后较差,提示炎症程度与早期矛盾运动可能存在一定相关性。后续可以通过结构方程模型等方法进一步验证炎症程度与早期矛盾运动现象的关系,从而构建更贴近真实世界的多模态数据,以期为评估预后和促进早期疾病干预的评分模型提供有力支持。
本研究的局限性在于:本研究为单中心、回顾性、小样本研究,所得结论仍有待后续更大规模、多中心、前瞻性研究确证;本研究MACEs事件发生率较高,可能与多支病变患者较多,预期2次血运重建及其之前的心绞痛等事件没有剔除等因素有关,因而存在一定局限性;心肌应变能力的下降并非是AMI严重程度、左室功能下降的唯一因素,本文并未纳入心肌应变率、心肌扭转角度等磁共振参数进一步研究;通过多因素分析消除混杂因素影响,无法完全排除选择偏倚。
综上所述,与非矛盾运动组相比,矛盾运动组患者的BNP、NLR、LGE%、LVESVi、微循环障碍容积升高,而淋巴细胞计数、LAEF、LVEF、心肌梗死节段应变和整体心肌应变显著均降低。NLR、梗死节段周向应变、整体纵向应变是矛盾运动的独立预测因素;矛盾运动组MACEs事件发生率明显高于非矛盾运动组,其中矛盾运动、纤维蛋白原、LGE%是AMI患者在接受罪犯血管血运重建后发生MACEs临床事件的独立危险因素。未来可充分运用CMR技术实现“病理影像化”,进一步深入探讨AMI后的矛盾运动现象,为患者制定更加个性化、精准的治疗方案,达到改善患者预后的目的。
参考文献:
[1] " Hu SS. Epidemiology and current management of cerebrovascular disease in China[J]. J Geriatr Cardiol, 2024, 21(5): 465-74.
[2] " Yan Y, Guo JC, Wang X, et al. Postprocedural anticoagulation after primary percutaneous coronary intervention for ST‑segment-elevation myocardial infarction: a multicenter, randomized, double-blind trial[J]. Circulation, 2024, 149(16): 1258-67.
[3] " 中华医学会超声医学分会超声心动图学组, 中国医师协会心血管分会超声心动图专业委员会. 超声心动图评估心脏收缩和舒张功能临床应用指南[J]. 中华超声影像学杂志, 2020, 29(6): 461-77.
[4] " Marcos-Garcés V, Perez N, Gavara J, et al. Risk score for early risk prediction by cardiac magnetic resonance after acute myocardial infarction[J]. Int J Cardiol, 2022, 349: 150-4.
[5] " Lange T, Backhaus SJ, Schulz A, et al. Cardiovascular magnetic resonance‑derived left atrioventricular coupling index and major adverse cardiac events in patients following acute myocardial infarction[J]. J Cardiovasc Magn Reson, 2023, 25(1): 24.
[6] " Sun Z, Wang Y, Hu YY, et al. Left ventricular dyssynchrony measured by cardiovascular magnetic resonance-feature tracking in anterior ST‑elevation myocardial infarction: relationship with microvascular occlusion myocardial damage[J]. Front Cardiovasc Med, 2023, 10: 1255063.
[7] " Correction to: 2023 ESC Guidelines for the management of acute coronary syndromes: developed by the task force on the management of acute coronary syndromes of the European Society of Cardiology (ESC)[J]. Eur Heart J, 2024, 45(13): 1145.
[8] " Smith SC Jr, Dove JT, Jacobs AK, et al. ACC/AHA guidelines for percutaneous coronary intervention (revision of the 1993 PTCA guidelines)-executive summary: a report of the American College of Cardiology/American Heart Association task force on practice guidelines (Committee to revise the 1993 guidelines for percutaneous transluminal coronary angioplasty) endorsed by the Society for Cardiac Angiography and Interventions[J]. Circulation, 2001, 103(24): 3019-41.
[9] " Gensini GG. A more meaningful scoring system for determining the severity of coronary heart disease[J]. Am J Cardiol, 1983, 51(3): 606.
[10] Cerqueira MD, Weissman NJ, Dilsizian V, et al. Standardized myocardial segmentation and nomenclature for tomographic imaging of the heart. A statement for healthcare professionals from the Cardiac Imaging Committee of the Council on Clinical Cardiology of the American Heart Association[J]. Circulation, 2002, 105(4): 539-42.
[11] "Martin SS, Aday AW, Almarzooq ZI, et al. 2024 heart disease and stroke statistics: a report of US and global data from the American heart association[J]. Circulation, 2024, 149(8): e347-913.
[12] "Moroni F, Seth M, Changezi HU, et al. Cause and preventability of in‑hospital mortality after PCI: a statewide root‑cause analysis of 1, 163 deaths[J]. PLoS One, 2024, 19(3): e0297596.
[13] Lange T, Gertz RJ, Schulz A, et al. Impact of myocardial deformation on risk prediction in patients following acute myocardial infarction[J]. Front Cardiovasc Med, 2023, 10: 1199936.
[14] "Schäfer M, Mitchell MB, Frank BS, et al. Myocardial strain-curve deformation patterns after Fontan operation[J]. Sci Rep, 2023, 13(1): 11912.
[15] "Smiseth OA, Donal E, Boe E, et al. Phenotyping heart failure by echocardiography: imaging of ventricular function and haemodynamics at rest and exercise[J]. Eur Heart J Cardiovasc Imaging, 2023, 24(10): 1329-42.
[16] "Moraru L, Mirea O, Toader D, et al. Lower limit of normality of segmental multilayer longitudinal strain in healthy adult subjects[J]. J Cardiovasc Dev Dis, 2024, 11(4): 102.
[17] "Isaak A, Kravchenko D, Mesropyan N, et al. Layer-specific strain analysis with cardiac MRI feature tracking in acute myocarditis[J]. Radiol Cardiothorac Imaging, 2022, 4(3): e210318.
[18] "Hao YH, Zhang R, Chen LH, et al. Distinguishing heart failure subtypes: the diagnostic power of different cardiac magnetic resonance imaging parameters[J]. Front Cardiovasc Med, 2024, 11: 1291735.
[19] "Tang HS, Kwan CT, He JL, et al. Prognostic utility of cardiac MRI myocardial strain parameters in patients with ischemic and nonischemic dilated cardiomyopathy: a multicenter study[J]. AJR Am J Roentgenol, 2023, 220(4): 524-38.
[20] Kumar D, Saha M, Guha S, et al. Strain imaging as an early predictor in acute myocardial infarction‑An augmented cross-sectional study[J]. Indian Heart J, 2024, 76(1): 31-5.
[21] "Lenell J, Lindahl B, Erlinge D, et al. Global longitudinal strain in long‑term risk prediction after acute coronary syndrome: an investigation of added prognostic value to ejection fraction[J]. Clin Res Cardiol, 2024. doi: 10.1007/s00392-024-02439-w.
[22] "李妙男, 丁丝雨, 姚卓亚, 等. 心脏磁共振可评估急性心肌梗死患者的早期心功能状态[J]. 分子影像学杂志, 2023, 46(4): 620-6.
[23] "Shin SH, Hung CL, Uno H, et al. Mechanical dyssynchrony after myocardial infarction in patients with left ventricular dysfunction, heart failure, or both[J]. Circulation, 2010, 121(9): 1096-103.
[24] "Gräni C, Stark AW, Fischer K, et al. Diagnostic performance of cardiac magnetic resonance segmental myocardial strain for detecting microvascular obstruction and late gadolinium enhancement in patients presenting after a ST-elevation myocardial infarction[J]. Front Cardiovasc Med, 2022, 9: 909204.
[25]Hundley WG, Bluemke DA, Bogaert J, et al. Society for Cardiovascular Magnetic Resonance (SCMR) guidelines for reporting cardiovascular magnetic resonance examinations[J]. J Cardiovasc Magn Reson, 2022, 24(1): 29.
[26] Feng X, Xu YS, Zeng M, et al. Optical coherence tomography assessment of coronary lesions associated with microvascular dysfunction in ST-segment elevation myocardial infarction[J]. Circ J, 2023, 87(11): 1625-32.
[27] "Liu J, Ao W, Zhou JW, et al. The correlation between PLR‑NLR and prognosis in acute myocardial infarction[J]. Am J Transl Res, 2021, 13(5): 4892-9.
[28] Jin ZQ, Wu Q, Chen SH, et al. The associations of two novel inflammation indexes, SII and SIRI with the risks for cardiovascular diseases and all-cause mortality: a ten-year follow-up study in 85, 154 individuals[J]. J Inflamm Res, 2021, 14: 131-40.
[29] "Gao Y, Li YQ, Chen XL, et al. The systemic inflammation index predicts poor clinical prognosis in patients with initially diagnosed acute coronary syndrome undergoing primary coronary angiography[J]. J Inflamm Res, 2023, 16: 5205-19.
(编辑:熊一凡)
收稿日期:2024-06-28
基金项目:国家自然科学基金(81970313);安徽省临床医学转化专项(202304295107020086);安徽省教育厅自然科学研究重点项目(2022AH051477);蚌埠医学院第一附属医院2022年度高新技术(2022050);512人才培育计划(by51201317)
Supported by National Natural Science Foundation of China (81970313)
作者简介:丁 "斌,住院医师,在读硕士研究生,E-mail: 1395720713@qq.com
通信作者:李妙男,副主任医师,副教授,博士,E-mail: 13855265385@163.com;王洪巨,主任医师,教授,博士生导师,E-mail: hongjuwang1@sina.com
