放射性碘125粒子植入联合程序性死亡受体-1单抗加化疗治疗中晚期非小细胞肺癌效果及对患者免疫功能的影响
2024-08-09马建增曹文丽唐乃玲任守雷
【摘要】目的 探讨放射性碘125粒子植入联合程序性死亡受体-1(PD-1)单抗加化疗治疗中晚期非小细胞肺癌(NSCLC)患者的效果,并分析其对患者免疫功能的影响,为临床提供参考。方法 选取2022年10月至2023年10月阳光融和医院收治的40例中晚期NSCLC患者为研究对象,按照随机数字表法分为对照组(20例)和观察组(20例),予以对照组患者PD-1单抗联合化疗治疗,予以观察组患者碘125粒子植入、PD-1单抗联合化疗治疗。比较两组患者疗效、免疫指标[CD3+、CD4+、CD8+T淋巴细胞百分比和CD4+/CD8+比值、免疫球蛋白(Ig)A、IgG]水平、卡诺夫斯基健康状况评分量表(KPS)评分和不良反应发生情况。结果 观察组患者客观有效率高于对照组(P<0.05)。两组患者治疗后CD8+T淋巴细胞百分比均降低,CD3+、CD4+T淋巴细胞百分比、CD4+/CD8+比值均升高,且观察组CD8+T淋巴细胞百分比低于对照组,CD3+、CD4+T淋巴细胞百分比、CD4+/CD8+比值均高于对照组(均P<0.05);组间IgA、 IgG 水平比较,差异无统计学意义(P>0.05)。治疗后,两组患者KPS评分均升高,且观察组高于对照组(P<0.05)。两组患者不良发应总发生率比较,差异无统计学意义(P>0.05)。结论 中晚期NSCLC患者接受碘125粒子植入、PD-1单抗联合化疗方案治疗可获得较高的有效性和安全性,并能改善免疫功能,提高其生存质量。
【关键词】放射性碘125粒子植入;程序性死亡受体-1;化疗;非小细胞肺癌;免疫功能
【中图分类号】R734.2 【文献标识码】A 【文章编号】2096-2665.2024.13.0035.04
DOI:10.3969/j.issn.2096-2665.2024.13.012
肺癌是常见恶性肿瘤之一,其中约80%为非小细胞肺癌(non-small cell lung cancer,NSCLC),由于早期无特异性症状,确诊时多为中、晚期,且超半数患者已不满足手术切除指征[1]。程序性死亡受体-1(PD-1)单抗是一种免疫治疗药物,能够阻断肿瘤细胞表面的PD-1受体与免疫细胞上的程序性死亡配体-1(PD-L1)之间的相互作用,从而激活免疫细胞攻击肿瘤细胞。化疗则是一种通过使用化学药物杀死肿瘤细胞的方法。虽然治疗中晚期NSCLC的药物不断更新迭代,传统治疗也在不断优化,但耐药、病情进展仍不可避免,故而探索联合用药十分必要。放射性碘125粒子植入通过植入肿瘤组织内的放射性粒子持续发射低剂量γ射线,对肿瘤细胞进行持续照射和杀伤。基于此,本研究探讨放射性碘125粒子植入联合PD-1单抗加化疗治疗中晚期NSCLC患者的效果,现报道如下。
1 资料与方法
1.1 一般资料 选取2022年10月至2023年10月阳光融和医院收治的40例中晚期NSCLC患者为研究对象,按照随机数字表法分为对照组(20例)和观察组(20例)。对照组患者中男性11例,女性9例;年龄52~70岁,平均年龄(59.24±5.76)岁;BMI 20~28 kg/m2,平均BMI(23.66±3.26)kg/m2;类型:腺癌10例,鳞状细胞癌10例;TNM分期[2]:Ⅲ期9例,Ⅳ期11例。观察组患者中男性12例,女性8例;年龄50~70岁,平均年龄(59.72±6.13)岁;BMI 18~27 kg/m2,平均BMI(23.45±3.16)kg/m2;类型:腺癌11例,鳞状细胞癌9例;TNM分期:Ⅲ期8例,Ⅳ期12例。两组患者一般资料比较,差异均无统计学意义(均P>0.05),组间具有可比性。本研究经阳光融和医院医学伦理委员会批准,患者及其家属均知情并签署知情同意书。纳入标准:⑴符合中晚期NSCLC的诊断标准[3],并经细胞学确诊;⑵伴远端转移或侵犯邻近器官而无法手术者;⑶预计生存时间≥3个月。排除标准:⑴伴有其他恶性肿瘤者;⑵合并肺栓塞、深静脉血栓者;⑶伴有神经系统疾病者;⑷对研究使用药物过敏、不耐受者。
1.2 治疗方法 对照组患者采用PD-1单抗加化疗。⑴化疗:每个化疗周期的第1天、第8天将25 mg/m2酒石酸长春瑞滨注射液(江苏豪森药业集团有限公司,国药准字H19990278,规格:1 mL∶10 mg)溶于125 mL的0.9%氯化钠溶液,在15~20 min内静脉滴注完成;第1天将60 mg/m2顺铂注射液(江苏豪森药业集团有限公司,国药准字H20040813,规格:6 mL∶30 mg)溶于250~500 mL的5%葡萄糖注射液中静脉滴注;或TP方案,第1天静脉滴注135~175 mg/m2紫杉醇注射液(无锡紫杉药业股份有限公司,国药准字H20067345,规格:5 mL∶30 mg),用0.9%氯化钠溶液或5%葡萄糖注射液稀释至0.3~1.2 mg/mL静脉滴注3 h,60 mg/m2顺铂用法同上。21 d为1个周期。⑵PD-1治疗:在化疗前30 min将200 mg信迪利单抗注射液[信达生物制药(苏州)有限公司,国药准字S20180016,规格:100 mg(10 mL)/瓶]用0.9%氯化钠溶液稀释至1.5~5.0 mg/mL,在30~60 min内静脉滴注完,1次/3周。观察组患者采用放射性碘125粒子植入联合PD-1单抗加化疗。碘125粒子植入:行X线计算机体层摄影成像系统(CT)(以色列通用电气医疗影像系统有限公司,国械注进20143065340,型号:Discovery NM/CT 670 Pro)增强扫描,将图像传送至放射性粒子治疗计划系统(TPS)(珠海和佳医疗设备股份有限公司,国械注准20183701716,型号:HGGR-2000),水平切面确定目标靶区(PTV),确定90%的PTV接受剂量(D90),PTV包括肿瘤总体积(GTV)及其边缘0.5~1.0 cm范围区域。PTV处方剂量为80~140 Gy,D90剂量为76~138 Gy。碘125粒子适度范围0.40~0.80 mCi,用量根据病灶大小和TPS系统计算。碘125粒子植入:局部麻醉,CT引导定位进针方向,穿刺病灶内0.5 cm处,植入碘125粒子[原子高科股份有限公司,国药准字H20045969,规格:11.1~37 MBq(0.3~1.0 mCi)],均匀分布在病灶内,1.0~1.5 cm3分布1个粒子,完成后行CT扫描,输入TPS验证剂量,若发现缺漏则补植。化疗和PD-1治疗均在碘125粒子植入后2周内开始,使用方法和剂量均同对照组一致。治疗期间密切关注患者病情、耐受情况,酌情调整用药,两组患者均在连续治疗2个化疗周期后评估疗效。
1.3 观察指标 ⑴比较两组患者疗效。根据实体瘤疗效评价标准(RECIST1.1)[4]评价,分为完全缓解(CR):病灶消失,维持时间≥4周;部分缓解(PR):病灶缩小≥50%,维持时间≥4周;疾病稳定(SD):病灶缩小<50%或增大≤25%;疾病进展(PD):病灶增大>25%或出现新病灶。客观有效率=[(CR+PR)例数/总例数]×100%;疾病控制率=[(CR+PR+SD)例数/总例数]×100%。⑵比较两组患者免疫指标水平。治疗前、治疗2个周期后,抽取患者肘静脉血5 mL,抗凝后用流式细胞仪[安捷伦生物(杭州)有限公司,浙械注准20192220121,型号:NovoCyte D2040R]检测T淋巴细胞亚群(CD3+、CD4+、CD8+T淋巴细胞百分比)水平,并计算CD4+/CD8+比值;另抽取患者肘静脉血 5 mL,以转速为3 000 r/min离心15 min(半径为13 cm),分离血清,采用酶联免疫吸附法检测免疫球蛋白(Ig)A、IgG水平。⑶比较两组患者生存质量。治疗前、治疗2个周期后,采用卡诺夫斯基健康状况评分量表(KPS)[5]进行评定,分值范围为0~100分,评分越高表示患者生存质量越好。⑷比较两组患者不良反应发生情况。不良反应包括恶心呕吐、腹泻腹痛、皮疹、骨髓抑制和白细胞减少。不良反应总发生率=各项不良反应发生例数/总例数×100%。
1.4 统计学分析 采用SPSS 22.0统计学软件进行数据处理。计数资料以[例(%)]表示,采用χ2检验,等级资料比较采用秩和检验;计量资料以(x)表示,采用t检验。以P<0.05为差异有统计学意义。
2 结果
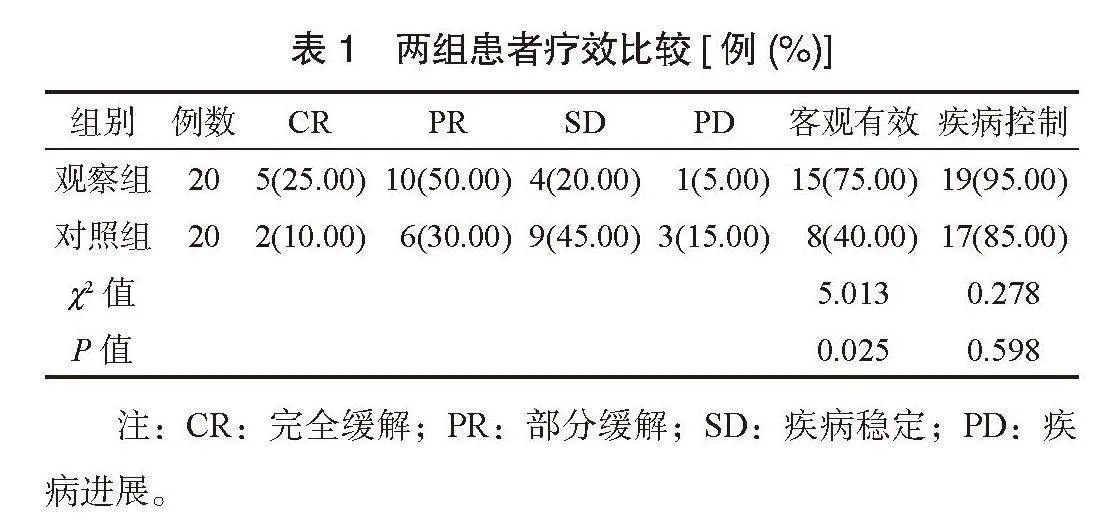
2.1 两组患者疗效比较 观察组患者客观有效率高于对照组,差异有统计学意义(P<0.05);两组患者疾病控制率比较,差异无统计学意义(P>0.05),见表1。
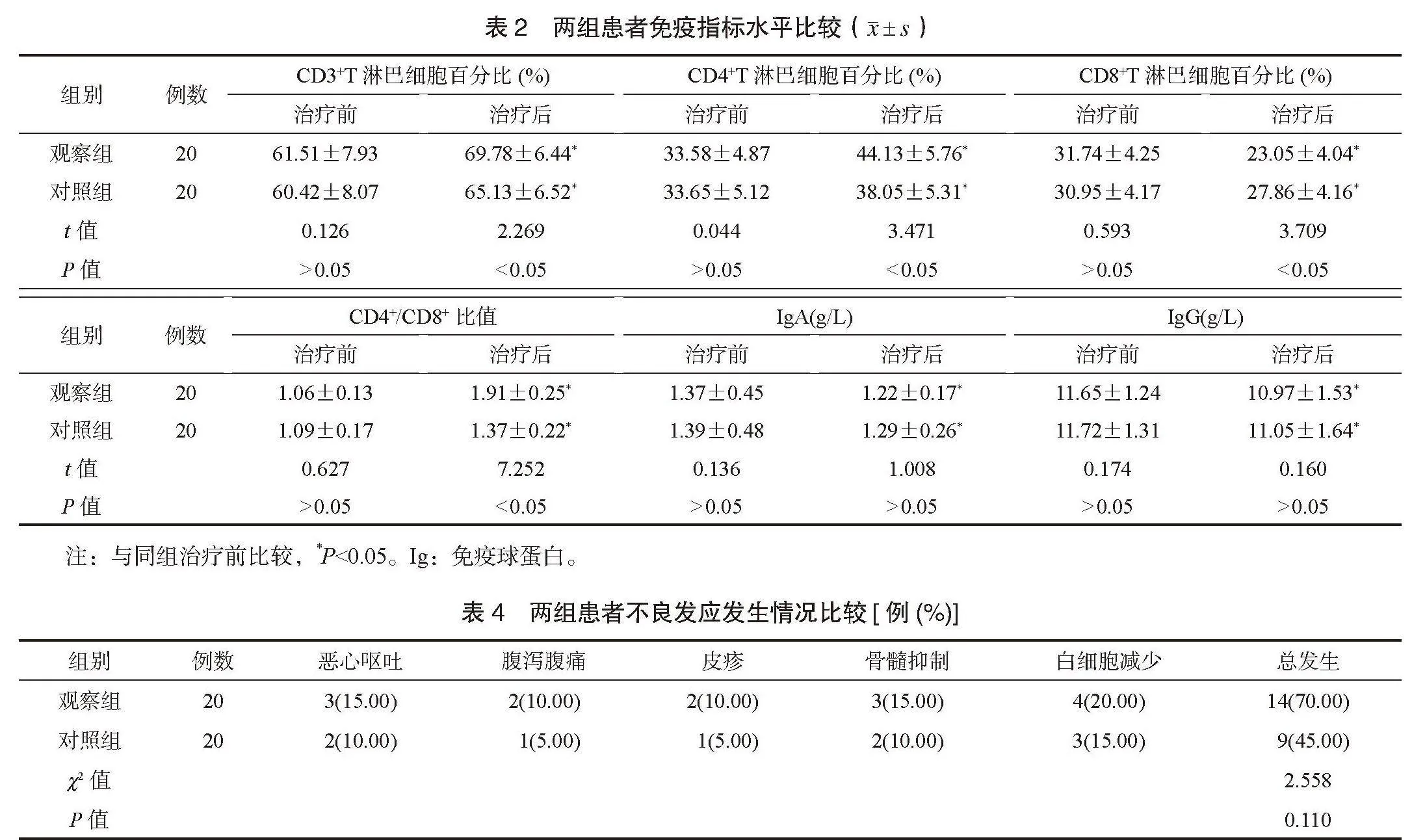
2.2 两组患者免疫指标水平比较 治疗前,两组患者T淋巴细胞亚群和IgA、IgG水平比较,差异均无统计学意义(P>0.05);两组患者治疗后CD8+T淋巴细胞百分比均降低,CD3+、CD4+T淋巴细胞百分比、CD4+/CD8+比值均升高,且观察组CD8+T淋巴细胞百分比低于对照组,CD3+、CD4+T淋巴细胞百分比、CD4+/CD8+比值均高于对照组,差异均有统计学意义(均P<0.05),组间IgA、 IgG 水平比较,差异无统计学意义(P>0.05),见表2。
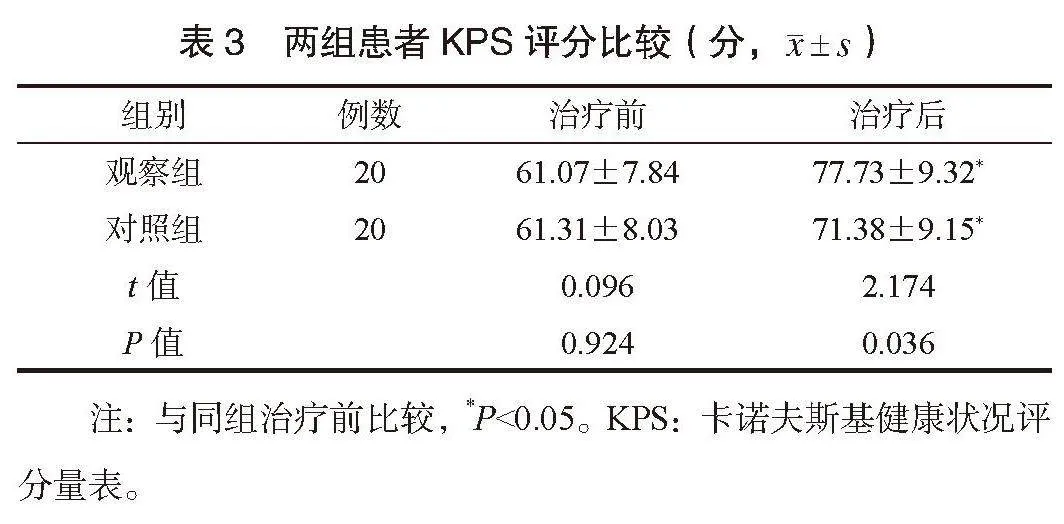
2.3 两组患者KPS评分比较 治疗前,两组患者KPS评分比较,差异均无统计学意义(P>0.05);两组患者治疗后KPS评分均升高,且观察组高于对照组,差异有统计学意义(P<0.05),见表3。
2.4 两组患者不良发应发生情况比较 两组患者不良发应总发生率比较,差异无统计学意义(P>0.05),见表4。
3 讨论
NSCLC患者早期基本无症状,多数患者确诊时已错过了最佳治疗时间,并且患者病灶容易发生转移,病死率较高。化疗曾是延长患者生存期的唯一方法,如今PD-1抑制剂已成为临床应用研究热点,而放疗联合PD-1单抗治疗可提高治疗效果和延长生存期[6]。碘125粒子植入是体内放疗方式,用于治疗宫颈癌、前列腺癌等均有良好效果,已广泛用于肺癌的治疗中,但碘125粒子植入是局部疗法,无法控制远端病灶,化疗可对远处病灶进行干预[7]。有研究显示,碘125粒子植入联合化疗对NSCLC患者免疫功能有明显影响,导致治疗效果不够理想[8]。故本研究将3种方式进行联合治疗,探讨该方案的效果。
本研究结果显示,观察组患者客观有效率高于对照组,但两组患者疾病控制率比较,差异无统计学意义,提示碘125粒子植入、PD-1单抗联合化疗联合方案在改善患者的效果更好。同时,本研究结果还显示,两组患者治疗后CD8+T淋巴细胞百分比均降低,CD3+、CD4+T淋巴细胞百分比、CD4+/CD8+比值均升高,且观察组上述指标改善情况均优于对照组;组间IgA、 IgG 水平比较,差异无统计学意义,提示联合方案可调节T淋巴细胞亚群水平,增强细胞免疫能力,但两组患者治疗前后IgA、IgG水平均无明显改变,说明两种治疗方式对肿瘤患者体液免疫功能影响小。临床研究已证实,同步放化疗可提高疾病控制和生存率,碘125粒子和化疗药物联用可增强放射性,化疗药物经血液途径杀灭肿瘤细胞,减少其远端转移,控制局部或全身病症;同时粒子植入让局部放射量增强,并可精准控制,在确保耐受同时提高疗效,但碘粒子植入联合化疗会抑制NSCLC患者免疫功能[9]。而PD-1单抗可阻断PD-1结合配体,致使调节性T细胞增加,免疫功能提高,诱导肿瘤细胞死亡,缓解免疫抑制状态[10]。
本研究结果显示,治疗2个周期后,观察组患者KPS评分高于对照组,两组患者不良反应发生率比较,差异无统计学意义,提示联合治疗方案可显著提高中晚期NSCLC患者生存质量,且,安全性良好。有研究发现,碘125粒子植入可延长复发或转移Ⅲ/Ⅳ期NSCLC患者的无进展生存率和总生存时间[11]。吴春蓉等[12]研究表明,化疗联合碘125粒子植入疗效好,PFS更长,也未有严重并发症,在改善患者生活质量和缓解病症上有明显优势。而PD-1单抗可通过阻断PD-1/PD-L1通路,激活免疫系统,促进内源性抗肿瘤效应增强,保持免疫内环境稳定,从而延长患者生存期。本研究比较两组患者不良反应发生率,发现组间差异不明显。这可能与碘125粒子半衰期长、可精准定位病灶内部有关,其可嵌入肿瘤内部直接作用,放射剂量也会随着扩散快速降低,可保证周围组织安全,毒性较低,对周围组织损伤较小;而PD-1单抗具有毒性小、药效持久的优势[13-14]。故碘125粒子植入可安全、有效提高免疫治疗效果,但碘125粒子与PD-1单抗间相互刺激、增敏作用尚需进一步试验研究。
综上所述,碘125粒子植入、PD-1单抗联合化疗治疗方案能缓解中晚期NSCLC患者病情,提高患者免疫功能、生存质量,安全性良好。
参考文献
阿米娜·苏建和,艾力·苏. 肺癌不同病理类型发病率的变化情况及其原因[J/CD]. 临床医药文献电子杂志, 2018, 5(22): 195.
王嘉,吴楠,吕超,等.国际抗癌联盟(UICC)第8版肺癌分期方案的验证[J].中国肿瘤临床, 2020, 47(10): 487-491.
中华医学会肿瘤学分会,中华医学会杂志社.中华医学会肿瘤学分会肺癌临床诊疗指南(2021版)[J].中华肿瘤杂志, 2021, 43(6): 591-621.
EISENHAUER E A, THERASSE P, BOGAERTS J, et al. New response evaluation criteria in solid tumours: Revised RECIST guideline (version 1. 1).[J]. European Journal of Cancer, 2009, 45(2): 228-247.
谭诗生,李杭,罗健,等.欧洲癌症研究与治疗组织研制的生活质量核心调查问卷第3版中文版生活质量调查问卷测评[J].中国临床康复, 2006, 10(4): 23-27.
杜欢,童亚兰,王敏. 2015年至2019年山西地区非小细胞肺癌流行病学特征及预后影响因素分析[J].肿瘤研究与临床, 2022, 34(1): 47-50.
李虎子,赵成,贺斌,等. 125I放射性粒子植入联合化疗治疗ⅢB期非小细胞肺癌的临床疗效及预后因素分析[J].介入放射学杂志, 2021, 30(7): 687-692.
熊潭有,梅同华. 125I粒子植入联合化疗治疗晚期肺癌疗效观察并预后分析[J].重庆医学, 2020, 49(3): 375-378.
袁鹏,李文会,岳天华,等.放射性125I粒子植入配合放化疗治疗非小细胞肺癌的疗效及对肿瘤标志物的影响[J].临床内科杂志, 2022, 39(3): 189-191.
义维丽,赵文成,黄东宁,等. PD-1单抗治疗非小细胞肺癌相关不良反应及其与疗效的相关性分析[J].中国癌症杂志, 2021, 31(3): 203-211.
李展,门翔,孙辉,等. 125I粒子植入术联合同步放化疗治疗局部晚期非小细胞肺癌的疗效[J].癌症进展, 2022, 20(6): 577-580.
吴春蓉,李波,向德兵,等.碘-125粒子植入近距离放疗联合化疗治疗老年晚期非小细胞肺癌的临床研究[J].广西医学, 2020, 42(19): 2487-2491.
王静宜,张媛媛,李小青,等.碘125粒子植入联合PD-1单抗加含铂化疗在晚期非小细胞肺癌中的有效性及安全性分析[J].重庆医学, 2023, 52(13): 1999-2004.
沈艳丽,李金金,陈献亮. 碘125粒子植入联合PD-1单抗加含铂化疗治疗晚期非小细胞肺癌的有效性及安全性[J]. 中国实用医刊, 2023, 50(23): 5-9.
基金项目:潍坊市卫生健康委员科研项目(编号:WFWSJK-2022-282)
作者简介:马建增,硕士研究生,主治医师,研究方向:肿瘤学。
通信作者:任守雷,硕士研究生,副主任医师,研究方向:肿瘤综合治疗。E-mail:rsl-boy-119@163.com
