达格列净中特定杂质分析及稳定性研究
2024-06-03范祥元杜陈侠
范祥元 杜陈侠
摘 要:为建立达格列净中的特定杂质DGL301分析方法,采用十四酸丙酰胺基团键合硅胶为填充剂(Poroshell 120Bonus-RP,100 mm×4.6 mm,2.7 μm或效能相当的色谱柱);流动相A:0.085%的磷酸水溶液;流动相B:乙腈;控制体积流量为1.0 mL/min进行梯度洗脱;检测波长为225 nm;柱温为25℃;进样体积10 μL。在优化的色谱条件下,主峰、特定杂质DGL301及其他杂质分离度符合要求;特定杂质DGL301在0.16~0.79 μg/mL的浓度范围内,呈现良好的线性关系,回归方程为A =24.869 C+0.5787,r =0.9992,检测限为17.56 ng·mL-1,定量限为59.85 ng·mL-1,RSD=0.9%(n =6),平均回收率为98.37%(n =9)。本方法可用于达格列净中特定杂质DGL301的检测。
关键词:达格列净,特定杂质,高效液相色谱法
DOI编码:10.3969/j.issn.1002-5944.2024.05.036
0 引 言
达格列净原研企业为百时美施贵宝公司和阿斯利康公司,其为SGLT2抑制剂,于2012年12月在欧盟获批上市,临床适应证为2型糖尿病,国家药品监督管理局已批准国内上市的生产企业仅有3家。研究表明,达格列净降糖通过二个途径实现降糖作用[1-2]:第一,通过调节抑制肾脏对葡萄糖的重吸收作用,第二、通过增加肾脏对葡萄糖的排泄作用。通过文献检索发现,关于达格列净的研究方向主要集中在临床领域,针对达格列净杂质分析研究报告很少,截至投稿,国内外针对达格列净杂质分析公开发表的文章不足10篇[3-7]。研究人员通过对合成工艺的深入研究,将产生可能性最大的DGL301定为特定杂质,而此杂质在进口标准未进行控制,已发表的文献中也未对此杂质进行报道。本实验建立了达格列净杂质分析方法,试验结果表明,该方法准确度高、专属性强、重复性好,可作为达格列净原料药杂质评价方法。
1 仪器与试药
气相色谱仪;梅特勒XS105电子天平。
达格列净原料药(宣城美诺华药业有限公司,批号为DGBB-9-210901、DGBB-9-210902、DGBB-9-210903);DGL301对照品(批号07-APR-20-16-01,纯度97.8%),达格列净对照品(宣城美诺华药业有限公司自制,批号D009-200402KB)。
盐酸、氢氧化钠、30%过氧化氢为分析纯,乙腈为色谱纯,水为纯化水,其他试剂为分析纯。
2 方法与结果
2.1 色谱条件
色谱柱:Agilent In f inity L ab Poroshell120Bonus-RP(100 mm×4.6 mm,2.7 μm);流动相A:0.085%的磷酸水溶液;流动相B:乙腈;梯度洗脱;流速为1.0 mL /min;检测波长为225 nm;柱温为25℃;进样体积10 μL。
2.2 溶液制备
稀释剂∶乙腈∶水=50∶50(V/V)
杂质储备溶液:称取DGL301杂质对照品3 mg,取稀释液溶解并稀释至浓度为0.03 mg/mL杂质储备溶液。
系统适用性溶液:称取达格列净对照品15 mg及雜质DGL301储备溶液0.5 mL,取稀释液溶解并稀释至DGL301浓度为0.03 μg/mL杂质储备溶液(达格列净:0.03 μg/mL)。
标准溶液: 称取达格列净对照品15 mg,取稀释液溶解并稀释至浓度为0.03 μg/mL。
样品溶液: 在50 mL容量瓶中加入本品15 mg,加入稀释剂超声处理至完全溶解,定容至刻度,摇匀。平行配制2份。
2.3 系统适应性试验
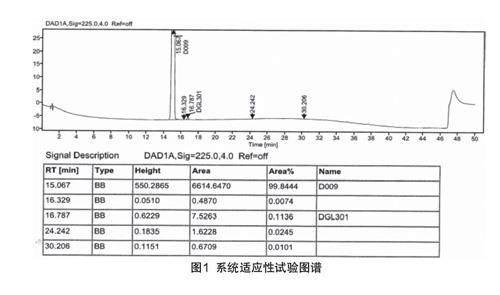
取系统适应性溶液按照规定的色谱条件进样,系统适应性试验图谱如图1所示。结果表明,主峰与杂质DGL301依次出峰,分离度为4.3,符合分析要求。
2.4 检测方法
测定法:精密量取供试品溶液和对照品溶液,分别注入液相色谱仪,记录色谱图。限度:按外标法以对照品溶液主峰峰面积计算,DGL不得大于0.10%,其他单个杂质不得大于0.10%,各杂质的和不得大于1.0%。供试品溶液色谱图中小于0.05%的杂质忽略不计。
2.5 专属性试验
(1)酸破坏。50 mL量瓶中加入精密称定的达格列净原料药15 mg(批号:DGBB-9-210901),移取1.0 mL盐酸溶液(浓度为5 mol/L)加入量瓶,摇匀后静置,调节水浴锅温度至60℃恒定,将其放置24小时后,取出并放至室温,加入1.0 mL氢氧化钠溶液(浓度为5 mol/L)作为中和试剂,加乙腈-水(50∶50)溶解并稀释至刻度,摇匀。
(2)碱破坏。50 mL量瓶中精密称定达格列净原料药15 mg(批号:DGBB-9-210901),移取1.0 mL氢氧化钠溶液(浓度为5 mol/L),摇匀后静置,调节水浴锅温度至60℃恒定,将其放置24小时后,取出并放至室温,加入1.0 mL盐酸溶液(浓度为5 mol/L)作为中和试剂,加乙腈-水(50∶50)溶解并稀释至刻度,摇匀。
(3)氧化破坏。50 mL量瓶中精密称定达格列净原料药(批号:DGBB-9-210901)15mg,加入30%过氧化氢,室温条件下放置24小时,加乙腈-水(50:50)溶解并稀释至刻度,摇匀。
(4)高温破坏。50 mL量瓶中精密称定达格列净原料药15 mg(批号:DGBB-9-210901),置50 mL量瓶中,加乙腈-水(50∶50)30 mL使溶解,调节水浴锅温度至60℃恒定,将其放置24小时后,取出并放至室温,加乙腈-水(50∶50)稀释至刻度,摇匀。
(5)光照破坏 。50 mL量瓶中精密称定达格列净原料药(批号:DGBB-9-210901)15 mg,加乙腈-水(50∶50)溶解并稀释至刻度,摇匀,于4500 Lx光照条件下放置3天。
精密量取上述溶液,分别注入液相色谱仪。结果显示,DGL301在高温、酸、碱等条件下均能与主峰及降解产物实现有效分离,此方法可以用于特征杂质DGL301的测定。
2.6 线性和范围
精密量取标准溶液和DGL301对照品贮备液,用乙腈-水(50∶50)逐步稀释,制成不同浓度的混合溶液作为系列线性溶液。
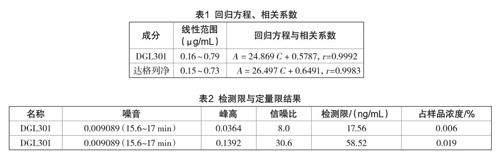
精密量取上述溶液各10 μL注入液相色谱仪,记录色谱图。结果见表1。
2.7 校正因子
对表3 中的数据进行计算的到特定杂质DGL301的校正因子为1.07。
2.8 检测限与定量限
取标准溶液及特定杂质DGL301储备溶液,用乙腈-水(50∶50)逐级稀释,计算结果见表2。
2.9 精密度试验
2.9.1 重复性
按照“2 . 2”项规定,制备6 份平行样,按照“2.1”项下规定的色谱条件检测,考察6份加标样品溶液中各杂质测试结果的相对标准偏差,RSD为0.9%,结果表明重复性好。
2.9.2 中间精密度
另一人按照“2. 2”项规定,制备6份平行样,按照“2.1”项下规定的色谱条件检测。计算2未测定人员中间精密度相对标准偏差R SD(n =12)为1.13%,因此,该分析方法具有良好的中间精密度。
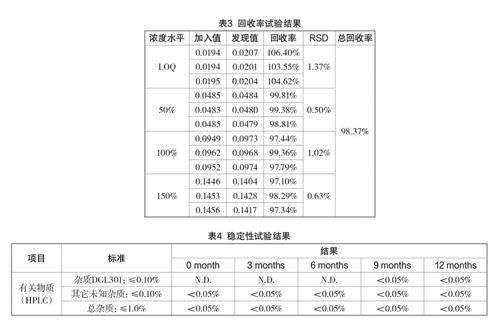
2.10 加样回收率(见表3)
从上述结果分析,在LOQ~150%浓度水平下,DGL301在各浓度下3份加标样品溶液中的回收率和回收率的相对标准偏差均在可接受标准范围内。
2.11 溶液的稳定性试验
标准溶液在常温下放置不同时间,0小时,5小时,10小时…25小时,48小时,比较不同时间点样品溶液和加标样品溶中各杂质结果与初始结果的绝对差异值,以及不同时间点标准溶液中主峰峰面积的相对偏差,结果总杂含量的RSD为6.08%,表明溶液在测试条件下稳定性良好。
2.12 耐用性试验
本试验考察了流速、检测波长、流动相比例对测定结果的影响。从结果来看,流动相中磷酸比例(±0.01%)、流速(±0.1 mL/min)、柱温(±2℃)、波长(±2 nm)的细微变化没有影响各杂质含量的检测,且满足可接受标准的要求。
2.13 稳定性研究
考察样品在室温条件下的长期稳定性,定期检测杂质成分,结果如表4所示。
3 结 论
本试验建立了达格列净特定杂质的分析方法,其H PL C检测方法通过方法学验证。结果表明,该方法简单易操作、灵敏度、专属性好,稳定性研究结果理想,可用于达格列净的特定杂质DGL301的测定。
参考文献
[1]COLE P, VICENTE M, CASTANER R. Dapagliflozin.SGLT2 inhibitor, Antidiabetic agent [J]. Drugs Future,2008,33(9):745-751.
[2]MENG W, ELLSWORTH B A, NIRSCHL A A, et al.Discovery of dapagliflozin: a potent, selective renal sodiumdependent glucose cotransporter 2 (SGLT2) inhibitor for the treatment of type 2 diabetes [J]. J Med Chem, 2008, 51(5):1145-1149.
[3]陈稳,郑津津,王晨.HPLC法测定达格列净原料药中有关物质[J].现代药物与临床,2015,30(9):1068-1071.
[4]周浩, 孟繁华, 孙磊,等. L C - M S / M S 法定量检测恩格列净原料药中杂质的含量[ J ] .国际药学研究杂志,2016,43(4):753-756.
[5]戴震,朱丽君.反相高效液相色谱法测定达格列净的有关物质[J].临床合理用药杂志,2017,10(23):100-101.
[6]郑云峰,吴高鑫,罗海荣.达格列净·(S)-(+)-1, 2-丙二醇·一水合物的合成及其有关物质的分离与结构鉴定[J].山东化工, 2018,47(15):48-50.
[7]白彦川,张孟孟,刘蕊,等.HPLC法测定達格列净起始物料有关物质[J].海峡药学.2022,34(4):83-88.
作者简介
范祥元,硕士研究生,研究方向为药物合成及药品质量标准研究。
杜陈侠,通信作者,本科,主管药师,研究方向为药事管理及药品质量分析。
(责任编辑:袁文静)
