贝伐珠单抗与紫杉醇脂质体方案联合治疗晚期胃癌的效果研究
2024-05-29王传水
王传水
胃癌是源于胃黏膜细胞的恶性肿瘤, 早期无明显症状, 部分患者伴有消化不良、饱胀感等轻微不适, 随着病情进展能够出现体重下降、腹痛以及厌食、贫血、消瘦等症状[1]。手术是胃癌患者获得根治的唯一可能手段, 而进展期患者则需要在手术的基础上联合化疗、生物靶向药物、放疗等综合治疗, 以便延长生存期限,改善生存质量[2]。目前, 如何通过合理且安全的用药方案提高晚期胃癌患者的治疗效果已成为临床学者研究的焦点。紫杉醇脂质体属于新型紫杉类抗肿瘤药物,可以与小管的β 位结合, 促使微管聚合成为束状或团状, 阻滞肿瘤细胞有丝分裂并诱导其调亡[3]。贝伐珠单抗是一种分子靶向药, 对于VEGF 具有抑制作用, 继而阻断新生血管形成途径, 抑制肿瘤细胞的增殖与分裂[4]。本研究选取2021 年8 月~2022 年7 月期间本院收治的98 例晚期胃癌患者作为研究对象, 探讨贝伐珠单抗与紫杉醇脂质体方案对此类患者的治疗效果,现报告如下。
1 资料与方法
1.1 一般资料 选取2021 年8 月~2022 年7 月期间本院收治的98 例晚期胃癌患者作为研究对象, 按照随机数字表法分为对照组及研究组, 每组49 例。对照组:男性27 例, 女性22 例;年龄51~79 岁, 平均年龄(62.45±5.85)岁;恶性肿瘤国际临床病期分类(TNM)分期:Ⅲ期28 例, Ⅳ期21 例;病理类型:高分化腺癌18 例, 低分化腺癌23 例, 黏液腺癌8 例。研究组:男性26 例, 女性23 例;年龄50~78 岁, 平均年龄(62.47±5.53)岁;TNM 分期:Ⅲ期27 例, Ⅳ期22 例;病理类型:高分化腺癌17 例, 低分化腺癌23 例, 黏液腺癌9 例。两组一般资料比较, 结果未见差异性(P>0.05), 有可比性。研究方案已向患者及其家属进行充分的告知, 并取得同意;医院伦理委员会对此次研究批准。
纳入标准:经病理结果证实为胃癌, TNM 分期为Ⅲ~Ⅳ期;预计生存期>3 个月;卡氏评分(KPS 评分)≥60 分;有清晰且直径在2 cm 以上的原发病灶。排除标准:肝肾功能不全;其他恶性肿瘤;糖尿病;严重心脑血管病变;凝血功能异常;机体状况差, 难以耐受化疗;免疫系统疾病;哺乳或妊娠女性;患有精神疾病。
1.2 方法 对照组采用紫杉醇脂质体(南京绿叶制药有限公司, 国药准字H20030357, 规格:30 mg/瓶)与地西他滨(正大天晴药业集团股份有限公司, 国药准字H20120066, 规格:50 mg)联合化疗治疗, 即紫杉醇脂质体135 mg/m2, 静脉滴注, 时间为3 h, d1、d8、d15、d22;地西他滨15 mg/m2, 静脉滴注, 时间为8 h, d1~3;治疗6 周为1 个周期, 持续治疗2 个周期。研究组在对照组基础上应用贝伐珠单抗(齐鲁制药有限公司, 国药准字S20190040, 规格:100 mg∶4 ml)治疗, 贝伐珠单抗7.5 mg/(kg·次), 静脉滴注, d1、d22;治疗6 周为1 个周期,持续治疗2 个周期。
1.3 观察指标及判定标准 ①临床疗效:参照实体瘤疗效标准(RECIST)1.1[5]进行疗效评价, 其中目标病灶消失为完全缓解;病灶减少≥30%为部分缓解;有新病灶或病灶增加≥20%为进展;病灶减少未达到部分缓解且增加未达到进展标准为稳定。总有效率=完全缓解率+部分缓解率。②血清生长因子水平:治疗前后分别采集患者空腹静脉血3~5 ml, 高速离心后分离血清, 以放射免疫分析法对IGF-1、TGF-β1、VEGF水平进行检测。③生活质量:治疗前后使用癌症患者QLQ-52 量表进行评价, 量表评分范围为0~100 分, 涵盖生理、心理、独立性、社会关系等6 个维度, 分值与生活质量呈正比。④不良反应:不良反应观察指标包括胃肠道反应、骨髓抑制、肝功能损害、周围神经毒性。
1.4 统计学方法 数据采用SPSS23.0 软件进行处理。计量资料以均数±标准差 (±s)表示, 采用t 检验;计数资料以率(%)表示, 采用χ2检验。P<0.05 表示差异具有统计学意义。
2 结果
2.1 两组临床疗效比较 研究组总有效率高于对照组(P<0.05)。见表1。
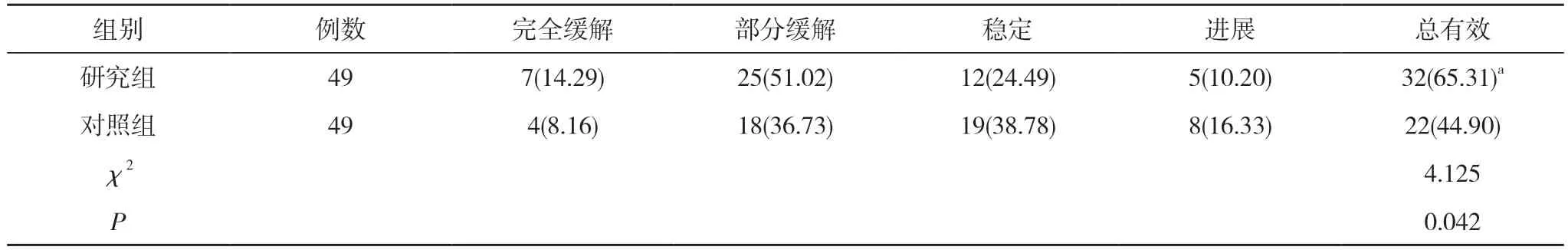
表1 两组临床疗效比较[n(%)]
2.2 两组血清生长因子水平比较 治疗前两组IGF-1、TGF-β1、VEGF 水平比较未见差异性(P>0.05);治疗后研究组IGF-1、TGF-β1、VEGF 水平较对照组低(P<0.05)。见表2。
表2 两组血清生长因子水平比较( ±s)

表2 两组血清生长因子水平比较( ±s)
注:与对照组比较, aP<0.05
组别 例数 IGF-1(ng/ml) TGF-β1(ng/ml) VEGF(ng/L)治疗前 治疗后 治疗前 治疗后 治疗前 治疗后研究组 49 126.65±10.56 82.65±5.23a 51.23±5.00 22.45±4.02a 202.65±16.85 92.45±10.25a对照组 49 125.65±9.85 90.56±5.03 51.24±4.89 28.95±4.47 200.65±15.98 104.52±11.57 t 0 7.631 0.010 7.568 0.603 5.466 P 1 0.000 0.992 0.000 0.548 0.000
2.3 两组生活质量比较 治疗前两组QLQ-52 评分比较, 结果未见差异性(P>0.05);治疗后研究组QLQ-52评分较对照组高(P<0.05)。见表3。
表3 两组生活质量比较( ±s, 分)
注:与对照组比较, aP<0.05
组别 例数 QLQ-52 评分治疗前 治疗后研究组 49 55.52±5.89 70.52±10.23a对照组 49 56.02±5.47 62.84±8.45 t 0.435 4.052 P 0.664 0.000
2.4 两组不良反应发生情况比较 两组胃肠道反应、骨髓抑制、肝功能损害、周围神经毒性发生率比较,结果未见差异性(P>0.05)。见表4。

表4 两组不良反应发生情况比较[n(%)]
3 讨论
胃癌是消化系统常见的恶性肿瘤, 现主要采用手术、化疗、靶向药物等综合方案治疗。据相关调查显示, 早期胃癌术后5 年生存率能够达到90.9%~100.0%,但晚期胃癌仍缺少有效的治疗手段, 5 年生存率不足30%[6]。因此, 亟需探寻可靠的治疗方案保障晚期胃癌患者的临床疗效, 提高其生活质量。
有研究发现, 胃癌作为一种实体肿瘤, 肿瘤血管为肿瘤细胞生长提供了充足的血液与营养, 其中VEGF对于肿瘤血管生成具有重要的诱导作用[7]。紫杉醇脂质体是一种新型紫杉醇制剂, 具有较强的药物水溶性与靶向作用, 可以促进微管双聚体装配成微管, 减少肿瘤细胞的分裂与生长[8]。贝伐珠单抗是一种新型抗VEGF 靶向药, 其通过与VEGF 受体进行特异性结合,可以增强血管通透性, 抑制肿瘤血液供应, 对抗残存或新生肿瘤细胞, 促使肿瘤血管退化, 继而达到抗肿瘤与重建肿瘤血管网络的功效[9]。本研究对49 例晚期胃癌患者应用了贝伐珠单抗与紫杉醇脂质体方案联合治疗, 结果发现研究组总有效率高于对照组(P<0.05)。可见两种药物协同作用能够有效提高晚期胃癌患者的临床疗效。
IGF-1、TGF-β1、VEGF 是评估肿瘤新生血管的可靠指标, 其中IGF-1 又称为促生长因子, 与肿瘤的发生、增殖及侵袭关系密切[10];TGF-β1具有双重性, 在早期正常细胞转化成肿瘤细胞时具有一定的抑制作用, 随着肿瘤细胞的进展则变成肿瘤生长刺激因子;VEGF 是肿瘤新血管生成的重要生长因子, 随着肿瘤病情进展其表达不断上调。本文研究结果显示, 治疗后研究组IGF-1、TGF-β1、VEGF 水平较对照组低(P<0.05)。紫杉醇脂质体对肿瘤细胞有丝分裂具有抑制作用, 并可以诱导其调亡, 而在此基础上联合贝伐珠单抗进一步抑制了肿瘤血管的生成、生长与转移, 调节血清生长因子水平, 保障疾病的治疗效果[11,12]。从安全性来看, 两组胃肠道反应、骨髓抑制、肝功能损害、周围神经毒性发生率比较, 结果未见差异性(P>0.05)。结果证实, 在紫杉醇脂质体化疗方案的基础上联合贝伐珠单抗并未增加患者的不良用药风险, 安全性较为理想。此外, 治疗后研究组QLQ-52 评分较对照组高(P<0.05)。可见晚期胃癌患者采用贝伐珠单抗与紫杉醇脂质体方案联合治疗能够有效改善生活质量, 考虑原因与其良好抗肿瘤功效、有效缓解相关症状有关[13]。
综上所述, 贝伐珠单抗与紫杉醇脂质体方案联合治疗晚期胃癌效果确切, 可以有效抑制血清生长因子,改善患者的生活质量, 具有临床推广价值。
