言之均有理是否都可行
2024-05-29廖旭杲
廖旭杲
摘要:解析了2023年高考中颇有争议的新课标卷第28题,对该实验大题的2个设问提出了一些个人思考.
关键词:2023年高考新课标卷;实验题;实践经验
中图分类号:G632文献标识码:A文章编号:1008-0333(2024)11-0137-03
2023年是云南、黑龙江、吉林、安徽、山西五省份“新教材、老高考”形式的首次高考,使用新课标卷,化学试题以理科综合的形式进行命制,保留“老教材、老高考”化学试题的“七选择、四大题”的题量,选择题题型与“老教材、老高考”题型一致,非选择题部分取消选考试题.其中实验大题沿袭去年风格,仍旧是有机实验试题,只不过在注重衔接的同时还是有适度的创新,以期更好地引导中学教学,现作分析如下,供大家讨论.
1 试题呈现与解析
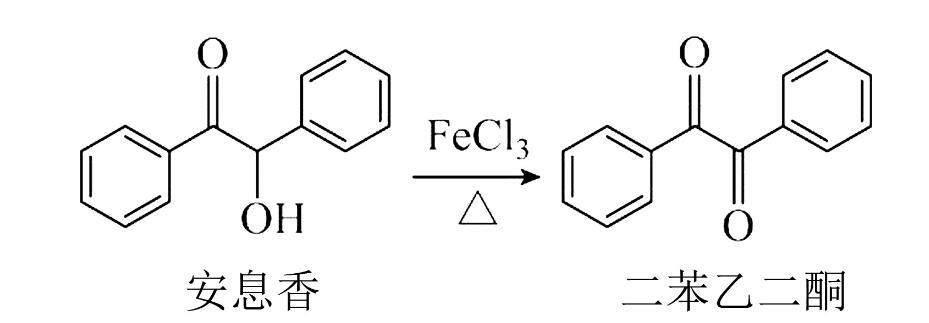
试题(2023年·新课标卷·28)实验室由安息香制备二苯乙二酮的反应式如下:
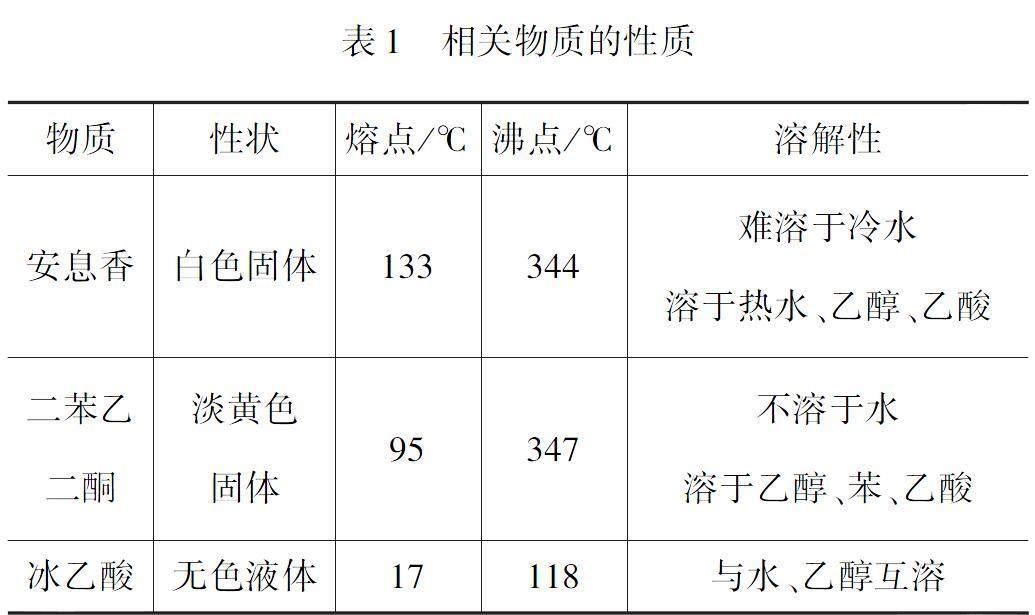
相关信息列表如表1:
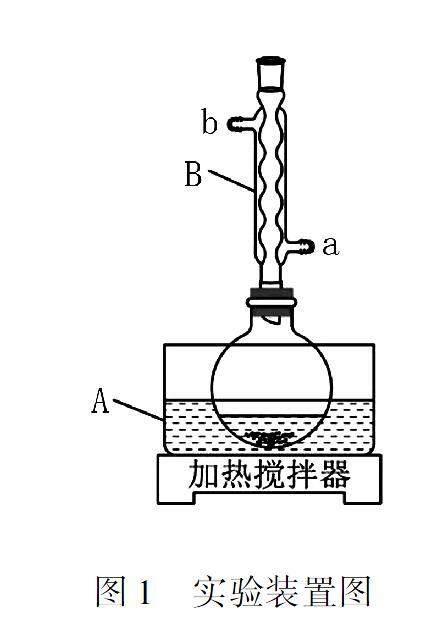
装置示意图如下图(图1)所示,实验步骤为:
①在圆底烧瓶中加入10 mL冰乙酸、5 mL水及9.0 g FeCl3·6H2O,边搅拌边加热,至固体全部溶解.
②停止加热,待沸腾平息后加入2.0 g安息香,加热回流45~60 min.
③加入50 mL水,煮沸后冷却,有黄色固体析出.
④过滤,并用冷水洗涤固体3次,得到粗品.
⑤粗品用75%的乙醇重结晶,干燥后得淡黄色结晶1.6 g.
回答下列问题:
(1)仪器A中应加入____________(填“水”或“油”)作为热传导介质.
(2)仪器B的名称是____________;冷却水应从____________(填“a”或“b”)口通入.
(3)实验步骤②中,安息香必须待沸腾平息后方可加入,其主要目的是____________.
(4)在本实验中,FeCl3为氧化剂且过量,其还原产物为____________;某同学尝试改进本实验:采用催化量的FeCl3并通入空气制备二苯乙二酮.该方案是否可行____________?简述判断理由____________.
(5)本实验步骤①~③在乙酸体系中进行,乙酸除作溶剂外,另一主要作用是防止____________.
(6)若粗品中混有少量____________未氧化的安息香,可用少量洗涤的方法除去(填标号).若要得到更高纯度的产品,可用重结晶的方法进一步提纯.
a.热水b.乙酸c.冷水d.乙醇
(7)本实验的产率最接近于____________(填标号).
a.85%b.80%c.75%d.70%
解析由题示信息写出由安息香制备二苯乙二酮的完整的化学方程式:
用冰乙酸作溶剂,FeCl3作氧化剂,为使FeCl3·6H2O更好地溶解,又添加了5 mL水,事先把氧化剂溶解在溶剂中,加热煮沸.待沸腾平息后投料,加入还原剂:2.0 g安息香,加热回流45~60 min待反应充分.结束时加50 mL水增大溶剂的极性,促进黄色产物二苯乙二酮析出.过滤,并用冷水洗涤除去可能吸附的CH3COOH、FeCl3、FeCl2、HCl等,获得粗产品,然后用75%的乙醇重结晶,得到较纯产品.
(1)因为溶剂乙酸的沸点相对较低,为118 ℃,仍高于水的沸点,所以采用油浴加热.油浴加热一般可控温100~300 ℃,多采用硅油.
(2)仪器B是球形冷凝管,用于回流原料,提高其利用率,根据逆流原理,冷却水应从下面的a口通入b口流出.
(3)添加安息香必须待沸腾平息后方可加入,否则可能导致反应液暴沸,发生危险.如同实验室里为防止暴沸往往在反应体系中添加有沸石或碎瓷片,如果某次实验中忘记了添加,则必须等到反应体系冷却后再添加沸石或碎瓷片[1].
(4)在本實验中,FeCl3为氧化剂,其还原产物为FeCl2,不可能被还原到Fe,因为是醋酸环境.
该同学的改进方法应该可行,催化量(少量)的FeCl3被还原为FeCl2,O2又会将FeCl2氧化为FeCl3,继续发挥氧化剂作用.从化学方程式
4FeCl2+O2+4HCl4FeCl3+2H2O
来看也不会使反应体系变得更加碱性,酸性保持,三价铁也不会水解.
(5)乙酸除作溶剂外,还可以抑制FeCl3水解生成Fe(OH)3.
(6)根据题表信息“安息香溶于热水、二苯乙二酮不溶于水”可选用热水洗涤除去粗品中混有少量未氧化的安息香.
(7)安息香(C14H12O2)→二苯乙二酮(C14H10O2)仅失去了“2H”,所以该实验中理论产量约为2.0 g,实际得1.6 g纯品,故产率接近1.62.0×100%=80%.此题命题人本意应该是估算即可,无需精确计算.
参考答案:
(1)油(2)(球形)冷凝管a
(3)防止热蒸气灼伤人,防止加入安息香时放出大量热,导致反应液暴沸
(4)FeCl2可行,少量的FeCl3被还原为FeCl2,O2又会将FeCl2氧化为FeCl3,继续发挥氧化剂作用
(5)FeCl3水解生成Fe(OH)3
(6)a(7)b
反思:由于高考后参考答案不再公布,关于此题的答案网上有不同的版本,尤其是第(3)小题和第(4)小题,争议较大.如第(3)小题,有老师拟的答案为:“防止温度过高,反应混合液挥发”,笔者倾向于学生由日常生活经验嫁接过来即可作答:沸腾产生热蒸气,若未等沸腾平息加入试剂,会导致实验操作者被蒸气烫伤.第(4)小题有老师认为不可行,给出的理由是“反应温度较高,过量的O2会与安息香反应生成副产物,导致产物产率低”,莫衷一是.笔者在上述解析中给出的意见是在请教了大学有机实验老师和一些博士生后给出的.
2 结束语
实验题无论取材于无机制备还是有机合成,所涉无非两方面:理解实验原理,把握操作细节.只是在有机合成的实验细节方面,中学师生普遍缺乏相应的经验,因为中学里有机制备做得少,合成乙酸乙酯大部分学校都做过,合成阿司匹林则由于乙酸酐属管制药品,大部分学校都不可能做学生实验,所以有机实验的经验相对而言确属短板,此次第(3)小问出山,有些难为中学师生了.第(4)小问也是令老师们把握不定,当然,参考答案未公布,也有一种可能,那就是,答可行或不可行均给分,只要后面的理由言之有理即可,希望如此.因为化学反应尤其是有机反应都很复杂,单方面分析容易偏颇,有很多的发明创造都是来自实验事故或意外,诸如顺铂的发现、导电高聚物的发现等.
参考文献:
[1] 杨琴.高校有机化学实验持续性教学探索:以安息香氧化制备二苯乙二酮为例[J].山东化工,2020,49(6):176-177.
[责任编辑:季春阳]
