基于CiteSpace的免疫相关不良事件研究热点及趋势分析
2024-05-20胡传军王静杨娇万晓蓉牟华陈彩娥
胡传军 王静 杨娇 万晓蓉 牟华 陈彩娥


ResearchhotspotsandtrendanalysisofimmunerelatedadverseeventsbasedonCiteSpace
HUChuanjun,WANGJing,YANGJiao,WANXiaorong,MOUHua,CHENCai′e,HEZhongyunTheFirstClinicalMedicalCollegeofChinaThreeGorgesUniversity,Hubei443000ChinaCorrespondingAuthorWANGJing,Email:1437638048@qq.com
Keywordscancer;immunerelatedadverseevents;adverseevents;visualanalysis;nursing
摘要目的:对免疫相关不良事件(irAEs)的研究热点及趋势进行可视化分析,以期为我国癌症病人irAEs的研究提供借鉴。方法:选择WebofScience核心合集数据库,以建库至2022年12月15日的irAEs文献记录为数据来源,采用CiteSpace软件绘制作者与机构、国家、关键词、突现词及时间线等可视化图谱。结果:共纳入2648篇文献,涉及65个国家和地区、652位作者及506个科研机构;发文量居前3位的国家分别为美国(1022篇),日本(534篇)、中国(341篇);研究机构中发文量排名居第1位的是美国的UniversityofTexasMDAndersonCancerCenter(154篇);irAEs研究热点涉及“immunecheckpointinhibitor”“adverseevent”“toxicity”“management”“safety”等多个方面。结论:irAEs的研究起步较晚,发展较快,国家与机构合作网络联系密切,该领域已形成了核心作者群;研究方向集中于irAEs机制研究、irAEs的预防以及irAEs管理3个方面。构建irAEs早期预测模式、危险因素探索、irAEs的评估量表开发及接受免疫疗法病人的生存护理是未来关注的方向。
关键词癌症;免疫相关不良事件;不良事件;可视化分析;护理
doi:10.12102/j.issn.20958668.2024.09.010
传统癌症治疗以放疗、化疗和手术治疗为主,随着治疗技术的不断发展与创新,免疫疗法成为癌症治疗的新型手段,并极大地改变了癌症病人的治疗前景[1]。近年来,多种类型免疫检查点抑制剂(immunecheckpointinhibitors,ICIs)相继出现并应用于临床,在各种癌症治疗中显示出持久而明显的疗效[2]。但在ICIs治疗癌症的同时,也会非特异性地激活免疫系统,破坏免疫稳定性,产生与治疗相关的特殊不良反应,导致免疫相关不良事件(immunerelatedadverseevents,irAEs)的发生。irAEs可累及全身各个脏器,致使免疫疗法暂时或永久中断甚至危及生命[3]。随着免疫疗法在癌症治疗方案中的使用越来越多,如何有效预防和管理irAEs是临床面临的重大考验。鉴于当前尚无研究探讨irAEs领域的研究现状、热点和发展趋势。因此,本研究基于CiteSpace从不同角度分析irAEs领域的知识基础、梳理irAEs的发展轨迹、探索irAEs研究热点与前沿等,以期更加全面、准确地了解目前的研究概况,为我国学者未来更深入地研究irAEs提供参考。
1资料与方法
1.1数据来源
选择WebofScience核心合集数据库,以TS=((tumorORcancer)AND(immunerelatedadverseevents))进行主题检索,检索时限为建库至2022年12月15日,共获得4158条文献记录,WebofScience文献类型限定为(article)AND语种(English)精炼文献记录,排除社论材料、会议摘要、信函等与主题不相关的文献及重复发表的文献记录1510条,最终纳入2648篇文献。
1.2分析方法
运用CiteSpace6.1.R3软件进行文献计量学分析。将WebofScience检索的文献记录以纯文本格式导出,以“download_**.txt”命名,导入CiteSpace6.1.R3软件进行数据转换,图谱节点参数设置:时间分区设置为2002年1月—2022年12月,时间切片设置为“1”;阈值设置为Top50,节点类型分别设置为:作者、机构、国家、关键词等类型,视图裁剪选择寻径法,分别绘制成相应的图谱,以实现对irAEs的可视化分析。
2结果
2.1发文量
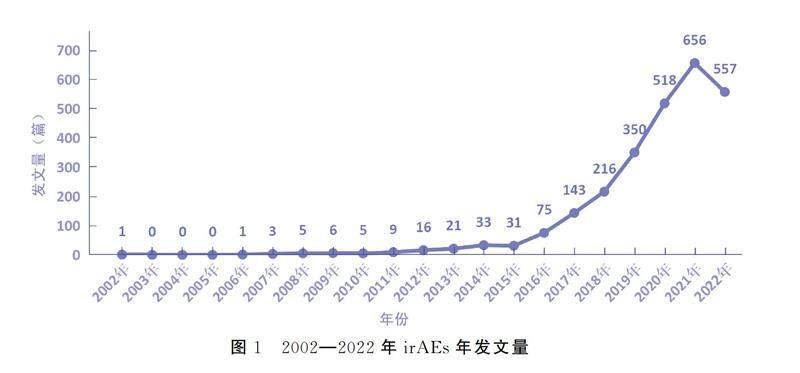
irAEs年度发文量见图1。结果显示,该研究领域起步相对较晚,首次发表文献在2002年,总体发文趋势大致分为2个阶段,第一阶段为2002—2014年,13年间该领域处于起步阶段,年发文量增长相对迟缓,2003—2005年该领域研究出现停滞现象,2014年发文量出现第1次高峰,年发文量为33篇;第二阶段为2015—2022年,该领域研究处于快速发展期,年发文量呈持续上升状态,2021年发文量达到峰值,为656篇,鉴于纳入文献截至2022年12月15日,2022年的年发文量存在一定缺失,较2021年有所下降。
2.2作者与研究机构
运用CiteSpace6.1.R3软件对2648篇文献的研究作者与机构的合作网络进行可视化分析,节点选择“author”及“institution”,结果见图2、图3。图谱网络密度(density)为0.0123,包含737个节点和3323条连线。图中颜色的冷暖代表了时间的远近,每个节点代表单个作者/机构,节点大小代表研究作者与机构的发文数量及学术影响力,节点间连线表示相互之间的合作关系,连线粗细代表作者或机构间合作的紧密性[4]。图谱中节点连线强度及网络密度紧密,表明各研究机构之间联系紧密,学术合作交流密切。分析发现,irAEs研究共涉及506个科研机构,主要分布在各大高校、医疗机构及癌症研究中心,美国研究机构发文量占据领先位置,得克萨斯大学安德森癌症研究中心(UniversityofTexasMDAndersonCancerCenter)發文量为154篇,居第1位,详见表1。从研究作者分析,本研究共涉及652名作者、506个科研机构,依据普莱斯定律,核心作者发文量需≥全部论文数量的50%,则认为该领域形成了核心作者群。其公式为M≈0.749×Nmax,计算可得M=3.84,本研究发现发表论文≥4篇的作者共166人,归入核心作者行列,核心作者发文量为1180篇,占54.75%,表明该研究领域中核心作者群已经形成[5]。图谱显示,该领域形成了多个研究团体,其中发文量最大、最核心的研究作者是以JohnsonDouglasB为核心的研究网络图谱,其次为HodiFStephen为代表的研究团队,发文量分别为27篇、21篇。
2.3研究国家
研究结果显示,共涉及65个国家和地区,发文量居前3位的分别是美国(1022篇)、日本(534篇)、中国(341篇),见图4。发文量排名居前10位的国家,见表2。irAEs的关注度与所在国家的经济水平有着较高关系,经济水平越高的国家对该领域的研究热度越高。美国等发达国家对irAEs的研究开展较早,并在该领域占有重要地位,中国作为癌症病人较高的国家,随着国内经济水平的提升,在该领域取得了重要的成果。
2.4文献共被引分析
文献及作者共被引分析有助于筛选相关领域具有一定影响力的文献,从而了解科研人员对研究领域的关注程度[6]。“Immunerelatedadverseeventsassociatedwithimmunecheckpointblockade”是近5年该研究领域被引频次最高的论文,主要研究与免疫检查点阻断相关的irAEs,发文时间是2018年,被引频次2047次;被引频次排名第2位的是“Adverseeffectsofimmunecheckpointinhibitors:epidemiology,managementandsurveillance”该研究主要概述了迄今为止出现的各种类型的irAEs,讨论了irAEs的流行病学及其动力学、危险因素、亚型和病理生理学,以及关于筛查和监测的新策略,同时强调了irAEs管理的重要性。发表时间在2019年,被引频次735次,近5年irAEs领域排名前10位高被引文献见表2。
2.5研究热点与前沿分析
2.5.1研究热点分析
关键词是对文献内容的高度概括,反映了文献的研究主题,可以从整体上了解作者表达的中心思想[7]。关键词出现的次数越多在图谱中显示的节点越大,字体也越大。研究结果显示,关键词“cancer”与“immunerelatedadverseevent”作为最基础的术语分别出现了386次和662次。irAEs的研究涉及的研究热点内容有“immunecheckpointinhibitor”(免疫检查点抑制剂)、“efficacy”(疗效)、“toxicity”(毒性)、“adverseevent”(不良事件)、“management”(管理)、“safety”(安全)等方面;免疫制剂关注的热点为“nivolumab”(纳武单抗)、“ipilimumab”(伊匹单抗)、“docetaxel”(多西他赛)、“pembrolizumab”(帕博利珠单抗)等;疾病关注度较高的为“nonsmallcelllungcancer”(非小细胞肺癌)、“melanoma”(黑色素瘤)、“celllungcancer”(细胞性肺癌)等;以及反映该领域研究方法的关键词,如“openlabel”(非盲法)、“multicenter”(多中心)等。见图5。从中可以看出有关ICIs是irAEs领域的热点研究话题。国际上对使用新药物及联合用药所产生的irAEs一直保持着较高的热度。
2.5.2关键词聚类分析
关键词聚类分析可展现当前研究热点领域,应用CiteSpace软件的Keyword功能,选择LLR算法对文献数据中的关键词进行聚类分析。聚类图谱显示,模块值为0.3665(>0.3),表明聚类划分出来的社团结构显著;平均轮廓值为0.6419(>0.5),表明聚类结果是合理的,图谱共形成7个聚类,依次为“lungcancer”(肺癌)、“headandneckcancer”(头颈癌)、“blockade”(阻断)、“criteria”(标准)、“nonsmallcelllungcancer”(非小细胞肺癌)、“Tcell”(T细胞)、“tumormicroenvironment”(肿瘤微环境),见图6。归纳聚类权重较大的关键词见表3。聚类图谱及详细信息显示,irAEs的研究热点癌症类型为headandneckcancer(头颈部癌症)、squamouscellcarcinoma(鳞状细胞癌)、melanoma(黑色素瘤)、metastaticrenalcellcarcinoma(转移性肾细胞癌)、nonsmallcelllungcancen(非小细胞肺癌)、colorectalcancer(大肠癌)等;研究主题主要包括irAE机制探索、模型预测、试验性研究、案例报告以及随访研究。目前,研究方向集中在irAE的机制研究、irAEs的预防和irAEs的管理;irAEs的干预围绕irAEs多学科诊疗建设、心理干预、健康教育、随访等内容展开;研究目的着重于提高免疫治疗效果,降低irAEs发生率,提高癌症病人的生存期。
2.5.3研究前沿分析
在高频关键词共现网络的基础上,进一步进行了突现词探索。关键词突现是指在短时间内出现频次极高的关键词,红色横线代表关键词突现持续时间,红线越长,说明该关键词热度持续时间越长、研究前沿越强。在关键词共现分析基础上,打开ControlPanel,点击Burstness,将MinimumDuration设置为1,其他默认值不做修改,点击View得到前25位突现关键词见图7。持续时间最久、强度最高的关键词是metastaticmelanoma(強度为56.96;持续时间为2006—2018年);目前突现强度最高的是casereport(9.79),其次是combinednivolumab(8.75)、outcome(5.69)和longtermsafety(5.00)。为了更清晰地展示irAEs研究主题发展规律,在关键词聚类分析的基础上,对其进行关键词timeline分析。见图8。结果显示,随着irAEs研究的深入,免疫治疗方式由单药治疗向联合治疗发展,研究方法由原始研究、病例报告向循证医学发展,涉及的癌症类型由少到多,并延伸了新的相关研究领域,如药物安全管理、感染控制、心理护理及安全行为管理等方面。
3讨论
3.1研究现状
从年发文量时序来看,irAEs领域研究起步较晚,2002年该领域开始被关注,2015年后逐渐成为研究热点。从研究空间分布来看,美国、日本、中国、法国为核心研究力量,各国内研究机构间合作交流较紧密,学术合作交流密切,形成了UniversityofTexasMDAndersonCancerCenter、MemSloanKetteringCancerCenter等多个核心机构,但不同国家之间研究机构交流合作相对较弱,未来有待进一步加强不同国家之间研究机构的交流与合作。目前,该研究领域中核心作者群已形成。研究作者早期以AllisonJP、MaioM为代表的研究团队,随着对该领域研究关注度的提升,后期形成了WolchokJD、RobertC等多个研究团队,近年来形成以JohnsonDB、HodiFS、ReynoldsKL为代表的多个研究团队。研究团队不仅内部交流合作频繁,且各研究团队之间的交流合作也较频繁,促进了该领域研究的快速发展。
3.2研究热点
本研究对irAEs研究领域的关键词进行整理,发现可以归纳为以下3个方面:1)irAEs机制研究,关键词包含“Tcell”“blockade”“immunecheckpointinhibitor”“toxicity”“antibody”等词汇。目前,irAEs的发生机制尚不明确,仍需要不断探索[89]。有研究者认为,irAEs的发生率和发病时间与所使用的免疫检查点抑制剂(ICPi)的类别和剂量、癌症的类型以及病人自身因素有關[9]。目前研究结果显示,irAEs的发生机制可能与抑制细胞毒性T淋巴细胞相关蛋白4(CTLA4)、细胞程序性死亡配体1(PDL1)或程序性死亡受体1(PD1)后所引起的调节性T细胞的功能降低、效应T细胞的过度激活、巨噬细胞与中性粒细胞的毒性作用、γ干扰素的大量释放以及B细胞产生的抗体等因素相关[1012]。提示临床医护人员在治疗过程中要关注不同癌症类型使用不同药物、不同剂量及病人自身免疫等因素。2)irAEs的预防,关键词包括:“nivolumab”“ipilimumab”“pembrolizumab”“efficacy”“survival”,涉及疾病包括“nonsmallcelllungcancer”“melanoma”“celllungcancer”“headandneckcancer”等。ICIs癌症病人的治疗模式,提高了部分癌症病人的生存率,但其诱发的各种irAEs,也限制了其在临床上的使用。研究表明,免疫治疗在肿瘤治疗中的有效率为25%~30%[13]。若在使用ICIs治疗前,能够对癌症病人可能发生的特定不良反应进行预测,并及时给予预防性处理,能为临床医师对病人的治疗效果的评估提供极大的帮助,亦能够降低甚至规避irAEs的发生,使得免疫治疗的临床获益最大化。目前,临床尚无有力的预测性指标来评估治疗风险及筛选最优的获益人群[14]。因此,为了准确预测免疫治疗效果,科研人员一边积极探索更加精准的肿瘤免疫治疗相关生物标记物,一边致力于探讨ICIs疗效与irAEs的发展的相关性。有研究者应用其他免疫调节剂与ICPis结合的方案预防irAEs,并取得一定效果。然而,迄今为止,此类联合用药的安全性和疗效尚未证明[15]。如何在维持疗效的同时减轻甚至规避其毒性的产生,未来需要进一步探索。3)irAEs的管理。关键词包括“adverseevent”“management”等。虽然目前正在对发生irAEs风险因素进行研究,但全面的预测模型尚未形成。现阶段irAEs的管理侧重于早期识别毒性和及时启动治疗。在管理理念与管理方式上,由于irAEs临床表现多样,毒性涉及身体多器官或系统,不同毒性发病时间各不相同[16]。“全程管理”是其核心理念,管理方式具体包括以下3个方面:1)irAEs的监测,受免疫反应的记忆性和延迟性的影响,irAEs可以发生在启动治疗后的任何时间点,甚至在毒性缓解期或停止免疫治疗后也可发生[17]。因此,在开始免疫治疗时,需要对病人进行全程监测。监测过程中,要求除医务人员之外的病人及家庭护理员参与,这有利于早期发现irAEs。此外,鼓励病人提醒医护人员他们正在接受或已经接受免疫治疗剂,主动报告健康状态的变化,每个医务人员都应该意识到irAEs的可能性。2)irAEs的识别与评估,irAEs的诊断尚无金标准,属于排他性诊断。irAEs发生的时间跨度较大,病人在非住院情况下,病人及家庭护理员能够早期识别irAEs相关症状,对于病人的治疗十分重要。因此,病人在开始治疗之前,以及在整个治疗和存活期间,病人和家庭护理人员应及时接受关于免疫治疗最新的健康教育,了解免疫疗法的作用机制以及可能出现的irAEs临床特征。此外,医务人员在治疗开始前应对病人开展基线调查,包括既往治疗的不良反应类型、严重程度、影响免疫状态的疾病,包括自身免疫性疾病、造血干细胞或器官移植、感染性疾病,如病毒性肝炎等方面[18]。其次,每次评估要注意观察病人全身皮肤与黏膜、循环与呼吸、营养状况与排泄、神经肌肉与关节活动情况及认知是否出现异常改变,并详细记录异常类型、范围、等级等重要信息,同时评估已有的检查、检验报告,便于对病人发生的irAEs及时进行鉴别诊断。鉴于当前缺乏irAEs症状及体征的量化评估工具,病人及家庭护理人员对irAEs的识别存在较大困难,建议未来加强irAEs症状及体征评估量化工具的开发,便于正确评估、定级与持续追踪[19]。3)irAEs的干预,大多数情况下,irAEs可以通过中断治疗和/或支持性治疗进行干预。由于irAEs可发生于多系统、多器官中,在干预过程中部分病人往往需要多学科协作,组建免疫检查点抑制剂毒性多学科诊疗(multidisciplinaryteam,MDT)十分必要。在美国,麻省总医院布列根和妇女医院建立了irAEsMDT,并提出了免疫治疗毒性管理团队和严重免疫治疗不良反应服务的概念;在日本,国立癌症研究中心为了对irAEs进行科学管理,组建了由40位不同学科专家的irAEsMDT团队。目前,我国irAEsMDT相对比较薄弱,MDT成员以肿瘤学科为主,其他学科专家参与度低。因此,我国相关专家开始积极探索irAEsMDT标准化建设,并形成了《免疫检查点抑制剂相关的毒性多学科诊疗协作组建设中国专家共识》[20],对irAEsMDT的组织框架和职责、标准流程、工作形式及评估方法等核心内容做了详细阐述,形成了irAEsMDT标准化的管理模式,积极推动了我国的irAEsMDT运行和发展。
随着ICPi疗法在各个肿瘤类型的应用,癌症病人的生存率得到提高,接受免疫疗法病人的生存护理概念再次成为护理专业的关注焦点[21]。在病人的整个癌症治疗过程中,需要制定长期的护理计划,为病人提供全面的护理。不仅是基于肿瘤类型和治疗方法进行的相关护理,也包含有关治疗的个性化信息、未来随访的需要、癌症和治疗相关毒性的测试与治疗、长期不良反应以及治疗完成后的健康促进等工作,确保病人的支持性及其他护理需求得到满足,并照顾到社会心理问题。因此,未来需要进一步明确护理人员的角色,并不断提升其知识水平,以满足病人护理的需求。本研究也存在一定局限。文献检索范围仅限于WebofScience数据库,可能存在因文献数据不完整,使结果存在一定偏差;纳入的文献质量参差不齐,对研究领域整体结构可能存在影响。目前,可视化图形主要以二维图谱展示,尚无更高维度层面的可视化展示,仍有待进一步探索。故未来的研究可检索多个文献数据库,增大样本量范围,多维度、多视角分析,促进irAEs的深入理解和研究。
参考文献:
[1]龙敏.肿瘤常见突变在肿瘤响应免疫治疗中的作用和机制研究[D].杭州:浙江大学,2021.
[2]WANGYT,LIUY,LIXH,etal.TCRcoexpressionsignaturepredictsimmunotherapyresistanceinNSCLC[J].FrontiersinPharmacology,2022,13:875149.
[3]ZHANGY,ZHANGXL,LIWL,etal.Biomarkersandriskfactorsfortheearlypredictionofimmunerelatedadverseevents:areview[J].HumanVaccines&Immunotherapeutics,2022,18(1):2018894.
[4]李杰,陈超美.CiteSpace:科技文本挖掘及可视化[M].3版.北京:首都经济贸易大学出版社,2022:1.
[5]徐健,毛进,叶光辉,等.基于核心作者研究兴趣相似性网络的社群隶属研究*——以国内情报学领域为例[J].图书情报工作,2018,62(12):5764.
[6]谷珊珊,许云,王晶惠.国内外癌因性疲乏的研究现状、热点演化与整合展望—基于文献计量学的可视化图谱分析[J].肿瘤防治研究,2022,49(5):418426.
[7]张婷,刘慧婷,沈兴蓉,等.基于CiteSpace的癌症患者生存管理研究现状及热点分析[J].山东第一医科大学(山东省医学科学院)学报,2022,43(10):777783.
[8]SANTOMASSOBD,NASTOUPILLJ,ADKINSS,etal.ManagementofimmunerelatedadverseeventsinpatientstreatedwithchimericantigenreceptorTcelltherapy:ASCOguideline[J].JournalofClinicalOncology,2021,39(35):39783992.
[9]SCHNEIDERBJ,NAIDOOJ,SANTOMASSOBD,etal.Managementofimmunerelatedadverseeventsinpatientstreatedwithimmunecheckpointinhibitortherapy:ASCOguidelineupdate[J].JClinOncol,2021,39(36):40734126.
[10]ANDOY,HAYASHIT,SUGIMOTOR,etal.Riskfactorsforcancerassociatedthrombosisinpatientsundergoingtreatmentwithimmunecheckpointinhibitors[J].InvestigationalNewDrugs,2020,38(4):12001206.
[11]BERGQVISTV,HERTERVIGE,GEDEONP,etal.Vedolizumabtreatmentforimmunecheckpointinhibitorinducedenterocolitis[J].CancerImmunologyImmunotherapy,2017,66(5):581592.
[12]MARTHEYL,MATEUSC,MUSSINIC,etal.CancerimmunotherapywithantiCTLA4monoclonalantibodiesinducesaninflammatoryboweldisease[J].JournalofCrohn′sandColitis,2016,10(4):395401.
[13]RASCHIE,GATTIM,GELSOMINOF,etal.Lessonstobelearntfromrealworldstudiesonimmunerelatedadverseeventswithcheckpointinhibitors:aclinicalperspectivefrompharmacovigilance[J].TargetedOncology,2020,15(4):449466.
[14]KUMARV,CHAUDHARYN,GARGM,etal.Currentdiagnosisandmanagementofimmunerelatedadverseevents(irAEs)inducedbyimmunecheckpointinhibitortherapy[J].FrontiersinPharmacology,2017,8:49.
[15]DEFELICEKM,GUPTAA,RAKSHITS,etal.Ipilimumabinducedcolitisinpatientswithmetastaticmelanoma[J].MelanomaResearch,2015,25(4):321327.
[16]POSTOWMA,SIDLOWR,HELLMANNMD.Immunerelatedadverseeventsassociatedwithimmunecheckpointblockade[J].TheNewEnglandJournalofMedicine,2018,378(2):158168.
[17]LEEYJ,KIMHT,WONCH,etal.Characterizationandprognosticsignificanceofcutaneousadverseeventstoantiprogrammedcelldeath1therapy[J].JournalofKoreanMedicalScience,2019,34(26):e186.
[18]中國临床肿瘤学会指南工作委员会组织.中国临床肿瘤学会(CSCO)免疫检查点抑制剂相关的毒性管理指南2021[M].北京:人民卫生出版社,2021:1.
[19]马艳梅,刘玉,倪宏,等.免疫检查点抑制剂治疗相关不良反应的护理[J].护理研究,2021,35(16):29662970.
[20]王俊.《免疫检查点抑制剂相关的毒性多学科诊疗协作组建设中国专家共识》解读[J].中国肿瘤生物治疗杂志,2022,29(11):985988.
[21]O′REILLYA,HUGHESP,MANNJ,etal.Animmunotherapysurvivorpopulation:healthrelatedqualityoflifeandtoxicityinpatientswithmetastaticmelanomatreatedwithimmunecheckpointinhibitors[J].SupportiveCareinCancer,2020,28(2):561570.
