高盐食品基质中砷含量的测定
2024-05-16戴瑞平刘花梅舒露唐丽君黎申英李彪张梅玲刘涛黄宗兰
戴瑞平,刘花梅,舒露,唐丽君*,黎申英,李彪,张梅玲,刘涛,黄宗兰
(1.江西省检验检测认证总院食品检验检测研究院,江西南昌 330052)(2.江西省检验检测认证总院检测认证技术发展研究院,江西南昌 330029)
现行食品中总砷的测定标准为GB 5009.11-2014《食品安全国家标准 食品中总砷及无机砷的测定》,测定方法有电感耦合等离子体质谱(ICP-MS)法、氢化物发生原子荧光光谱(HG-AFS)法和银盐法。目前食品中砷在实验室的日常检验,使用频率较高的测定方法是稳定性、准确性和灵敏度都更占优势的ICP-MS 法[1,2],而HG-AFS 法由于干扰少、灵敏度高、稳定性好也被广泛应用[3,4],银盐法由于操作烦琐、加入太多试剂易引入本底和灵敏度低等原因,在实验室中应用的并不多。样品前处理方式有微波消解法、高压密闭消解法、湿法消解和干灰化法等。微波消解法由于加入试剂少,有机物消解较为彻底,而且整个消解过程是在密闭环境中,元素挥发损失少,因此被广泛应用于元素前处理过程[5,6]。高压密闭消解法的消解过程会用到不锈钢高压罐,操作不当会产生安全隐患[7],实际检测过程中使用的较少。干灰化法是通过马弗炉的高温有效破坏食品中的有机物,但是砷元素在高温易挥发,因此必须加入氧化镁覆盖以减少砷元素的损失[8]。目前湿法消解是GB 5009.11-2014 中HG-AFS 法指定的前处理方式之一,也是应用最为广泛的消解方式之一,湿法消解中加入的高氯酸和浓硫酸能有效提高消解液的温度,从而彻底消解样品中的有机物,但是硝酸消耗量大,耗时长也是湿法消解的一个短板。
高盐高基体的食品样品一般指含有较高浓度的氯化钠或者其他盐类物质的食品,比如经过盐腌制的板鸭、腊肉和咸鸭蛋等,加入了较多调味料的榨菜、即食水产制品和火锅底料等,或者加入了高浓度矿物质的保健食品等等。高盐食品基质中总砷的测定是一个难点问题,对于HG-AFS 法,未充分消解的复杂基质试样中砷不能完全被还原而使测定结果偏低[8],而消解过程中产生的一些有机质同样会对砷的电感耦合等离子体质谱信号产生增敏效应[9-11]。此外,在ICP-MS 法的标准测定模式(STD 模式)中,高盐食品基质中的氯在测定过程中会产生氩氯分子离子峰严重干扰砷的测定,因此STD 模式不适用于高盐高基体食品样品中砷的测定;在ICP-MS法的动能歧视测定模式(KED 模式)中,一般采用碰撞气氦气减小分子离子峰的干扰,但氦气同时会减小目标砷离子的灵敏度而影响测定的稳定性和准确度,而且高盐高基体对ICP-MS 法测定信号值的抑制与分析元素的电离能和质量数有关系[12,13],因此单纯依靠内标元素校正高盐基质的基体效应并不太现实。除了以上两种测定模式,ICP-MS 法的动态反应模式(DRC 模式)则是使用高活性的反应气体如氢气、氧气、甲烷气、氨气等作为工作气体,在反应池中工作气体与带电离子经过电荷转移、质子转移、原子转移及化合反应等过程实现消除干扰的目的,其中氧气可以与砷反应生成氧化砷离子,从而消除高盐基体产生的氩氯分子离子峰干扰。
DRC 模式虽然能够解决高盐基体产生的氩氯分子离子等质谱干扰,但是对于高盐高基体等复杂样品产生的基体效应却不产生作用,因此,本研究将基体匹配的方式与动态反应池技术结合起来,则能够解决高盐高基体样品中砷测定的一些难点问题[14,15]。基于日常实验室中常用的砷前处理方式和检测方法,本研究将详细探讨湿法消解和微波消解法对食品中总砷测定的影响,分析前处理方式对ICP-MS 法与HG-AFS 法测定的影响,研究有机基质、氯含量和内标校正元素等因素对高盐高基体中砷的ICP-MS 法测定信号值的影响,建立一种高盐食品基质中砷含量的基体匹配-DRC-ICP-MS 测定方法。本研究分析了高盐食品基质中砷测定的几个关键影响因素,将基体匹配的方法与动态反应池技术结合解决高盐高基体样品中质谱干扰和基体干扰对砷元素测定的影响,同时也为复杂食品样品中砷含量的测定提供一种思路。
1 材料与方法
1.1 仪器、试剂与材料
AFS-9700 双道原子荧光光度计,北京海光仪器公司;PE 2000P 电感耦合等离子体质谱仪,美国PerkinElmer 公司;Mars 6 微波消解仪,美国CEM公司;GS25-20A 赶酸仪,天津市莱玻特瑞仪器设备有限公司。
砷单元素标准溶液(1 000 mg/L),国家有色金属及电子材料分析测试中心;锗、铟内标单元素标准溶液(1 000 mg/L),国家有色金属及电子材料分析测试中心;亚砷酸根溶液标准物质(GBW 08666-21071),砷酸根溶液标准物质(GBW 08667-22051),一甲基砷溶液标准物质(GBW 08668-21101),二甲基砷溶液标准物质(GBW 08669-21071),砷甜菜碱溶液标准物质(GBW 08670-21101),无机砷和有机砷标准物质均购自中国计量科学研究院。
浓硫酸、高氯酸、过氧化氢、氢氧化钾、氯化钠(优级纯),国药集团化学试剂有限公司;硼氢化钾(优级纯),旭化成化学(山东)有限公司;抗坏血酸(分析纯),国药集团化学试剂有限公司;硝酸(优级纯),苏州晶瑞化学股份有限公司。
实验用水均为二次去离子水。
实验中涉及的实际样品,如板鸭、腊肉、榨菜、火锅底料、椒麻虾(水产制品)、即食鱿鱼(水产制品)、咸鸭蛋、酱油、保健食品、大米、婴幼儿辅助食品和婴幼儿配方奶粉均来自日常检验工作中所收集。
1.2 实验方法
1.2.1 溶液配制
砷单元素标准溶液和锗、铟内标单元素标准溶液用5%硝酸(体积分数,下同)或氯化钠基质溶液逐级稀释至所需浓度;
亚砷酸根溶液、砷酸根溶液、一甲基砷溶液、二甲基砷溶液、砷甜菜碱溶液标准物质用二次水逐级稀释至所需浓度。
氯化钠系列基质溶液:分别称取适量氯化钠,用5%硝酸定容即为氯化钠系列基质溶液(质量分数,以氯含量计)。
基体匹配标准工作溶液的配制:用阴性氯化钠基质溶液将砷单元素标准溶液逐级稀释至所需浓度。
1.2.2 样品前处理
样品的微波消解法和湿法消解分别按照GB 5009.11-2014 中5.2.1 微波消解法和12.2.1 湿法消解章节进行操作。
快速消解法:称取0.30 g 样品于50.0 mL 聚丙烯离心管中,缓慢加入1 mL 浓硝酸将所有样品均匀润湿,旋紧盖子并留1~2 圈的空隙防止反应太过剧烈,将离心管放置在120 ℃的可控温电热板上快速消解30 min,取下放冷后用水定容至10.0 mL 或25.0 mL。
1.2.3 实验步骤
1.2.3.1 氯含量对砷测定的影响
配制质量分数为0%、0.010%、0.020%、0.050%、0.10%、0.20%、0.50%、1.00%、2.00%、5.00% 的氯化钠基质溶液,其中分别包括空白基质溶液和含有20.0 μg/L 砷标准溶液的加标基质溶液,以考察氯离子对砷ICP-MS 信号值的影响。
1.2.3.2 内标校正元素的考察:
(1)配制质量浓度为200 μg/L 的锗内标溶液,然后分别往锗内标溶液中添加100 μg/mL 铁标准溶液和5.00 μg/mL 硒标准溶液,以考察铁元素和硒元素对锗内标ICP-MS 信号值的影响。
(2)配制质量分数为0%、0.010%、0.020%、0.050%、0.10%、0.20%、0.50%、1.00%、2.00%、5.00%的氯化钠基质溶液(含有200 μg/L 的锗内标溶液和铟内标溶液),其中分别包括空白基质溶液和含有20.0 μg/L 砷标准溶液的加标基质溶液,以考察锗内标和铟内标在氯化钠基质中对砷测定信号校正的影响。
1.2.3.3 添加回收实验
称取0.50 g 食盐样品,以φ=5%硝酸溶液溶解并定容至25.0 mL。对该样品进行4 水平6 平行加标回收实验(加标浓度为0.010、0.025、0.20、0.50 mg/kg),并测定加标回收率和RSD 值(相对标准偏差)。
1.2.4 仪器工作条件
微波消解仪工作条件如表1 所示,HG-AFS 和ICP-MS 仪器工作条件分别如表2 和表3 所示。

表1 微波消解仪工作参数Table 1 Microwave digestion instrument parameter

表2 HG-AFS仪器工作参数Table 2 HG-AFS instrument parameter
表3 ICP-MS仪器工作参数Table 3 ICP-MS instrument parameter
1.3 数据处理
实验过程涉及的所有数据均为多次测定后的平均值,其中氯含量和内标元素对砷测定的影响相关数据(图1 和图2),以不含氯离子的5%硝酸空白溶液为基准,分别对不同浓度的含氯基质溶液中砷的ICP-MS 计数强度值进行归一化处理,再进行图表化处理。

图1 氯含量对砷测定的影响Fig.1 Effect of chlorine content on arsenic determination

图2 锗内标和铟内标对砷测定的影响Fig.2 Effect of germanium and indium internal standard on the determination of arsenic
2 结果与分析
2.1 消解方式对砷测定的影响
氢化物发生原子荧光光谱法测定食品中总砷的原理,是将样品中各种形态砷彻底消解处理成无机砷形态,加入硫脲-抗坏血酸溶液使五价砷预还原为三价砷,再进行上机测定。如果样品中的有机砷没有彻底消解成无机砷形态,仪器无法进行测定,也必然会造成测定结果偏小。但是不同样品中的砷形态并不相同,这就会使得相同的消解方式对不同样品的消解效果并不一样。实验采用了湿法消解和微波消解法两种消解方式对20.0 μg/L(以砷计)的三价砷、五价砷、一甲基砷、二甲基砷和砷甜菜碱进行前处理,然后分别通过HG-AFS 和ICP-MS 测定回收率,结果如表4 所示。

表4 湿法消解和微波消解测定结果对比Table 4 Comparison of determination results between wet digestion and microwave digestion
由表4 数据中可以看出,湿法消解处理5 种砷形态,HG-AFS 测定总砷的回收率范围为81.20%~110.80%,总体上在可接受范围,但是砷甜菜碱的回收率还是偏低。微波消解条件参考GB 5009.11-2014附录A,但在此基础上,将最终的保持温度提高至200 ℃。其中三价砷、五价砷和一甲基砷组分HG-AFS 测定回收率范围为98.55%~104.40%,说明这3 种砷形态在此微波消解条件下,基本上消解完全,而二甲基砷和砷甜菜碱的HG-AFS 测定回收率分别只有37.15%和0.60%,说明二甲基砷和砷甜菜碱的微波消解效果很差,在HG-AFS 测定条件下很难被还原测定。湿法消解过程中会加入硫酸和高氯酸,其沸点分别为337 ℃和203 ℃,当消解至硫酸的白烟冒出,试样溶液中温度能达到300 ℃左右,砷甜菜碱的HG-AFS 测定回收率依然偏低(81.20%),而微波消解法设定的保持温度200 ℃,更难以完全消解砷甜菜碱等有机砷形态。同样是微波消解法处理,五种砷形态的ICP-MS 测定回收率范围为95.80%~103.35%,原因在于即使各种砷形态未消解完全,以分子形态存在于试样溶液中,在电感耦合等离子体中心通道7 000 K 左右的高温下,依然能够被电离,最终进入四级杆和检测器中被检测[1,2]。
在实际检验过程中,有些检验员为了省时省力,经常会使用微波消解法的试样溶液进行HG-AFS 法测定,对于某些特定产品,比如大米中砷形态主要以三价砷、五价砷和二甲基砷的形式存在[1],当二甲基砷等有机砷形态含量不高时,HG-AFS 测定结果和ICP-MS 测定结果之间可能不会有太大的差异。海产品(如海藻、海鱼、甲壳类、贝类等)中砷主要以砷糖和砷甜菜碱的形式存在[16,17],但是GB 2762-2017 中对于水产动物及其制品只有无机砷的限量要求,并未对总砷的限量进行相关规定,一般这类样品总砷含量会远远超出无机砷限量要求,因此只需要进行无机砷含量测定。但是对于一些添加了藻类或者水产动物及制品的婴幼儿辅助食品,按照国标要求,可以先进行总砷含量测定,此时如果按照微波消解法处理样品,再进行HG-AFS 测定,必然会造成结果的偏差。
因此,对于食品中总砷含量的测定,应严格按照国家标准进行样品前处理和测定,尤其是对于氢化物发生原子荧光光谱法测定食品中总砷,应严格按照湿法消解或者干法消解进行样品处理,在保证样品消解完全的前提下,尽量防止试样溶液在最后赶酸的过程中飞溅而损失。
2.2 ICP-MS测定砷影响因素的考察
2.2.1 有机质对砷测定的影响
实验采用快速消解法消解大米样品[18,19],考察了样品中未充分消解的有机质对砷测定的影响。本研究中采取快速消解法的优点是能在最大限度减少试剂用量的前提下,减少消解过程中引入的污染,提高检测的灵敏度和准确度,这种方法一般用于样品中易提取的铅、镉等元素的前处理和石墨炉原子吸收光谱法测定。但是未充分消解的样品基质可能会对待测元素产生基体干扰效应。快速消解法前处理大米样品,尽管样品未充分消解,大米中的砷也不可能消解充分,但是由表4 的数据可知,这并不会影响样品中总砷ICP-MS 法的测定。实验发现,快速消解法-ICP-MS 测定结果(定容体积为10.0 mL 和25.0 mL)分别比微波消解法-ICP-MS 测定结果偏大45%和22%,定容体积越小干扰越大,说明快速消解产生的基质会严重干扰ICP-MS 测定大米中总砷的含量。
实验中采用了74Ge和115In内标以校正基体效应,结果发现快速消解产生的基体对74Ge 和115In 内标的响应信号值并无太大的影响,而是单纯增大75As 的响应信号值,内标回收率总体上都在90%~110%范围内。因此,在使用ICP-MS 法测定食品中的总砷时,应该对样品进行充分消解,将样品中的有机物消解成无机物状态才能将对砷测定的基体效应降至最低。
2.2.2 氯含量对砷测定的影响
HG-AFS 测定食品中总砷对样品前处理同样有着较高的要求,但是ICP-MS 测定食品中总砷也并非是万无一失,因为ICP-MS 测定砷的质量数为75As,会受到分子离子峰40Ar35Cl+的严重干扰,而大部分食品样品中都含有不同含量的氯,尤其是高盐高基体的食品样品。
实验考察了ICP-MS 的STD 模式和KED 模式测定5%硝酸空白溶液和砷单元素标准溶液(20.0 μg/L,5%硝酸基质)在不同氯含量(包括0%、0.010%、0.020%、0.050%、0.10%、0.20%、0.50%、1.00%、2.00%、5.00%,质量浓度,下同)的氯化钠基质中的计数强度值,分别以不含氯离子的5%硝酸基质中砷的计数强度值为1 进行归一化处理,结果如图1 所示。
在STD 测定模式中,砷的本底值随着基质中氯浓度的提高而增大的非常明显,当氯的浓度为5.00%时,砷的本底值比5%硝酸基质中砷的计数强度值增大了300 多倍(图1a 中a 曲线);而在KED 测定模式中,在氦气的碰撞下(流量3.50 mL/min),氯的体积分数为5.00%时,砷的本底值仅比5%硝酸基质中砷的计数强度值增大了18 倍左右(图1a 中b 曲线),说明KED 模式能有效的改善基质中氯产生的分子离子峰(ArCl+)对砷测定的干扰。
砷标准溶液(20.0 μg/L)在不同浓度含氯基质中的信号响应值比较如图1b 所示。砷在含氯基质(氯化钠)中同时存在ArCl+的正干扰效应和基体干扰的负效应,在STD 测定模式中,5.00%含氯基质中砷的信号响应值比不含氯基质中砷的计数强度值增长了1 倍左右,这主要得益于ArCl+的正干扰效应大于氯化钠基体抑制效应;而在KED 测定模式中砷的计数强度随着氯含量的增大而逐渐减小,出现这种现象的原因主要是,碰撞气氦气能很大程度抑制ArCl+分子离子的正干扰,从而使得基体抑制效应大于分子离子的正干扰[20]。
2.2.3 内标校正元素的考察
在实际ICP-MS 测定的过程中,一般的做法都是KED 测定模式配合内标校正以减少分子离子峰的干扰,同时校准基体效应和仪器信号的漂移。ICP-MS 测定方法选用内标元素的原则首先要求内标元素在样品中含量越低越好,这样才不会干扰待测元素的测定,其次是要求待测元素和内标元素质量数相近,具有相似的电离行为,ICP-MS 测定食品中总砷一般会选用锗元素(Ge)作为内标,锗元素有较多同位素,常用的有72Ge+和74Ge+,而分子离子峰56Fe16O+和74Se+分别会干扰72Ge+和74Ge+的测定。本研究在日常检验食品样品中监控了近300个铁和硒含量较高的样品,发现保健食品中铁元素含量的范围为15~450 mg/100 g,硒元素含量的范围为0.020~15 mg/100 g;婴幼儿辅助食品和婴幼儿配方奶粉中铁元素含量的范围为4~10 mg/100 g,硒元素含量的范围为5~50 μg/100 g。因此实验考察了100 μg/mL 铁标准溶液和5 μg/mL 硒标准溶液(样品中铁含量以450 mg/100 g 计,硒含量以15 mg/100 g计,以称样量0.50 g,定容体积为25.0 mL 计算)对200 μg/L 锗内标的影响,结果如表5 所示。
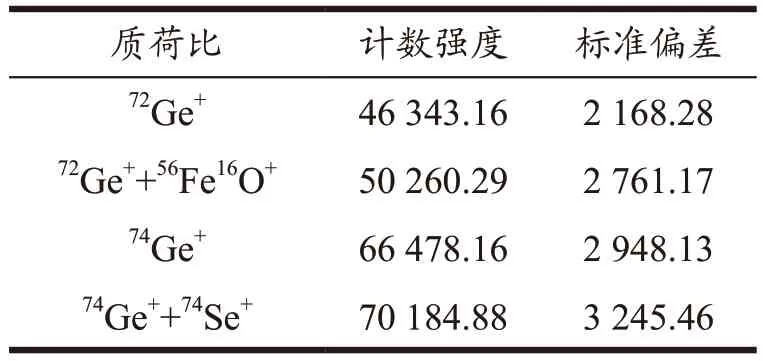
表5 铁元素和硒元素对锗内标测定的影响Table 5 Effect of iron and selenium on determination of germanium internal standard
从表5 中数据可以看出,72Ge 和74Ge 分别受56Fe16O+和74Se 干扰的影响,信号值都有所提高,ICP-MS 测定食品中总砷含量,通过内标校正基体效应和仪器信号漂移,以待测元素质谱信号与内标元素质谱信号的强度比与待测元素的浓度成正比进行定量分析,由56Fe16O+和74Se 干扰锗内标信号值造成最终砷校准浓度分别偏小7.79%和5.28%。很多样品中都含有较高浓度的铁元素,甚至可以达到百分含量级别,而硒元素一般含量较低,且74Se 丰度较低(0.87%),因此56Fe16O+对72Ge 的干扰一般会比74Se 对74Ge 的干扰更大,而且74Ge 同位素丰度(36.54%)比72Ge 同位素丰度(27.43%)更大,因此74Ge 可能更适合作为ICP-MS 测定食品中总砷的内标元素。但是对于硒含量很高的样品,74Se 的干扰依然会造成总砷校准浓度5.28%左右的负偏差,对于这种情况,可以选择115In 或者其他内标元素。
实验考察了在高盐基体中锗内标(74Ge)和铟内标(115In)对砷的ICP-MS 测定信号值的校准结果,如图2 所示。
以5%硝酸基质中的砷标准溶液(20.0 μg/L)的计数强度和内标元素的计数强度分别进行归一化处理,并将I(砷)/I(内标)(I为归一化后的计数强度值)为纵坐标做图,从理论上来讲,如果内标能够校正分子离子峰和基体效应的干扰,则校正后的I(砷)/I(内标)比值都应与5%硝酸基质中的比值保持一致,即为初始值1。但是在STD 测定模式中,校正后的I(砷)/I(Ge)和I(砷)/I(In)比值最高达到5.0左右,这说明STD 模式测定氯化钠基质中的砷时,ArCl+的干扰太过严重,导致砷的响应值快速增大,而氯化钠基体效应导致内标元素的回收率降至40%左右,综合影响导致校正后的I(砷)/I(内标)比值偏大很多,因此STD 测定模式完全不适用于氯化钠高盐基体中砷的测定。在KED 测定模式中,ArCl+的干扰大为减小,I(砷)/I(内标)比值的影响因素主要来源于氯化钠的基体干扰,而氯化钠基体效应对于质量数比较接近的元素的抑制作用较为相似,校正后的I(砷)/I(Ge)范围为1.05~1.13,校正后的I(砷)/I(In)范围为0.89~1.12。
值得注意的是,尽管KED 模式可以消除大部分ArCl+的干扰,内标也可以校正基体效应的干扰,但是以上数据都是砷标准溶液在理想环境中测试得出的,在氯化钠基质中,74Ge 和115In 内标的回收率从100%降至20%~40%,I(砷)/I(内标)比值校正的准确性与内标的信号响应值有着非常大的关系,当内标回收率大大超出了80%~120%的安全范围,即使I(砷)/I(内标)比值在可以接受的误差范围内,也说明砷的测定数据已经失信,其准确度需要得到严格的评价。
2.2.4 动态反应测定模式的考察
当测定高盐高基体的样品时,一方面样品中的氯会产生很强的ArCl+正干扰,另一方面高盐基体中大量电离的离子会占用离子通道,强烈抑制待测样品和内标元素的响应信号值,此时可以尝试ICP-MS 中的DRC 模式。DRC 模式是使用高活性的反应气体如O2、H2、NH3等作为工作气体,在反应池中工作气体与带电离子经过电荷转移、质子转移、原子转移及化合反应等过程实现消除干扰的目的。测定高盐高基体样品中的砷时,可以引入反应气O2,75As+与16O+发生分子碰撞化合反应生成75As16O+,从而避开40Ar35Cl+对75As+的干扰。实验测试了砷标准溶液(20.0 μg/L)在2.00% NaCl基质中,氧气流速和低质量数切割系数RPq 对75As16O+信号值的影响,结果如图3 所示。当氧气流速为0.80 mL/min 时,信号值达到最大。随着氧气流速的增大,在充当反应气的同时,多余的氧气也会碰撞已生成的75As16O+离子,从而降低其灵敏度。而随着RPq 值的增大,AsO+离子的信号响应值先增大后减小,并在0.30 处达到最大。综合考虑待测离子灵敏度和信噪比的影响,最终选择氧气流速为0.80 mL/min,RPq 值为0.30。在DRC 测定模式中,由于74Ge16O1H+离子会干扰75As16O+离子的测定,所以锗元素不适合DRC 模式中砷的测定,实际检测过程中可以选用115In 作为内标。
2.3 方法的准确度
通过引入反应气氧气,DRC 测定模式可以避开ArCl+的干扰,但是基体效应对信号响应值的抑制依然没有解决。为了得到准确的测定值,实验采用基体匹配法校正高盐基体的抑制效应,并按照实验方法对食盐样品(称样量0.50 g,定容体积25.0 mL)进行了4 个浓度水平的加标回收实验,每个浓度水平平行测定6 次,计算回收率和测定值的RSD(相对标准偏差),结果如表6 所示。总砷的加标回收率范围为91.50%~110.80%,RSDs 为0.76%~7.22%,符合GB/T 27404-2008《实验室质量控制规范食品理化检测》附录F 规定对于回收率和精密度的要求。按照仪器工作条件对阴性氯化钠基质溶液平行测定21 次,以3 倍标准偏差(s)计算检出限(3s),所得结果为0.003 mg/kg,以10 倍标准偏差(s)计算定量限(10s),所得结果为0.010 mg/kg,本方法检出限和定量限与GB 5009.11-2014 中第一篇第一法的检出限和定量限相当,说明本研究构建的检测方法稳定性好、适用性强。

表6 精密度和回收率实验结果Table 6 Results of tests for precision and recovery (n=6)
2.4 样品分析
采用本法和GB 5009.11-2014 中第一篇第一法(对照法)分别对不同氯含量的样品(往质量浓度为0.010%、0.020%、0.050%、0.10%、0.20%、0.50%、1.00%、2.00%、5.00%的阴性氯化钠基质溶液中添加20.00 μg/L 的砷标准溶液)进行测定,每个样品平行测定6 次。由于氯对砷的ICP-MS 测定信号值有严重的ArCl+分子离子干扰,因此参考GB 5009.11-2014 中第一篇第一法,选用KED 测定模式和氦气为碰撞气,测定75As+离子的信号值,本法选用DRC 测定模式和氧气为反应气,以基体匹配的方式测定75As16O+离子的信号值,并都选择115In为内标,测定结果如表7 所示。采用t检验法对测定结果进行统计,计算的t值均大于t0.90,10(1.81,双边),这说明本法和对照法测定值之间存在显著性差异,随着氯含量的增大,对照法测定值偏大10%左右,测定样品空白值也随着增大,内标回收率降至20%~40%,测定稳定性和准确度受到影响,而本法采用基体匹配的方式,样品空白小,内标回收率也能控制在90%~110%之间,测定值准确,方法稳定可靠。
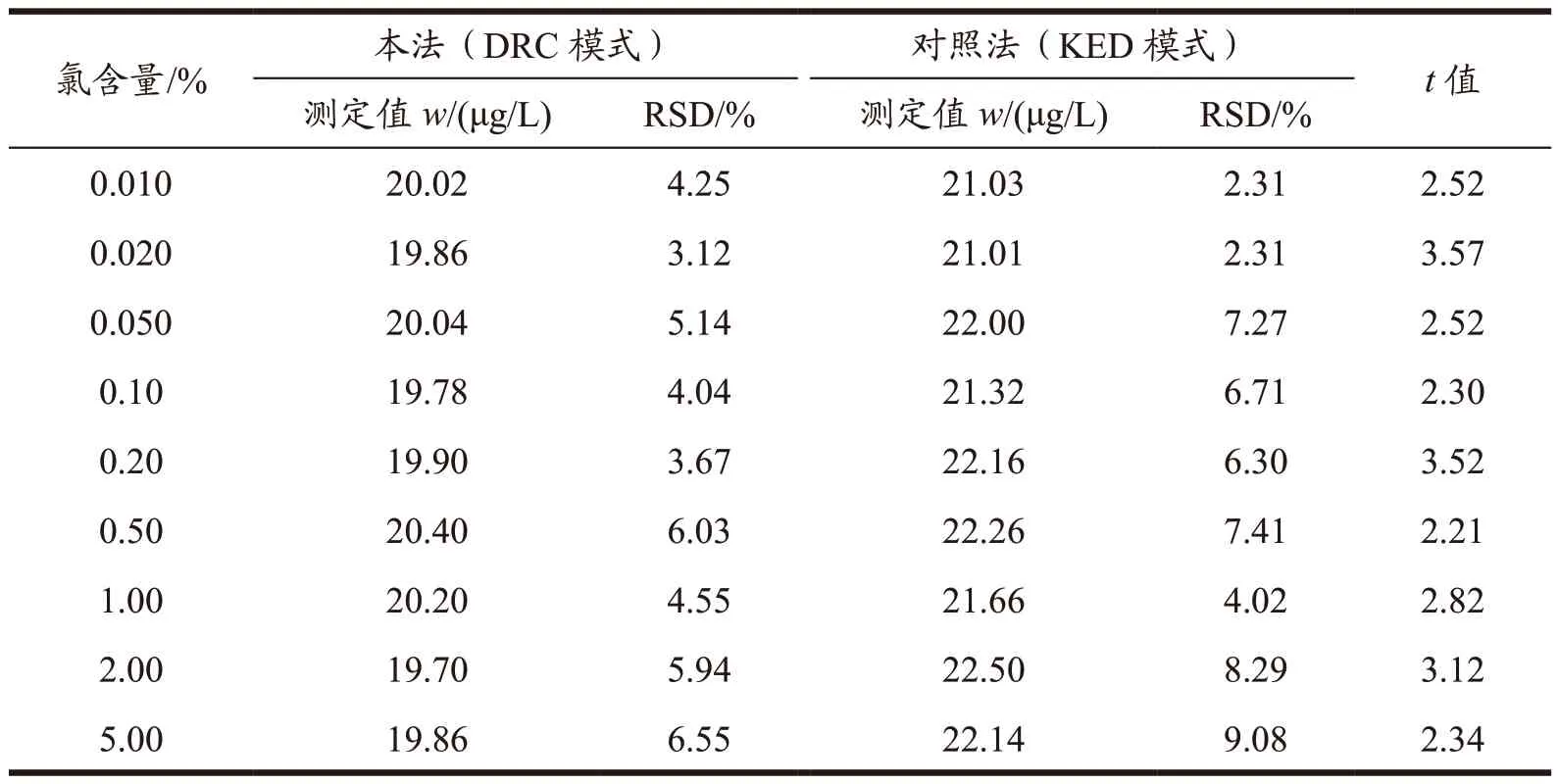
表7 样品的分析结果Table 7 Sample analysis results
不同氯含量中砷的DRC 模式和KED 模式测定值有显著性差异,因此采用本法、GB 5009.11-2014中第一篇第一法(对照法1,ICP-MS 的KED 测定模式)和GB 5009.11-2014 中第一篇第二法(对照法2,HG-AFS 法)分别对实际高盐基质食品样品进行测定,并分别进行添加测试加标回收率。(测试样品:板鸭、腊肉、榨菜、火锅底料、椒麻虾(水产制品)、即食鱿鱼(水产制品)、咸鸭蛋、酱油、保健食品,称样量0.50 g,定容体积25 mL,加标量为0.50 mg/kg),测定结果如表8 所示。本法和HG-AFS 测定高盐基体食品样品数据比较吻合,但是HG-AFS 法测定检出限较高,9 个样品中只有3个样品检出,ICP-MS 的KED 模式测定数据和加标回收率相较于本法都偏大一些,因此本法采用ICP-MS 的动态反应测定模式结合基体匹配的方式测定高盐基体食品样品中总砷,能在保证较低检出限的同时得到较为准确的测定结果。
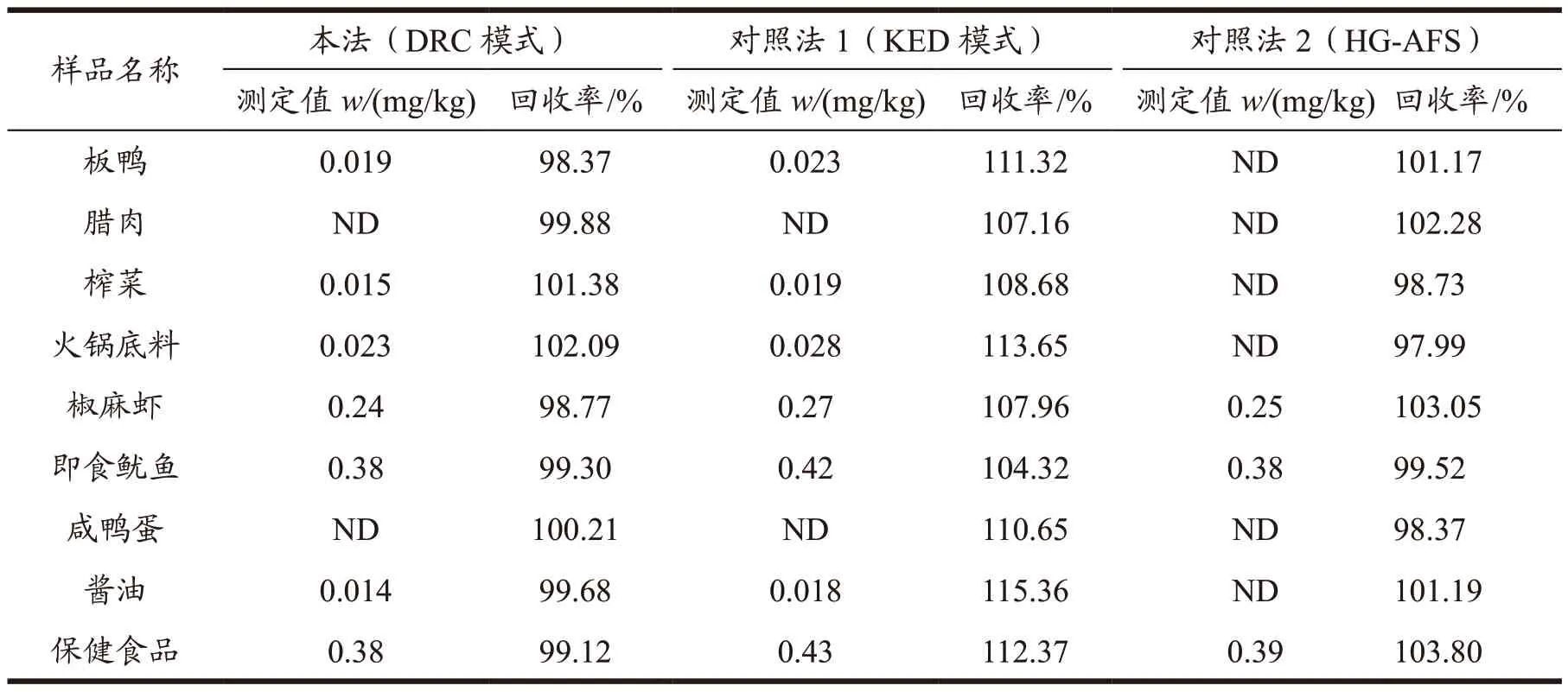
表8 高盐食品样品的分析结果Table 8 High salt food sample analysis results
3 结论
本研究深入探究了GB 5009.11-2014《食品安全国家标准 食品中总砷及无机砷的测定》中存在的一些问题,实验发现不同砷形态需要的消解温度并不一样,微波消解法消解不了大部分的有机形态砷,因此对于HG-AFS 法测定食品中总砷,前处理方法必需通过湿法消解或者干法消解等方法,提高消解温度将不同砷形态彻底消解才能完全测定。ICP-MS法测定食品中总砷,会受到试样溶液中有机质和高盐基体效应的影响,其中有机质对砷灵敏度信号值产生增敏效应,而高盐基体则会同时产生ArCl+分子离子正干扰和基体抑制效应。内标元素72Ge 和74Ge 分别会受到56Fe16O+和74Se 干扰的影响,对样品中铁元素和硒元素的含量和丰度比进行分析,得出74Ge 可能更适合作为ICP-MS 法测定食品中总砷的内标元素的结论。通过优化引入氧气的流速和低质量切割系数(RPq)等仪器参数,采用ICP-MS的动态反应测定模式(DRC)结合基体匹配的方式测定高盐高基体食品中的总砷,可以避免氩氯分子离子的干扰和减小基体效应的影响,测定方法灵敏度高,检出限较低。本研究对于高盐高基体等复杂食品基质中总砷含量的测定,具有较高的参考价值和借鉴意义。
