使用二代冷冻球囊消融右下肺静脉难易程度的影响因素
2024-05-09张坤孙光瑶白金龙王沛泽方丕华
张坤 孙光瑶 白金龙 王沛泽 方丕华
心房颤动(房颤)是临床常见的心律失常,应用二代冷冻球囊消融治疗房颤取得良好的效果,消融治疗的基本目标是达到肺静脉隔离(pulmonary vein isolation, PVI)[1-2]。在操作过程中,右下肺静脉是公认的最具有挑战性的[3],有时需要多次操作或通过射频消融补点才能实现肺静脉隔离。本研究通过回顾性分析探索影响右下肺静脉隔离的解剖学因素,以进一步提高电隔离右下肺静脉的操作技巧。
1 对象与方法
1.1 研究对象
回顾性分析2019年6月至2022年3月在泰达国际心血管病医院首次使用二代冷冻球囊消融的房颤患者234例。依据右下肺静脉消融次数分为困难组(56例)和容易组(178例)。消融困难组标准定义为冷冻球囊消融术中需要进行3次及以上冷冻消融或者需要射频消融补点进行电隔离的肺静脉,因温度下降过快(通常低于–55℃)提前终止冷冻而进行后续巩固消融的病例除外;仅需要1次或2次冷冻消融即完成电隔离的肺静脉定义为容易组。患者均明确诊断为房颤且具有导管消融适应证。排除标准:合并中至重度瓣膜病,左心房血栓,可逆原因导致房颤,3个月内心肌梗死,有抗凝禁忌证患者,房颤消融史,肾功能不全,妊娠,有严重合并症,纽约心脏病协会(New York Heart Association,NYHA)心功能分级Ⅳ级。所有患者术前均签署知情同意书,该研究符合2013年《赫尔辛基宣言》的要求。
1.2 术前准备
所有患者术前行左心房C T 血管造影(C T angiography,CTA)检查明确肺静脉解剖。所有患者术前完善各项血液检验,行经胸超声心动图、经食管超声心动图检查,未使用口服抗凝药的患者术前使用依诺肝素抗凝治疗,已使用华法林或新型口服抗凝药的患者围术期不间断使用。
1.3 手术方法
局部麻醉下穿刺左侧股静脉放置10极冠状静脉窦导管和右心室4极导管。穿刺右侧股静脉行房间隔穿刺,穿刺后即刻给予普通肝素(100 IU/kg)抗凝,监测活化凝血时间(activated clotting time,ACT)维持在250~350 s。穿刺成功后交换可调控导管鞘(FlexCath Advance,美敦力公司,美国)至左心房。沿鞘管送入直径28 mm的二代冷冻球囊(Arctic Front Advance,美敦力公司,美国),并通过内芯送入8极环形导管(Achieve,20 mm,美敦力公司,美国)记录肺静脉电位(pulmonary vein potential ,PVP),由左至右进行冷冻球囊消融。冷冻消融方案:使用注射对比剂方法判断封堵情况,上肺静脉使用近端封堵技术避免球囊过深;每一根肺静脉如隔离时间(time to isolation, TTI)≤60 s或者60 s达到–40℃,则一次性冷冻180 s,但最低温度不低于–58℃;如TTI>60 s或温度下降不理想,则停止冷冻消融,调整球囊再次封堵后冷冻消融,如不能完全封堵,使用分段电隔离,消融2~4次,消融时间120~180 s;如反复消融不能电隔离,则射频消融补点。
1.4 主要观察指标
冷冻球囊消融术中实时记录冷冻过程中TTI、最低温度(Tn)、冷冻消融次数、累积消融时间。实时记录PVP,定义为在冷冻消融过程中至少有1对Achieve电极信号通道可记录到PVP,冷冻消融过程中可明确观察到PVP的延迟、消失。手术时间指静脉穿刺至器械撤出体内的时间。所有患者的肺静脉CTA均由有5年以上工作经验的影像医师分析并测量肺静脉开口的最大内径和最小内径(即长径和短径),内径比定义为长径/短径(图1B)。肺静脉内径和角度均通过分析CTA图像测量,在CTA三维重建图上,在右前斜位测量右下肺静脉主干中线或主要下分支(分支开口于近段且发育粗大)至垂直轴的角度,定义为肺静脉下向成角(图1C)。在CTA横切面上,肺静脉主干中心线与矢状轴的成角定义为肺静脉后向成角(图1D)。在横切面上,取主动脉根部无冠窦(non-coronarycusp,NCC)窦底切面为基线,计算下肺静脉开口处下缘切面与基线切面的间距,定义为下肺静脉开口下缘相对高度(高于NCC切面为正值,低于NCC切面为负值);测量上肺静脉开口下缘与下肺静脉开口上缘的间距,定义为两肺静脉间间距(图2)。分支类型:右下肺静脉有分支在主干开口至分支开口≤5 mm定义为早分支,有两条及以上早分支定义为多分支(图3)。冷冻球囊消融术有一定的学习曲线,特别是针对右下肺静脉的操作,术者的熟练度有直接的关系[4]。本研究中,为评估术者手术熟练度这一因素对操作的影响,结合我中心冷冻球囊消融术开展的实际情况,以手术日期排序,2019年度的病例定义为早期病例,2020年度及以后的病例定义为后期病例。
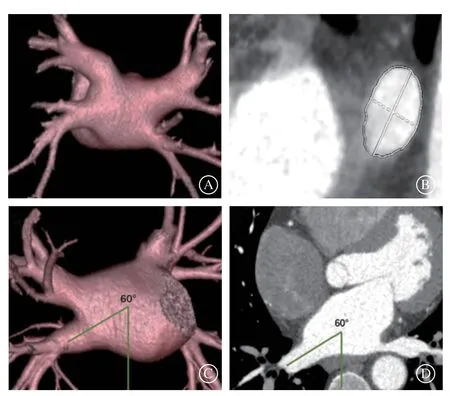
图1 肺静脉三维重建及内径、角度测量 A.肺静脉三维重建;B.肺静脉内径测量;C.肺静脉下向成角;D.肺静脉后向成角Figure 1 3D reconstruction and measurement of inner diameter and angle of pulmonary veins
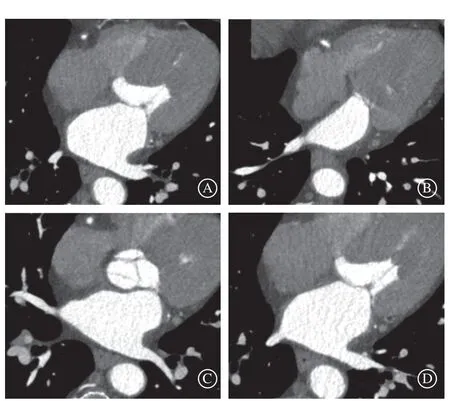
图2 右下肺静脉高度及两肺静脉间距测量 A.无冠窦基底部切面(SL–98.0 mm);B.右下肺静脉开口下缘切面(SL –115.0 mm);C.右上肺静脉开口下缘切面(SL –88 mm);D.右下肺开口上缘切面(SL–100 mm);计算右下肺静脉相对高度为B 切面与A 切面SL 差值–17 mm,右侧两肺静脉间距为C 切面与D 切面间距12 mmFigure 2 Measurement the height of RIPV and distance between the two pulmonary veins

图3 右下肺静脉分支情况 A.无早分支;B.1 早分支;C.多分支Figure 3 Schematic diagram of the right lower pulmonary vein branch
1.5 统计学分析
所有数据采用SPSS 26.0软件进行统计学分析。对连续性变量进行正态性检验,符合正态分布的连续性变量采用(±s)表示,非正态分布的连续变量采用[M(Q1,Q3)]表示,组间比较采用独立样本t检验或t’检验;计数资料以百分比表示,应用χ2检验或其校正检验。采用Logistic回归分析影响肺静脉冷冻难易的因素,向前步进法。针对有意义的因素绘制受试者工作特征(receiver operatingcharacteristic,ROC)曲线,计算ROC曲线下面积(area under curve,AUC),并根据约登指数确定最佳截断值。以P<0.05为差异有统计学意义。
2 结果
2.1 两组患者基线资料比较
本研究共计纳入234例患者,年龄(62.8±8.1)岁,其中女87 例(37.2%),阵发性房颤16 4 例(70.1%)。两组间基线资料比较,差异均无统计学意义(均P>0.05,表1)。

表1 两组患者基线资料比较Table 1 Patient characteristics at baseline
2.2 两组患者手术情况比较
所有患者均术中实现肺静脉隔离,容易组中126例(70.8%)患者通过单次冷冻隔离肺静脉,52例(29.2%)患者通过2次冷冻隔离肺静脉。困难组中,通过3次冷冻隔离的患者有31例(55.4%),4次及以上冷冻隔离25例(44.6%),有2例困难组病例需行射频消融补点。困难组患者手术时间明显较长,X线曝光时间和X线剂量亦明显增加(均P<0.05),PVP实时记录率困难组较低(33.9%比49.4%,P=0.042),冷冻最低温度容易组更低[(–48.0±6.2)℃比(–44.6±6.5)℃;P<0.001]。在困难组患者中,早期病例的比例更高(46.4%比19.7%,P<0.001;表2)。

表2 两组患者冷冻消融参数比较Table 2 Comparison of procedural data
2.3 右下肺静脉解剖特点
两组患者右下肺静脉下向成角可见明显差异,容易组(59.5±12.3)°,困难组(65.1±14.6)°,差异有统计学意义(P=0.005);内径、内径比、两肺间距、开口高度、后向成角、早分支等解剖特点比较,差异均无统计学意义(均P>0.05,表3)。

表3 两组患者右下肺静脉解剖特点比较Table 3 Comparison of anatomical characteristics of RIPV
2.4 Logistic回归分析
纳入上述解剖因素和手术时期(早期病例、后期病例)进行Logistic回归分析,下向成角和早期病例是影响肺静脉消融难易程度的独立危险因素(OR0.968,95%CI0.943~0.993,P=0.013;OR0.285,95%CI0.143~0.565,P=0.001)。ROC曲线(图4)分析显示,使用下向成角预测右下肺静脉封堵困难的AUC 0.745(95%CI0.668~0.822,P<0.001),提示该指标具有良好的预测价值;当下向成角的最佳截断值为63.5°时,敏感度67.9%,特异度71.9%。

图4 下向成角影响RIPV 封堵的ROC 曲线Figure 4 ROC curve of downward angle inf luence on RIPV Sealing
3 讨论
目前,临床上治疗房颤使用二代冷冻球囊进行肺静脉隔离具有良好的安全性和有效性[5],是治疗房颤特别是阵发性房颤的一线方案[6-7]。由于大多数房颤是由肺静脉内的异常电活动所促发的[8],所以肺静脉隔离的持久性直接决定了消融治疗的远期效果,循证医学证据显示冷冻球囊消融具有良好的临床效果[9]。而冷冻球囊由于其相对固定的球囊形态使得操作难易度与肺静脉的解剖结构有一定的相关性,术前使用肺静脉CTA评估肺静脉及其分支走行具有重要的价值,而且会对远期预后产生影响。
目前,已经有研究探讨肺静脉的解剖形态如肺静脉内径、椭圆比、肺静脉角度等解剖参数可以影响冷冻球囊消融的效果[10]。Yalin等[11]研究发现,肺静脉解剖异常如肺静脉共干的患者在冷冻消融术后有更高的房性心动过速的发作。亦有研究发现右上肺静脉的内径与上腔静脉的间距等解剖参数与膈神经损伤具有相关性[12]。同时,肺静脉隔离困难需要射频消融补点隔离,也预示着更高的房颤复发率[13]。目前,已经有相关研究显示肺静脉解剖结构影响冷冻温度和手术疗效[14-15],并且充分了解肺静脉解剖参数也可以预测手术难度[16-17]。
目前临床上一致认为右下肺静脉的操作难度是最大的,学习曲线最长[4,18]。在本研究中的确发现,术者的手术熟练度对于右下肺静脉的操作具有显著影响。在临床实践中,熟练度更高的术者,可灵活操作球囊呈多种角度进行尝试封堵,比如“曲棍球”技术,需要对肺静脉走行以及导管操作有深刻的理解。本研究中,右下肺静脉封堵困难组和容易组患者,容易组的右下肺静脉封堵的下向成角小于困难组,统计显示最佳截断值为63.5°,即当下向成角角度大于63.5°时,即右下肺静脉封堵较为水平时,预示着可能封堵较为困难。分析其原因,可能与水平走行的肺静脉,难以做成“曲棍球”形态进行封堵。同时,操作难易与术者熟练度有明显关系,熟练度提高,可选择更为理想的分支,更容易实现“曲棍球”形态,封堵更好,右下肺静脉封堵球囊冷冻成功的概率越高。既往针对复发病例的研究显示右下肺静脉下缘是容易有电位恢复的位置[19]。一项多中心的研究显示使用二代冷冻球囊后,左侧肺静脉的损伤“漏点”有所减少,而右肺静脉并没有显著差异[20]。
有研究显示,单次冷冻策略与进行额外的巩固消融相比,具有相似的疗效[21]。在本研究中封堵良好的病例多采用单次冷冻的方法,可以节省时间,提高手术效率。容易组中,球囊最低温度明显低于困难组,PVP记录率高于困难组,预示着隔离困难的肺静脉,可能出现PVP恢复的概率增大。但是,远期复发率与冷冻困难的相关性,有待进一步研究。由于冷冻球囊操作中,可调弯鞘管的支撑力是影响球囊封堵效果的重要因素,这可能与穿刺房间隔的位置有关系,但是缺少直观的指标来衡量,研究中无法对穿刺房间隔位置进行精确的统计和评估,随着心腔内超声的不断应用,可能对这一因素进行详细的研究。
本研究主要有以下不足:(1)单中心的回顾性研究,样本量有限;(2)研究中以肺静脉隔离为终点,没有进一步研究两组间手术远期成功率的差异,有待进一步研究分析右下肺静脉封堵隔离难度和房颤远期复发的关系。
总之,右下肺静脉的下向成角和术者熟练度是影响冷冻消融难易程度的主要因素。
利益冲突 所有作者均声明不存在利益冲突
