药物涂层球囊在经皮冠状动脉介入治疗中的应用效果分析
2024-05-08马苏林
马苏林
(北京核工业医院心血管内科,北京 102413)
经皮冠状动脉介入治疗在冠心病的治疗中十分常用。支架和球囊作为介入治疗中最常用的器械,近年来发展迅速[1]。器械的结构和特性决定了其性能,在实际使用中,医生会根据不同类型器械的特点采取不同的策略和技术。临床诊疗工作中,支架、球囊等器械的选择主要是根据靶血管病变的特点,操作者可以根据器械的性能做出综合判断[2]。每种器械都有自己的特点,因此临床介入医生面临着复杂的器械选择问题。熟悉器械并有确切的循证医学证据支持,能够在很大程度上提高介入治疗的成功率,减少术后并发症。介入治疗的发展离不开这些重要器械的改革[3]。随着生物医学工程技术的发展,冠状动脉介入治疗已从开始的经皮腔内冠状动脉成形术发展到药物洗脱支架置入术,能够减少冠状动脉再狭窄的发生[4]。如今,在经皮冠状动脉介入治疗中,支架是使用最普遍的医疗器械,通常由不锈钢、镍钛合金或钴铬合金制成。心脏支架最初出现于20世纪80年代,经历了裸金属支架(BMS)、药物洗脱支架(DES)和生物可吸收支架(BVS)等技术演变。每一次技术升级都在一定程度上弥补了前一代技术的不足,药物洗脱支架可谓是介入医学领域的最大革新和亮点。但药物洗脱支架置入术仍有一定的再狭窄概率[5]。另外,临床尚未形成统一、科学地处理冠状动脉分叉病变、小血管病变的方法[6]。近几年来,药物涂层球囊导管受到了广泛的研究和讨论。该技术是一种新型的技术手段,它利用球囊作为药物载体,球囊膨胀期间能够迅速转移抗细胞增殖药物,作用于靶病变血管,使冠状动脉快速吸收药物,有效预防血管再狭窄的发生[7]。而与药物洗脱支架相比,这种方法不需要在血管中预留永久性植入物,减少了后续冠状动脉的正性重塑,并可预防炎症反应的发生[8]。采用这一方法可以扩大冠心病的诊断范围并选择更有效的治疗手段。本文就药物涂层球囊在经皮冠状动脉介入治疗中的应用效果进行探讨分析[9],现详细报道如下。
1 资料与方法
1.1 基线资料
于2019 年1 月至2020 年12 月期间抽取冠心病患者60 例。这些患者均接受了经皮冠状动脉介入治疗。采用随机数表法将患者分为对照组和观察组,各30 例。对照组中包括16 名男性和14 名女性,年龄在42 ~79 岁之间,平均年龄为(60.93±1.46)岁。观察组中包括17 名男性和13 名女性,年龄在42 ~80 岁之间,平均年龄为(60.93±1.51)岁。两组基线资料差异无统计学意义(P>0.05),可对比。
1.2 方法
患者入院后,口服300 mg 阿司匹林和300 mg 氯吡格雷,之后每日服1 次阿司匹林(100 mg/次)、1 次氯吡格雷(75 mg/次)。手术时,使用普通肝素(剂量100 U/kg)抗凝,手术过程中每小时追加肝素1000 U,同时对活化凝血时间进行测定,指导调整肝素用量。所有患者均采取桡动脉穿刺,取常规体位开展冠状动脉造影,了解病变冠状动脉的具体情况。对照组:采用普通球囊(Sprinter 快速交换球囊)扩张冠状动脉,按1:3 比例稀释造影剂,为球囊充气加压,控制初次充盈的时间为30 s,压力为8 个大气压,逐渐增加充气时间和压力,最终达到90 s,在排空球囊后将其撤出。研究组:采用药物涂层球囊(Vesselin)扩张冠状动脉,使用高亲脂性紫杉醇进行涂层,球囊直径2 ~3 mm,先用普通球囊对靶病变位置进行扩张,当内膜未出现明显撕裂、夹层时送进药物涂层球囊,直到靶病变位置,完成扩张,扩张速度1 atm/5 s,渐渐增加到6 atm,直至达到最大压力并维持此状态30 ~60 s,同时确保球囊两侧均超过病灶区域至少3 mm 的长度。术后两组均持续随访6 个月。
1.3 观察指标
(1)观察并比较两组治疗后动量冠状动脉造影结果,包括血管(右冠状动脉、回旋支、前降支)病变段直径、血管长度 。(2)比较两组术前、术后即刻及术后6 个月的病变段最小管腔直径 。(3)比较两组晚期管腔丢失情况。
1.4 统计学方法
2 结果
2.1 两组治疗后定量 冠状动脉造影结果
治疗后定量冠状动脉造影结果显示,两组的血管直径、血管长度差异无统计学意义(P>0.05)。详见表1。
表1 两组治疗后定量冠状动脉造影结果(mm,±s)
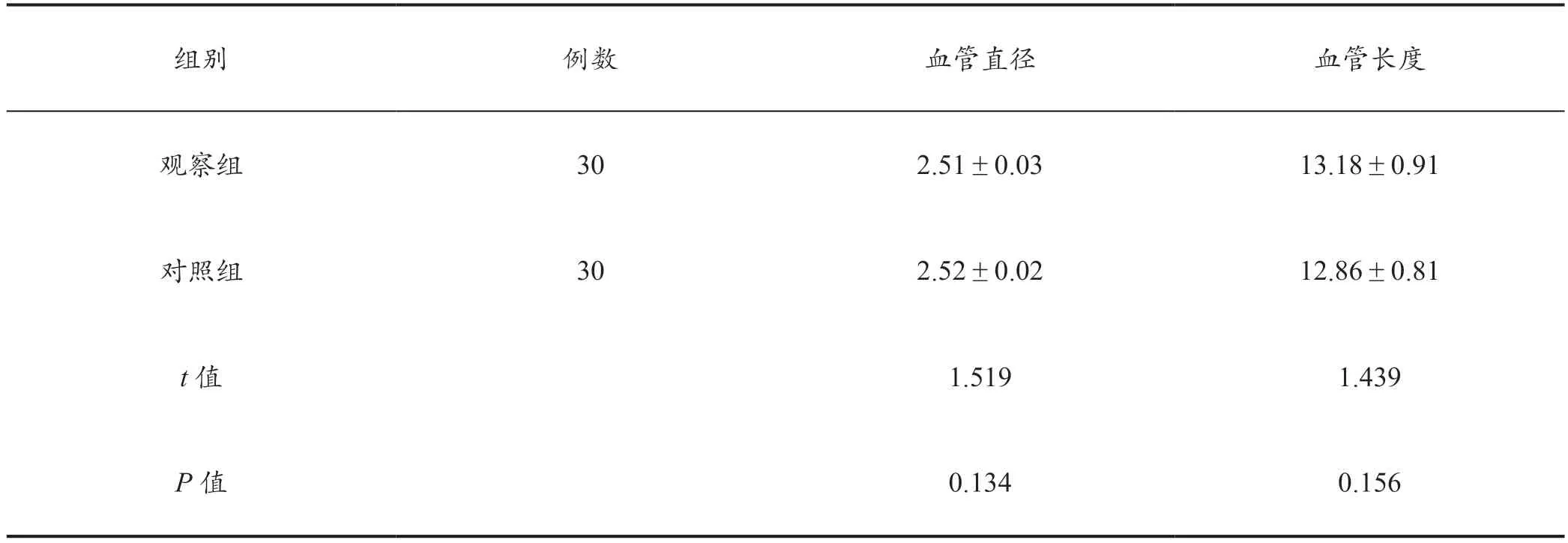
表1 两组治疗后定量冠状动脉造影结果(mm,±s)
组别 例数 血管直径 血管长度观察组 30 2.51±0.03 13.18±0.91对照组 30 2.52±0.02 12.86±0.81 t 值 1.519 1.439 P 值 0.134 0.156
2.2 两组手术与随访数据
术前,两组的最小管腔直径差异无统计学意义(P>0.05)。术后即刻及术后6 个月,观察组的最小管腔直径均大于对照组,差异有统计学意义(P<0.05)。观察组晚期管腔丢失小于对照组,差异有统计学意义(P<0.05)。详见表2。
表2 两组手术与随访数据(mm,±s)
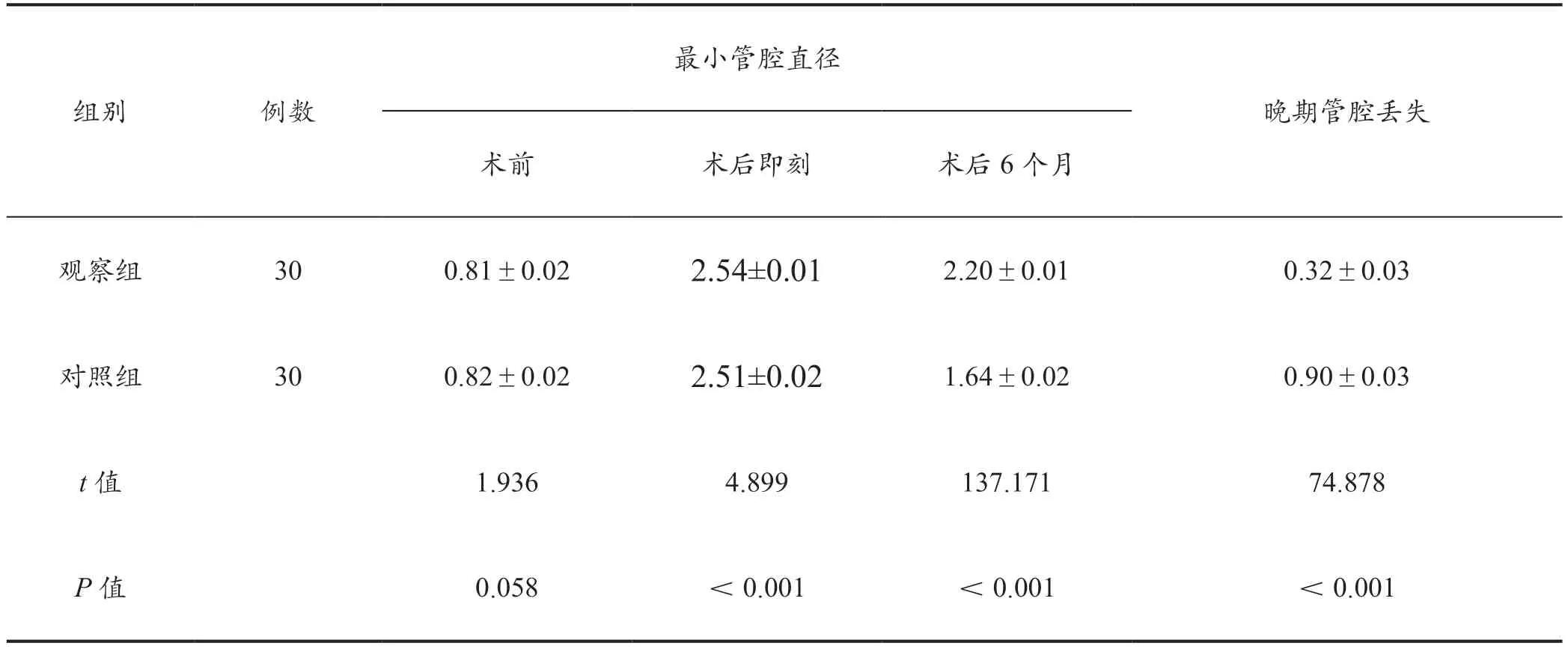
表2 两组手术与随访数据(mm,±s)
最小管腔直径组别 例数晚期管腔丢失术前 术后即刻 术后6 个月观察组 30 0.81±0.02 2.54±0.01 2.20±0.01 0.32±0.03对照组 30 0.82±0.02 2.51±0.02 1.64±0.02 0.90±0.03 t 值 1.936 4.899 137.171 74.878 P 值 0.058 <0.001 <0.001 <0.001
3 讨论
经皮冠状动脉介入治疗是一种通过心导管技术来扩张狭窄的冠状动脉以改善心肌血液循环的方法,包括经皮腔内冠状动脉成形术和冠状动脉内支架植入术。介入手术技术及器械的发展能优化手术过程,减少术后并发症,为患者提供更大的益处[10]。近年来随着经皮冠状动脉介入治疗技术的发展,各种新型介入器械层出不穷,其中最常见的器械是球囊和支架。在实际操作过程中,对于冠状动脉小血管病变患者而言,由于血管管腔相对较小,若使用支架介入治疗,可能因为支架膨胀不全而引发再狭窄[11]。如果仅仅使用普通的球囊扩张,除了弹性回缩外,术中还可能对血管壁造成撕裂等损伤,后续产生严重的副作用,如急性管腔收缩、管口横截面损失等[12]。即便术中没有发生任何并发症,术后2 ~3 个月也极易因内膜增生而出现再狭窄,这意味着再次血运重建的可能性无法避免。我们应仔细权衡各种治疗方案的益处和风险,除了要注意血管解剖外,还要考虑患者的临床情况、技术因素和现实情况[13]。2014 年,欧洲心脏病学会指南推荐药物涂层球囊和新一代DES 作为支架内再狭窄(ISR)治疗的首选策略[14]。
目前,临床尚未形成统一、科学地处理冠状动脉分叉病变、小血管病变的方法,研究该患者群体冠状动脉介入治疗中采用药物涂层球囊的效果,能够进一步优化手术策略,为心血管疾病的治疗提供更好的路径,减少手术并发症,改善冠心病患者的预后[15]。与传统支架相比,药物涂层球囊具有诸多优势,越来越多的临床研究证实了它在治疗冠状动脉小血管病变、冠状动脉分叉病变、冠状动脉慢性完全闭塞病变和冠状动脉弥漫性病变等方面的优势[16]。首先,药物涂层球囊没有金属框架,有助于维持涂层药剂分配的一致性,使得药剂能在特定血管壁部位实现均衡覆盖,并且能够保持初始的血管解剖形态,避免在治疗冠状动脉小血管病变和分叉病变时对血流造成影响。另外,当处理ISR 问题时,药物涂层球囊能有效规避需要采用双层支架进一步缩小血管管腔 的问题,大量试验已经证实ISR 是药物涂层球囊治疗的适应证之一。再者,药物涂层球囊不含聚合物基体,可降低慢性炎症反应与晚期血栓形成的可能性,因此有可能缩短双重抗血小板治疗时间(仅需治疗1 ~3 个月)[17]。除了以上提到的患者群体之外,药物涂层球囊相较于支架,更适用于那些高出血风险患者,如血友病、有出血病史、消化道溃疡或严重肾功能损伤群体。对于正在服用抗凝剂或近期接受过手术治疗的患者,如心房颤动患者、人工心脏瓣膜置换术后患者、血管内皮功能异常或短期内发生过ISR 的患者,药物涂层球囊十分适用,同时还适用于不愿意接受支架植入的患者[18]。
基于循证医学,我们应为患者制定个体化治疗方案,并灵活参考指南。最近几年,药物涂层球囊为冠心病的治疗开辟了新途径。药物涂层球囊携带有抗血管内膜增生药物,药物释放后可抑制血管内膜增生,进而抑制平滑肌细胞增殖,预防靶病变血管再狭窄。紫杉醇属于紫杉烷化合物,具有较高的亲脂性,吸附率高,可抑制血管内膜增生,对细胞骨架形成产生抑制,阻断细胞有丝分裂,阻止平滑肌细胞快速增殖,预防内膜炎症反应的发生[19]。目前,紫杉醇是药物涂层球囊中最常用的药物涂层成分,在冠状动脉介入治疗中具有显著优势。涂层球囊能够高效释放药物,贴近血管壁,确保药物浓度,使血管迅速吸收,发挥抗血管内膜增生的作用。使用药物涂层球囊时,药物释放比支架的网格梁更均匀,能够解决药物释放不均的问题。特别是在处理分叉病变时,在侧支血管使用药物涂层球囊可以全面释放药物,防止侧支血管开口无药物覆盖,预防血管开口处再狭窄。此外,药物涂层球囊无需金属支架支撑,可以保持原始血管的解剖结构,预防异常血流出现,更适用于冠状动脉分叉病变和小血管病变的处理。此外,药物覆盖的球囊没有留下任何金属网状结构或聚合物基质,可以降低因植入异物而引发血栓的风险,从而缩短双抗治疗的时间,降低并发症的发生风险[20]。
综上所述,在经皮冠状动脉介入治疗中使用药物涂层球囊效果显著,可有效预防再狭窄的发生。
