低浓度聚丙烯酰胺含量的检测及溶液离子的影响
2024-05-03邹文杰余可馨
饶 博,邹文杰,赵 伟,余可馨
1) 北京低碳清洁能源研究院,煤炭开采水资源保护与利用国家重点实验室,北京 102211 2) 北京科技大学土木与资源工程学院,北京100083
混凝法运行稳定、处理效率高、实用性强、成本低,是水处理中必不可少的重要单元.絮凝作用的对象主要是水中的憎液溶胶及悬浮颗粒,絮体也可共沉淀去除部分溶解性物质,絮凝剂的类型直接决定了絮凝效果的好坏.聚丙烯酰胺由于其优良的絮凝性能和较低的单体价格,常作为絮凝剂用于废水处理[1-2].聚丙烯酰胺可分为非离子型、阴离子型和阳离子型,活性基团为酰胺基,可通过吸附、电中和和架桥作用絮凝微细颗粒形成絮体.聚丙烯酰胺可单独使用,也可与无机盐絮凝剂配合处理选矿废水,处理每吨干矿泥聚丙烯酰胺用量可达几十克[3-4].然而,处理后的废水因含残余聚丙烯酰胺(PAM)较大程度影响了水质及其回用,若回用于选煤选矿等生产工艺易造成浮选指标变差等问题[5].
在选矿废水处理系统中,聚丙烯酰胺的浓度范围大致为0~10 mg·L-1[6].目前检测聚丙烯酰胺最常用的方法主要有紫外分光光度法、淀粉-碘化镉法[7]、浊度法[8]、黏度法[9]、荧光分光光度法[10]、沉淀法[11]、滤浓缩薄膜干燥法[12]、尺寸排阻色谱法[13]和放射性标记法[14].淀粉-碘化镉光度法检测范围约在0.1~60 mg·L-1,检出限高、操作复杂、测量范围窄,对溶液环境有较高要求.浊度法操作简便,但其所需的检测样品量大,并且其检测结果会受到重金属离子和阴离子表面活性剂的干扰,检测浓度范围在100~300 mg·L-1,在测定环境温度较高或较低和样品较少时均不宜采用.黏度法要求部分水解聚丙烯酰胺(HPAM)溶液的黏度和浓度的变化成正比关系,仅能用于已知组分的纯净体系,且分子量大小、水解度、离子强度、溶液环境和剪切速率都会影响聚合物黏度,实际应用时受到很大限制.荧光分光光度法会受到水体中有机物的干扰,并且操作复杂、实验反应速度缓慢.沉淀法仅在聚丙烯酰胺浓度很高时使用,另外当样品中含有盐或表面活性剂时,需将样品溶液渗析后才能检测,使得此方法的分析成本较高,而且不能满足现场实时监测的需求.超滤浓缩薄膜干燥法虽然准确度高且不受试样HPAM分子质量变化及水解度的影响,但样品预处理等需要做一系列繁复的准备工作.色谱法和发光定氮法检测快速准确、抗干扰能力强,但需要设备昂贵且技术培训时间长.Gibbons 和Örmeci[15]使用台式紫外-可见分光光度计测量水中聚合物的浓度,聚合物浓度与样品在纯水中的吸光度之间存在很强的线性关系,200 nm波长下的检出限约为0.5 mg·L-1.研究人员还指出,检测极限可能因不同的聚合物而异,使用聚合物的最大吸光度构建线性曲线将提高方法的灵敏度并提高检测极限.Momani[16]使用紫外分光光度法检测蒸馏水中其中聚丙烯酰胺浓度,结果表明所有聚合物在191.5 nm处的检出限均低于0.1 mg·L-1.
聚丙烯酰胺及其水溶液的光学特性是其化学组分分析和浓度光学检测的基础[17].Adliene[18]等通过紫外-可见分光光度法对聚丙烯酰胺凝胶的光学性能进行了分析.Pilařovd[19]等应用光学层析成像方法测量了聚丙烯酰胺凝胶的吸光度并在680 nm波长处构建其剂量响应曲线.此外,矿物加工过程中选矿废水处理后需要循环利用,水系统中各种离子反复积累造成循环水溶液环境复杂[20-21],高盐度会导致聚合物出现压缩构象和显著压缩的双电层排斥现象[22],聚合物吸附行为和絮凝性能都发生很大变化.Rui[23]等发现溶液中离子与聚丙烯酰胺配位相互作用的影响程度顺序为Fe3+>Cr3+>Ca2+>Mg2+>Na+,Ca2+由于其松散的水合壳层,可以直接与丙烯酸阴离子相互作用,通过强静电引力与丙烯酸阴离子形成稳定的偶极对,导致聚合物的聚集.Chen[24]等采用原子力显微镜(AFM)对腐殖酸的大分子结构进行形貌分析,观察到不同溶液环境下大分子的构象变化.研究满足选矿废水中聚丙烯酰胺检测浓度范围和精度的快度检测方法,对研究矿物加工过程或水处理过程中聚丙烯酰胺的时空迁移规律,考察其对后续回用或后续水处理环节的影响的必要前提.目前,鲜有研究报道选矿废水中阳离子对聚丙烯酰胺及其水溶液的光学特性和浓度光学检测的影响,本文系统研究紫外分光光度法对选矿废水处理常用的4种类型聚丙烯酰胺的检测性能和灵敏度,确定检测以上4类聚丙烯酰胺的检出限,研究选矿废水中典型阳离子类型及浓度对紫外分光光度法检测聚丙烯酰胺浓度的影响,并通过AFM对其影响机理进行分析.本研究实现聚丙烯酰胺的快速定量检测,对开展选矿水处理中聚丙烯酰胺的迁移规律研究具有重要意义,对其他工业水处理及生活用水处理具有指导意义.
1 试验材料与方法
1.1 样品准备
试验所用4种聚丙烯酰胺的结构参数见表1.试验所用的试剂,阴离子型聚丙烯酰胺APAM-18,APAM-12,APAM-3的平均分子量为18×106,12×106,3×106,均购自国药集团化学试剂有限公司.阳离子型聚丙烯酰胺CPAM-8的平均分子量为8×106,购自艾科达化学试剂有限公司.试验所用于调整水化学性质的氯化钾,无水氯化钙均为分析纯,购自西陇化工厂有限公司.溶液配置均采用去离子水.
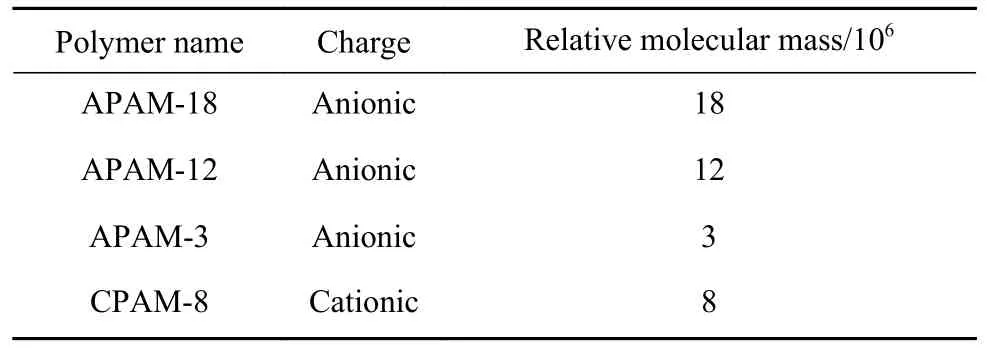
表1 聚丙烯酰胺的结构参数Table 1 Structure parameters of polyacrylamide
首先,配制质量分数为0.1%的聚丙烯酰胺原液,用牛角勺以最少的次数取0.25 g聚丙烯酰胺至干燥洁净的称量瓶中,准确到0.001 g,同时按0.1%的溶液浓度求出稀释水的体积Vp.
式中:VP为添加水量,mL;G为聚丙烯酰胺的质量,g;C是商品絮凝剂的纯度,%;CP是所配制的絮凝剂水溶液浓度,%;ρ为水的密度,ρ=1 kg·L-1.
称量将所求出的超纯水并注入500 mL烧杯中,将烧杯置于磁力搅拌器上,调整转速使液体产生强烈涡流,将称量的絮凝剂均匀分散地撒在涡流面上,待絮凝剂全部撒完后,磁力搅拌器转速调至300~400 r·min-1搅拌2 h,使絮凝剂颗粒完全溶解.若搅拌完毕后仍有未溶解的聚团颗粒则需重新配制.
配置待测样品溶液,分别移取一定体积的上述质量分数为0.1%的聚丙烯酰胺原液至容量瓶中配置成0.1、0.2、0.4、0.8、1 mg·L-1的低浓度范围的聚丙烯酰胺溶液,2、5、6、8、10 mg·L-1的中浓度范围的聚丙烯酰胺溶液,12、15、16、20 mg·L-1等高浓度范围的聚丙烯酰胺溶液.
配置不同离子类型和浓度溶液环境的聚丙烯酰胺待测溶液,移取一定体积质量分数为0.1%的聚丙烯酰胺原液于容量瓶中,分别加入一定质量的KCl或CaCl2,分别配置成背景溶液为10、30、50、70、100 mmol·L-1K+与1、3、5、7、10 mmol·L-1Ca2+的20 mg·L-1聚丙烯酰胺溶液.
制备AFM检测样品,取2 cm×2 cm的硅片及金片浸泡在质量分数为2%的SDS溶液中不少于30 min,用超纯水反复冲洗后用高纯氮气吹干,将硅片及金片置于紫外臭氧仪中10 min;用去离子水、KCl和CaCl2分别配置成背景溶液为10、100 mmol·L-1K+与1、10 mmol·L-1Ca2+的20 mg·L-1APAM-3与CPAM-8溶液,移取少量APAM-3与CPAM-8溶液分别滴在硅片和金片上,放进真空干燥箱30 ℃干燥4 h;使用布鲁克科技有限公司的Dimension ICON型原子力显微镜以接触模式,室温下空气中观测阳离子对聚丙烯酰胺的构象变化的影响,扫描范围为80 μm×80 μm.
1.2 试验方法
物质的吸收光谱具有与其结构相关的特征性,本文所用美国赛默飞科技公司的GENESYS™180 UV-Vis分光光度计可对整个紫外光谱或可见光光谱进行实时分析,该仪器的采样频率为1 min,吸收波长范围为190~1100 nm,波长分辨率为2 nm,吸光度工作范围为0~1;使用1 cm石英比色皿进行吸光度测量,使用去离子水作为空白进行校准.
每个实验组至少重复三次,对于每个重复,使用新制备的聚合物储备溶液,并在每个聚体浓度下记录至少七个数据点.如Berthouex和Brown[25]所述,可采用美国环境保护局(US Environmental Protection Agency)批准的方法检出限(MDL)用于确定紫外分光光度法检测聚丙烯酰胺浓度的最低检出限.
式中:MDL是基于加标样品的方法检出限,mg·L-1;n为实验重复次数;n-1为自由度;t(n-1,0.99)为常数(实验重复次数为7,自由度6,置信度为99%时t为3.143);SS为n次加标样品分析的样品标准偏差.
2 结果与讨论
2.1 去离子水中聚丙烯酰胺的浓度检测
在去离子水中测定了4种聚丙烯酰胺在三个浓度范围内的吸收光谱:0.1~1、1~10和10~20 mg·L-1.通过计算聚丙烯酰胺所选浓度范围的最低检出限,以确定该方法在低、中、高聚合物浓度内的检测能力和灵敏度.
图1为去离子水中APAM-18浓度范围分别为0.1~1、1~10、10~20 mg·L-1时,在200~750 nm波长范围内扫描所得的吸收光谱.可见,絮凝剂APAM-18的紫外吸收光谱中在194 nm处吸光度存在峰值,在194~240 nm间吸光度逐渐降低,在240 nm之外没有显著的吸光度,因此选择在190~300 nm波长范围内构建吸收光谱.由图1(a)、(b)、(c),在0.1~20 mg·L-1的浓度范围内,测得的吸光度值范围为0.01~0.3,絮凝剂APAM-18浓度增加导致吸光度值的增加,线性回归分析表明在0.1~1、1~10、10~20 mg·L-1这3个浓度范围内,絮凝剂浓度和样品的紫外线吸光度之间存在相关性不同的线性关系.尽管对<1 mg·L-1的低PAM浓度吸光度测量显示出一些噪声,但紫外分光光度计仍然能够检测到聚丙烯酰胺浓度的极小增量(0.1 mg·L-1).
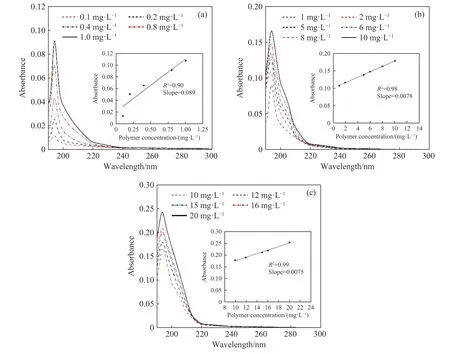
图1 去离子水中APAM-18在(a) 0.1~1 mg·L-1、(b) 1~10 mg·L-1、(c) 10~20 mg·L-1浓度范围内的吸收光谱(插图:194 nm处吸光度和浓度的线性回归曲线)Fig.1 Absorbance spectra of APAM-18 in distilled water: Concentrations from 0.1 to 1 mg·L-1 (a), concentrations from 1 to 10 mg·L-1 (b),concentrations from 10 to 20 mg·L-1 (c) (Insets: linear regression of the sample absorbance and polymer concentration at 194 nm)
图2~4分别为APAM-12、APAM-3、CPAM-8在去离子水中的紫外吸收光谱,可知,4种PAM的浓度和吸光度之间均存在线性关系,表2为在194 nm处样品吸光度和聚合物浓度的线性回归方程及参数,4种PAM吸光度与浓度间存在置信区间为95%的强线性关系的线性关系,通过构建校准曲线来确定水中未知的PAM浓度是可行的.
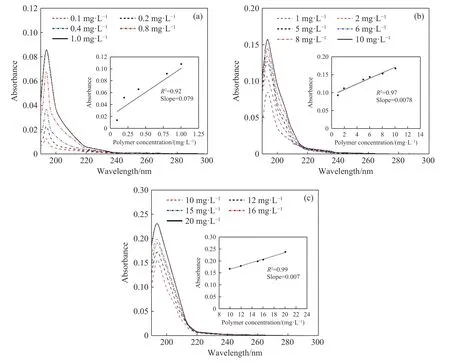
图2 0.1~1 mg·L-1 (a)、1~10 mg·L-1 (b)、10~20 mg·L-1 (c)的APAM-12在去离子水中的吸收光谱(插图:194 nm处样品吸光度和聚合物浓度的线性回归曲线)Fig.2 Absorbance spectra of APAM-12 in distilled water: concentrations from 0.1 to 1 mg·L-1 (a); concentrations from 1 to 10 mg·L-1 (b);concentrations from 10 to 20 mg·L-1 (c) (Insets: linear regression of the sample absorbance and polymer concentration at 194 nm)

图3 0.1~1 mg·L-1 (a)、1~10 mg·L-1 (b)、10~20 mg·L-1 (c)的APAM-3在去离子水中的吸收光谱(插图:194 nm处样品吸光度和聚合物浓度的线性回归曲线)Fig.3 Absorbance spectra of APAM-3 in distilled water: concentrations from 0.1 to 1 mg·L-1 (a); concentrations from 1 to 10 mg·L-1 (b); concentrations from 10 to 20 mg·L-1 (c) (Insets: linear regression of the sample absorbance and polymer concentration at 194 nm)

图4 0.1~1 mg·L-1 (a)、1~10 mg·L-1 (b)、10~20 mg·L-1 (c)的CPAM-8在去离子水中的吸收光谱(插图:194 nm处样品吸光度和聚合物浓度的线性回归曲线)Fig.4 Absorbance spectra of CPAM-8 in distilled water: concentrations from 0.1 to 1 mg·L-1 (a), concentrations from 1 to 10 mg·L-1 (b), concentrations from 10 to 20 mg·L-1 (c) (Insets: linear regression of the sample absorbance and polymer concentration at 194 nm)

表2 194 nm处样品吸光度和聚合物浓度的线性回归方程及参数Table 2 Linear regression and parameters of the sample absorbance and polymer concentration at 194 nm
紫外分光光度法是根据聚丙烯酰胺的酰胺基吸光度建立的研究方法,水解度、分子量与溶液黏度对该方法干扰很小,该方法可以适用于不同类型的PAM浓度的检测.因此,依据公式(2)所述MDL方法确定去离子水中APAM-18、APAM-12、APAM-3、CPAM-8等4种PAM的检出限值分别为0.08、0.05、0.09和0.06 mg·L-1,该方法能够检测到浓度低至0.1 mg·L-1的聚合物的吸光度,即在194 nm特征波长处通过紫外分光光度计的吸光度检测具有较高的灵敏度.
2.2 K+、Ca2+离子对紫外吸收光谱的影响
选矿废水中常见的难免金属阳离子主要包括K+,Na+,Ca2+,Mg2+等[26],本试验选取K+和Ca2+分别为一价和二价金属阳离子的代表,用KCl与CaCl2将20 mg·L-1聚丙烯酰胺溶液的离子浓度分别配置为10、30、50、70、100 mmol·L-1K+与1、3、5、7、10 mmol·L-1Ca2+.
图5~8分别为0~100 mmol·L-1K+、0~10 mmol·L-1Ca2+中APAM-18、APAM-12、APAM-3、CPAM-8的吸收光谱.随着K+和Ca2+浓度的增加,聚丙烯酰胺溶液吸光度特征峰的强度逐渐降低,最大吸收波长在不断红移.K+和Ca2+浓度分别超过50 mmol·L-1和5 mmol·L-1时,吸光度特征峰的强度降速减缓.因此,为了提高紫外分光光度法对不同溶液环境中聚丙烯酰胺浓度检测的准确性,需先进行水样的水质分析,并在相当水质条件下构建波长与吸光度的标准曲线,使用聚合物的最大吸光度建立吸光度与浓度的关系曲线,以提高该检测方法的准确性及灵敏度.

图5 金属阳离子浓度对APAM-18吸光度的影响.(a) 0~100 mmol·L-1 K+、(b) 0~10 mmol·L-1 Ca2+Fig.5 Effect of 0-100 mmol·L-1 K+ (a) and 0-10 mmol·L-1 Ca2+ (b) on the absorbance of APAM-18
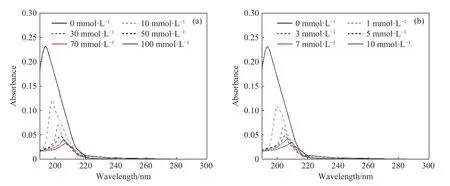
图6 金属阳离子浓度对APAM-12吸光度的影响.(a) 0~100 mmol·L-1 K+、(b) 0~10 mmol·L-1 Ca2+Fig.6 Effect of 0-100 mmol·L-1 K+ (a) and 0-10 mmol·L-1 Ca2+ (b) on the absorbance of APAM-12
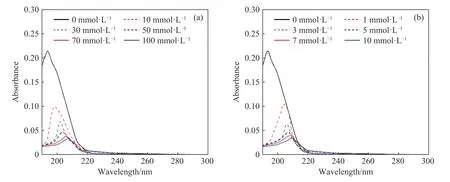
图7 金属阳离子浓度对APAM-3吸光度的影响.(a) 0~100 mmol·L-1 K+;(b) 0~10 mmol·L-1 Ca2+Fig.7 Effect of 0-100 mmol·L-1 K+ (a) and 0-10 mmol·L-1 Ca2+ (b) on the absorbance of APAM-3

图8 金属阳离子浓度对CPAM-8吸光度的影响.(a) 0~100 mmol·L-1 K+;(b) 0~10 mmol·L-1 Ca2+Fig.8 Effect of 0-100 mmol·L-1 K+ (a) and 0-10 mmol·L-1 Ca2+ (b) on the absorbance of CPAM-8
紫外分光光度法是根据聚丙烯酰胺的活性基团酰胺基吸光度建立的研究方法,紫外吸收光谱反映了分子中价电子跃迁时的能量变化与化合物所含发色基团之间的关系[27].分子发生共轭作用、引入助色基团或带色团和有机化合物溶质空间结构的变化(空间位阻、顺反异构、跨环效应)皆会引起紫外-可见光谱的变化.有研究表明纤毛动力蛋白(DPCD)处理可以使得原肌球(TM)蛋白空间构象发生明显改变,紫外吸收峰发生蓝移[28].Yang[29]等研究发现超声联合甘露糖处理可以让β-乳球蛋白后起空间结构展开,使更多芳香族氨基酸残基暴露在分子表面,增加了紫外吸收强度.此外,溶液化学环境的变化也会对紫外-可见光谱产生影响,从而影响紫外分光光度法的检测效果.pH升高使得溶解性有机质(DOM)相对分子质量、分子缩合度、腐殖化程度逐渐增大[30],导致紫外-可见吸收光谱(UV-vis)参数变化,最高吸光度特征峰强度增大.极性溶剂一般使n→π*吸收带发生蓝移,吸收强度(εmax)随之增加,极性溶剂又使π→π*吸收带发生红移,而εmax随之略有降低[31].
由前文数据可得,溶液中阳离子浓度变化也会对紫外-可见光谱产生不可忽视的影响.有研究报道,在KCl溶液中疏水性聚丙烯稀酰胺(HMPAM)在氧化铝表面吸附量增加,表明了K+使得HPAM构象更加卷曲[32].具有不同盐度的PAM测量黏度以及所报道的流体动力学尺寸测量结果表明,与低盐度条件下相比,PAM链在高盐度溶液中的构象更加卷曲,平面构象也发生变化[33].
由图5、6、7、8所见,20 mg·L-1聚丙烯酰胺溶液中分别加入浓度为0~100 mmol·L-1K+与0~10 mmol·L-1Ca2+,均对吸光度产生了较大影响.浓度相差较大的0~100 mmol·L-1K+与0~10 mmol·L-1Ca2+的背景溶液条件下,PAM溶液吸光度特征峰的强度降低幅度相似.有研究表明,溶液中的一价、二价阳离子会导致聚丙烯酰胺出现压缩构象和显著压缩的双电层排斥现象.相比于一价阳离子K+溶液,二价阳离子Ca2+溶液的阳离子扩散系数较低,溶液中阴离子浓度较高,消减了双电层的厚度[34].在相同离子质量浓度条件下,二价阳离子(Ca2+)作用下HPAM的黏度损失率是一价阳离子(K+)的4倍[35],表明同浓度条件下,二价阳离子比一价阳离子更具有压缩扩散双分子层、使聚合物大分子发生卷曲的性质.
2.3 K+和Ca2+对聚丙烯酰胺分子构象的影响
进一步采用AFM对聚合物形貌进行扫描,考察K+和Ca2+对聚丙烯酰胺分子构象的影响.KCl的溶度为10、100 mmol·L-1,CaCl2的浓度为1、10 mmol·L-1.分别以APAM-3与CPAM-8为2种聚丙烯酰胺的代表,为了降低絮凝剂分子与基底之间的相互作用对分子构象的影响,将阴离子型的APAM-3稀溶液滴在表面荷负电的二氧化硅基底上,将阳离子型的CPAM-8稀溶液沉积在表面荷正电的金基底上,真空干燥器中干燥后进行形貌扫描.图9为K+浓度对APAM-3分子构象的影响.

图9 K+浓度对20 mg·L-1 APAM-3分子构象的影响(扫描范围80 μm×80 μm).(a)二氧化硅基底(Rq 1.01 nm); (b) 0 mmol·L-1 (Rq 24.3 nm);(c) 10 mmol·L-1 (Rq 80.4 nm); (d) 100 mmol·L-1 (Rq 124 nm)Fig.9 Effect of metal cation (K+) concentration on the molecular configuration of 20 mg·L-1 APAM-3 (scan area 80 μm×80 μm): (a) silicon substrate(Rq 1.01 nm); (b) 0 mmol·L-1 (Rq 24.3 nm); (c) 10 mmol·L-1 (Rq 80.4 nm); (d) 100 mmol·L-1 (Rq 124 nm)
由图9可得,二氧化硅基底的粗糙度(Rq)为1.01 nm,不同离子浓度环境APAM-3基本呈单分子层状态沉积在二氧化硅基底表面,APAM-3的分子构象有较显著的变化.去离子水溶液环境中APAM-3的Rq为24.3 nm,背景溶液分别为10 mmol·L-1与100 mmol·L-1KCl时,Rq分别增加至80.4 nm、120 nm,形貌图中聚合物的亮点明显增多,分子链由线条树枝状向点块状转变,分子链宽度增加,说明APAM-3分子在高盐度溶液中发生聚团,在100 mmol·L-1KCl条件下APAM-3最为卷曲.
图10为二价金属阳离子(Ca2+)浓度下CPAM-12分子形貌图.由图10可见,金基底的粗糙度(Rq)为1.9 nm,CPAM-12呈单分子层状态沉积在金基底表面,背景溶液分别从去离子水、1 mmol·L-1CaCl2到10 mmol·L-1CaCl2,AFM形貌图的Rq从38.1 nm增加到120 nm和145 nm,CPAM-12的分子构象从典型的线性树枝状转变为支链短而粗的聚团状,10 mmol·L-1CaCl2的高盐溶液环境中已经团聚为凝胶块状.

图10 二价金属阳离子(Ca2+)浓度对20 mg·L-1 CPAM-12分子构象的影响(扫描范围80 μm×80 μm).(a)金基底 (Rq 1.9 nm);(b) 0 mmol·L-1(Rq 38.1 nm);(c) 1 mmol·L-1 (Rq 120 nm);(d) 10 mmol·L-1 (Rq 145 nm)Fig.10 Effect of metal cation (Ca2+) concentration on the molecular configuration of 20 mg·L-1 CPAM-12 (scan area 80 μm×80 μm): (a) gold substrate(Rq 1.9 nm); (b) 0 mmol·L-1 (Rq 38.1 nm); (c) 1 mmol·L-1 (Rq 120 nm); (d) 10 mmol·L-1 (Rq 145 nm)
由图9和10,20 mg·L-1APAM-3与CPAM-12溶液中分别加入浓度为0~100 mmol·L-1KCl与0~10 mmol·L-1CaCl2,均使絮凝剂的分子构象发生了较大变化.背景溶液为去离子水时,APAM-3与CPAM-12的Rq分别为24.3 nm和38.1 nm,背景溶液分别为10、100 mmol·L-1KCl与1、10 mmol·L-1CaCl2时,APAM-3与CPAM-12的Rq增长幅度整体相似,表明10 mmol·L-1KCl与1 mmol·L-1CaCl2、100 mmol·L-1KCl与10 mmol·L-1CaCl2对聚丙烯酰胺分子构象的影响程度相当,即Ca2+浓度对絮凝剂分子构象的影响较K+更加显著.选矿废水中典型一价、二价阳离子(K+和Ca2+)对聚丙烯酰胺分子构象的影响与其对紫外吸收光谱的影响结果相一致.
3 结论
本文探索了低检出限的低浓度PAM快速检测方法,在190~300 nm波长范围内建立了4种类型及分子量不同PAM的紫外吸收光谱,确定该方法对PAM的检测性能、灵敏度及检测限.研究选矿废水中典型阳离子类型及浓度对PAM浓度的影响,并通过AFM对其影响机理进行分析.结果表明,4种类型PAM的峰值吸光度均在波长为194 nm处测得,检出限均低于0.1 mg·L-1,具有较高的检测性能和灵敏度.在所考察的K+与Ca2+浓度范围内,随着K+与Ca2+浓度的增加,聚丙烯酰胺溶液吸光度特征峰的强度逐渐降低,最大吸收波长在不断红移.在去离子水中,分别沉积在二氧化硅和金基底的APAM-3与CPAM-12的表面形貌粗糙度(Rq)分别为24.3 nm和38.1 nm.随着K+和Ca2+浓度分别从10 mmol·L-1和1 mmol·L-1增加到100 mmol·L-1和10 mmol·L-1时,Rq分别从80.4 nm和120 nm增加到124 nm和145 nm,表明PAM链在溶液中的构象逐渐变卷曲,使紫外光谱特征吸收峰的峰值降低.同时,10 mmol·L-1和100 mmol·L-1一价阳离子(K+)与1 mmol·L-1和10 mmol·L-1二价阳离子(Ca2+)对聚丙烯酰胺平面构象变化的影响程度基本相同.本研究实现了聚丙烯酰胺的快速定量检测,对开展选矿水处理中聚丙烯酰胺的迁移规律研究具有重要意义.
