基于压力-应变曲线评估心力衰竭病人整体无效做功对心脏再同步化治疗应答的预测价值
2024-04-29黄志勇吴杰莹刘誉红罗伟权刘娟娟
黄志勇 吴杰莹 刘誉红 罗伟权 刘娟娟
摘要 目的:采用压力-应变曲线(PSL)测定心脏整体无效做功(GWW),评估射血分数减低心力衰竭(HFrEF)病人术前GWW对心脏再同步化治疗(CRT)应答的预测价值,及其与长期不良预后的关系。方法:选取2018年1月—2019年1月在中山市中医院接受CRT治疗的50例HFrEF病人为研究对象,于术前及术后9个月测量常规超声心动图参数,并采用基于二维斑点追踪应变成像的压力-应变曲线(PSL)测定包括GWW在内的心肌做功参数,应用受试者工作特征(ROC)曲线分析术前GWW对CRT应答的预测价值,应用Cox回归分析模型分析术前GWW与CRT应答及不良事件的关系。CRT应答为从基线检查到术后9个月随访期间左心室舒张末期容积(LVEDV)缩小≥15%,有CRT应答病人列为有效组,其余为无效组。研究的终点为CRT应答或随访期间的全因死亡。结果:与术前相比,有效组术后的LVEDV、左心室舒张末期内径(LVEDD)和左心室收縮末期容积(LVESV)较术前均减小,左室射血分数(LVEF)较术前增大;有效组术后的GWW下降,整体有效做功(GCW)、整体做功指数(GWI)、整体做功效率(GWE)均增高,差异有统计学意义(P<0.05)。术前无效组的GWW与GCW均低于有效组(P<0.05)。ROC曲线分析显示,相较于其他心肌做功参数,术前GWW预测CRT应答的ROC曲线下面积(AUC)最大,其AUC为0.78[95%CI(0.69,0.88), P<0.01],当GWW为175 mmHg%时预测CRT应答的特异度为85.7%,敏感度为67.8%。Cox回归分析模型显示,对HFrEF病人接受CRT的已知预后因素进行校正后,GWW<175 mmHg%与全因死亡的相对风险增加相关[校正HR=2.04,95%CI(1.10,3.84),P=0.024];将GWW添加到包含已知CRT预后因子的基线模型中,该模型呈正相关(改善χ2=4.85,P=0.028);GWW相较于其他心肌做功参数,与CRT应答和预后的相关性最佳。结论:HFrEF病人术前低GWW(<175 mmHg%)与CRT候选者无应答以及全因死亡风险相对增加有关,术前GWW是改善CRT选择的一个预示参数。
关键词 射血分数减的低心力衰竭;超声心动描记术;二维斑点追踪应变成像;心肌应变;心肌做功;心脏再同步化治疗
doi:10.12102/j.issn.1672-1349.2024.03.019
基金项目 中山市社会公益科技研究项目(No.2022B1091)
作者单位 中山市中医院(广东中山 528400),E-mail:407371975@qq.com
引用信息 黄志勇,吴杰莹,刘誉红,等.基于压力-应变曲线评估心力衰竭病人整体无效做功对心脏再同步化治疗应答的预测价值[J].中西医结合心脑血管病杂志,2024,22(3):502-508.
心脏再同步化治疗(CRT)是治疗射血分数减低、QRS持续性时间延长心力衰竭病人的有效方法[1]。风险分层仍然是心力衰竭病人治疗的关键,30%的病人在CRT后不能改善,甚至可能恶化[2]。因此,识别CRT不良预后的预测因素至关重要。近期研究表明,超声心动图有助于识别CRT后出现左室逆重构和预后改善的射血分数减低的心力衰竭(HFrEF)病人[3]。在左束支传导阻滞病人中,收缩早期右室和室间隔首先被激动,产生室间隔的特异性运动即室间隔抖动(septal flash,SF)使未激活的左室侧壁先向右拉伸[4-5],由于左室电活动传导延迟,左室侧壁收缩延迟,在收缩晚期出现收缩后收缩,使室间隔再向左拉伸,同时伴随左室心尖的特征性顺时针运动,产生心尖摆动征(apical rocking,Ap Rock)[6]。SF和Ap Rock的识别与左室逆重构和CRT预后存在相关性[7],但其存在局限性,因为识别这些特征高度依赖超声医师的经验,此外,这些指标只考虑到左室激活延迟,并未结合残余心肌收缩力的影响,这是CRT改善左室功能的先决条件。同时结合了二维斑点追踪应变成像及非侵入性左心室实时压力的压力-应变曲线(PSL)能够定量评价心肌做功,组内及组间的重复性好,目前已在临床中应用[8-11]。尽管既往研究已聚焦于心肌做功参数与CRT应答之间的关系[12-14],但缺少关于评价残余心肌收缩力的心脏整体无效做功(GWW)与临床预后的相关性研究,且结果存在分歧[13,15]。因此,本研究采用PSL测定心GWW,评估HFrEF病人术前GWW对CRT应答的预测价值,以及与长期不良预后的关系。
1 资料与方法
1.1 一般资料
本研究来源于一项前瞻性队列研究,选择2018年1月—2019年1月
在中山市中医院接受CRT治疗并成功植入起搏器的50例HFrEF病人为受试者。将术后9个月随访期间左心室舒张末期容积(LVEDV)缩小≥15%的病人列为CRT治疗有效组,其余为无效组。
受试者纳入标准:符合纽约心脏病协会(NYHA)心功能分级Ⅲ级或Ⅳ级的HFrEF病人;QRS持续时间延长,完全性左束支传导阻滞(LBBB)病人≥120 ms,或非LBBB病人≥150 ms;左心室舒张末期内径(LVEDD)>55 mm,左室射血分数(LVEF)≤35%。
排除标准:近期(<3个月)发生急性冠状动脉综合征或冠状动脉血运重建;原发性二尖瓣或主动脉瓣病变(中度及以上);先天性心脏病;因锁骨下动脉、腋动脉、肱动脉狭窄性病变而影响测量肱动脉血压;因图像质量差或心内膜显示不清而不能进行斑点追踪应变分析。
1.2 临床资料收集
包括病人性别、年龄、冠心病史、心房颤动史、NYHA分级、QRS持续时间、LBBB、SF和/或Ap Rock、血浆N-末端脑钠肽前体(NT-proBNP)水平等。
1.3 CRT设备植入
由电生理学医师植入,目标位置是冠状窦静脉的基外侧、前外侧或后外侧,用于定位LV导线。室间隔间时间设置为0,设定短感知房室间期(80~100 ms)和起搏房室间期(130 ms)以促进双心室起搏,出院前应注意在心电图和连续检测中确认是否存在真性融合波、假性融合波。
1.4 超声心动图检查
1.4.1 仪器与软件
使用GE Vivid E9超声诊断仪采集图像,配备M5S-D超声探头(1.7~3.4 MHz)及上臂袖带同步血压计,设置成像帧频50~80(65±10)帧/s。使用EchoPAC对图像进行应变分析。
1.4.2 图像采集与记录实时血压
病人取左侧卧位,在胸骨旁长轴切面测量LVEDD、左心室收缩末期内径(LVESD)及左房内径(LAD);在心尖四腔心切面及二腔心切面采用双平面Simpson法测量LVEDV、左心室收缩末期容积(LVESV)及LVEF。同步连接心电图,嘱病人平静呼吸,连续采集至少5个心动周期的左心室心尖三腔、四腔、两腔切面二维动态图像。于心尖五腔心切面采集主动脉瓣频谱多普勒血流频谱。收集起搏器植入术前1 d、出院前和出院9个月随访时的图像。同步连接上臂袖带血压计,记录实时肱动脉血压数值。左心室机电不同步通过胸骨旁短轴或长轴切面的SF或心尖四腔心切面的Ap Rock来确定。
1.4.3 图像分析与参数获取
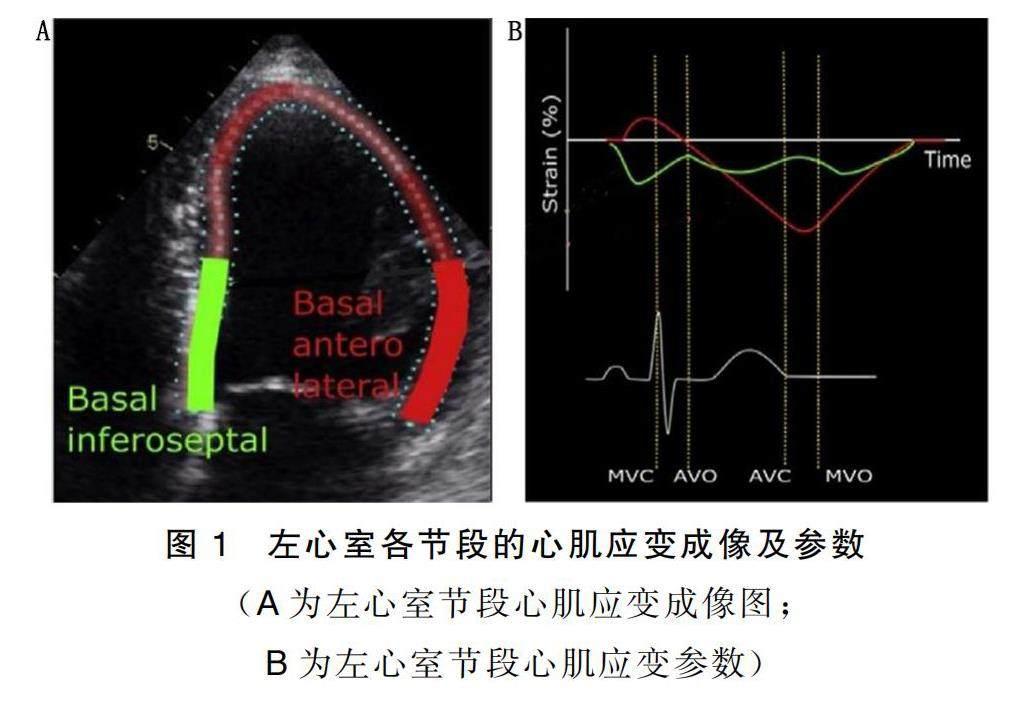
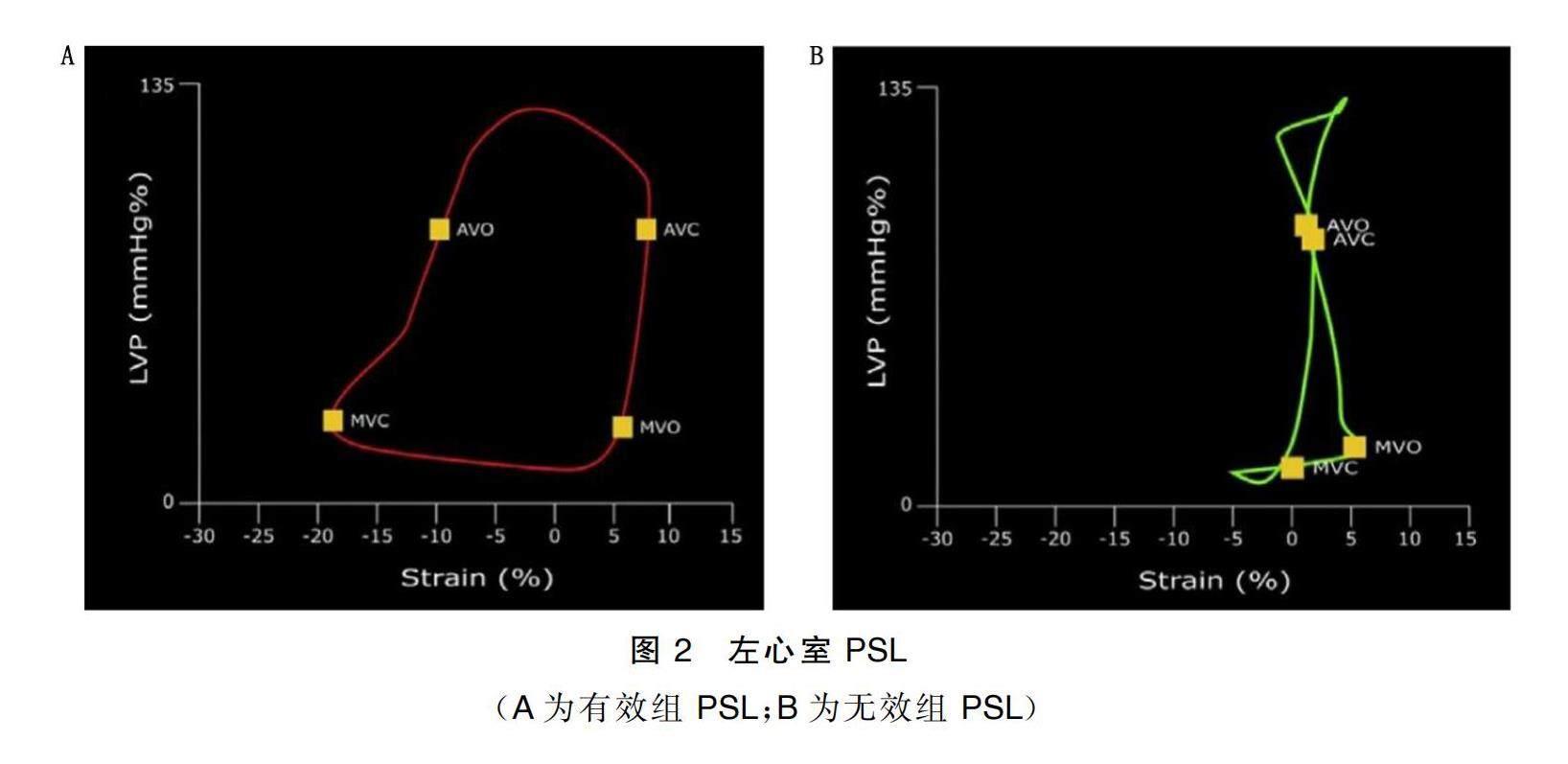
将DICOM格式的原始图像导入Echo PAC工作站进行脱机分析。首先通过主动脉瓣多普勒频谱,确定主动脉瓣启闭时间,标记Event timing,然后进入AFI模式,依次选取左心室心尖三腔、四腔、两腔心切面的二维动态图像,于收缩末期自动追踪左室心内膜边界生成感兴趣区(ROI),并手动调整ROI,以确保最佳的追踪效果。图像分析完成后,系统自动生成左心室整体及17个节段的心肌应变参数(见图1);点击Myocardiac Work输入采集图像时的实时肱动脉血压数值,可获得
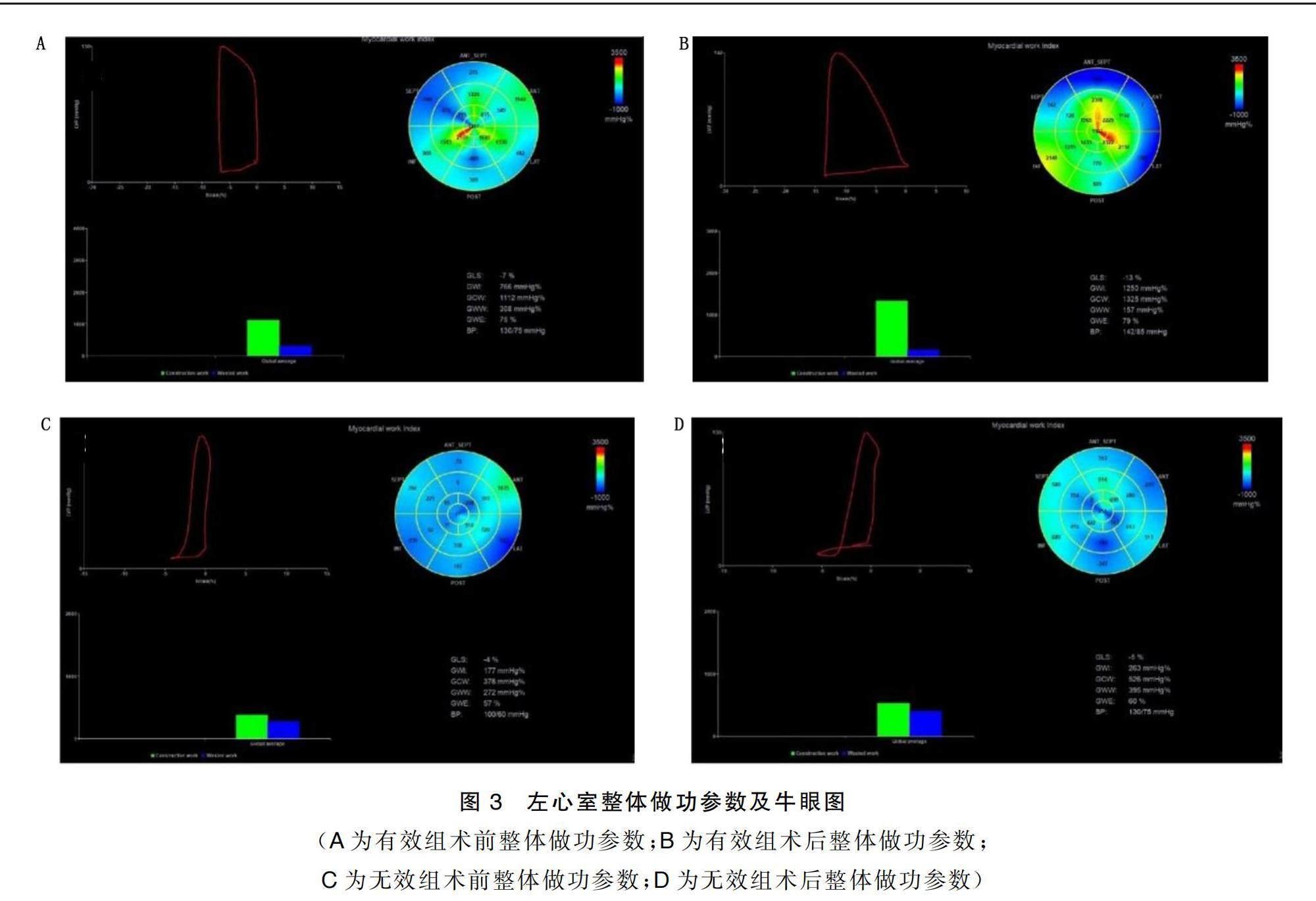
PSL(见图2);点击Advanced即可获得左心室整体纵向应变(GLS)、整体做功指数(GWI)、整体有效做功(GCW)、整体无效做功(GWW)、整体做功效率(GWE)及GWI的牛眼图(见图3)。
1.5 结局指标
CRT应答定义为从基线检查到9个月随访期间LVEDV相对减少≥15%。在随访期间,通过访谈和/或电话联系医生、病人和亲属记录终点事件,主要研究终点为全因死亡率,如果死亡与心力衰竭、心肌梗死、心律失常或猝死相关,则考虑是心源性死亡。
1.6 统计学处理
应用SPSS 25.0统计软件分析数据。符合正态分布的定量资料以均数±标准差(x-±s)表示,组间比较采用独立样本t检验;不符合正态分布的定量资料以中位数(四分位数)[M(P25,P75)]表示,组间比较采用Kruskal-Wallis秩和检验。定性资料以例数、百分比(%)表示,组间比较采用χ2检验或Fisher精确概率法。应用受试者工作特征(ROC)曲线获得GWW预测CRT应答的曲线下面积(AUC)、最佳截点值以及灵敏度和特异度。使用多因素Logistic回归分析低GWW是否为CRT术后不良事件的独立危险因素。使用Cox比例风险回归模型分析CRT术后不良事件的危险因素,并确定风险比(HR)。建立Kaplan-Meier生存曲线,用Log-rank检验比较组间差异。以P<0.05为差异有统计学意义。
2 结 果
2.1 两组临床资料比较
将CRT术后9个月较术前LVEDV相对减少≥15%定义为CRT应答。研究人群为50例接受CRT治疗的HFrEF病人,年龄(71±10)岁,其中36例病人治疗有效。术前有效组(36例)与无效组(14例)病人的年龄、性别、糖尿病、冠心病、心房颤动史、NYHA Ⅲ级或Ⅳ级、超声特异性征象(SF或Ap Rock)等比较差异无统计学意义(P>0.05),有效组的QRS宽度及QRS宽度>150 ms所占比例均大于无效组,有效组LBBB所占比例大于无效组,有效组血脑钠肽水平低于无效组,差异均有统计学意义(P<0.001)。详见表1。
2.2 超声心动图常规参数比较
术前有效组的LVEDD、LVEDV、LVESV低于无效组(P<0.05),LVEF高于无效组(P<0.05),有效组与无效组的LAD差异无统计学意义(P>0.05)。与术前相比,有效组术后的LVEDD、LVEDV和LVESV较术前均减小(P<0.05),LVEF较术前增大(P<0.05),有效组与无效组的LAD较术前无明显减小(P>0.05)。详见表2。
2.3 左心室心肌做功参数及GLS比较
术前无效组的GWW与GCW均低于有效组(P<0.05),其余参数比较差异均无统计学意义。与术前相比,有效组术后的GWW下降,GCW、GWI、GWE均增高,差异有统计学意义(P<0.05);无效组各参数比较差异均无统计学意义(P>0.05)。详见表3。
2.4 左心室心肌做功参数对CRT应答的预测因素
总结ROC曲线分析结果,GWW和GCW为具有高AUC的CRT应答预测因素(GWW为0.78,GCW为0.72),其中GWW的AUC最大,以175 mmHg%为截断值区分CRT有无应答的特异度为85.7%,敏感度为67.8%。详见表4。
2.5 GWW与CRT预后的关系
在3年的随访期间,有15例病人死亡(30%)。在左心室心肌做功参数中,GWW相较于其他心肌做功参数,与CRT应答和预后的相关性最佳。GWW<175 mmHg%的3年生存率为62%[95%CI(50%,75%)],GWW≥175 mmHg%的3年生存率为83%[95%CI(77%,89%),P=0.002]。对HFrEF病人接受CRT的已知预后因素进行校正后,与GWW≥175 mmHg%相比,GWW<175 mmHg%与全因死亡的相对风险增加相关[校正HR=2.04,95%CI(1.10,3.84),P=0.024];将GWW添加到包含已知CRT预后因子的基线模型中,该模型呈正相关(改善χ2=4.85,P=0.028)。详见表5、表6及图4。
3 讨 论
对HFrEF病人进行风险分层以改善死亡风险十分重要。一项CARE-HF随机对照试验显示,CRT使QRS时限延长的HFrEF病人显著获益,在平均29个月的随访期间,全因死亡率降低36%,因心力衰竭恶化的非计划住院治疗减少了50%以上[16]。不协调的室壁运动再同步化可以使左室逆重构,但约30%的心力衰竭病人可能对CRT无应答,因此,寻找新的简单指标以帮助完善CRT适应证是一个重要的研究领域[17-18]。
Russell等[19]研究显示,无创评估心肌做功,定量评估各节段PSL面积可以无创获得心肌做功参数,PSL与使用有创导管测量的做功相关性良好。研究表明,在等候CRT的病人中,PSL无创评估左室功能与PET评估的残余心肌代谢活性相关[19-20]。应用斑点追踪超声心动图进行全自动评价心肌做功简便易行,且观察者内与观察者间重复性好[8,19]。各节段心肌的无效做功对应节段运动过程中在反方向运动所做功。GWW为左心室各节段无效做功的平均值。Russell等[20]提出,与没有LBBB的心肌病病人和健康人对照组相比,患LBBB的心肌病病人的GWW增加。GWW能够全面定量评估心肌浪费的能量。在LBBB和/或激活延迟的病人中,浪费的能量是变化的,正如本研究中GWW的分布一样。事实上,多个复杂的因素影响病人的GWW。首先,左室的几何形状和扩张显著影响心肌做功[21]。根据定义,功是力与长度的乘积,面积对应于压力-容积环,纵向缩短很大程度反映左室容积的变化,左室心肌做功可以近似用压力和应变曲线参数计算。心肌做功高度依赖于左室壁应力,左室壁应力随着左室扩张而增加,但PSL没有考虑到这个问题。在两个不同大小的左心室中,扩张者收缩期室壁应力高于未扩张者,可能导致左室心肌做功的低估。左室节段曲率半径和室壁厚度的评估先前应用于无创推导室壁应力,以克服这一局限性,但在日常临床工作中开展较为烦琐[22]。采用肱动脉收缩压只是估测左室收缩压,没有考虑左室舒张压和反射波增加的压力,尽管如此,验证性研究已经证明通过超声心动图无创评价心肌做功的准确性[23]。心肌缺血时出现的收缩不同步和收缩后收缩,都可能导致射血效率降低和无效做功增加[24]。虽然Chan等[25]发现非缺血性心肌病病人的GWW值高于缺血性心肌病病人,但研究中并未发现GWW<175 mmHg%与临床结局之间存在显著的相互作用。Aalen等[17]发现心脏磁共振评价的心肌做功和室间隔活力均可预测CRT应答,并具有增量预测价值。
本研究常规超声心动图显示,与术前相比,有效组术后的LVEDD、LVEDV和LVESV较术前均减小,LVEF较术前增大,表明术后左心室收缩功能明显改善;有效组术后的GWW下降,GCW 、GWI、GWE均增高,这说明有效组术后心肌做功效率、做功能力显著提升,且心肌做功相关参数可以有效地评估CRT病人术后心脏收缩功能。这可能与CRT病人术前不同节段心肌收缩达峰时间的不同有关。正常人不同节段心肌的电机械活动的起始时间虽然不同,但其收缩达峰时间相同,收缩期左心室各节段心肌同步收缩,将血液泵入主动脉。而心力衰竭病人,尤其左束支传导阻滞的病人,其左心室后侧壁的电机械活动呈病理性滞后,使该节段心肌收缩达峰时间显著延迟,CRT术后使后侧壁的心肌电机械活动提前,使各节段心肌收缩达峰同步,增加心肌运动的协调性,减少无效功。
本研究发现,术前低水平GWW(<175 mmHg%)与死亡风险相对增加相关,而GWW<175 mmHg%与大概率CRT无反应相关。因为GWW低不仅反映了机电不同步对左室壁拉伸的影响,还考虑到左室几何形态和扩张情况。Lim等[26]先前报道过,应变延迟指数作为一种心肌无效做功的参数,与CRT是否应答相关。Galli等[12]在一项包括97例病人的研究中发现,GWW与CRT应答相关,但其预测价值低于GCW。随访中观察到GCW与心源性死亡的发生之间独立相关,但GWW与心源性死亡之间相关性不明显[13]。Van Der等[15]的一项研究包括153例接受CRT病人随访中发现,整体无效做功比值与死亡率呈独立相关。本研究中,术前GWW、CRT应答和死亡率之间呈强相关。虽然SF和/或心尖摇摆特征与CRT应答相关,但如既往研究所述,其鉴别诊断价值低于GWW。随访中,SF和/或心尖摇摆特征与CRT应答和死亡率都没有显著相关性。这可能是由于SF和/或心尖摇摆特征识别是定性评价,在临床应用中可重复性或许存在一定问题[7]。本研究心肌做功参数中,GWW与CRT应答和死亡率之间的关系最强,与Galli等[12-14]的研究结果不一致,这可能与样本量、事件发生率和研究终点(全因死亡率与心源性死亡)存在差异有关。虽然间隔运动和做功在CRT应答的病理机制中非常重要,但观察到GWW和间隔无效做功对CRT是否应答具有相似的鉴别诊断价值。因此,倾向选择将GWW应用于临床工作中,因为这个参数目前能够从软件中半自动获得,CRT对临床结局的影响至少部分取决于术前无效做功,有效的再同步化治疗能够降低GWW。
PSL评价术前GWW重复性好,较低的GWW与HFrEF病人的长期不良预后和CRT应答率低相关。GWW<175 mmHg%为HFrEF病人提供增量预测价值。但在缺乏随机对照研究的情况下,即使大多数术前GWW<175 mmHg%的病人似乎没有从CRT中获益,这些病人也不应被排除在CRT之外,临床诊疗仍应依据当前指南。因此,本研究结果表明,术前GWW较低的病人应在CRT术后仔细监测,以确保在其临床状况恶化前及时接受更高级别治疗(如心脏移植、左心室或双心室辅助装置等)。
参考文献:
[1] PONIKOWSKI P,VOORS A A,ANKER S D,et al.2016 ESC Guidelines for the diagnosis and treatment of acute and chronic heart failure:the Task Force for the diagnosis and treatment of acute and chronic heart failure of the European Society of Cardiology(ESC)Developed with the special contribution of the Heart Failure Association(HFA)of the ESC[J].European Heart Journal,2016,37(27):2129-2200.
[2] HOLZMEISTER J,LECLERCQ C.Implantable cardioverter defibrillators and cardiac resynchronisation therapy[J].Lancet,2011,378:722-730.
[3] MARECHAUX S,MENET A,GUYOMAR Y,et al.Role of echocardiography before cardiac resynchronization therapy:new advances and current developments[J].Echocardiography,2016,33:1745-52.
[4] PARSAI C,BIJNENS B,SUTHERLAND G R,et al.Toward understanding response to cardiac resynchronization therapy:left ventricular dyssynchrony is only one of multiple mechanisms[J].European Heart Journal,2009,30(8):940-949.
[5] BRUNET-BERNARD A,MARECHAUX S,FAUCHIER L,et al.Combined score using clinical,electrocardiographic,and echocardiographic parameters to predict left ventricular remodeling in patients having had cardiac resynchronization therapy six months earlier[J].Am J Cardiol,2014,113:2045-2051.
[6] GHANI A,DELNOY P P H M,OTTERVANGER J P,et al.Association of apical rocking with long-term major adverse cardiac events in patients undergoing cardiac resynchronization therapy[J].European Heart Journal-Cardiovascular Imaging,2016,17(2):146-153.
[7] STANKOVIC I,PRINZ C,CIARKA A,et al.Relationship of visually assessed apical rocking and septal flash to response and long-term survival following cardiac resynchronization therapy(PREDICT-CRT)[J].European Heart Journal-Cardiovascular Imaging,2016,17(3):262-269.
[8] VECERA J,PENICKA M,ERIKSEN M,et al.Wasted septal work in left ventricular dyssynchrony:a novel principle to predict response to cardiac resynchronization therapy[J].European Heart Journal - Cardiovascular Imaging,2016,17(6):624-632.
[9] EL MAHDIUI M,VAN DER BIJL P,ABOU R,et al.Global left ventricular myocardial work efficiency in healthy individuals and patients with cardiovascular disease[J].J Am Soc Echocardiogr,2019,32:1120-1127.
[10] MEIMOUN P,ABDANI S,STRACCHI V,et al.Usefulness of noninvasive myocardial work to predict left ventricular recovery and acute complications after acute anterior myocardial infarction treated by percutaneous coronary intervention[J].J Am Soc Echocardiogr,2020,33:1180-1190.
[11] HIEMSTRA Y L,VAN DER BIJL P,EL MAHDIUI M,et al.Myocardial work in nonobstructive hypertrophic cardiomyopathy:implications for outcome[J].J Am Soc Echocardiogr,2020,33:1201-1208.
[12] GALLI E,LECLERCQ C,HUBERT A,et al.Role of myocardial constructive work in the identification of responders to CRT[J].European Heart Journal-Cardiovascular Imaging,2018,19(9):1010-1018.
[13] GALLI E,HUBERT A,LE ROLLE V,et al.Myocardial constructive work and cardiac mortality in resynchronization therapy candidates[J].Am Heart J,2019,212:53-63.
[14] GALLI E,LECLERCQ C,FOURNET M,et al.Value of myocardial work estimation in the prediction of response to cardiac resynchronization therapy[J].J Am Soc Echocardiogr,2018,31:220-230.
[15] VAN DER BIJL P,VO N M,KOSTYUKEVICH M V,et al.Prognostic implications of global,left ventricular myocardial work efficiency before cardiac resynchronization therapy[J].European Heart Journal-Cardiovascular Imaging,2019,20(12):1388-1394.
[16] CLELAND J G F,DAUBERT J C,ERDMANN E,et al.The effect of cardiac resynchronization on morbidity and mortality in heart failure[J].The New England Journal of Medicine,2005,352(15):1539-1549.
[17] AALEN J M,DONAL E,LARSEN C K,et al.Imaging predictors of response to cardiac resynchronization therapy:left ventricular work asymmetry by echocardiography and septal viability by cardiac magnetic resonance[J].European Heart Journal,2020,41(39):3813-3823.
[18] AALEN J M,REMME E W,LARSEN C K,et al.Mechanism of abnormal septal motion in left bundle branch block:role of left ventricular wall interactions and myocardial scar[J].JACC Cardiovascular Imaging,2019,12(12):2402-2413.
[19] RUSSELL K,ERIKSEN M,AABERGE L,et al.A novel clinical method for quantification of regional left ventricular pressure-strain loop area:a non-invasive index of myocardial work[J].European Heart Journal,2012,33(6):724-733.
[20] RUSSELL K,SMISETH O A,GJESDAL O,et al.Mechanism of prolonged electromechanical delay in late activated myocardium during left bundle branch block[J].Am J Physiol Heart Circ Physiol,2011,301:H2334-2343.
[21] BOE E,SKULSTAD H,SMISETH O A.Myocardial work by echocardiography:a novel method ready for clinical testing[J].European Heart Journal-Cardiovascular Imaging,2019,20(1):18-20.
[22] CVIJIC M,DUCHENNE J,?NL? S,et al.Timing of myocardial shortening determines left ventricular regional myocardial work and regional remodelling in hearts with conduction delays[J].European Heart Journal-Cardiovascular Imaging,2018,19(8):941-949.
[23] HUBERT A,LE ROLLE V,LECLERCQ C,et al.Estimation of myocardial work from pressure-strain loops analysis:an experimental evaluation[J].European Heart Journal-Cardiovascular Imaging,2018,19(12):1372-1379.
[24] SABATINO J,DE ROSA S,LEO I,et al.Non-invasive myocardial work is reduced during transient acute coronary occlusion[J].PLoS One,2020,15:e0244397.
[25] CHAN J,EDWARDS N F A,KHANDHERIA B K,et al.A new approach to assess myocardial work by non-invasive left ventricular pressure-strain relations in hypertension and dilated cardiomyopathy[J].European Heart Journal-Cardiovascular Imaging,2019,20(1):31-39.
[26] LIM P,BUAKHAMSRI A,POPOVIC Z B,et al.Longitudinal strain delay index by speckle tracking imaging:a new marker of response to cardiac resynchronization therapy[J].Circulation,2008,118:1130-1137.
(收稿日期:2022-11-25)
(本文编辑 王雅洁)
