棘突纵割双开门椎管扩大成形术治疗多节段重度颈椎后纵韧带骨化症的长期疗效
2024-04-19蒋继乐何达李祖昌李楠
蒋继乐,何达,李祖昌,李楠
颈后路椎管成形术是临床上治疗颈椎后纵韧带骨化症(ossification of posterior longitudinal ligament,OPLL)的常用手术方法,其能够有效地扩大椎管容积、解除脊髓压迫、缓解神经损害症状。其中双开门手术因对称性好、固定牢靠等优势更受临床医师青睐[1]。首都医科大学附属北京积水潭医院自2001年开始采用棘突纵割双开门椎管扩大成形术(spinous process splitting laminoplasty using coralline hydroxyapatite,SLAC)治疗颈椎OPLL 患者。该术式缩短了手术时间,减少了术中出血量,术后3 个月可达到门轴侧骨型融合[2],获得了良好的临床效果[3]。但由于椎管成形术为间接减压,长期疗效与原发病灶的进展、颈椎曲度的变化等因素密切相关,尚需要长期临床随访验证。同时对于重度狭窄的颈椎OPLL,手术方式尚存争议,尤其是椎管占位超过60%的重度压迫患者,术后神经恢复效果往往较差[4]。部分学者认为,重度狭窄的患者单纯后路手术无法获得满意的减压效果[5],常需要一期或分期前路手术进行治疗[6],或者行单纯前路手术[7]。单一后路手术治疗重度狭窄的骨性压迫患者能否达到与压迫较轻患者同样的疗效,目前临床上仍有争议。为此,本研究拟探讨SLAC 治疗多节段重度颈椎OPLL的长期疗效。
1 资料与方法
1.1 一般资料
纳入标准:①诊断为多节段(≥3 个节段)颈椎OPLL,保守治疗无效,脊髓压迫症状明显进展;②随访超过9 年;③临床资料完整。排除标准:①行一期或分期前路手术的患者;②合并颈椎肿瘤、感染、外伤等其他颈椎疾病的患者;③同期行颈椎内固定术(椎弓根螺钉或者侧块螺钉内固定术)的患者。
2005 年5 月至2011 年7 月首都医科大学附属北京积水潭医院采用颈椎SLAC治疗235例多节段颈椎OPLL患者。依据上述纳入与排除标准,共47例患者纳入本研究。其中男25 例,女22 例,年龄32~72 岁,平均(51.1±14.5)岁。患者以行走不稳、精细动作受限、双手麻木等脊髓压迫症状为主。
本研究经首都医科大学附属北京积水潭医院伦理委员会审批通过(积伦科审字第202012-02 号),患者均签署知情同意书。
1.2 手术方法
所有患者均接受SLAC,手术方法参考既往文献[8]:患者全身麻醉后,取俯卧位,取颈后正中切口,暴露C3~C7 棘突,其中保留C2 和C7 棘突肌肉止点,于C3行全椎板切除术,避免C3进行双开门后棘突对半棘肌的刺激,在C7 头侧行部分椎板切除,从C4 椎板头端至C6/7 之间穿入套管,在套管引导下穿入线锯,并纵行劈开C4~C6 棘突;用高速磨钻在C4~C6 两侧椎板与侧块连接处开槽,切除一侧皮质,然后沿棘突正中掀开棘突,行双开门椎管成形术,术中可见硬膜囊后移伴搏动,使用磨钻在C4~C6 棘突上打眼,并植入珊瑚人工骨,使用丝线固定人工骨,逐层关闭切口。
对于C2 后方有压迫的患者,行C2 穹窿下减压,保留C2棘突和半棘肌在C2棘突的附着点,磨钻磨除C2尾端1/2椎板进行充分减压。
对于C7 后方有压迫者,需行C7 后方彻底减压,术中棘突纵割的节段延长至C7,切除T1 头侧部分椎板,手术节段为C3~T1。
1.3 随访计划与观察指标
术后3 个月、6 个月、1 年及之后每年定期随访。术后6 个月、术后2 年和末次随访时采用颈椎改良日本骨科协会(modified Japanese Orthopedic Association,mJOA)评分、颈椎功能障碍指数(neck disability index, NDI)评估患者神经功能,同时计算颈椎mJOA评分改善率,计算公式为:颈椎mJOA评分改善率=(术后颈椎mJOA 评分-术前颈椎mJOA 评分)/(17-术前颈椎mJOA 评分)×100%;将患者术后短期随访时最高的颈椎mJOA 评分和NDI 定义为术后最佳颈椎mJOA评分和最佳NDI。
术后3 个月和末次随访时行颈椎X 线检查。颈椎X 线片测量矢状面参数,包括过屈位、中立位及过伸位C2~C7 Cobb 角、C7 倾斜角、C2~C7 矢状面垂直距离(sagittal vertical axis, SVA)。 颈椎前凸角(cervical lordosis, CL)定义为中立位C2~C7 Cobb角。由于放大倍率不同,本研究使用相对SVA 值(relative SVA, rSVA)取代C2~C7 SVA 绝对值,rSVA=C2~C7 SVA/C4椎体前后缘的直径。同时计算椎管占位率及颈椎活动度,计算公式为:椎管占位率=(压迫最严重水平的椎管宽度-椎管有效宽度)/椎管宽度。颈椎活动度=过伸位C2~C7 Cobb 角-过屈位C2~C7 Cobb角。同时观察患者轴性症状和C5 神经根麻痹发生情况。
1.4 统计学方法
采用SPSS 22.0软件进行统计学分析。计量资料符合正态分布,以均数±标准差表示。重复测量资料的比较采用方差分析;两组间的比较采用t检验。计数资料的比较采用χ2检验。以P<0.05 为差异有统计学意义。
2 结果
2.1 一般资料
47 例患者随访108~182 个月,平均(131.5±24.1)个月。
20 例患者椎管占位率<60%(压迫组),27 例患者椎管占位率≥60%(重度压迫组)。压迫组与重度压迫组患者年龄、性别差异均无统计学意义,具有可比性(P均>0.05,表1)。

表1 压迫组与重度压迫组患者一般资料比较
2.2 神经功能
患者的神经功能大多在术后6个月达到满意的恢复效果,少数患者需要1~2 年达到神经功能的恢复。与术前相比,47例患者术后神经功能恢复最佳时颈椎mJOA评分增加(3.6±2.4)分,NDI降低(4.8±7.3)%;与术后神经功能恢复最佳时相比,47例患者末次随访时颈椎mJOA评分降低(0.6±2.1)分,NDI增加(0.8±2.7)%,见表2。
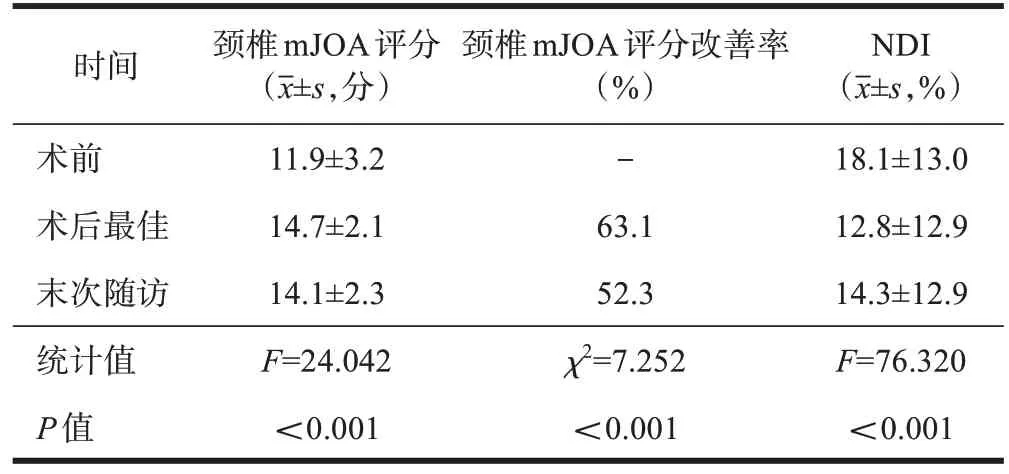
表2 患者手术前后神经功能评分比较(n=47)
手术前后压迫组与重度压迫组患者颈椎mJOA评分、颈椎mJOA 评分改善率、NDI 差异均无统计学意义(P均>0.05,表3)。
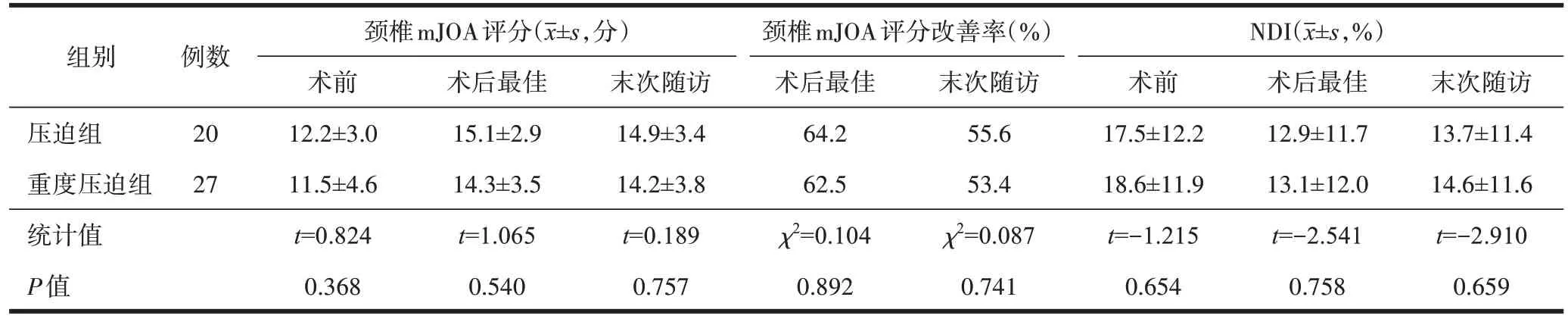
表3 手术前后压迫组与重度压迫组患者临床功能评分比较
2.3 影像学指标
末次随访时,47 例患者CL 由术前的14.4°±10.2°下降至12.1°±11.6°,但差异无统计学意义(P=0.087);末次随访时,47 例患者过屈位C2~C7 Cobb 角、过伸位C2~C7 Cobb 角、颈椎活动度、rSVA、C7 倾斜角与术前比较差异均有统计学意义(P均<0.05,表4)。
表4 患者术前与末次随访时影像学指标比较(n=47,±s)

表4 患者术前与末次随访时影像学指标比较(n=47,±s)
时间术前末次随访t值P值CL(°)14.4±10.2 12.1±11.6 1.410 0.087过屈位C2-C7 Cobb角(°)-14.8±12.7-5.5±11.1 6.894<0.001过伸位C2-C7 Cobb角(°)22.1±10.3 15.3±8.8 8.121 0.01颈椎活动度(°)38.1±12.6 22.6±11.7 9.121<0.001 rSVA(mm)0.7±0.8 1.3±0.6-0.412<0.001 C7倾斜角(°)17.4±7.9 23.9±11.6-6.923<0.001
术前、末次随访时压迫组与重度压迫组患者CL、颈椎活动度、rSVA、C7 倾斜角差异均无统计学意义(P均>0.05,表5)。
表5 术前、末次随访时压迫组与重度压迫组患者影像学指标比较(±s)
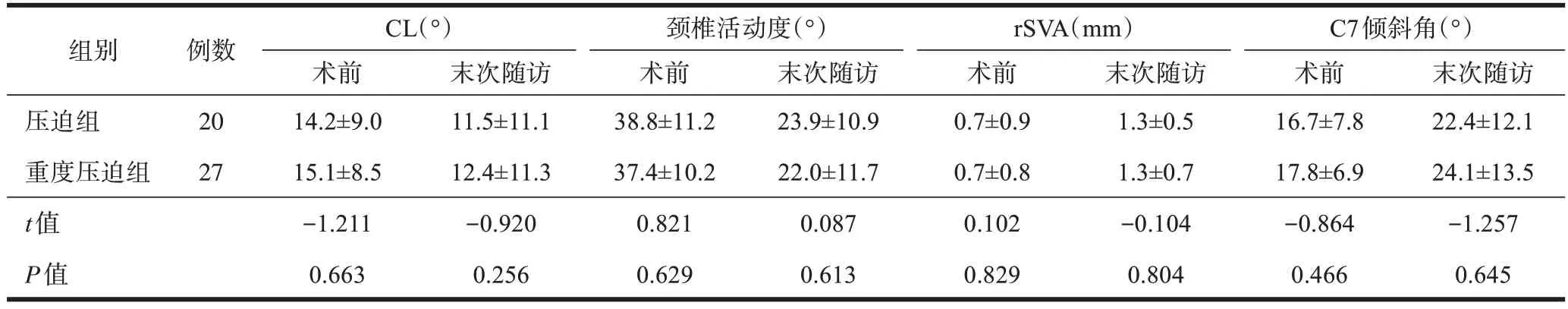
表5 术前、末次随访时压迫组与重度压迫组患者影像学指标比较(±s)
组别例数CL(°)术前14.2±9.0 15.1±8.5-1.211 0.663末次随访1.3±0.5 1.3±0.7-0.104 0.804末次随访11.5±11.1 12.4±11.3-0.920 0.256颈椎活动度(°)术前38.8±11.2 37.4±10.2 0.821 0.629末次随访23.9±10.9 22.0±11.7 0.087 0.613 rSVA(mm)术前0.7±0.9 0.7±0.8 0.102 0.829压迫组重度压迫组t值P值20 27 C7倾斜角(°)术前16.7±7.8 17.8±6.9-0.864 0.466末次随访22.4±12.1 24.1±13.5-1.257 0.645
2.4 术后并发症发生情况
本组47例患者中,10例(21.3%)患者术后出现轴性症状,轴性症状均持续至末次随访时,症状包括颈肩部僵硬、伤口周围疼痛、牵拉或紧绷等。2 例(4.3%)患者术后出现C5 神经根麻痹,术后半年均自行缓解。随访过程中2例患者出现神经症状加重;1例患者在外院诊断为肌萎缩,术后症状未见明显缓解,于外院神经内科继续治疗(术前颈椎mJOA评分11分,末次随访时9分);1例患者术后早期随访神经功能改善(术前颈椎mJOA评分11分,术后2年随访时14分),4 年前出现言语不清、行动不便(末次随访时颈椎mJOA评分6分),未至神经内科就诊。
压迫组与重度压迫组患者术后轴性症状、C5 神经根麻痹、神经症状加重等并发症发生率差异均无统计学意义(P均>0.05,表6)。

表6 压迫组与重度压迫组患者术后并发症发生率比较[例(%)]
典型病例见图1。

图1 患者,男,57岁,因多节段颈椎OPLL采用SLAC治疗
3 讨论
3.1 SLAC的长期疗效
既往国内SLAC相关长期随访研究较少,仅有2篇文献报道,分别来自北京大学第三医院[9]和中国人民解放军空军军医大学西京医院[10],中位随访时间分别为3 年和6 年,但纳入患者随访时间长短不一,难以观察长期疗效。本研究结果显示,SLAC 能够有效改善颈椎OPLL 患者的神经功能,并保持长期疗效,颈椎mJOA评分从术前的(11.9±3.2)分上升到术后神经功能恢复最佳时的(14.7±2.1)分,并一直保持至末次随访时的(14.1±2.3)分,这与既往其他椎管成形术远期疗效类似[11]。
值得注意的是,SLAC 术后神经功能恢复最佳时神经功能评分明显改善,但长期随访过程中仍有部分下降。本研究中,术后颈椎mJOA改善率最高能够达到63.1%,但末次随访时仅维持至52.3%。Moon等[12]观察到,对于颈椎OPLL 患者,前路手术和后路手术的恢复过程并不完全一致,以术后4 年为界,术后短期内后路手术颈椎JOA 改善率较好,而长期随访前路手术的疗效更确切[13]。这可能与前路手术直接切除病灶有关系。
3.2 重度压迫的颈椎OPLL患者的疗效
本研究结果显示,压迫组患者术前mJOA评分为(12.2±3.0)分,重度压迫组患者为(11.5±4.6)分,两者之间差异无统计学意义(P=0.368)。影像学检查提示重度压迫并不意味着神经症状更重。既往研究也显示,颈椎OPLL 患者临床症状与病程、年龄、外伤病史和磁共振成像(magnetic resonance imaging, MRI)高信号表现相关性更强[14],而并不直接与椎管占位率相关。也有学者尝试使用计算机断层扫描(computed tomography, CT)测量三维上的椎管占位容积[15],发现与平面上椎管占位率相比,三维上的椎管占位容积能更好地反映对神经的压迫情况。
本研究结果显示,后路手术能够明显减轻椎管占位率>60%的重度压迫组患者的神经症状,与压迫组患者相比差异无统计学意义(P>0.05)。两组患者颈椎mJOA 评分、NDI和并发症发生率差异均无统计学意义(P均>0.05)。但也有学者认为,对于重度压迫的患者,前路椎体次全切术疗效更佳,尤其是长期随访疗效差异更明显[16]。但也有研究认为,手术方式与具体骨化灶形态有关,与椎管占位率无明显相关性[17]。
除此之外,本研究中患者平均年龄为(51.1±14.5)岁,对于年龄更大的患者来说,后路手术疗效更好,因为前路手术时间长、术中出血量多及其他术后并发症可能会影响术后疗效[18],尤其是短期疗效[19]。
3.3 影响长期随访疗效的因素
晚期神经功能恶化是颈后路术后长期随访过程中的常见并发症,但随着后路手术技术的改进,对颈后路肌肉韧带复合体保护的重视,该并发症发生率明显下降。在一项长期随访研究中,15%的患者出现颈椎JOA 评分降低2 分以上,尤其是术后10 年,仅2%的患者出现骨化灶进展[14]。本研究中共有2 例(4.3%)患者出现神经功能恶化,但与骨化灶进展无明显关系。
颈椎曲度是另一个影响手术效果的关键因素[20]。由于后路手术是依靠前凸实现的间接减压,因此能否保持前凸角度是维持良好手术效果的关键。本研究中,末次随访时患者CL 由术前的14.4°±10.2°下降至末次随访时的12.1°±11.6°,保持了良好的前凸。Lau 等[21]的研究也显示,术后前凸维持得越好,神经功能恢复越好,疼痛评分越低。
颈椎活动度的变化与症状之间也有明显的相关性,研究显示颈椎活动度更大的患者症状常更为严重[22],提示颈椎活动度也是颈椎OPLL 患者预后不佳的一个危险因素[23]。本研究中,虽然SLAC 并没有固定颈椎,但两组患者术后颈椎活动度均明显下降。
3.4 本研究的局限性
本研究缺乏前路手术作为对照,有待进一步开展多中心的前后路手术对比研究,明确多节段颈椎OPLL患者的最佳治疗方案。
4 结论
长期临床和影像学随访发现,后路双开门椎管成形术能够有效地治疗多节段颈椎OPLL 患者,明显改善神经功能,维持颈椎前凸,并保持术后远期疗效。对于重度压迫的患者,SLAC能够获得同样满意的疗效。
【利益冲突】所有作者均声明不存在利益冲突
