利拉鲁肽联合二甲双胍与缬沙坦治疗合并骨质疏松的糖尿病肾病患者的疗效
2024-04-07张丽莎程玲阴苗苗张楠张静王海芳
张丽莎,程玲,阴苗苗,张楠,张静,王海芳
(邯郸市第一医院,1.内分泌一科;2.检验科,河北 邯郸 056000)
糖尿病肾病为2型糖尿病常见并发症,患者蛋白尿呈持续性、肾小球滤过率降低、血压升高,故其也是导致终末期肾病的最常见原因[1-2]。骨质疏松特征为骨微结构损坏和骨量下降,可引起骨质脆弱,骨折风险加大[3]。由于糖尿病肾病患者肾功能受损,胰岛素缺乏,因此常伴有骨质疏松症状[4]。目前,临床中针对合并骨质疏松的糖尿病肾病患者的研究较少,该类患者的治疗应采用药物组合治疗的方式,治疗目的在于控制血压、血糖,改善肾功能及骨代谢。二甲双胍是常用的降糖药物,可降低胰岛素抵抗和血糖[5],缬沙坦可保护肾功能、降低血压[6],二者联合使用,可发挥协同作用。利拉鲁肽作为人源化胰高血糖素样肽-1受体激动剂[7],能加速胰岛素分泌、减缓胰高血糖素分泌、延缓胃排空、抑制食欲和体重,适用于2型糖尿病及糖尿病肾病患者,尤其对于肥胖或超重的糖尿病患者疗效显著[8]。二甲双胍联合利拉鲁肽或缬沙坦治疗糖尿病及糖尿病肾病已有报道,但目前尚无三者联合用药的相关报道。本研究旨在探讨利拉鲁肽联合二甲双胍与缬沙坦对合并骨质疏松的糖尿病肾病患者血糖水平、骨代谢、肾功能及血管内皮功能的影响。
1 资料与方法
1.1 一般资料
纳入2020年1月至2022年6月邯郸市第一医院收治的204例糖尿病肾病合并骨质疏松患者为研究对象。其中男性119例,女性85例;年龄(62.66±10.35)岁。纳入标准:(1)糖尿病肾病、骨质疏松诊断标准均满足者;(2)年龄40~75岁;(3)无利拉鲁肽、二甲双胍、缬沙坦等药物使用禁忌者;(4)完整的临床资料。排除标准:(1)恶性肿瘤者;(2)合并严重肾衰竭、肝功能不全者;(3)合并其他肾脏病患者;(4)泌尿系统感染患者;(5)哺乳期、妊娠期妇女;(6)有甲状旁腺、甲状腺相关疾病;(7)近3个月患者服用对骨代谢有影响的药物。按照不同治理方式分为对照组(n=102)及观察组(n=102)。本研究经医院伦理委员会批准,患者已签同意书。两组患者一般资料比较,差异无统计学意义(P>0.05)。见表1。
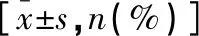
表1 两组患者一般资料比较
1.2 方法
两组患者入院后均给与健康指导,包括合理饮食、控制体重等。对照组采取二甲双胍联合缬沙坦治疗,盐酸二甲双胍片(江苏苏中药业)口服初始剂量为0.25 g/次,2~3次/ d,10~15 d后适当调整剂量,最大剂量<2 g/d;缬沙坦胶囊(北京诺华制药)口服,80 mg /次,1次/d,降压效果不满意者可增加至160 mg/d。观察组在上述基础上于腹部注射利拉鲁肽[诺和诺德(中国)制药]治疗,以0.6 mg/(次·d)为初始剂量,7 d后增加剂量,1.2 mg /(次·d)。两组患者均连续治疗12周。
1.3 观察指标
(1)一般资料:收集年龄、性别、有无高血压、体质量指数(BMI)。(2)血糖水平:采用BS-350S全自动生化分析仪(迈瑞生物医疗电子股份公司)检测两组空腹血糖(FBG)、糖化血红蛋白(HbA1C)及餐后2 h血糖(2 h-PBG)。(3)肾功能指标:BS-350S全自动生化分析仪测定两组患者尿酸(UA)、血尿素氮(BUN)。(4)骨代谢指标:采用电化学发光法检测两组血清总Ⅰ型前胶原氨基端延长肽(t-PINP)、骨钙素N端中分子片段(N-MID)、β-胶原特殊序列(β-CTx)水平。(5)内皮功能指标:分别采用硝酸还原酶法检测血清一氧化氮(NO)、放射免疫法检测内皮素1(ET-1)。
1.4 统计学分析
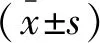
2 结果
2.1 两组患者FPG、2h-PBG、HbA1C水平比较
治疗前,两组患者FPG、2 h-PBG、HbA1C水平比较,差异均无统计学意义(P>0.05)。治疗后,两组患者FPG、2 h-PBG、HbA1C水平均降低,且观察组低于对照组(P<0.05)。见表2。
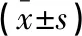
表2 两组患者FPG、2h-PBG、HbA1C水平比较
2.2 两组患者UA、BUN比较
治疗前,两组患者UA、BUN水平比较,差异均无统计学意义(P>0.05)。治疗后,两组患者UA、BUN水平均降低,且观察组低于对照组(P<0.05)。见表3。
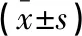
表3 两组患者UA、BUN比较
2.3 两组患者骨转换指标比较
治疗前,两组患者t-PINP、N-MID、β-CTx水平比较,差异均无统计学意义(P>0.05)。治疗后,两组患者t-PINP、N-MID水平均升高,β-CTx水平均降低,且t-PINP、N-MID水平观察组高于对照组,β-CTx水平观察组低于对照组(P<0.05)。见表4。
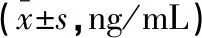
表4 两组患者骨转换指标比较
2.4 两组患者血管内皮功能比较
治疗前,两组患者NO、ET-1指标比较,差异均无统计学意义(P>0.05)。治疗后,两组患者NO水平均升高,且观察组高于对照组(P<0.05);两组患者ET-1水平均降低,且观察组低于对照组(P<0.05)。见表5。
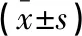
表5 两组患者血管内皮功能比较
3 讨论
糖尿病肾病患者钙、磷代谢紊乱,更易发生骨质疏松,相关研究[9-10]表明,约有30%~40%糖尿病肾病患者发生骨质疏松。糖尿病肾病药物治疗目前以控制血糖、血压,保护肾功能为主[11]。二甲双胍是糖尿病治疗的药物之一,通过减慢肝脏分解糖原和糖新生,加速肌肉对糖的摄取和利用,降低血糖[12];缬沙坦为血管紧张素Ⅱ受体的拮抗剂,通过阻止血管紧张素Ⅱ同受体结合,从而降低血压、扩张血管、抑制肾脏的肾素-血管紧张素-醛固酮系统和降低蛋白尿,常用于肾脏及心血管疾病的治疗中[13]。利拉鲁肽可模拟体内胰高血糖素样肽-1作用,促进胰岛素的分泌,相较于传统降糖药,降糖效果持久,并具有消炎降脂功能。由于利拉鲁肽作为葡萄糖浓度依赖性的降糖药,不易发生低血糖事件,更适用于与其他药物的联合治疗。
高血糖毒性是糖尿病肾病患者发生骨质疏松的重要诱因。本研究中,观察组患者治疗后FPG、2 h-PBG、HbA1C均低于对照组,提示利拉鲁肽联合二甲双胍和缬沙坦降糖效果显著,其作用机制可能如下:(1)利拉鲁肽加快胰岛素分泌,减缓分泌胰高血糖素,促进血糖分解;(2)利拉鲁肽与胃肠及中枢神经GLP-1受体结合,增加患者饱腹感,延缓肠道排空,降低患者食欲,促进脂肪分解,控制患者体脂状态,改善胰岛素抵抗情况。利拉鲁肽与二甲双胍联合降糖,缓解微血管病变,恢复骨骼血供和营养;并缓解渗透性利尿,降低钙、磷排泄,增加血液钙、磷浓度,减少骨吸收。Tamborlane等[14]以青少年2型糖尿病为研究对象,发现利拉鲁肽联合二甲双胍组患者HbA1C、FBG的下降水平高于单独使用二甲双胍组患者。姚胜红等[15]以血糖控制欠佳的糖尿病肾脏疾病患者为研究对象,发现利拉鲁肽能降低HbAlc、FPG、2h-PBG水平,并减少胰岛素使用量。
肾脏是维持钙磷代谢、尿钙、血钙平衡的重要器官。本研究中,观察组患者治疗后UA、BUN均低于治疗前,提示利拉鲁肽还具有保护患者肾功能的作用,分析原因可能为:(1)利拉鲁肽与肾小球血管内皮中的GLP-1受体结合,降低肾小球内的血流阻力和肾小球内压、蛋白尿,保护肾小球的结构和功能;(2)利拉鲁肽抑制TLR-4/MyD88/NF-κB信号通路,激活抗氧化基因,减少炎症反应及自由基的生成,降低肾损伤。利拉鲁肽通过保护肾功能,增加肾小管钙磷重吸收,增强肾脏排酸能力,减轻骨组织钙、镁离子流失;同时肾功能恢复,可促进1,25-二羟维生素D3分泌,增强钙吸收能力。Shaman等[16]发现,利拉鲁肽能使2型糖尿病者的尿蛋白量减少,保护肾功能,且效果在已发生慢性肾病的患者中更为明显。汤巍等[17]以糖尿病大鼠为实验对象,推测利拉鲁肽可能通过干预炎症及氧化应激反应中的相关因子和信号通路,发挥保护肾功能的作用。
本研究中,治疗后观察组患者t-PINP、β-CTx均低于对照组,N-MID高于对照组,提示联合利拉鲁肽有利于改善患者骨代谢。分析原因可能如下:(1)治疗后患者血糖水平下降,减轻高糖对骨代谢的不利影响;(2)利拉鲁肽通过调节骨代谢相关的信号通路,加速骨形成、减缓骨吸收、从而使骨代谢维持平衡。林霞等[18]以骨质疏松大鼠为实验对象,发现利拉鲁肽能激活O3a/Wnt信号通路,从而提升大鼠骨密度。Li等[19]在小鼠实验中发现,利拉鲁肽能抑制破骨细胞的形成和骨吸收,并通过对NF-κB/MAPK-NFATc1信号通路的抑制,表现出对骨病的治疗作用。本研究还发现,相较于对照组,观察组患者NO较高、ET-1较低,提示利拉鲁肽能进一步恢复血管内皮功能,这可能与利拉鲁肽下调纤溶酶原激活物抑制剂-1和血管粘附分子的表达、减少活性氧簇和血栓生成、保护内皮细胞结构和功能相关。来静等[20]通过大鼠实验发现,利拉鲁肽可作用PI3k/Akt信号通路,保护肺微血管内皮细胞功能。徐伟等[21]以肥胖2型糖尿病患者为研究对象,发现利拉鲁肽联合二甲双胍能够改善血管内皮功能,控制体内炎症和糖脂代谢状态,且具有良好的安全性。
综上,利拉鲁肽联合二甲双胍与缬沙坦治疗合并骨质疏松的糖尿病肾病患者疗效确切,有利于降低患者血糖水平,促进骨生成、抑制骨吸收,改善肾功能及血管内皮功能。
