吉西他滨膀胱灌注化疗在非肌层浸润性膀胱癌术后患者中的应用效果△
2024-04-07欧阳威张文元赵俊杨彦峰
欧阳威,张文元,赵俊,杨彦峰
吉安市中心人民医院(上海市东方医院吉安医院)泌尿外科,江西 吉安 343000
膀胱癌是指发生在膀胱黏膜上的恶性肿瘤,是泌尿系统常见的恶性肿瘤。流行病学调查数据显示,膀胱癌的发病率居全部泌尿系统肿瘤首位,对患者的生命健康造成严重威胁[1-2]。非肌层浸润性膀胱癌也称浅表性膀胱癌,是指膀胱癌细胞侵袭黏膜下肌层组织,未出现远处转移。非肌层浸润性膀胱癌的首选治疗方法是手术切除,以经尿道膀胱肿瘤电切术为主要术式,其对膀胱癌患者具有良好的治疗效果[3-4]。但临床研究显示,经尿道膀胱肿瘤电切术后患者存在一定的复发率,因此,术后需要给予辅助治疗以提高治疗效果[5]。既往对于膀胱癌术后患者可采取灌注化疗,化疗药物通过灌注的方式直接到达病灶局部,可以更好地杀灭术后残存的膀胱癌细胞[6]。选取何种化疗药物进行灌注给药,是目前临床研究的重点。吉西他滨是一种新型化疗药物,属于嘧啶核苷类抗肿瘤药物,能够抑制肿瘤细胞DNA 合成,从而抑制肿瘤细胞的生长和增殖,具有良好的抗肿瘤效果[7]。本研究探讨吉西他滨膀胱灌注化疗在非肌层浸润性膀胱癌术后患者中的应用效果,现报道如下。
1 资料与方法
1.1 一般资料
选取2021 年1 月至2023 年8 月吉安市中心人民医院收治的非肌层浸润性膀胱癌患者。纳入标准:①符合《中国泌尿外科疾病诊断治疗指南手册》[8]中非肌层浸润性膀胱癌的诊断标准,经CT、超声、膀胱镜、组织病理学检查确诊为非肌层浸润性膀胱癌;②具有手术治疗指征,行根治性手术治疗;③术后进行灌注化疗。排除标准:①未按照化疗方案进行化疗;②中途出现严重并发症导致化疗中断。依据纳入和排除标准,本研究共纳入120例非肌层浸润性膀胱癌患者,根据术后治疗方法的不同分为对照组(吡柔比星膀胱灌注化疗)和观察组(吉西他滨膀胱灌注化疗),每组60 例。对照组 中,男50 例,女10 例;年 龄40~80 岁,平 均(63.44±8.10)岁;肿瘤直径1~6 cm,平均(3.49±1.03)cm;TNM 分期:Ⅰb 期19 例,Ⅱa 期24 例,Ⅱb期17 例;美国麻醉医师协会(American Society of Anesthesiologists,ASA)分级:Ⅰ级35 例,Ⅱ级25例。观察组中,男48 例,女12 例;年龄40~82 岁,平均(64.97±8.41)岁;肿瘤直径1~6 cm,平均(3.52±1.01)cm;TNM 分期:Ⅰb 期29 例,Ⅱa 期20例,Ⅱb 期11 例;ASA 分级:Ⅰ级39 例,Ⅱ级21例。两组患者的性别、年龄、肿瘤直径、TNM 分期、ASA 分级比较,差异均无统计学意义(P﹥0.05),具有可比性。本研究经医院伦理委员会审批通过,所有患者均知情同意。
1.2 治疗方法
对照组患者术后给予吡柔比星膀胱灌注化疗,具体方案:术后1 周,将盐酸吡柔比星25 mg/m2加入40 ml 5%葡萄糖注射液中,经膀胱灌注给药,每周1 次,4 周为1 个疗程,共治疗2 个疗程。
观察组患者术后给予吉西他滨膀胱灌注化疗,具体方案:术后1 周,将吉西他滨1.0 g/m2加入40 ml 0.9%氯化钠注射液中,经膀胱灌注给药,每周1 次,4 周为1 个疗程,共治疗2 个疗程。治疗期间关注两组患者的生理指标变化,并进行营养干预、康复训练指导等。
1.3 观察指标及评价标准
①临床疗效:采用实体瘤疗效评价标准(response evaluation criteria in solid tumor,RECIST)[9]评价两组患者的临床疗效。肿瘤病灶完全消失,至少维持4 周为完全缓解(complete response,CR);肿瘤病灶长径总和与基线相比减少≥30%,至少维持4 周为部分缓解(partial response,PR);肿瘤病灶长径总和与基线相比减少﹤30%或增加﹤20%为疾病稳定(stable disease,SD);肿瘤病灶长径总和与基线相比增加≥20%或出现新病灶为疾病进展(progressive disease,PD)。疾病控制率=(CR+PR+SD)例数/总例数×100%。②肿瘤标志物水平:分别于治疗前后采集两组患者肘静脉血约3 ml,3500 r/min 离心15 min,离心半径为8 cm,取上层血清,采用生化分析仪检测癌胚抗原(carcinoembryonic antigen,CEA)水平。分别于治疗前后采集两组患者第一次晨尿,立即送检,采用反向间接血凝试验检测尿纤维蛋白原降解产物(fibrinogen degradation product,FDP)水平。③生活质量:分别于治疗前、治疗结束后3 个月采用欧洲癌症研究与治疗组织生命质量测定量表(European Organization for Research and Treatment of Cancer quality of life questionnaire core 30,EORTC QLQ-C30)[10]评价两组患者的生活质量,本研究选取躯体功能、角色功能、社会功能、总体健康4 个维度,每个维度总分均为100 分,评分越高表明生活质量越好。④不良反应发生情况:统计并比较两组患者治疗期间的不良反应发生情况,包括恶心呕吐、骨髓抑制、血小板减少、肝肾功能异常、白细胞减少。
1.4 统计学方法
采用SPSS 25.0 软件对数据进行统计分析,计量资料以均数±标准差(±s)表示,组间比较采用两独立样本t检验,组内比较采用配对t检验;计数资料以例数和率(%)表示,组间比较采用χ2检验;以P﹤0.05 为差异有统计学意义。
2 结果
2.1 临床疗效的比较
观察组患者的疾病控制率为88.33%(53/60),明显高于对照组患者的68.33%(41/60),差异有统计学意义(χ2=7.070,P=0.008)。(表1)

表1 两组患者的临床疗效[n(%)]*
2.2 肿瘤标志物水平的比较
治疗前,两组患者血清CEA、尿FDP 水平比较,差异均无统计学意义(P﹥0.05)。治疗后,两组患者血清CEA、尿FDP 水平均低于本组治疗前,观察组患者血清CEA、尿FDP 水平均低于对照组,差异均有统计学意义(P﹤0.05)。(表2)
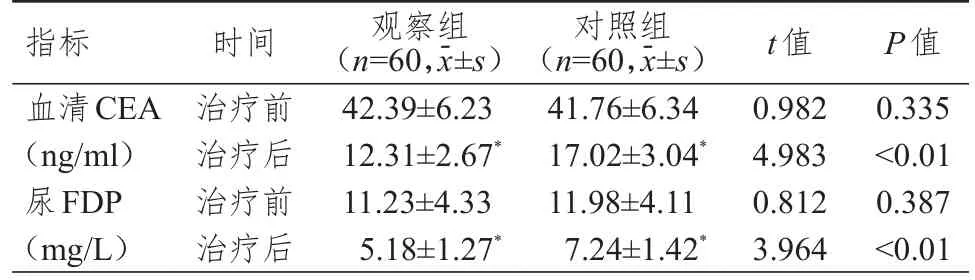
表2 治疗前后两组患者肿瘤标志物水平的比较
2.3 生活质量的比较
治疗前,两组患者躯体功能、角色功能、社会功能、总体健康评分比较,差异均无统计学意义(P﹥0.05)。治疗后,两组患者躯体功能、角色功能、社会功能、总体健康评分均高于本组治疗前,观察组患者躯体功能、角色功能、社会功能、总体健康评分均高于对照组,差异均有统计学意义(P﹤0.05)。(表3)

表3 治疗前后两组患者EORTC QLQ-C30 评分比较
2.4 不良反应发生情况的比较
治疗期间,观察组患者的不良反应总发生率为16.67%(10/60),与对照组患者的20.00%(12/60)比较,差异无统计学意义(χ2=0.465,P=0.512)。(表4)

表4 两组患者的不良反应发生情况[n(%)]
3 讨论
膀胱癌是泌尿系统常见的恶性肿瘤,发病率居泌尿系统肿瘤首位,其发病受多种因素影响,包括遗传、不良饮食和生活习惯、吸烟以及接触致癌物质等[11]。通常情况下,经尿道膀胱肿瘤电切术后仍然有肿瘤细胞残留,这是导致膀胱癌患者术后复发的主要原因。
本研究结果显示,观察组患者的疾病控制率明显高于对照组(P﹤0.01)。表明吉西他滨膀胱灌注化疗可提高非肌层浸润性膀胱癌术后患者的临床疗效。分析原因如下,吉西他滨属于一种新型胞嘧啶核苷衍生物,该药进入患者机体后,被脱氧胞嘧啶激酶活化,产生的活性代谢产物可进入肿瘤细胞的DNA 中,并作用于肿瘤细胞周期的G1/S期,抑制核苷酸还原酶的活性,使脱氧核苷三磷酸酯减少,进而抑制肿瘤细胞DNA 链的延伸,抑制肿瘤细胞增殖和分裂[12-13]。此外,吉西他滨还可通过影响多个信号通路,增强凋亡相关蛋白的表达,从而促使肿瘤细胞凋亡[14-15]。膀胱癌患者病情进展过程中伴有多种肿瘤标志物异常表达,血清CEA、尿FDP 均是非肌层浸润性膀胱癌患者病情进展过程中高表达的标志物。本研究结果显示,治疗后,两组患者血清CEA、尿FDP 水平均低于本组治疗前,观察组患者血清CEA、尿FDP 水平均低于对照组,差异均有统计学意义(P﹤0.05)。表明吉西他滨膀胱灌注化疗可降低非肌层浸润性膀胱癌术后患者的肿瘤标志物水平。本研究结果还显示,治疗后,两组患者躯体功能、角色功能、社会功能、总体健康评分均高于本组治疗前,观察组患者躯体功能、角色功能、社会功能、总体健康评分均高于对照组,差异均有统计学意义(P﹤0.05)。表明吉西他滨膀胱灌注化疗可提高非肌层浸润性膀胱癌术后患者的生活质量,与相关文献报道的结果一致[16]。治疗期间,两组患者的不良反应总发生率比较,差异无统计学意义(P﹥0.05)。表明吉西他滨膀胱灌注化疗应用于非肌层浸润性膀胱癌术后患者,未增加不良反应,安全性良好。
综上所述,吉西他滨膀胱灌注化疗可提高非肌层浸润性膀胱癌术后患者的临床疗效和生活质量,降低肿瘤标志物水平,且安全性良好。
