鼻胰管在重症急性胰腺炎腹腔感染合并胰瘘病人中的应用效果分析
2024-03-26朱孔凡朱忠超李蔚常剑
朱孔凡,朱忠超,李蔚,常剑
武汉大学人民医院胰腺外科,湖北 武汉 430060
重症急性胰腺炎(severe acute pancreatitis,SAP)是一种常见但危及生命的腹部急危重症[1],其死亡率高,病情复杂、发展迅速,涉及多个器官系统[2]。SAP 约占所有急性胰腺炎病例的20%,全身性损伤表现为器官衰竭[3]。当下SAP 的诊治已经进入一个微创治疗的时代,但是仍然存在约15%较高的院内病死率[4]。有研究表明,腹腔感染是造成SAP 病人死亡的主要危险因素之一[5]。SAP 合并腹腔感染发生率为20%~30%,病死率高达80%,往往合并有各种腹腔感染,包括胰瘘[6]。在治疗SAP 合并腹腔感染的过程中,目前均采用Step-up升阶梯的治疗原则,腹腔穿刺引流(abdominal paracentesis drainage,APD)是临床治疗中不可缺少的一步[7],胰瘘也成了SAP 腹腔感染常见且严重的并发症之一[8]。胰腺周围脓肿发生胰瘘的风险高达60%[9],可导致胰瘘迁延不愈、腹腔内出血、感染性休克,甚至死亡。目前尚未找到避免胰瘘发生的有效方法[10]。近年来,内镜介入治疗在SAP 合并胰瘘治疗中的作用凸显,尤以经内镜逆行胰胆管造影(endoscopic retrograde cholangiopancreatography,ERCP)为主[11],ERCP 能够显示胰瘘位置、大小及流出情况[12]。有研究表明,内镜下鼻胰管引流术(endoscopic naso-pancreatic drainage,ENPD)既可以通过引流降低胰管压力,将胰液通过鼻胰管引流至体外,促进瘘管愈合[13];亦可以避免胰管支架置入后脱落,带来的不利。因此,本中心将鼻胰管应用于SAP 腹腔感染合并胰瘘的病人,发现该治疗方式能够起到良好的治疗效果,为临床实践提供了依据,现报告如下。
资料与方法
一、一般资料
回顾分析2019年6月至2021年1月期间在我院确诊的47 例SAP 腹腔感染合并胰瘘病人病例资料。本研究将病人是否经过ERCP 留置鼻胰管,分为研究组(ERCP 术中置入鼻胰管,22 例)与对照组(25 例)。本研究经本院医学伦理委员会审批通过(伦审号:WDRY2022-K276)。病人入院后48 h 内记录下列指标:年龄、性别、体重指数、病因、急性生理学与慢性健康状况评分系统Ⅱ(APACHE Ⅱ)及急性胰腺炎Balthazar CT 评分。其中APACHE Ⅱ评分用于评估病人整体病情,预测病人死亡风险及预后。
二、纳入与排除标准
1. 病例纳入标准 (1)所有病例均符合《中国急性胰腺炎诊治指南(2021)》[14]中SAP相关诊断标准,即在具备急性胰腺炎诊断标准的基础上合并有持续性(>48 h)的器官功能衰竭。(2)均证实合并腹腔感染,且具备以下症状:①临床出现腹部疼痛、腹肌紧张、腹部压痛或反跳痛、腹腔积液等症状;②胰腺坏死组织/腹腔脓液病原菌培养呈阳性[6];③符合全身炎症反应综合征诊断标准中的2 项及以上[15]。(3)均符合2005年国际胰腺外科研究组(ISGPS)发布的术后胰瘘诊断标准:引流液淀粉酶浓度高于血清淀粉酶正常值上限的3倍,影像学支持胰管不连续诊断,且胰瘘持续4 周以上[16]。同时符合以上3 项即纳入SAP 腹腔感染合并胰瘘病例。(4)病人临床资料完整。(5)病人及其家属均签署了治疗知情同意书。
2. 排除标准 (1)伴有恶性肿瘤、血液系统疾病者;(2)存在药物过敏、严重精神障碍;(3)合并严重心肺基础疾病者;(4)治疗依从性差者;(5)存在ERCP手术禁忌病人。
三、治疗方法
两组病人入院时均予以常规治疗:禁食、胃肠减压、解痉、镇痛、静脉/肠内营养支持及预防性抗生素使用等,经证实合并腹腔感染或者消化道梗阻等症状者均采用腹腔经皮穿刺置管引流术(percutaneous catheter drainage,PCD)等常规治疗[创伤递升式(Step-up)策略]。研究组22 例病人在予以常规治疗的基础上,联合经ERCP 介导下置入鼻胰管。手术过程:病人术前禁饮禁食8 h,麻醉专科医师对病人行麻醉评估,病人术中取俯卧位,实施静脉全身麻醉。所有内镜操作均由同一组有经验的医师完成,手术医师应用TJF260 十二指肠镜(日本Olympus)通过导丝引导法置入鼻胰管。鼻胰管经胃、鼻腔引出,外接一次性引流袋,将其妥善固定,防止脱落。术中监测生命体征,术后待病人麻醉苏醒后转回病房治疗,观察引流胰液量、颜色和性质。若发现病人鼻胰管引流不畅时,及时予以疏通,使鼻胰管在整个治疗过程中保持通畅引流。
四、评价指标
主要记录两组病人白细胞恢复正常所需的时间;同时对所有病人的引流液进行观察,记录病人带管时间;并对两组病人的住院时间及期间并发症的发生情况进行统计分析。
五、统计学方法
采用SPSS 22.0 统计学软件对所得数据作统计学分析,正态分布的计量资料采用±s表示,组间比较用t检验;计数资料采用构成比或率(%)表示,组间比较用χ2检验,以P<0.05为差异有统计学意义。
结 果
一、病人一般临床资料比较
两组病人在年龄、性别、病因及疾病评分等一般资料方面比较差异均无统计学意义(均P>0.05),具有可比性(表1)。

表1 重症急性胰腺炎腹腔感染合并胰瘘病人常规治疗组(对照组)与联合经内镜逆行胰胆管造影介导下置入鼻胰管组(研究组)临床资料比较
二、两组病人并发症及治疗情况比较
与对照组比较,研究组带管时间和脓毒症、腹腔出血、假性囊肿并发症发生率明显降低,两组比较差异均有统计学意义(均P<0.05),而两组的白细胞升高持续时间和住院时间差异均无统计学意义(均P>0.05),详见表2。

表2 重症急性胰腺炎腹腔感染合并胰瘘常规治疗组(对照组)与联合经内镜逆行胰胆管造影介导下置入鼻胰管组(研究组)病人并发症及治疗情况比较
三、临床案例治疗情况
1 例64 岁男性病人,因腹痛腹胀1 周由外院转入。病人鼻胰管引流手术前、后腹部CT 变化:该病人在腹腔穿刺前腹腔大面积坏死合并胰周感染(图1A),经腹腔穿刺引流后1 个月,病人出现梗阻性黄疸及持续性胰瘘(图1B),每日瘘量在150~300 mL,在ERCP 下行鼻胰管置入,胰液外引流及7.5F塑料胆道支架置入(图1C、D),鼻胰管置入1 周后,腹部CT 显示胰周积液明显减少(图1E),鼻胰管置入1个月后,拔出腹腔引流管,胰瘘愈合(图1F)。
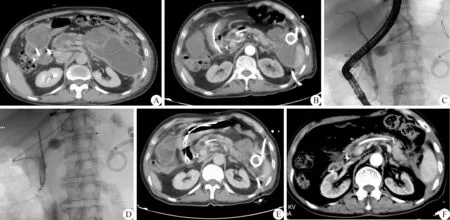
图1 1 例64 岁男性病人,因腹痛腹胀1 周由外院转入
讨 论
胰瘘在SAP 诊治当中得到了越来越多的认识,C 级胰瘘是一种可能危及生命的严重并发症[17]。胰瘘涉及并发症的风险包括严重脓毒症、腹腔内出血、ICU住院时间延长、治疗费用增加和生活质量下降等[18]。瘘管形成的机制与主胰管和小胰管的损伤有关[9]。而胰腺坏死及胰周广泛积液被广泛认为是SAP 术后胰瘘的危险因素。糖尿病及血糖控制不佳与较高的腹腔感染及术后胰瘘发生率相关,导致术后胰瘘风险比非糖尿病病人高10 倍[19]。胰瘘作为胰腺炎相关术后严重的并发症之一,死亡率高达45%[20]。即使在治疗大量胰腺病例的机构中,SAP 腹腔感染术后胰瘘发生率仍为10%~20%[21]。如何有效减少胰瘘的发生并及时进行治疗,是临床亟待解决的问题。
随着ERCP 及内镜超声技术的成熟,通过胰管支架或经胃壁穿刺引流等手段治疗可使更多的胰瘘病人免于外科手术。胰管支架置入已被证明是内镜下治疗胰瘘的有效方式[22-25]。然而,瑞典的一项单中心研究并未证实支架置入术在预防具有临床意义的胰瘘方面的功效。相反,在支架置入术病人中,B 级和C 级胰瘘更为常见,住院时间更长[26]。由此可见,尽管有许多预防胰瘘的技术,但至今没有一种完全有效的方法。
内镜下鼻胰管引流术可以通过引流降低胰管压力,将胰液通过鼻胰管引流至体外,既可避免胰管支架脱落,亦可以促进瘘管愈合。但目前鼻胰管引流术相关研究样本量较小,多为小样本研究[13]。有研究介绍了2例内镜治疗对低密度脂蛋白移植术后发生的胰瘘有效[27]。Kuroki 等[28]回顾了6 例在局部胰腺切除术中使用内窥镜鼻胰引流管进行术中胰腺造影,可有效预防局部胰腺切除术后胰瘘的发生。Costamagna 等[12]研究者共有16 例连续胰瘘病人在保守治疗失败后尝试进行内镜治疗,在12 例成功治疗的病人中,经过平均24.7 个月的随访,11 例幸存病人中没有瘘管复发。而且已有研究表明ENPD 是一种有效的胰液引流方法,可能在SAP 的治疗中发挥重要作用[29]。因此,本研究首次将鼻胰管用于SAP 腹腔感染合并胰瘘病人,结果显示,研究组带管时间显著减少,且治疗期间脓毒血症、腹腔出血和假性囊肿发生率明显下降(P<0.05),可见鼻胰管置入不仅能有效缓解SAP 腹腔感染并发症的发生率,而且还可以促进瘘管愈合。
本研究通过对22 例行ERCP 介导的鼻胰管置入治疗的SAP 腹腔感染合并胰瘘病人病例资料分析,发现该治疗方法能有效改善其临床症状,促进病人病情恢复。本研究显示该方法治疗SAP 腹腔感染合并胰瘘安全、有效且微创,后续在科学的临床研究指导下,值得进一步临床推广使用。虽然现有研究结果令人满意,但本研究不足之处在于研究病例数为单中心小样本的回顾性研究,其有效性及安全性需要多中心大量临床样本去进一步研究验证。因此,ERCP 介导的鼻胰管置入是SAP 腹腔感染合并胰瘘病人治疗中值得尝试的一种方法,且该方法值得大样本去进一步研究验证。
利益冲突所有作者均声明不存在利益冲突
