杞参益智方改善D-半乳糖注射亚急性衰老模型小鼠学习与记忆能力的效应评价研究
2024-03-14陈杨朱梓强陆韫青郑嘉妮曹程仝佳祥李璇郭盛康宏杰段金廒朱悦
陈杨,朱梓强,陆韫青,郑嘉妮,曹程,仝佳祥,李璇,郭盛,康宏杰,段金廒,朱悦
(1.南京中医药大学药学院,江苏省方剂研究重点实验室/江苏省方剂高技术研究重点实验室/中药资源产业化与方剂创新药物国家地方联合工程研究中心/江苏省中药资源产业化过程协同创新中心,江苏 南京 210023;2.宁夏枸杞创新中心,宁夏 银川 750000)
全球已进入老龄化社会,老年人口的快速增加导致相关的医疗保健等养老问题日趋严峻[1]。老年期痴呆症是一种因脑老化导致的中枢神经系统退行性疾病,表现为记忆、智力、语言及日常生活能力等大脑高级功能的全面障碍,尤其以阿尔茨海默病(Alzheimer’s disease,AD)发病率最高。预计到2050年,中国AD患者人数将超过3 000万,给社会和家庭带来巨大的负担与压力[2]。研究认为,AD患者脑内皮层与海马的β淀粉样蛋白(Amyloid-β peptide,Aβ)沉积导致脑内产生大量氧自由基,加剧氧化应激损伤,氧自由基同时激活小胶质细胞释放大量促炎因子产生炎性应激损伤,氧化应激与炎性应激综合作用导致海马神经元凋亡,是AD重要的病理机制[3-4]。目前AD临床治疗的一线药物主要是胆碱酯酶抑制剂如多奈哌齐与N-甲基-D-天冬氨酸受体(N-Methyl-D-aspartic acid receptor,NMDA)受体阻断剂美金刚等。然而心功能不全患者慎用或禁用胆碱酯酶抑制剂[5],同时AD重在预防以及干预窗口应提早到轻度认知功能障碍(Mild cognitive impairment,MCI)阶段也已经取得共识[6]。
中医根据AD临床表现,将其归属于“健忘”与“痴呆”范畴,并认为患者年龄增长,肾精肝血亏虚,导致心脾失养,运化无力,渐致髓海失养,记忆衰退而成痴呆[7]。AD病位虽在脑,却与心肝脾肾功能失调密切相关。杞参益智方系在《圣济总录》所载经典方剂二精丸(枸杞子与黄精)的基础上,结合防治AD中药材的用药频次统计分析与现代药理学研究成果,加味人参、益智仁组成,同时有助于改善二精丸滋腻易影响脾胃运化功能的不足。全方滋补肝肾、益精填髓、养心安神。处方组成均为药食两用中药,安全性高,更适合AD的预防与长期用药的要求。本研究通过皮下注射D-半乳糖构建亚急性衰老小鼠模型,评价杞参益智方改善模型动物学习与记忆效用,为开发AD防治产品提供理论科学支持。
1 材料
1.1 实验动物
健康SPF级C57BL/6小鼠,雄性,体质量18~22 g,购自斯贝福(北京)生物技术有限公司,动物许可证号:SCXK(京)2019-0010。动物在南京中医药大学实验动物中心SPF级环境中常规饲养,本实验获得南京中医药大学动物实验伦理委员会的批准(批准号:202111A045)。
1.2 药材
枸杞子(LyciumbarbarumL.,批号:2106157)、黄精(PolygonatumsibiricumRed.,批号:237200516)、人参(PanaxginsengC. A. Mey.,批号:109200125)、益智仁(AlpiniaoxyphyllaMiq.,批号:45200618)采购于亳州市紫锐药业有限公司,经段金廒教授鉴定为正品药材。
1.3 实验试剂
D-半乳糖(N13GS167640)购自上海源叶生物科技有限公司;多奈哌齐(GD18339)购自萨恩化学技术有限公司;PAGE凝胶快速制备试剂盒(PG112)、三色预染蛋白Marker(180-6003)购自上海雅酶生物医药科技有限公司;BCA蛋白浓度测定试剂盒(P0009)、RIPA裂解液(P0013B)购自上海碧云天生物技术有限公司;小鼠肿瘤坏死因子α(TNF-α)ELISA试剂盒(AF2132-A)、小鼠白细胞介素(IL)-6 ELISA试剂盒(AF2163-A)、小鼠IL-1β ELISA试剂盒(AF2040-A)购自湖南艾方生物科技有限公司;小鼠超氧化物歧化酶(SOD)检测试剂盒(A001-3-2)、还原性谷胱甘肽(GSH)检测试剂盒(A006-2-1)、丙二醛(MDA)检测试剂盒(A003-4-1)均购自南京建成生物工程研究所。ECL化学发光液(180-5001)购自上海天能公司;抗体β-actin(66009-1-Ig)、Nrf-2(16396-1-AP)、HO-1(10701-1-LG)、Cleaved Caspase-3(25128-1-AP)购自Proteintech公司;抗体Caspase-3 (9662)、NF-κB p65(8242)与p-NF-κB p65(3033)购自CST公司;HRP-Linked Anti-mouse IgG(BA1050)、HRP-Linked Anti-rabbit IgG(BA1054)均购自博士德公司。
1.4 实验仪器
小鼠脑立体定位仪(68000)购自深圳市瑞沃德生命科技有限公司;动物行为学影像采集系统(JLBehv)购自上海吉量生物科技有限公司;倒置显微镜(AXIO Vert A1)购自瑞士Zeiss公司;旋转蒸发仪(Rotavapor R-210)购自瑞士Buchi公司;贝克曼离心机(Microfuge 22R)购自南京百瑞达生物科技有限公司;组织研磨机(Tissuelyer-48)购自上海净业信发展有限公司;多功能酶标仪(ENSPIRE)购自Perkin-Elmer公司;凝胶成像系统(ChemiDoc XRS+Imaging System)购自美国Bio-Rad公司;干式恒温金属浴(SBH130D)购自英国STUART公司。
2 方法
2.1 杞参益智方水提取物的制备
按照处方比例称取枸杞子50 g,黄精50 g,人参30 g,益智仁30 g,加入10倍量水回流提取1.5 h,再加8倍量水回流提取2次各1 h,合并提取液,浓缩至生药含量为1 g·mL-1。
2.2 D-半乳糖注射动物模型的建立及给药
将健康雄性小鼠适应性饲养1周,随机分为5组,分别为空白组、模型组、杞参益智方低剂量组、杞参益智方高剂量组和多奈哌齐(阳性药)组,每组12只。模型组及各给药组小鼠每天皮下注射D-半乳糖600 mg·kg-1,空白组小鼠注射等量的生理盐水,连续造模6周[8]。杞参益智方水提取液用生理盐水分别配制成浓度为0.5、1 g·mL-1的溶液,多奈哌齐用生理盐水配制成浓度为0.2 mg·mL-1的溶液。造模第12天起,除空白组和模型组外,其余各组每日同时以相应的给药量进行灌胃给药,给药体积均为0.01 mL·g-1。给药剂量设置为:杞参益智方低剂量组1.33 g·kg-1·d-1;杞参益智方高剂量组2.67 g·kg-1·d-1;多奈哌齐组2 mg·kg-1·d-1。连续给药30 d。空白组与模型组给予等量生理盐水灌胃。
2.3 行为学检测
给药30 d后进行Morris水迷宫实验和Y迷宫实验,评价模型小鼠学习与记忆能力,具体方法参照课题组已发表的文章[9]。
2.4 TUNEL染色法检测海马区细胞凋亡
行为学测试结束后,小鼠颈椎脱臼处死并解剖取出全脑组织,生理盐水润洗,每组取6只动物全脑组织,放入4%多聚甲醛中固定24 h,依次用乙醇进行梯度脱水,放入二甲苯至透明后包埋,并用切片机切片,切片厚度约5 μm,放于载玻片上展平,并于60 ℃烘箱内烘烤,制得各组动物脑组织病理切片。将所得的脑组织石蜡切片脱蜡。根据TUNEL试剂盒检测步骤进行检测,并用倒置显微镜进行拍照,检测各组动物海马区的细胞凋亡水平。
2.5 氧化应激因子表达检测
行为学检测后,解剖获得海马组织,称取相应质量的组织,加入10倍量PBS,低温研磨,离心取上清待测,按照试剂盒说明书检测SOD活力和MDA、GSH含量。
2.6 致炎因子水平检测
行为学检测后,解剖获得海马组织,称取相应质量的组织,加入10倍量PBS,低温研磨,离心取上清待测,按照ELISA试剂盒检测说明书检测IL-6、IL-1β、TNF-α的含量。
2.7 Western blot检测
称取海马组织,加入10倍量含有蛋白酶抑制剂(Cocktail)的RIPA裂解液,研磨后冰浴30 min,离心取上清,按照BCA试剂盒的步骤测定蛋白浓度,98 ℃加热15 min,使蛋白变性。按照蛋白凝胶试剂盒实验步骤制备10%和12.5%的PAGE凝胶,120 V电泳1.5 h,300 mA转膜2 h,用5%脱脂奶粉放在摇床上封闭1 h,加入一抗(Nrf2 Rabbit mAb、HO-1 Rabbit mAb、Caspase-3 Rabbit mAb、Cleaved Caspase-3 Rabbit mAb抗体稀释比例为1∶2 000;NF-κB p65 Rabbit mAb、p-NF-κB p65 Rabbit mAb抗体稀释比例为1∶1 500;β-actin Rabbit mAb抗体稀释比例为1∶10 000),4 ℃摇床过夜,二抗(HRP-Linked Anti-mouse IgG,HRP-Linked Anti-rabbit IgG,稀释比例1∶10 000)孵育1 h,成像系统曝光并采集。
2.8 统计学方法
3 结果
3.1 杞参益智方对D-半乳糖注射亚急性衰老模型小鼠学习与记忆行为的影响
水迷宫实验考察结果如图1所示,与空白组小鼠相比,模型组小鼠潜伏期与上台前路程显著增加(P<0.01),穿越平台次数显著减少(P<0.05),表明D-半乳糖皮下注射导致了小鼠学习与记忆能力损伤。杞参益智方水提物高、低剂量组显著减少模型小鼠潜伏期和上台前路程(P<0.05,P<0.01),穿越平台次数显著增加(P<0.05,P<0.01)。其中高剂量组作用趋势强于低剂量组。

注:与空白组比较,#P<0.05,##P<0.01;与模型组比较,
Y迷宫实验结果如图2所示,与空白组小鼠相比,模型小鼠的新臂探索时间和次数显著减少(P<0.05,P<0.01)。杞参益智方低剂量组和高剂量组均能显著增加模型小鼠新臂探索时间和次数(P<0.05)。

注:与空白组比较,#P<0.05,##P<0.01;与模型组比较,
上述研究表明,杞参益智方能够显著改善亚急性衰老模型小鼠受损的学习与记忆能力。
3.2 杞参益智方对D-半乳糖注射亚急性衰老模型小鼠海马组织凋亡的影响
结果如图3所示,与空白组小鼠相比,模型组小鼠海马组织凋亡细胞数量显著增多(P<0.01),杞参益智方低、高剂量组显著减少了模型小鼠海马组织凋亡细胞数量(P<0.01),作用趋势相似。
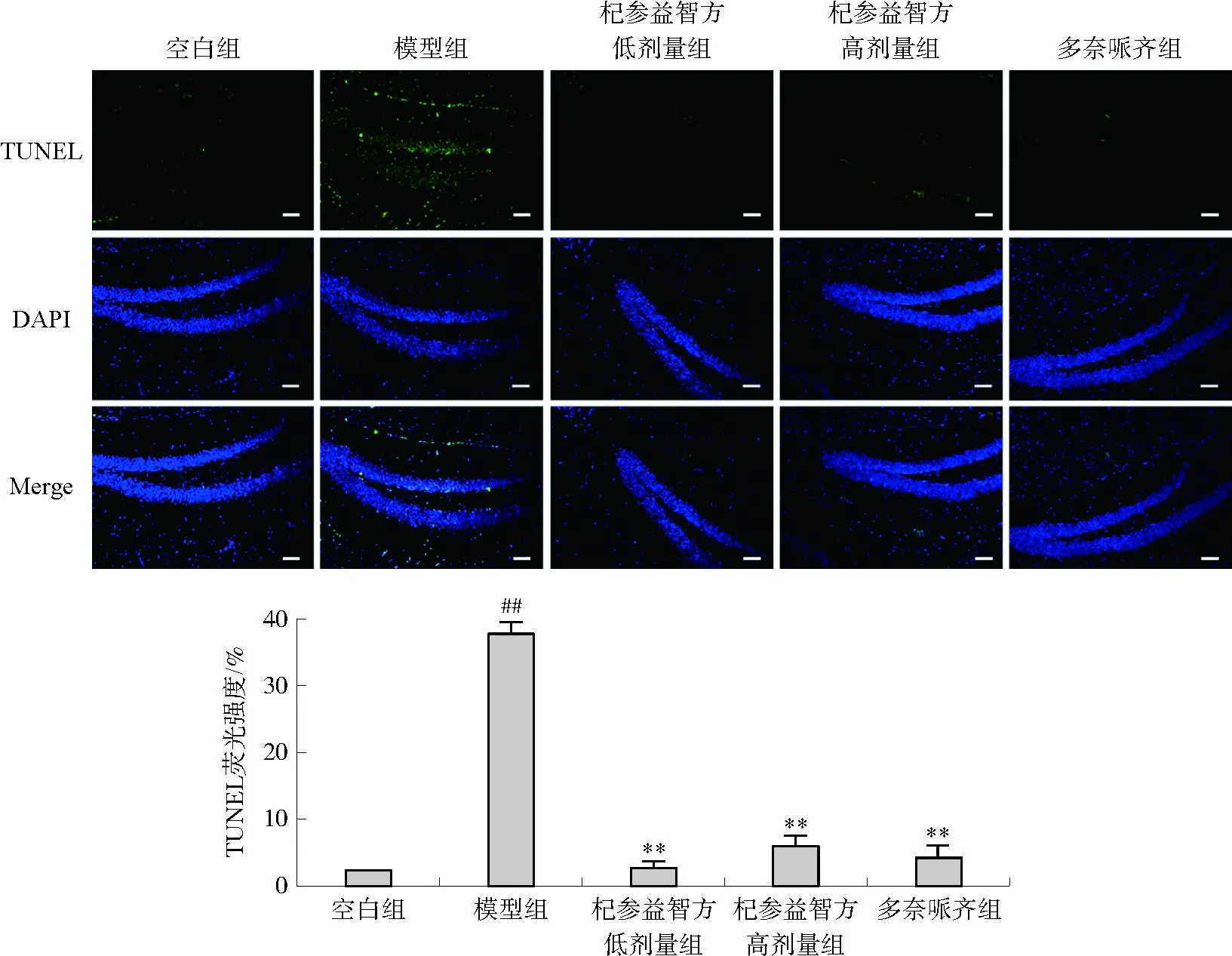
注:与空白组比较,##P<0.01;与模型组比较,
3.3 杞参益智方对D-半乳糖注射亚急性衰老模型小鼠海马组织氧化应激因子表达的影响
结果如图4所示。模型组较空白组小鼠SOD活力和GSH含量显著降低(P<0.05),MDA含量显著升高(P<0.05),表明模型小鼠脑内氧化应激加剧。杞参益智方低、高剂量组均能够显著提高SOD活力和GSH含量(P<0.05),显著降低MDA含量(P<0.05),表明杞参益智方能够降低氧化产物的生成,提高抗氧化因子的表达,从而减缓氧化应激。其中高剂量组在提高GSH表达与降低MDA表达上的作用趋势略强于低剂量组。

注:与空白组比较,#P<0.05;与模型组比较,
3.4 杞参益智方对D-半乳糖注射亚急性衰老模型小鼠海马炎性因子水平的影响
结果如图5所示,与空白组小鼠相比,模型组小鼠海马中IL-1β、IL-6和TNF-α水平显著上升(P<0.05,P<0.01),杞参益智方能够降低上述致炎细胞因子表达的水平(P<0.05,P<0.01)。
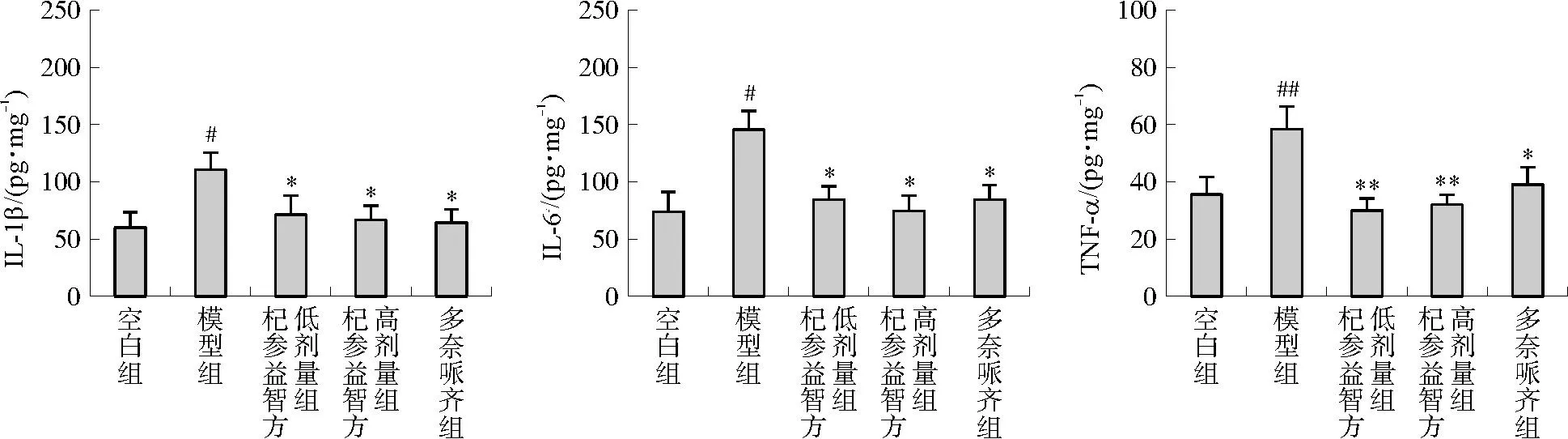
注:与空白组比较,#P<0.05,##P<0.01;与模型组比较,
3.5 杞参益智方对D-半乳糖注射亚急性衰老模型小鼠海马组织凋亡通路蛋白表达的影响
用Western blot法检测小鼠海马组织中凋亡通路蛋白Cleaved Caspase-3与Caspase-3表达,结果如图6所示。与空白组相比,模型组小鼠海马Cleaved Caspase-3与Caspase-3表达均显著升高(P<0.05),Cleaved Caspase-3/Caspase-3比值也显著升高(P<0.05)。杞参益智方能够显著抑制上述2种蛋白的表达(P<0.05),下调Cleaved Caspase-3/Caspase-3比值(P<0.05),表明杞参益智方能够抑制海马细胞凋亡通路的激活。高剂量组的作用趋势略强于低剂量组。

注:与空白组比较,#P<0.05;与模型组比较,
3.6 杞参益智方对D-半乳糖注射亚急性衰老模型小鼠海马组织抗氧化通路蛋白表达的影响
采用Western blot法检测受试动物海马组织中抗氧化关键信号通路蛋白Nrf2与HO-1的表达,结果如图7所示。模型组小鼠海马组织蛋白Nrf2和HO-1的表达水平较空白组显著下调(P<0.05)。与模型组相比,杞参益智方显著增加模型动物海马组织Nrf2和HO-1的表达(P<0.05,P<0.01),提示杞参益智方可通过调控Nrf2/HO-1信号通路发挥抗氧化作用。高剂量组的上调作用趋势略强于低剂量组。

注:与空白组比较,#P<0.05;与模型组比较,
3.7 杞参益智方对D-半乳糖注射亚急性衰老模型小鼠海马组织NF-κB蛋白表达的影响
采用Western blot法检测小鼠海马组织中炎性通路关键蛋白NF-κB与其磷酸化蛋白p-NF-κB表达,结果如图8所示。与空白组相比,模型组小鼠海马p-NF-κB表达与p-NF-κB/NF-κB比值显著升高(P<0.05),杞参益智方能够显著下调p-NF-κB表达与p-NF-κB/NF-κB比值(P<0.05),提示杞参益智方能够抑制海马细胞炎性通路的激活。
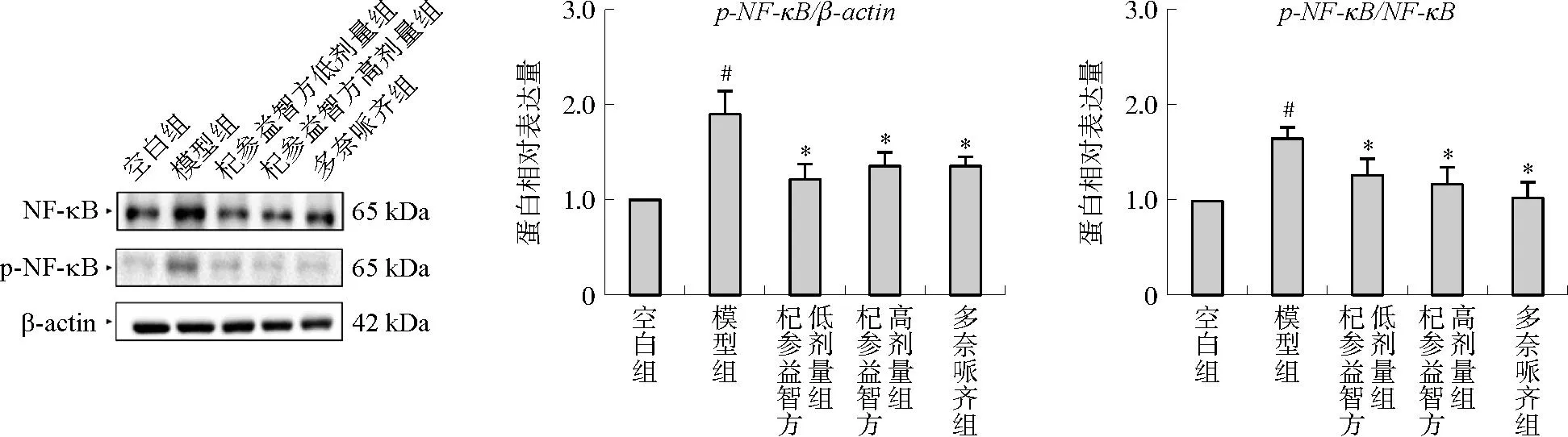
注:与空白组比较,#P<0.05;与模型组比较,
4 讨论
迄今为止,1956年Harman提出的线粒体自由基学说是衰老损伤发生机制中最具有影响力的学说。该学说认为随着年龄增长,细胞代谢过程中产生的自由基不断增加而清除能力逐渐降低[10]。ROS急剧增加,导致抗氧化剂GSH和抗氧化酶SOD显著降低,氧化剂MDA急剧增加,破环细胞微环境平衡,损害氧化合成酶和脱氢酶,导致线粒体能量转化停止,线粒体通透性增加,Ca2+体内平衡被破坏,浓度升高,引起线粒体功能障碍[11-12]。线粒体是氧化还原的重要场所,线粒体的缺陷会加剧神经变性。大脑相比于人体其他组织的耗氧量更高,因此氧化应激损伤在脑衰老中作用更加凸显[13]。Nrf2是细胞抗氧化防御系统的关键蛋白,对神经元氧化损伤的保护起着至关重要的作用[14]。生理状况下,Nrf2与抗氧化反应元件相互作用,增强抗氧化酶的表达,调节下游靶基因HO-1的表达,发挥抗氧化作用。而氧化应激下氧化还原平衡被破坏,Nrf2/HO-1信号通路被抑制,导致氧自由基过度增加,引起炎症细胞浸润并导致NF-κB信号通路激活,导致IL-1β、IL-6与TNF-α等炎性介质过度释放。在氧化应激与炎性应激的综合作用下, Caspase凋亡通路激活,最终导致细胞凋亡[15]。同时,Aβ沉积会激活海马区小胶质细胞,释放大量炎症因子[16],进一步放大小胶质细胞炎症级联反应,与氧化应激损伤交织而最终导致细胞凋亡[17]。给动物长期连续注射D-半乳糖会使细胞内半乳糖浓度增高,破坏并消耗机体抗氧化防御系统,加剧自由基脂质过氧化反应,导致脂褐质增多与器官功能减退,出现与自然衰老动物相似的生理生化改变,从而被广泛用于抗衰老药物的研究[18]。本研究表明,杞参益智方能够增加模型动物海马中SOD活力和GSH含量(P<0.05),降低MDA的表达(P<0.05),同时提升Nrf2与HO-1的表达(P<0.05,P<0.01),表现出显著的抗氧化作用。同时该方还能够抑制炎性因子IL-1β、IL-6与TNF-α的表达水平(P<0.05,P<0.01),下调炎性通路关键蛋白p-NF-κB表达与p-NF-κB/NF-κB比值(P<0.05),并减少模型动物海马区细胞凋亡(P<0.01),抑制凋亡通路关键蛋白Caspase-3与Cleaved Caspase-3表达(P<0.05),体现了中药复方多层次、多靶点与多通路调控的综合治疗优势。
杞参益智方是在中医“助气固精,保镇丹田”的经典方剂二精丸基础上加味而成。二精丸中黄精与枸杞子均为中医益精填髓、滋补肝肾之要药,与中医理论中AD疾病肾精亏虚、髓海失养的基本病机高度吻合。但肾精需得元气资助,方能濡养脏腑。人参大补元气,不仅使气血生化有源,还可推动气血上荣于脑。黄精质滋黏腻,易助湿滞气,年老之人本就脾肾功能渐衰,久服有碍脾之嫌,故辅以益智仁温肾以助肾阳,暖脾以滋脾运,又取其芳香之气,补而不滞。四药相合,使肾精得充,气血可化,神志可复。该方四味药均为药食同源的药材,安全性好,有利于长期用药。
杞参益智方中的4味药及其活性成分均有改善痴呆模型动物学习与记忆能力的现代报道。枸杞多糖可以改善APP/PS1小鼠海马区淀粉样蛋白沉积,改善小鼠受损突触的可塑性,并促进海马神经新生[19]。黄精中薯蓣皂苷元能够显著改善痴呆大鼠的空间学习记忆能力,降低氧化应激与炎症应激水平,保护神经元免受损伤并抑制乙酰胆碱酯酶活性[20]。人参所含的多种人参皂苷Rb1、Rg1、Re等也可通过改善模型小鼠体内氧化应激水平,降低ROS的表达,上调Nrf2/GPX-1/ERK/CREB信号通路,改善模型小鼠神经损伤[21-24]。益智仁不同极性提取物能够调节痴呆动物胆碱能系统,改善其学习与记忆能力[25]。因此杞参益智方改善痴呆模型可能是方中各成分共同作用的结果。
本研究初步评价了杞参益智方改善衰老模型动物学习与记忆能力的效用,后续我们将深入研究方中发挥作用的主要活性成分,并对其作用机制进行进一步深入研究,以期为将该方防治老年期痴呆产品开发提供更多的现代科学依据。
