神经肌肉电刺激联合口腔感觉训练对重症病毒性脑炎合并吞咽障碍患儿的康复效果
2024-03-14马贵林孙素真王泽熙
马贵林 孙素真 王泽熙
河北省儿童医院,河北 石家庄 050031
重症病毒性脑炎(severe viral encephalitis,SVE)是因各种病毒感染引发的弥漫性的脑实质性炎症,好发于幼儿和儿童,具有发病急、预后差的特征[1-5]。SVE 患儿除了发热、呕吐、头痛、抽搐、颅内压升高等常见症状外,还具有频繁的惊厥或持续性惊厥、程度不一的意识障碍、吞咽障碍等表现,如不能进行及时、有效治疗,甚至发生颅脑神经损伤、脑疝、肢体瘫痪、呼吸循环衰竭引发死亡[6-9]。研究证实,SVE的病死率高达30%,而30%~50%的SVE 患儿遗留神经相关后遗症,如智力障碍、意识障碍、吞咽障碍、肢体瘫痪等[10-13]。目前,临床治疗SVE 患儿并无特效方案,以去高热、降颅内压、控制惊厥、保护脑神经等对症治疗为主。吞咽障碍是SVE 患儿常见并发症,主要表现为饮水呛咳、流涎、进食困难、发音障碍等,如不能得到有效控制,患儿可能发生误吸、营养不良、吸入性肺炎、窒息等,威胁患儿的生命健康[14]。因此,针对SVE 合并吞咽障碍患儿,采用有效的康复治疗措施治疗吞咽障碍,对促进SVE 患儿康复至关重要。口腔感觉训练可通过触觉、运动、本体感觉刺激,改善口腔器官的感知和运动功能,用于吞咽障碍患者的康复治疗具有一定的疗效,但对神经功能改善有限[15]。神 经 肌 肉 电 刺 激(neuromuscular electrical stimulation,NMES)可通过刺激吞咽肌群和吞咽功能神经使口腔、喉部等肌肉和神经处于兴奋状态,促进口腔和喉部神经功能的恢复[16]。基于此,本研究选取河北省儿童医院2021-01—2023-03 收治的108 例SVE合并吞咽障碍患儿,探讨NMES联合口腔感觉训练的康复效果。
1 资料与方法
1.1 临床资料选择河北省儿童医院2021-01—2023-03 收治的SVE 合并吞咽障碍患儿108 例。随机数字表法分为口腔感觉训练组和NMES 联合组各54 例。口腔感觉训练组男31 例,女23 例;年龄1~14(7.31±2.64)岁;病程1~9(4.67±2.13)d。NMES 联合组男34 例,女20 例;年龄1~12(7.22±2.74)岁;病程1~10(4.72±2.17)d。2 组患者一般资料具有均衡可比性(P>0.05)。本研究通过河北省儿童医院医学伦理会的审批。
纳入标准:均符合SVE 相关诊断标准,且经脑脊液、脑电图、脑部MRI 检查确诊;洼田饮水试验证实具有吞咽功能障碍,且吞咽功能障碍分级:Ⅲ~Ⅳ级;患儿家属同意本研究康复方案。排除标准:伴发有癫痫病变;合并细菌、真菌、结核杆菌等引发的神经相关感染病变;伴发先天性脑病或其他脑部损伤性病变;伴发咽喉畸形;伴发智力障碍。
1.2 方法2 组患者均给予以抗病毒、降颅内压、去高热、控制惊厥、保护脑神经等对症支持治疗。在此基础上,口腔感觉训练组给予口腔感觉运动训练。(1)冰刺激:用蘸冰水的棉棒反复摩擦刺激软腭部、腭舌弓、咽部及咽后壁,4~5 次/d,如患儿发生呕吐,需及时终止;(2)味觉刺激:将蘸有酸、甜、苦、辣不同味道液体的棉棒置于舌部对应味蕾的敏感区,反复进行刺激,4~5 s/次,间歇30 s 左右进行下一个味道的刺激,3 次/d;(3)K 点刺激:K 点在磨牙后三角,即腭舌弓与翼突的下颌帆中央的凹陷区域,对K 点进行刺激可促进患儿进行吞咽反射;(4)口面部震动性刺激:采用振动棒震动口腔的内颊部、舌及面部。(5)气脉冲感觉性刺激:气囊连接导气管,将导气管置于患儿的前咽弓、舌根、咽后壁,按压气囊,对口咽部进行气脉冲刺激;(6)吞咽器官运动训练:指导患儿进行噘嘴、鼓腮、闭唇、咂舌、移动上下颌、舌外伸等运动,10 min/次,3 次/d。(7)摄食训练:患儿置于30°~60°的仰卧姿势,头稍微前屈,用勺子喂流质或软滑的半流质食物。小勺置于患儿舌根,避免误吸,每勺吞咽后,再进行空咽2~3 次。喂食遵循少量多次、循序渐进的原则。共训练4周。
NMES联合组在口腔感觉训练基础上进行NMES康复治疗。采用吞咽神经肌肉电刺激仪(生产厂家:河北好博医疗器械有限公司,苏械注准:20172260252,型号:HB62BE)。选择双通道模式,口部吞咽障碍,2个电极分别贴在舌骨的上方及面瘫侧颊部;咽部吞咽障碍,将2个电极分别贴在舌骨的上方及甲状软骨的切迹处;食管吞咽障碍,2个电极贴在正中线垂直的位置。设定仪器参数,输出脉冲频率设置为50~100 Hz,双向方波,脉冲宽度设置为100~300 μs,持续时间≥1 s,主电机输出电流为0~25 mA。脉冲刺激强度从0 开始,缓慢增加,以肌肉出现收缩及患儿可耐受为宜。电刺激治疗过程中,引导患儿做吞咽动作,20 min/次,1 次/d,5 次/周,共治疗4 周。2 组患儿康复治疗4周后,评估康复效果。
1.3 观察指标
1.3.1 康复效果:康复治疗4 周后,采用洼田饮水试验[17]评估患儿的康复效果。患儿端坐或30°的仰卧位喝30 mL 温开水,观察饮水情况及呛咳发生情况,进行吞咽功能分级。Ⅰ级:可一次性喝完,且无呛咳发生;Ⅱ级:可分2次喝完,且无呛咳发生;Ⅲ级:可一次性喝完,但有呛咳情况发生;Ⅳ级:需2次以上才能喝完,且有呛咳发生;Ⅴ级:呛咳频繁,且难以喝完。治愈:吞咽功能障碍消失,洼田饮水试验显示为Ⅰ级;有效:吞咽功能障碍改善明显,洼田饮水试验显示为Ⅱ级;无效:吞咽功能障碍改善不明显,洼田饮水试验显示依然在Ⅲ级及以上。康复总有效率为治愈率与有效率之和。
1.3.2 吞咽功能:康复治疗前及治疗4周后,采用吞咽障碍调查量表(dysphagia disorders survey,DDS)[11]评估患儿的吞咽功能。DDS量表共包含15个条目,口腔期:0~15分,咽期:0~6分,食管期:0~3分,分值与吞咽障碍严重程度呈正比。
1.3.3 神经功能指标:康复治疗前及治疗4 周后,采集患者空腹静脉血5 mL,2 500 r/min 离心10 min(离心半径为8 cm),收集上层血清。采用ELISA 法检测患儿血清脑源性的神经营养因子(BDNF)及神经元特异性的烯醇化酶(NSE)水平。
1.3.4 营养状况:康复治疗前及治疗4 周后,采用主观的综合性营养评分量表(subjective global assessment,SGA)[12]评估患儿的营养状况。SGA 量表包括体质量变化、饮食变化、活动能力、胃肠道不适症状、疾病影响、肌肉消耗、皮下脂肪消耗等项目。分为重度营养不良(1~2 分)、轻中度营养不良(3~5分)、营养良好(6~7 分)3 个等级,得分与营养状态呈正比。
1.3.5 生活质量:康复治疗前及治疗4 周后,采用吞咽障碍特异性生存质量量表(swallowing quality of life,SWAL-QOL)评估患儿的生活质量。SWAL-QOL量表包括食物选择、食欲、进食时间、患者负担、症状发生的频率、心理健康状况、交流、恐惧、社交、劳累、睡眠等共44个条目,每条目1~5分,总分44~220分,分值与生活质量呈正比。
1.4 统计学方法采用SPSS 26.0软件统计数据,计量资料以均数±标准差(x±s)描述,行t检验;计数资料以率(%)描述,行χ2检验。P<0.05 为差异有统计学意义。
2 结果
2.1 2 组患者康复效果比较康复治疗4 周后,NMES联合组康复总有效率为92.59%(50/54),明显高于口腔感觉训练组的72.22%(39/54)(P<0.05),见表1。

表1 2组患者康复总有效率比较 [n(%)]Table 1 Comparison of total rehabilitation efficiency between two groups [n(%)]
2.2 2 组患者吞咽功能比较康复治疗前,2 组患者口腔期、咽期、食管期DDS 评分比较,差异无统计学意义(P>0.05);康复治疗4周后,2组患者口腔期、咽期、食管期DDS 评分均明显降低,但NMES 联合组各期DDS 评分降低幅度大于口腔感觉训练组(P<0.05),见表2。
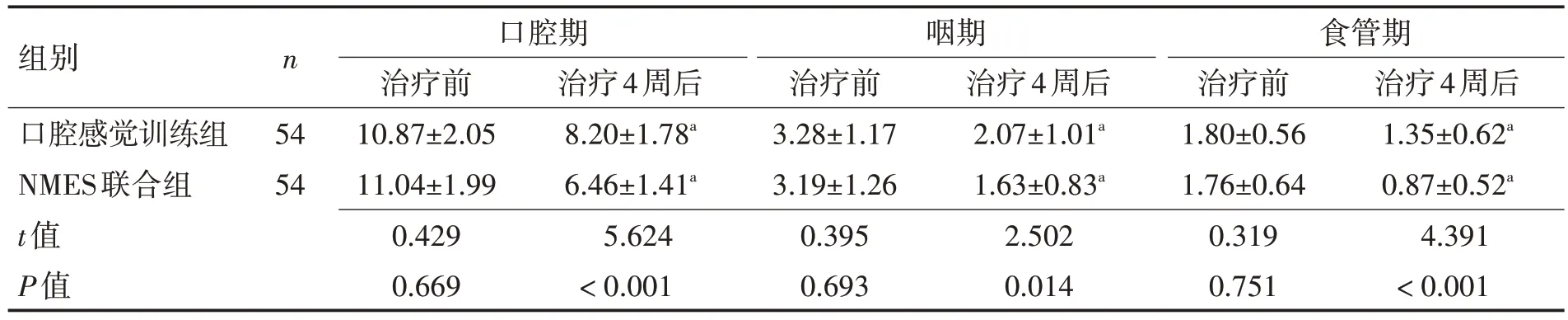
表2 2组患者吞咽功能DDS评分比较 (分,x±s)Table 2 Comparison of swallowing function DDS scores between two groups (points,x±s)
2.3 2 组患者神经功能指标比较康复治疗前,2 组患者血清BDNF、NSE 水平比较,差异无统计学意义(P>0.05);康复治疗4 周后,2 组患者血清BDNF 水平明显升高,血清NSE 水平明显降低,且NMES 联合组血清BDNF水平高于口腔感觉训练组,血清NSE水平低于口腔感觉训练组(P<0.05),见表3。
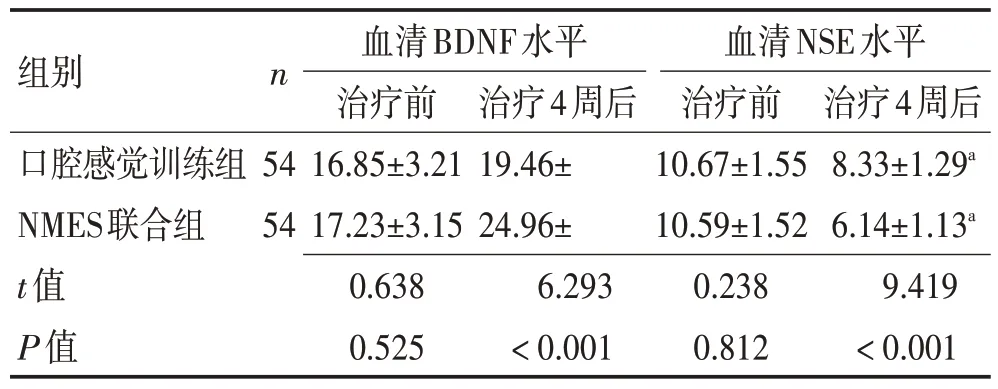
表3 2组患者血清BDNF、NSE水平比较 (μg/L,x±s)Table 3 Comparison of serum BDNF and NSE levels between two groups (μg/L,x±s)
2.4 2 组患者营养状况和生活质量比较康复治疗前,2组患者SGA 评分、SWAL-QOL 评分比较,差异无统计学意义(P>0.05);康复治疗4 周后,2 组患者SGA评分、SWAL-QOL评分均明显升高且NMES联合组SGA 评分、SWAL-QOL 评分明显高于口腔感觉训练组(P<0.05),见表4。
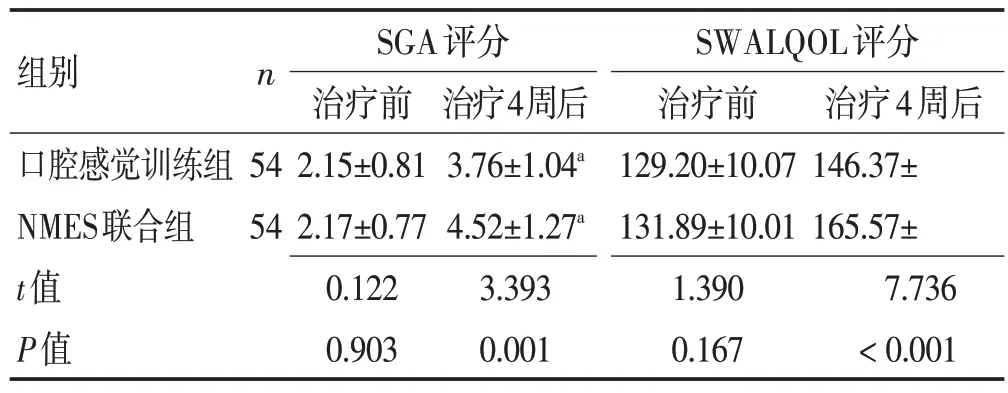
表4 2组患者SGA评分、SWAL-QOL评分比较 (分,x±s)Table 4 Comparison of SGA scores and SWAL-QOL scores between two groups(points,x±s)
3 讨论
SVE 是一种累及机体中枢神经系统的感染性病变,儿童的免疫系统及血脑屏障尚未完全发育成熟,因此,该病在儿童中发病率较高[18-19]。SVE 发病后,病毒可直接损伤患儿的脑神经,更能引发脑组织的异常代谢、缺氧缺血,进一步引发炎性应激反应,加重脑神经细胞的损伤,导致患儿预后较差,可能遗留神经相关后遗症。吞咽障碍是其常见的神经相关后遗症,而吞咽障碍不仅会导致患儿营养不良,更可能引发反复性的呼吸道感染,甚至发生窒息[20-24]。因此,对并发吞咽障碍的SVE 患儿,在积极进行对症治疗的同时,采取有效的方案针对吞咽障碍进行康复治疗对患儿的预后至关重要[25-32]。
本研究将NMES 联合口腔感觉训练用于SVE 合并吞咽障碍患儿的康复治疗中,结果显示,康复治疗4周后,NMES联合组康复总有效率、口腔期、咽期、食管期DDS 评分、血清BDNF 水平明显高于口腔感觉训练组,血清NSE 水平低于口腔感觉训练组,表明NMES 联合口腔感觉训练可有效提升SVE 合并吞咽障碍患儿的康复效果,进一步改善吞咽功能和神经功能。NMES 联合口腔感觉训练可提升患者的吞咽功能,改善营养不良状况。随着SVE 病情进展,血清BDNF、NGF 水平均能有效反映机体脑神经功能损伤的程度。口腔感觉训练作为一种吞咽障碍康复方法,可通过冰刺激、味觉刺激、K 点刺激、口面部震动性刺激、气脉冲感觉性刺激、吞咽器官运动训练、摄食训练等方法增强吞咽相关肌群的功能,虽然对改善吞咽功能有一定作用,但对神经功能的改善较小,且训练周期较长,患儿康复训练依从性降低,影响整体康复效果[33-34]。本研究采取的NMES 康复治疗,是通过电刺激吞咽功能相关的神经和肌肉,使细胞动作电位发生去极化,激活瘫痪的肌群,使其重新进行收缩,达到控制吞咽运动的效果。电刺激的过程中,低频脉冲电流可提高神经和肌肉的兴奋性,提升颌舌骨肌的肌力,使肌肉重新进行收缩,还可效刺激大脑组织中的高级运动中枢,提升脑部神经元的活性,调控咽部神经,创建新的反射弧,使中枢到咽喉运动的神经通路得以恢复,进而提升患儿的吞咽控制能力,改善吞咽功能和神经功能[35]。在口腔感觉训练的基础上进行NMES康复治疗起到携协同增效的作用,可以进一步提升康复效果,改善吞咽功能和神经功能。
本研究还证实,康复治疗4 周后,2 组患者SGA评分、SWAL-QOL 评分均明显升高,且NMES 联合组SGA 评分、SWAL-QOL 评分明显高于口腔感觉训练组,表明NMES 联合口腔感觉训练可有效改善SVE合并吞咽障碍患儿的营养不良状况[36]。在口腔感觉训练基础上进行NMES 康复治疗,在舌骨的上方、面瘫侧颊部、甲状软骨的切迹处放置电极贴片,通过电刺激舌咽、喉返及舌下神经和肌肉,可增强颏舌骨肌、下颌骨肌的肌力,促进吞咽相关受损神经元的恢复,通过胸骨舌骨肌、甲状舌骨肌的电流传递,增强控制吞咽功能的肌肉控制力量,改善吞咽功能,患儿可更好地进食,从而改善营养不良状况,提升患儿生活质量[37]。
NMES 联合口腔感觉训练用于SVE 合并吞咽障碍患儿康复治疗,可有效提升SVE 合并吞咽障碍患儿的康复效果,进一步改善吞咽功能和神经功能,改善患儿的营养不良状况,提升患儿生活质量。
