氟诺哌齐对新西兰家兔胚胎-胎仔发育毒性及毒代动力学
2024-03-07毛闪闪李芳蔡桂红朱云凯许旭崔艳君周文曹敏周莉
毛闪闪,李芳,蔡桂红,朱云凯,许旭,崔艳君,周文,曹敏,周莉
(1.湖北天勤生物科技股份有限公司武汉分公司,湖北武汉 430075;2.江苏康缘药业股份有限公司,江苏连云港 222000;3.中药制药过程控制与智能制造技术全国重点实验室,江苏连云港 222000)
乙酰胆碱酯酶(acetylcholin esterase,AChE)抑制剂是临床上用于阿尔茨海默病(Alzheimer disease,AD)治疗的一线药物,氟诺哌齐(fronopezil)对AChE 具有选择性抑制活性,且具备高亲和力和慢解离动力学特征,比同类药物药效维持时间长;口服生物利用度高,组织分布广泛,脑组织内药物浓度高(为血浆药物浓度的4.4 倍);安全性良好,基因KCNH2(hERG)和遗传毒性测试均显示阴性,但相关生殖毒性的研究未见报道[1-3]。本研究采用新西兰家兔,根据国家食品药品监督管理局《药物生殖毒性研究技术指导原则》的要求[4-5],自胚胎着床至硬腭闭合期间,即妊娠第6~18 天(GD6-18)ig 给予不同剂量氟诺哌齐,观察其对妊娠新西兰家兔母体(孕兔)、胚胎和胎仔发育的影响,为母体孕期接触氟诺哌齐对胎儿造成的影响提供非临床试验数据,为其临床广泛应用提供理论依据。
1 材料与方法
1.1 药品、试剂和主要仪器
氟诺哌齐(类白色粉末)(批号190801),江苏康缘药业股份有限公司。ELISA 试剂盒,武汉伊莱瑞特生物科技股份有限公司;羟丙基甲基纤维素(批号D1908084),德国aladdin公司;聚乙二醇400(批号20190625),国药集团化学试剂有限公司;环磷酰胺(批号20191026),山东西亚化学工业有限公司。
LS220A分析天平,瑞士Precisa公司;AX1502ZH/E电子天平,奥豪斯仪器有限公司;imark 酶标仪,美国Bio-Rad 公司;TSQ Quantum Access Max 三重四极杆液质联用仪,美国Thermo 公司;色谱柱Ultimate XB-C18(2.1 mm×50 mm,5 μm),上海月旭科技股份有限公司。
1.2 动物
新西兰家兔,普通级,雌性140 只,雄性18 只,购自邳州市东方养殖有限公司,动物生产合格证号SCXK(苏)2017-0002。新西兰家兔饲养在湖北天勤生物科技有限公司安评中心普通级兔观察室,实验开始前检疫7 d,交配期饲养于1000 mm×700 mm×450 mm不锈钢兔交配笼内,交配前和交配成功后饲养于500 mm×700 mm×450 mm 连体不锈钢兔笼内,单笼饲养,自由饮水、摄食,温度18~26 ℃(日温差≤4 ℃),湿度40%~70%,每小时换气次数≥8次,工作照度≥200 Lux,动物照度100~200 Lux,每12 h明暗交替(光照时间7∶00-19∶00)。本试验所涉及的动物管理、使用和相关操作均经湖北天勤生物科技有限公司武汉分公司实验动物管理和使用委员会审核和批准。
1.3 实验分组和处理
挑选发情雌兔放入雄兔笼内,交配成功当天为GD0,根据孕兔妊娠顺序进行随机分组,分为溶媒对照(1%羟丙基甲基纤维素+1.5%聚乙二醇400水溶液)、环磷酰胺18 mg·kg-1及氟诺哌齐3.6,9.0 和22.5 mg·kg-1(相当于药效起效剂量的20,50 和125 倍)组。于GD6-18溶媒对照组和氟诺哌齐组分别ig 给药,每天1 次,连续13 d;于GD6-20环磷酰胺组ig给予环磷酰胺,每天1次,连续15 d。
1.4 观察指标[6-7]
1.4.1 孕兔
①一般状况:试验期间每天1~2 次观察动物的外观、行为活动及异常分娩等情况;②GD0,GD3,GD6,GD10,GD13,GD15,GD18,GD20,GD24和GD28测量体重,GD0-1,GD6-7,GD13-14,GD19-20和GD27-28测量摄食量;③GD28剖宫检查内脏,计数黄体数,称量子宫连胎重,称量胎盘重,检查活胎、死胎和吸收胎数,计算着床数;④GD5,GD18和GD28分别采集血样,离心提取血清,ELISA 检测血清中黄体生成素、卵泡刺激素、孕酮、雌二醇和睾酮水平。
1.4.2 胎仔
GD28①检查胎仔性别、重量、顶臀长和尾长;②检查胎仔外观、内脏和骨骼等[8-9]。
1.5 伴随毒代动力学
1.5.1 方法学建立
据前期委托方提供的毒代动力学检测方法和本实验室预试验中建立的检测方法,采用DC511267作为内标,建立氟诺哌齐的兔毒代动力学高效液相色谱串联质谱法,并进行方法学验证。色谱条件:Ultimate XB-C18 柱(2.1 mm×50 mm,5 μm),柱温40 ℃,流动相A 为0.1%甲酸水溶液,流动相B 为0.1%甲酸乙腈溶液,梯度洗脱程序为0.01~1.0 min,5%B~10%B;1.0~1.6 min,10%B~50%B;1.6~2.6 min,50%B;2.6~2.61 min,50%B~5%B;2.61~3.2 min,5%B。流速0.6 mL·min-1,进样体积2.0 μL。质谱条件:采用电喷雾电离源,正离子扫描,多反应监测模式,雾化气50 psi,辅助加热气60 psi,源温500 ℃,离子喷雾电压5000 V,去簇电压80 eV,氟诺哌齐检测离子对m/z416.2/138.1,碎裂电压16 kv;DC511267 检测离子对m/z422.1/402.2,碎裂电压22 kv。数据采集时间3.2 min。
1.5.2 毒代动力学
设氟诺哌齐3.6,9.0 和22.5 mg·kg-13 个剂量组[5]进行毒代动力学研究。首次(GD6)和末次(GD18)分别于给药前和给药后0.25,0.5,1,1.5,3,6,10 和24 h耳缘静脉采血约0.5 mL,置于预先加有肝素钠20 μL的抗凝管中,静置1~2 h后4 ℃3500×g离心10 min,取上层血浆样本置-80 ℃冻存待测。采用液质联用法分析血浆和组织中氟诺哌齐浓度,拟合得到达峰时间(Tmax)、血药峰浓度(Cmax)和药时曲线下面积(AUC0-t)。
1.5.3 组织药物浓度
GD18给药后采集氟诺哌齐各剂量组孕兔24 h血样后,GD19再次给药,在约达到血药浓度峰值时(约给药后1 h)处死孕兔,取孕兔血浆、羊水和胎盘,同时取胎仔组织,匀浆、离心、分装后置-80 ℃冻存待测。
1.6 统计学分析
2 结果
2.1 氟诺哌齐对孕兔妊娠期间一般状况的影响
由表1 可知,GD0-28期间ig 给药后,7 只孕兔流产(其中溶媒对照组1 只,环磷酰胺组5 只,氟诺哌齐3.6 mg·kg-1组1 只);4 只阴道出血(环磷酰胺组);其余动物活动正常,被毛浓密有光泽,眼睛鲜红而有精神,呼吸正常,鼻部无血性分泌物,与溶媒对照组相比无明显异常。
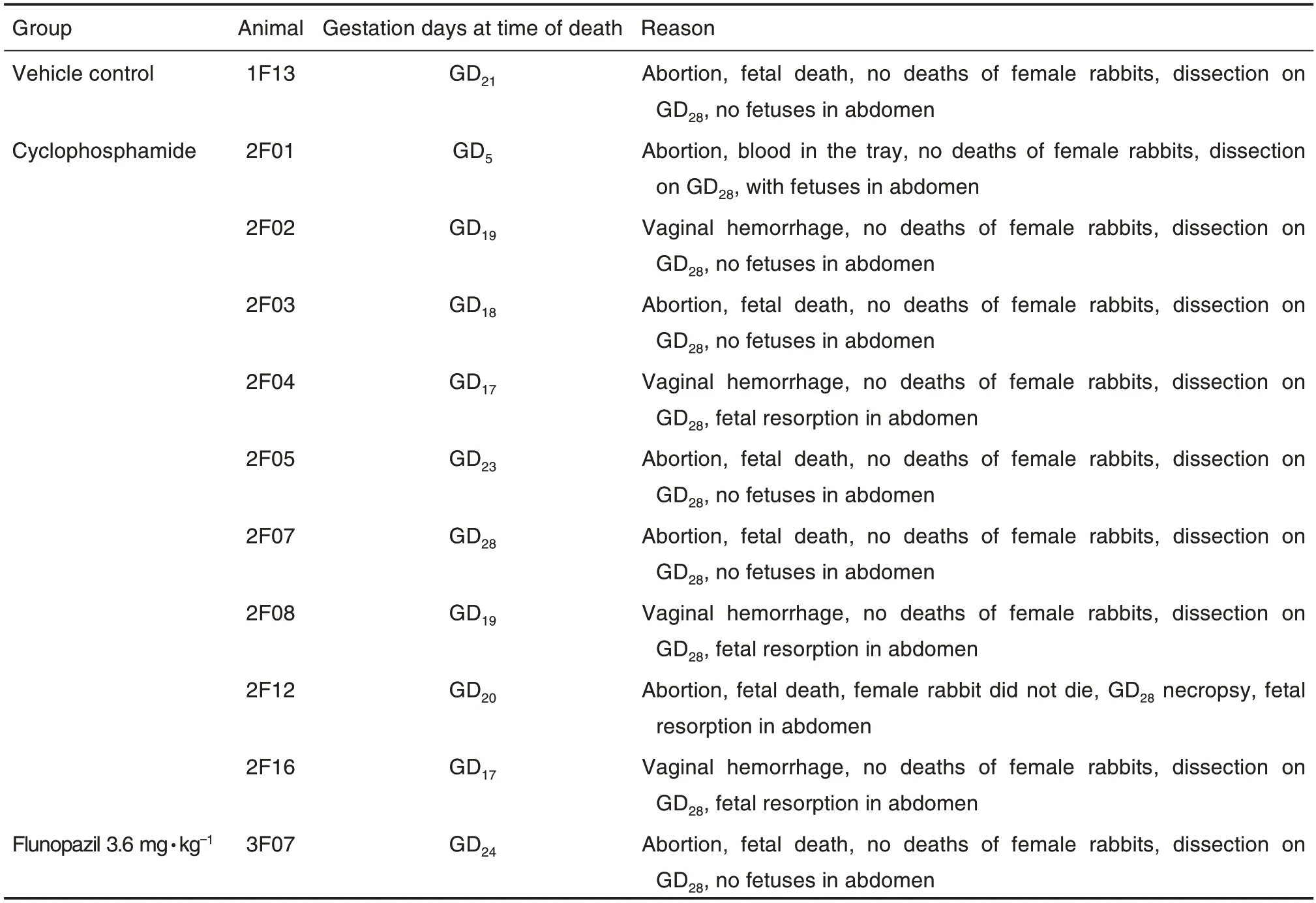
Tab.1 Abnormal signs and manifestations of animals after fronopezil ig administration in embryo-fetal developmental toxicity and concomitant toxicokinetic tests(phase Ⅱ)
2.2 氟诺哌齐对孕兔妊娠期间体重和宫外增重的影响
由图1 和图2 可知,与溶媒对照组比较,妊娠期间氟诺哌齐各剂量组体重和妊娠期宫外增重(GD28体重-GD6体重-子宫连胎重)均未见统计学差异。
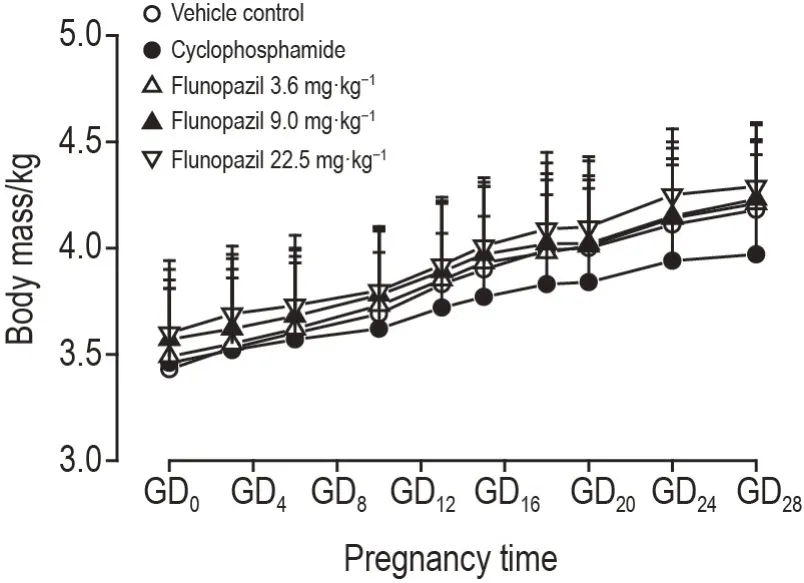
Fig.1 Effect of fronopezil ig administration on body mass of pregnant rabbits in embryo-fetal developmental toxicity and concomitant toxicokinetic tests(phaseⅡ).See Tab.1 for the rabbit treatment.±s,n=17(vehicle control,flunopazil 9 and 22.5 mg·kg-1 group),18(cyclophosphamide group),16(flunopazil 3.6 mg·kg-1 group).
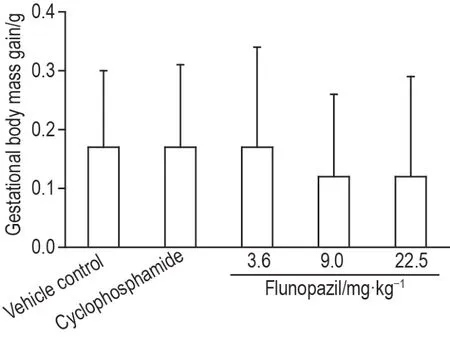
Fig.2 Effect of fronopezil ig administration on extrauterine body mass gain of pregnant rabbits in embryofetal developmental toxicity and concomitant toxicokinetic tests.See Tab.1 for the rabbit treatment.±s,n=17(vehicle control,flunopazil 9 and 22.5 mg·kg-1 group),18(cyclophosphamide group),16(flunopazil 3.6 mg·kg-1 group).
2.3 氟诺哌齐对孕兔妊娠期间摄食量的影响
由表2可知,与溶媒对照组比较,氟诺哌齐各剂量组摄食量均未见明显差异。
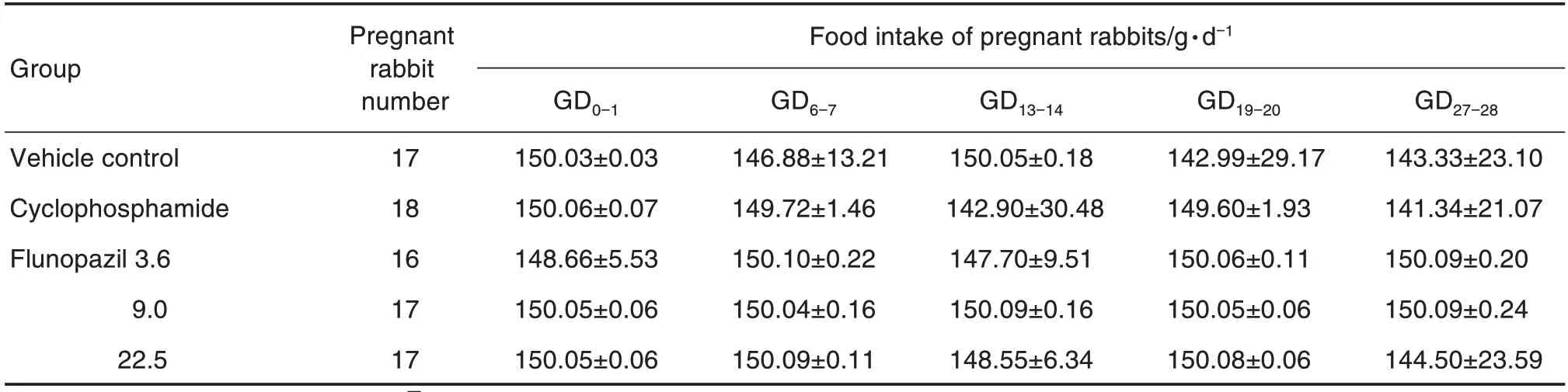
Tab.2 Effect of fronopezil ig administration on food consumption of female rabbits during pregnancy in rabbit embryo-fetal developmental toxicity and concomitant toxicokinetic tests(phaseⅡ)
2.4 氟诺哌齐对孕兔胚胎发育指标的影响
由表3 可知,所有组别大体解剖内脏未见明显异常;与溶媒对照组比较,氟诺哌齐各剂量组平均活胎数、平均黄体数、平均着床数、吸收胎率和死胎率均无明显差异;仅9.0 mg·kg-1组活胎率高于溶媒对照组(P<0.05);环磷酰胺组活胎率明显低于溶媒对照组(P<0.01),吸收胎率明显高于溶媒对照组(P<0.01)。
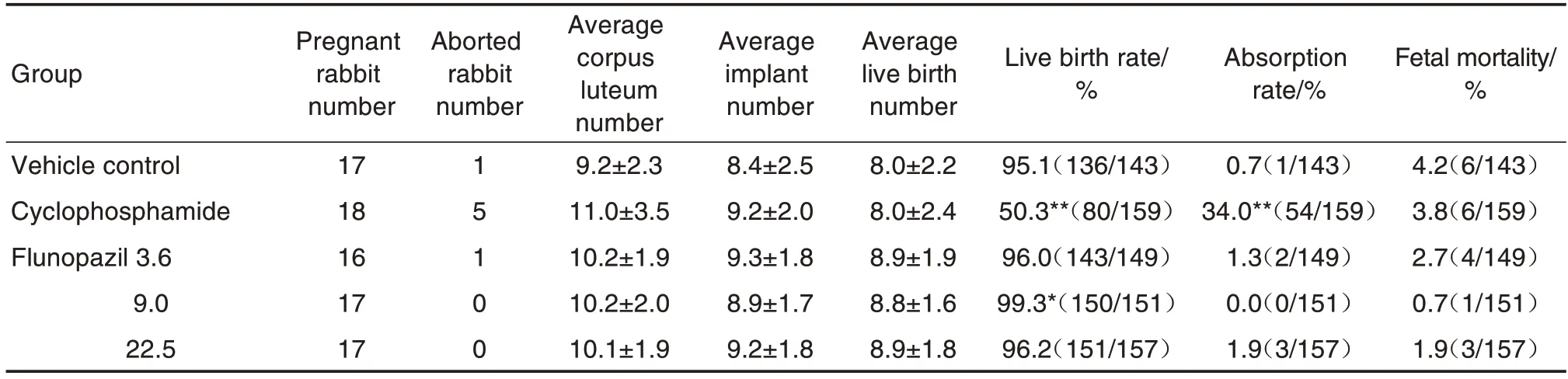
Tab.3 Effect of flunopazil on pregnancy outcomes in pregnant rabbits
2.5 氟诺哌齐对孕兔激素水平的影响
由表4 可知,与同期溶媒对照组比较,GD5,GD18和GD28氟诺哌齐各剂量组激素水平均未见明显差异。与GD5溶媒对照组比较,GD18溶媒对照组黄体生成素、卵泡刺激素和孕酮水平升高(P<0.01),环磷酰胺及氟诺哌齐3.6 和22.5 mg·kg-1组孕酮水平升高(P<0.05,P<0.01);GD28溶媒对照组黄体生成素和卵泡刺激素水平升高(P<0.01),环磷酰胺组孕酮和睾酮水平降低(P<0.05,P<0.01),氟诺哌齐3.6 mg·kg-1组雌二醇和孕酮水平降低(P<0.05,P<0.01),9.0 mg·kg-1组孕酮水平降低(P<0.01),22.5 mg·kg-1组卵泡刺激素水平升高(P<0.01),雌二醇水平降低(P<0.05)。

Tab.4 Effect of flunopazil on hormone levels in pregnant rabbits
2.6 氟诺哌齐对孕兔胎仔发育的影响
由表5可知,与溶媒对照组比较,氟诺哌齐各剂量组胎仔的窝平均体重、顶臀长、尾长和胎盘重量未见明显差异;环磷酰胺组胎仔体重、顶臀长和尾长均有不同程度降低(P<0.01)。
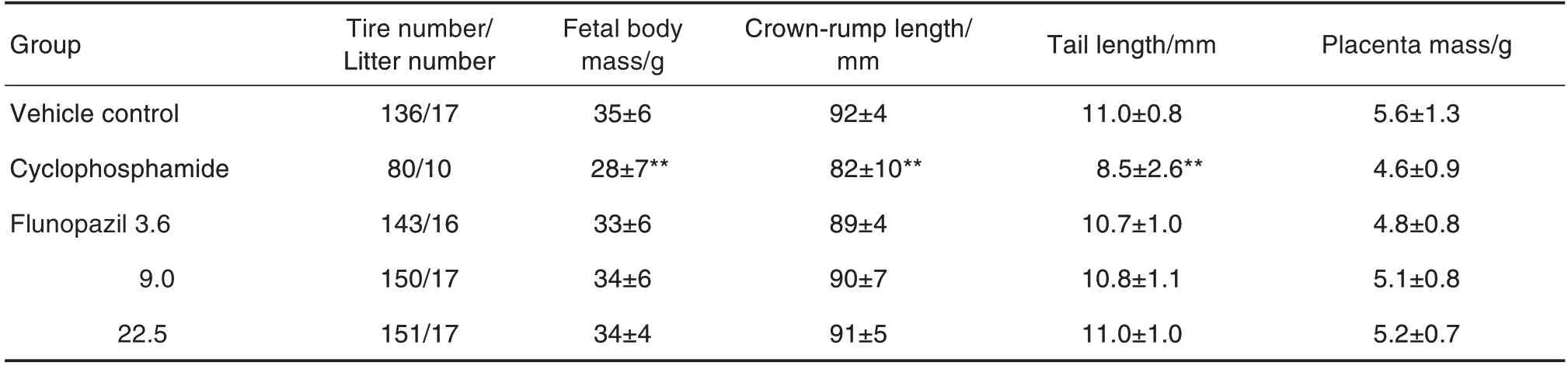
Tab.5 Effect of flunopazil on growth and development of fetal rabbits
由表6和图3(C 和E)可知,溶媒对照组和氟诺哌齐各剂量组共检查580 只胎仔外观和内脏,未见外观和内脏畸形胎仔。
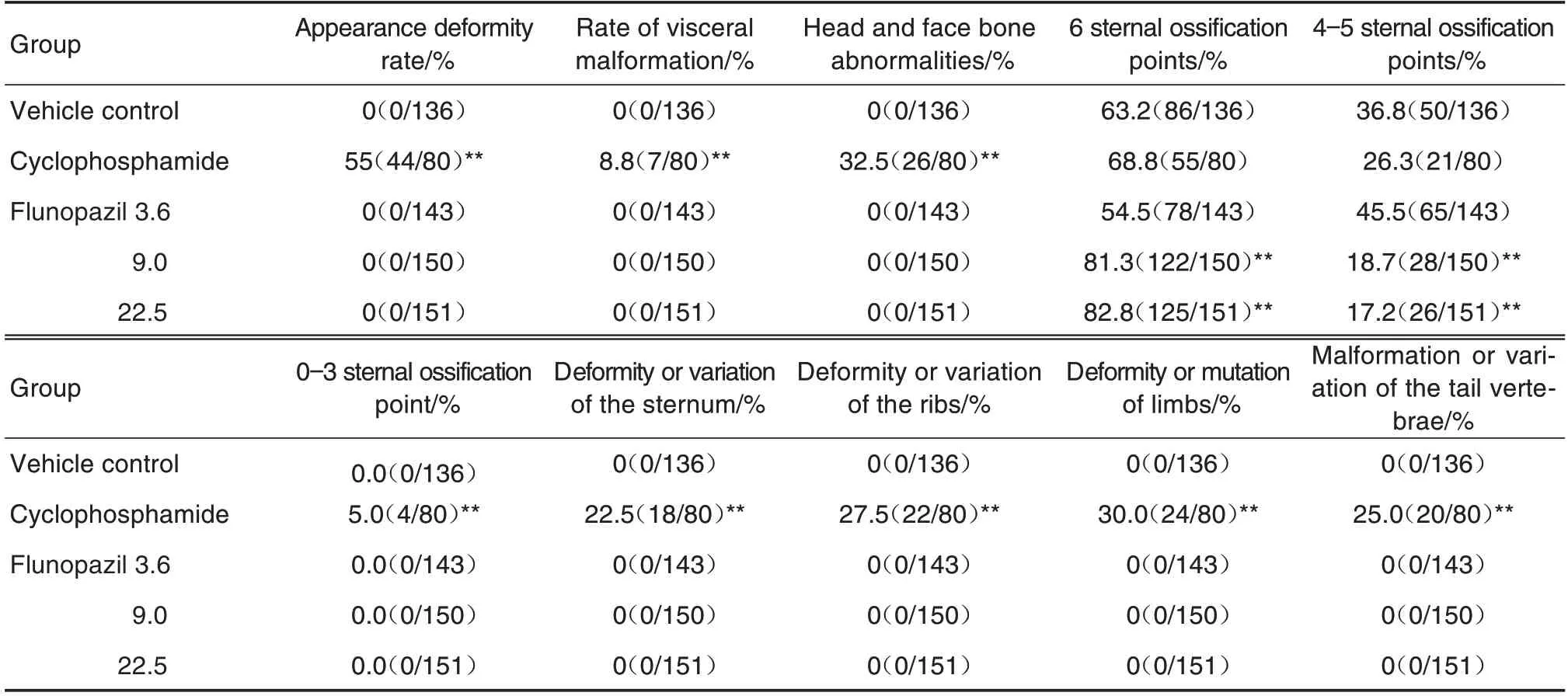
Tab.6 Effect of flunopazil on appearance,viscera and bone of fetal rabbits
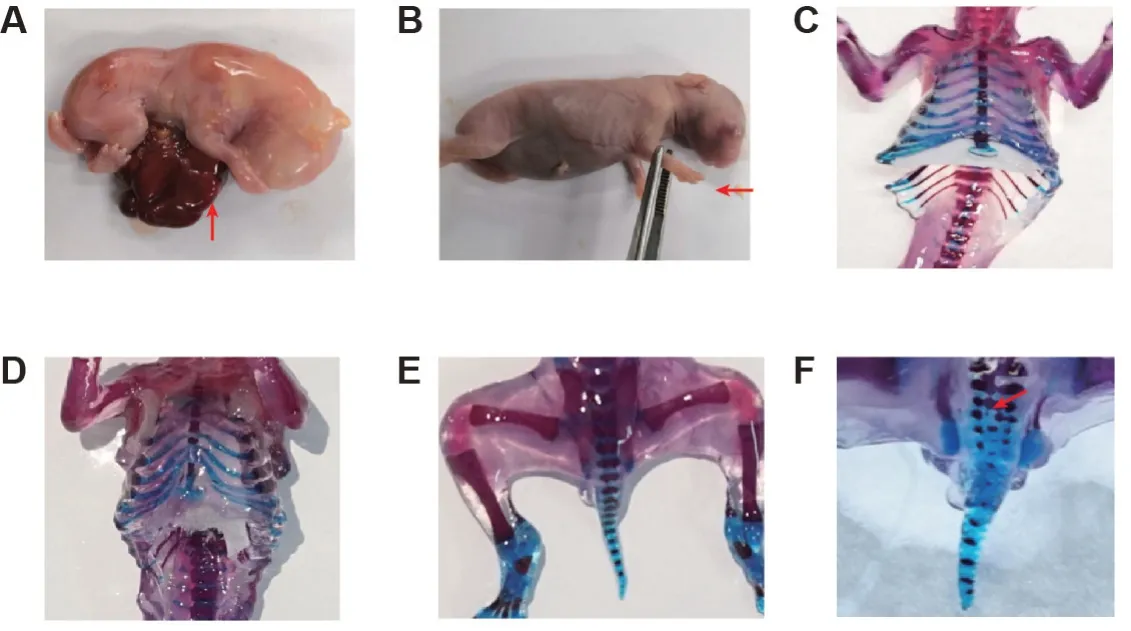
Fig.3 Effect of flunopzil on fetal appearance,viscera and bone in developmental toxicity of embryos and fetuses in rabbits(phase Ⅱ).See Tab.1 for the rabbit treatment.A:gastroschisis(arrow)in the 2F06 positive control group;B:fewer fingers(arrow)in the 2F06 positive control group;C:breastbone of normal fetus in 1F01 solvent control group;D:the fifth sternum is missing in the 2F10 positive control group;E:caudal vertebrae of normal fetus in 5F03 high-dose group;F:caudal ossification and caudal fusion in 2F10 positive control group(arrow).
由表6 和图3 可知,采用双染法对580 只胎仔进行骨骼染色,溶媒对照组和氟诺哌齐各剂量组未检查出头面部骨、肋骨、四肢、胸骨和尾椎的畸形或变异。与溶媒对照组比较,氟诺哌齐9.0和22.5 mg·kg-1胸骨骨化点为6 个的胎仔增多(P<0.01),胸骨骨化点为4~5 个的胎仔减少(P<0.01),各剂量组未见胸骨骨化点为0~3个的胎仔。
环磷酰胺组外观:主要表现为皮下出血35.0%(28/80)、口唇异常6.3%(5/80)、少指/趾26.3%(21/80)、足内翻20.0%(16/80)、短尾11.3%(9/80)、腹裂2.5%(2/80)、无眼1.3%(1/80)和卷尾15.0%(12/80),整体异常或畸形率(55.0%)明显高于溶媒对照组(P<0.01)。环磷酰胺组共检查10 窝80 只胎仔内脏,其中7 只(8.8%)胎仔内脏畸形,主要表现为肝叶增多、不规则、形状异常、肾盂扩张、肾皮质与髓质分界不清和心室扩张,与溶媒对照组相比具有统计学差异(P<0.01)。胸骨节骨化点为6 个、4~5 个和≤3 个的分别为55 只(68.8%)、21 只(26.3%)和4 只(5.0%),其中胸骨节为4~5 个胎仔数明显低于溶媒对照组(P<0.05),胸骨节骨化点<3的胎仔数和头面部骨异常率明显高于溶媒对照组(P<0.01)。环磷酰胺组畸形表现为胸骨融合、胸骨裂和胸骨骨化不全,肋骨融合和肋骨错位,尾椎融合、尾椎骨化不全和尾椎排列不齐,指(趾)缺失等,(表6及图3A,B,D和F)。
2.7 氟诺哌齐伴随毒动学
2.7.1 孕兔体内药动学
由图4 和表7 可知,孕兔首次、末次给药后,随着时间延长,氟诺哌齐血药浓度呈现逐渐增加趋势,达峰后,逐渐减少。AUC0-24h值与给药剂量呈线性关系(首次给药r=0.9957;末次给药r=0.9830),Cmax值均与给药剂量呈非线性关系。氟诺哌齐3.6,9.0,22.5 mg·kg-1末次给药Cmax值与首次比值分别为0.839,1.226 和1.128;AUC(0-24h),与首次的比值分别为0.963,0.993和0.813。
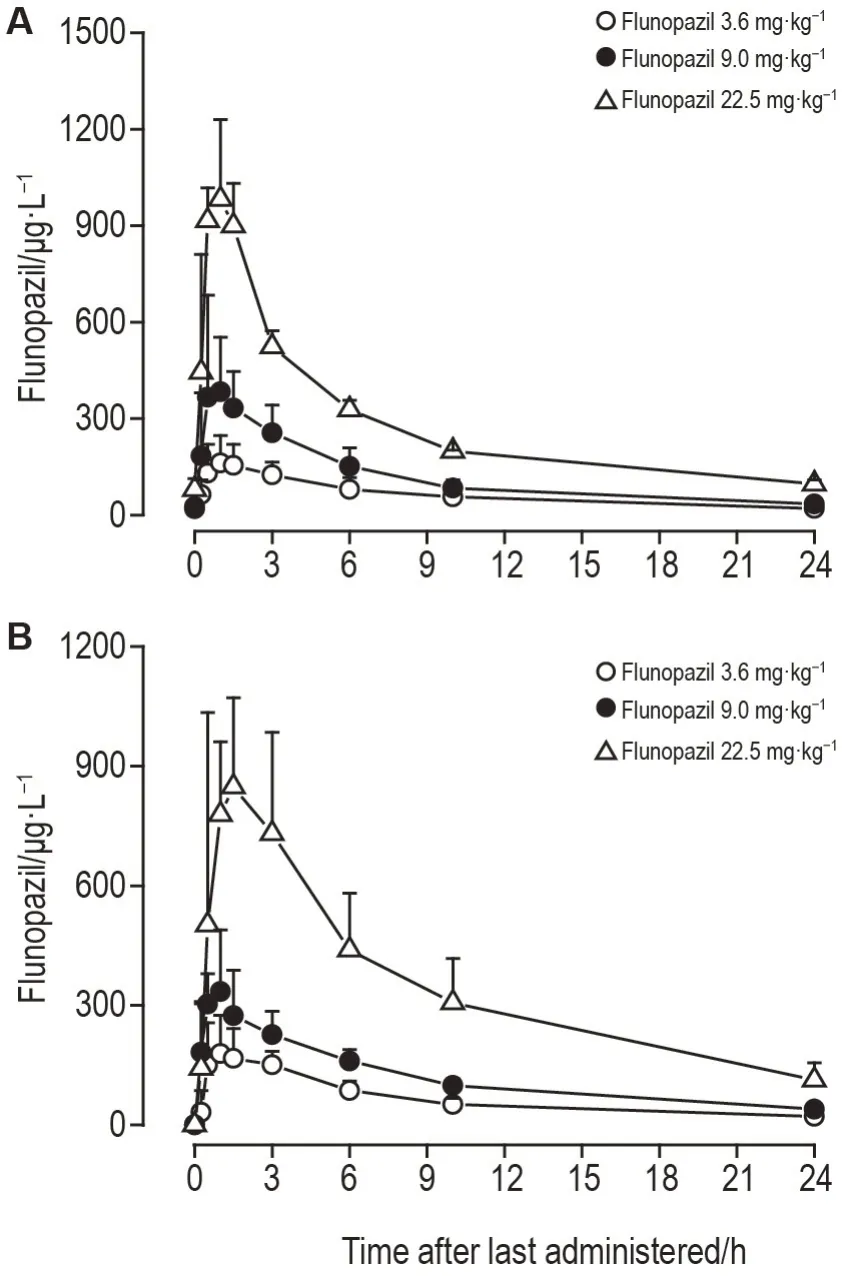
Fig.4 First(GD6,A)and last(GD18,B)blood concentration-time curve of flunopazil in pregnant rabbits after ig administration.See Tab.1 for the rabbit treatment.±s,n=7.
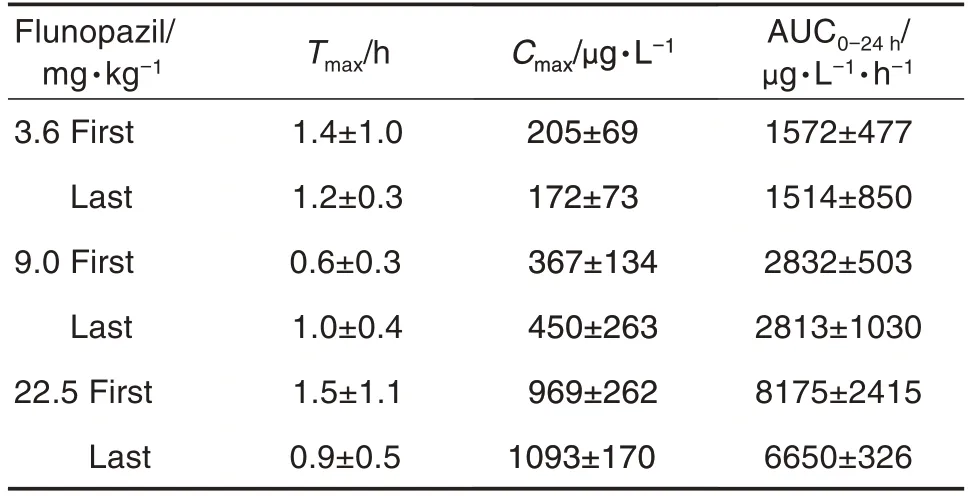
Tab.7 Concomitant toxicity kinetic parameters of flunopazil in pregrant rabbits
2.7.2 组织分布
由表8 可知,GD19给药后,采集1 h 孕兔血浆、羊水、胎仔和胎盘组织匀浆进行药物浓度检测,结果表明,氟诺哌齐3.6、9.0 和22.5 mg·kg-1组孕兔血浆药物浓度呈逐渐增加趋势,比值为1∶2.78∶10.74,羊水、胎仔和胎盘中药物浓度比值分别为1∶3.11∶8.37,1∶3.23∶6.35和1∶3.09∶8.79。
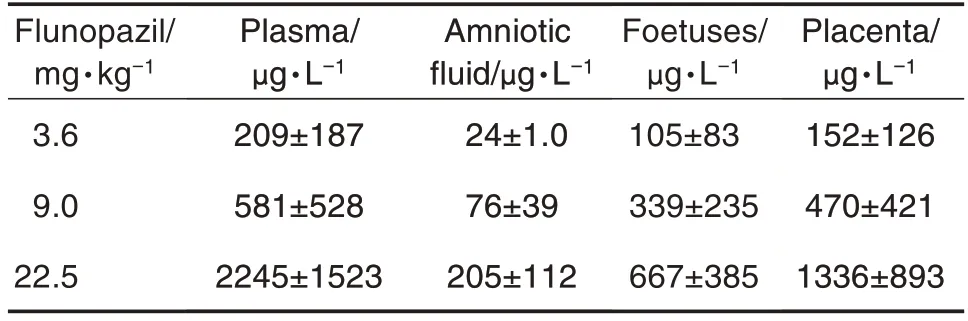
Tab.8 Tissue drug concentrations of flunomazil in pregnant rabbits after ig administration
3 讨论
本研究采用氟诺哌齐3 个剂量对妊娠期孕兔ig给药,各剂量组孕兔妊娠期各时间点的一般状况、体重、摄食量均未见明显差异,表明氟诺哌齐没有造成明显的母体毒性。据孕兔的妊娠结局,各剂量组胎仔的平均黄体数和平均着床数等均未见明显差异,表明氟诺哌齐对亲代的生殖能力未产生明显影响。氟诺哌齐各剂量组胎仔的窝均体重、顶臀长和尾长未见明显差异,表明未对胎仔的体格生长发育产生毒性作用。
氟诺哌齐各剂量组胎仔外观、内脏和骨骼检查均未见变异或畸形。为考察氟诺哌齐对孕兔激素是否有影响[10],本研究进行了激素水平检测。与GD5比较,溶媒对照组GD18和GD28黄体生成素、卵泡刺激素及GD18孕酮水平均升高。溶媒对照组给予的是含1%羟丙基甲基纤维素和1.5%聚乙二醇400的水溶液,二者均为普通药用辅料,故认为激素水平的改变与妊娠有一定关系;氟诺哌齐各剂量组卵泡和激素、孕酮和雌二醇水平有一定波动,变化范围均在溶媒对照组波动范围内或附近,与同期溶媒对照组比较无明显差异;且未发现对妊娠结局以及胚胎-胎仔发育产生影响。一定程度内的激素波动属于正常范围内的波动,但提示临床给予大剂量氟诺哌齐时,应注意监测激素水平的变化。
本研究根据文献[11]设计了环磷酰胺的剂量,试验中环磷酰胺组流产略多,考虑可能与阳性药的生产厂家、批号和动物的个体差异等有关。阳性对照环磷酰胺采用的是对妊娠期孕兔ig 给药,主要目的是为了验证试验系统,为生殖毒性试验阳性指标的判定提供依据。与溶媒对照组比较,环磷酰胺组孕兔妊娠期各时间点的体重、摄食量均未见明显差异,但流产数量较多,同时孕兔的活胎率降低,吸收胎率升高,表明环磷酰胺具有一定的胚胎毒性;环磷酰胺组胎仔的窝均体重、顶臀长和尾长均低于溶媒对照组,其胎仔外观、内脏和骨骼畸形或变异均高于溶媒对照组,表明环磷酰胺对胎仔的体格生长发育产生明显影响,并具致畸作用。据报道,新西兰家兔(GD6-20)ig 给予环磷酰胺18 mg·kg-1,胎仔外观检查发现口唇异常、缺指和眼球缺失等[12],与本研究结果一致。
伴随毒代动力学结果表明,孕兔在3.6~22.5 mg·kg-1剂量范围内ig 给予氟诺哌齐后,首次给药(GD6)和末次给药(GD18)平均Cmax和AUC(0-24h)随剂量增加而增大;与GD6比较,GD18的平均Cmax和AUC(0-24h)均无明显增加;3.6,9.0和22.5 mg·kg-1蓄积因子〔AUC(0-24h)末次/首次比值〕约为1,认为受试物在孕兔体内无明显蓄积;孕兔血药浓度、羊水、胎仔和胎盘中药物浓度均随剂量增加呈现逐渐增加趋势,羊水中药物浓度在1∶3.11∶8.37 之间,胎仔和胎盘在1∶3.23∶6.35和1∶3.09∶8.79之间,约等于剂量比1∶2.5∶6.25,表明受试物可透过胎盘屏障。结合胎仔的各项检查结果,认为氟诺哌齐不会对胚胎-胎仔发育产生明显影响。
在本试验条件下,ig 给予氟诺哌齐对孕兔妊娠期体重、体增重、摄食量、妊娠结局(平均黄体数、平均着床数、平均活胎数、活胎率和吸收胎率)以及胎仔外观、内脏和骨骼等均未引起明显变化;仅在GD18或GD28卵泡刺激素、雌二醇和孕酮水平有一定程度波动,提示临床给予大剂量氟诺哌齐时应注意监测激素水平的变化。伴随毒代动力学研究表明,氟诺哌齐可透过胎盘屏障,但在孕兔体内无明显蓄积。综上,氟诺哌齐对孕兔、胚胎-胎仔发育毒性的未见有害作用剂量为22.5 mg·kg-1,为药效起效剂量的125倍。
