载药栓塞微球TACE 联合阿帕替尼及卡瑞利珠单抗治疗巨块型肝细胞癌
2024-02-28陈金威任建庄段旭华陈鹏飞朱兴书
陈金威,任建庄,段旭华,陈鹏飞,朱兴书
(郑州大学第一附属医院放射介入科,河南 郑州 450052)
原发性肝细胞癌(hepatocellular carcinoma, HCC)是常见恶性肿瘤,死亡率居全球第3 位[1]。巨块型HCC 指直径≥10 cm 的HCC,具有形态不规则、常伴大血管侵袭及肝内转移等特征,多数患者确诊时已失去手术机会[1]。TACE 是治疗不可手术切除HCC 的主要方法,但可导致热休克蛋白70(heat shock protein 70, HSP70)、缺氧诱导因子-1α(hypoxia inducible factor-1α, HIF-1α)、程序性死亡受体-1(programmed cell death protein-1, PD-1)及血管内皮生长因子受体(vascular endothelial growth factor receptor, VEGF)表达增加而促进肿瘤复发和转移[2]。卡瑞利珠单抗与阿帕替尼联合治疗(简称双艾治疗)是晚期HCC 的一线标准治疗方案,客观反应率(objective response rate,ORR)为46%,患者1 年总生存期(overall survival,OS)率达75%[3];同时,已有研究[4]表明TACE 联合靶向药物及免疫治疗可提高中晚期HCC 的临床效益。本研究观察载药栓塞微球TACE(drug-eluting bead TACE, D-TACE)联合双艾治疗用于巨块型HCC 的价值。
1 资料与方法
1.1 研究对象 回顾性分析2018 年12 月—2020 年12 月35 例于郑州大学第一附属医院接受D-TACE 联合双艾治疗的巨块型HCC 患者,男29 例、女6 例,年龄36~70 岁、平均(55.3±9.2)岁;肿瘤直径10.10~20.90 cm、平均(13.24±2.50)cm。纳入标准:①非弥漫性HCC(病灶单发或2~3个),肿瘤直径之和≥10 cm,巴塞罗那分期(Barcelona clinic liver cancer, BCLC)B~C 期;②符合《原发性肝癌诊疗规范》(2022 年版)临床诊断标准,或经病理组织学/细胞学确诊为不可手术切除HCC,且无法接受姑息性手术或放射治疗,并至少有1 个可测量病灶;③治疗前1 周内美国东部肿瘤协作组织体力状态(Eastern Cooperative Oncology Group performance status, ECOG PS)评分0~1;④HCC 占全肝体积的60%以下,患者预期寿命>3 个月;⑤无严重合并症,如高血压、冠心病和精神病,无严重过敏史;⑥肝功能Child-Pugh 分级A~B,肾功能正常,凝血功能正常或经治疗后正常;⑦患者接受随访,并签署知情同意书。排除标准:①门静脉主干癌栓占管腔≥50%;②肝胆管细胞癌、混合细胞癌、纤维板层细胞癌;③既往6 个月内有消化道出血史或有明确胃肠道出血倾向;④凝血功能异常/具有出血倾向/正接受溶栓或抗凝治疗;⑤全身器官衰竭。见表1。本研究经医院伦理委员会批准(2024-kY-0019)。
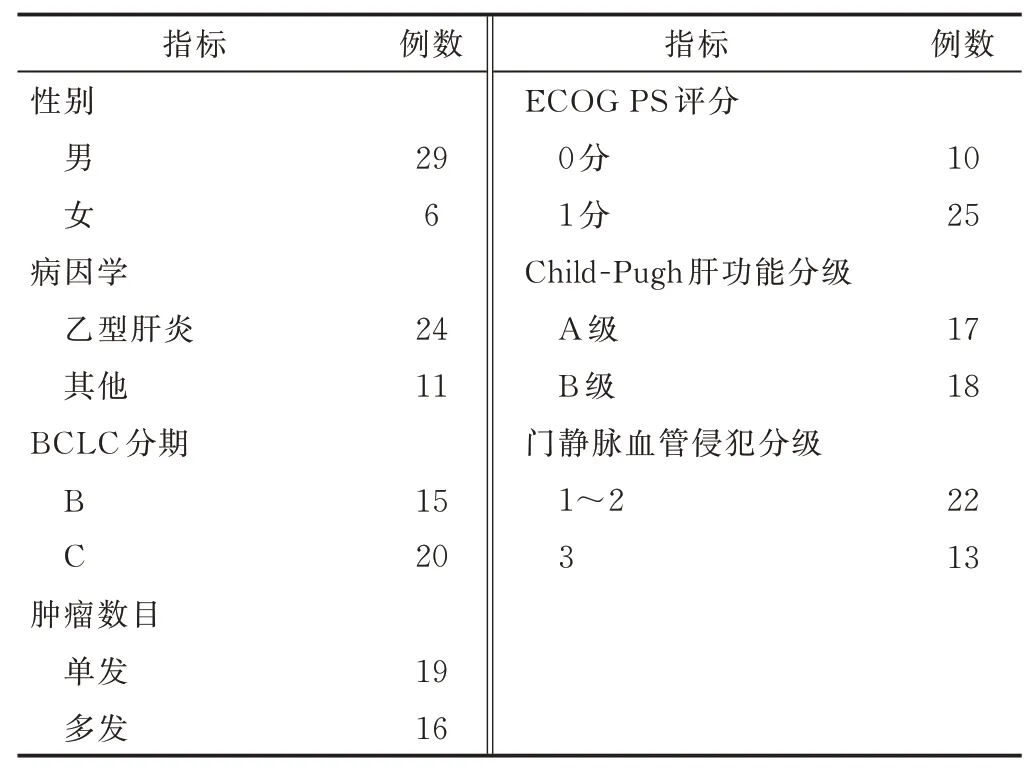
表1 35 例接受D-TACE 联合双艾治疗的巨块型HCC 患者一般资料
1.2 联合治疗
1.2.1 D-TACE 由2 名具有10 年以上介入经验的副主任医师完成。以GE Discovery IGS 740 数字减影血管造影(digital subtract angiography, DSA)机为引导设备。嘱患者仰卧,予腹股沟区常规消毒、铺巾,采用改良Seldinger 穿刺法穿刺股动脉,置入5F 血管鞘(Cordis,402-605X),引入5F 导管(Cook,RH)行肝总动脉造影,明确肿瘤位置及供血动脉;将2.4F 微导管(恒瑞,C24150ST-G18190AN)超选择至肿瘤供血动脉,灌注100 mg 奥沙利铂(艾恒,江苏恒瑞),之后注入聚乙烯醇栓塞微球(Callispheres,苏州恒瑞迦俐生生物医药科技,加载60 mg 吡柔比星)进行栓塞,以肿瘤供血动脉血流瘀滞、异常肿瘤染色基本消失为栓塞终点,必要时追加300~500 μm 空白栓塞微球或350~560 μm 明胶海绵。见图1。
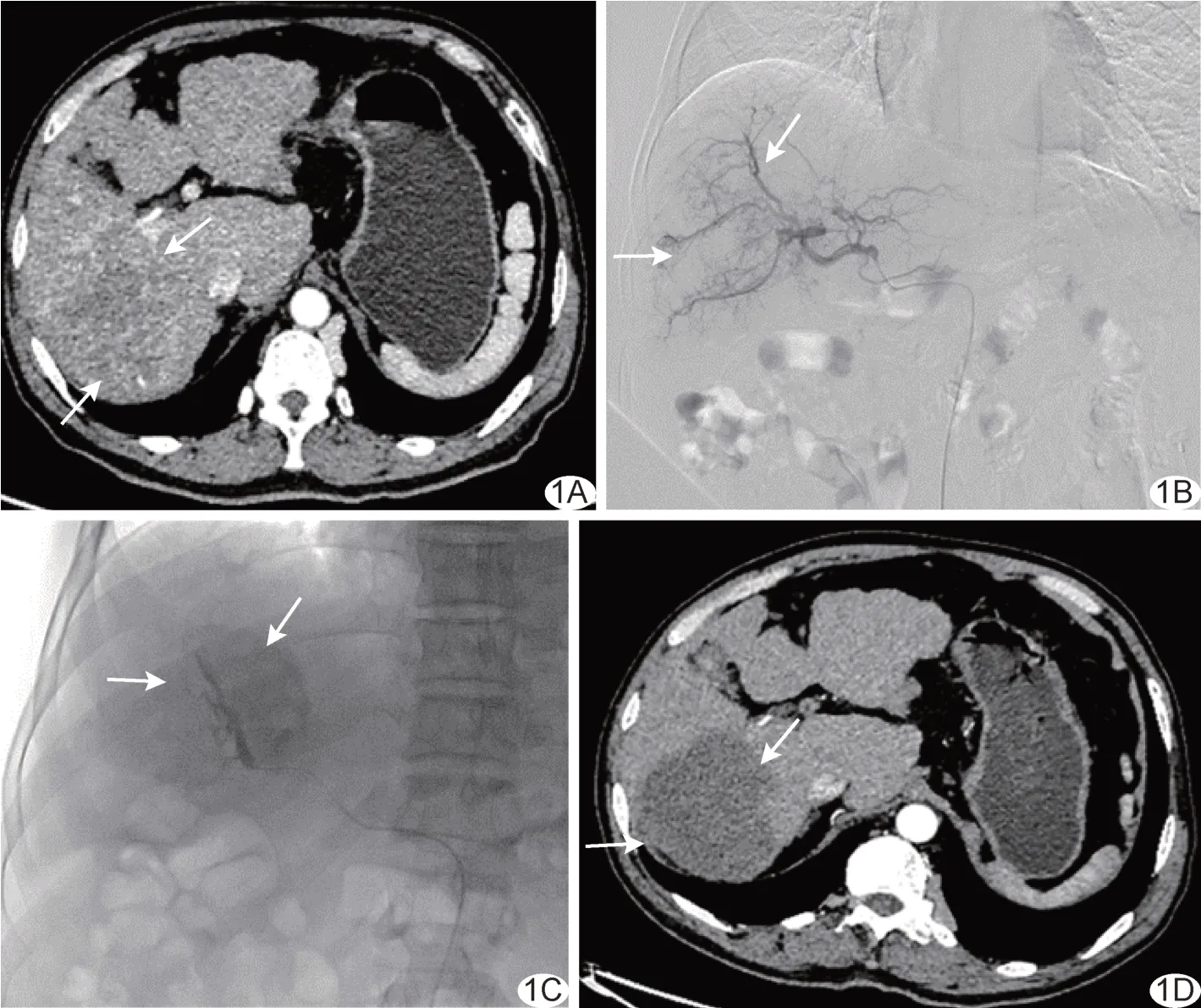
图1 患者男,63 岁,巨块型HCC A.治疗前腹部增强CT 图示肝右叶巨大占位,可见不均匀强化;B.DSA 图示肿瘤染色; C.以Callispheres 载药微球栓塞后,肿瘤染色基本消失; D.联合治疗4 周后增强CT 图示肿瘤体积较前缩小,未见明显强化 (箭示病灶)
1.2.2 药物治疗 D-TACE 后第3 天始予口服甲磺酸阿帕替尼(艾坦,江苏恒瑞),起始剂量为250 mg/天;若治疗期间出现3 级及以上阿帕替尼相关不良反应,则将服药频率调整为每2天1次或停药,待不良反应减轻或消失后逐渐恢复原剂量。于D-TACE 后第1 周始予静脉滴注卡瑞利珠单抗(艾瑞卡,江苏恒瑞),每次200 mg、每3 周1 次;出现与PD-1 抑制剂有关的3 级及以上不良反应时暂停用药,直至不良反应缓解。
1.3 随访及疗效评估 于首次联合治疗1 个月后复查血常规、肝肾功能、肿瘤标志物及上腹部增强CT/MRI,于3、6、9 及12 个月后复查肿瘤标志物及上腹部增强CT/MRI;若残存活性肿瘤或肿瘤局部复发、肝功能无严重受损则再行D-TACE 治疗,2 次治疗间隔需>30 天。以患者死亡或失访为随访终点。
根据随访结果计算OS、无进展 生 存 期(progression free survival, PFS)、ORR、疾病控制率(disease control rate, DCR)等,以评估联合治疗疗效;OS 指自联合治疗开始至任何原因导致患者死亡或末次随访时间的时间间隔,PFS 指自联合治疗开始至肿瘤进展或任何原因导致患者死亡或末次随访时间间隔。根据随访CT/MRI 采用改良实体瘤疗效评价标准(modified respond evaluation criteria insolid tumors,mRECIST)将肿瘤情况分为完全缓解(complete response, CR)、部分缓解(partial response, PR)、疾病稳定(stable disease, SD)或疾病进展(progressive disease, PD)。采用美国国家癌症研究所不良事件标准评估治疗相关不良事件(treatment-related adverse event,TRAE)。
2 结果
35 例联合治疗均成功。共随访7~27 个月,中位时间21 个月。联合治疗后1、3、6 及12 个月,ORR 分别为65.71%(23/35)、71.43%(25/35)、65.71%(23/35)及60.71%(17/28),DCR 分别为94.29%(33/35)、88.57%(31/35)、80.00%(28/35)及67.86%(19/28)。见表2。截止至末次随访,35 例中位PFS 为8.09[95%CI(6.70,9.30)]个月,中位OS 为20.00[95%CI(16.30,23.70)]个月。见图2。
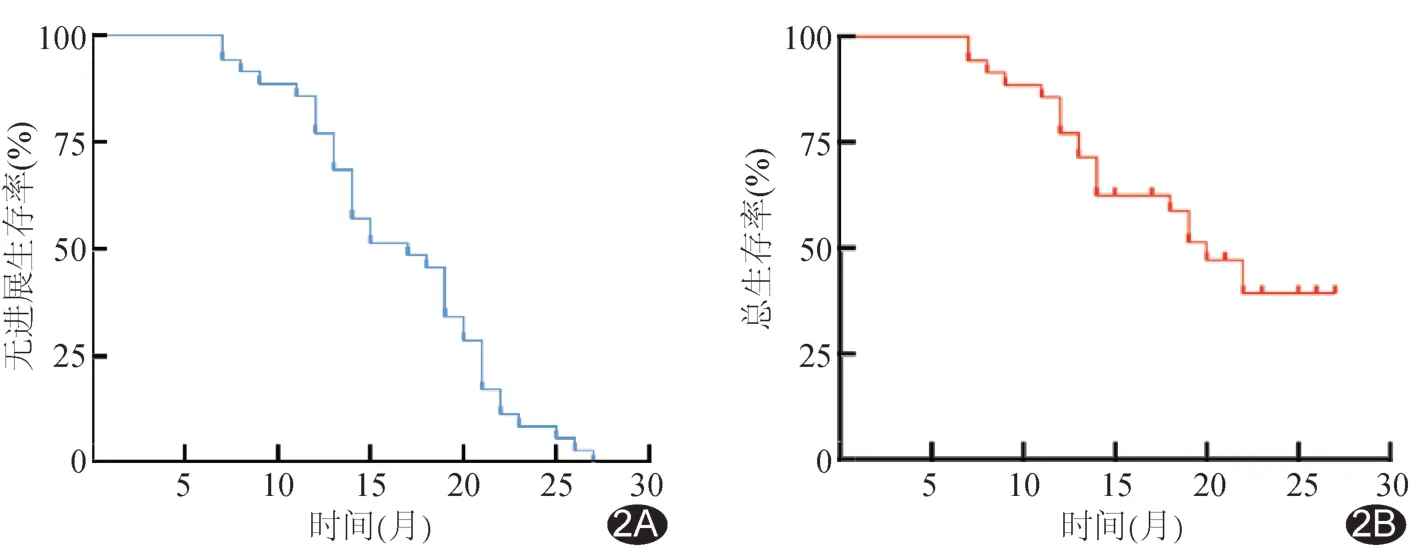
图2 D-TACE 联合双艾治疗巨块型HCC 后生存曲线 A.无进展生存率; B.总生存率
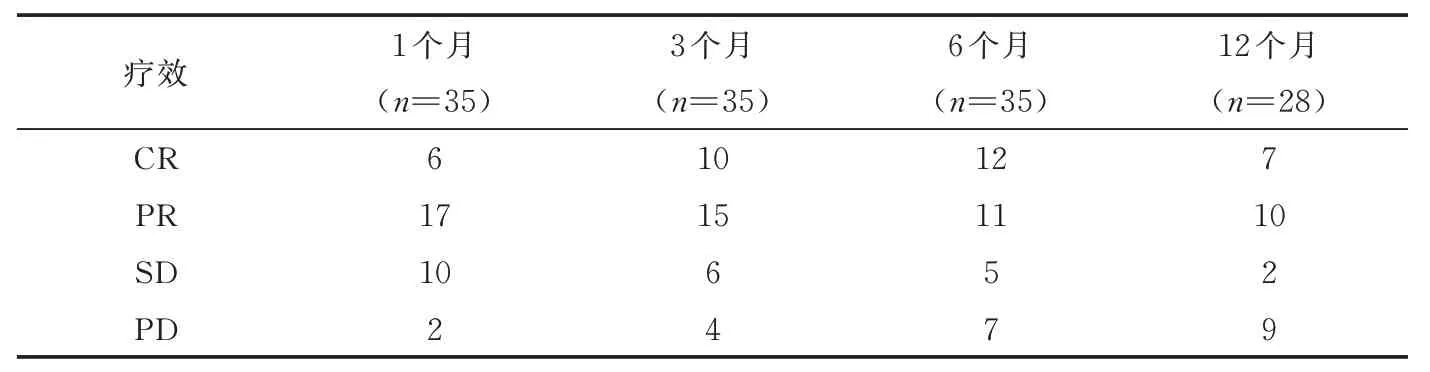
表2 D-TACE 联合双艾治疗巨块型HCC 后1、3、6 及12 个月疗效(例)
D-TACE TRAE 包括发热15 例、疼痛13 例、消化道反应9 例、肝脓肿1 例及肝损伤31 例,双艾治疗TRAE 包括乏力11 例、手足综合征11 例、高血压9 例、蛋白尿10 例、反应性毛细血管增生症8 例、腹泻7 例、皮疹4 例、上消化道出血1 例及免疫相关性肺炎1 例;均以1~2 级TRAE 为主(表3)。联合治疗中,31 例出现不同程度谷丙转氨酶和/或谷草转氨酶升高。
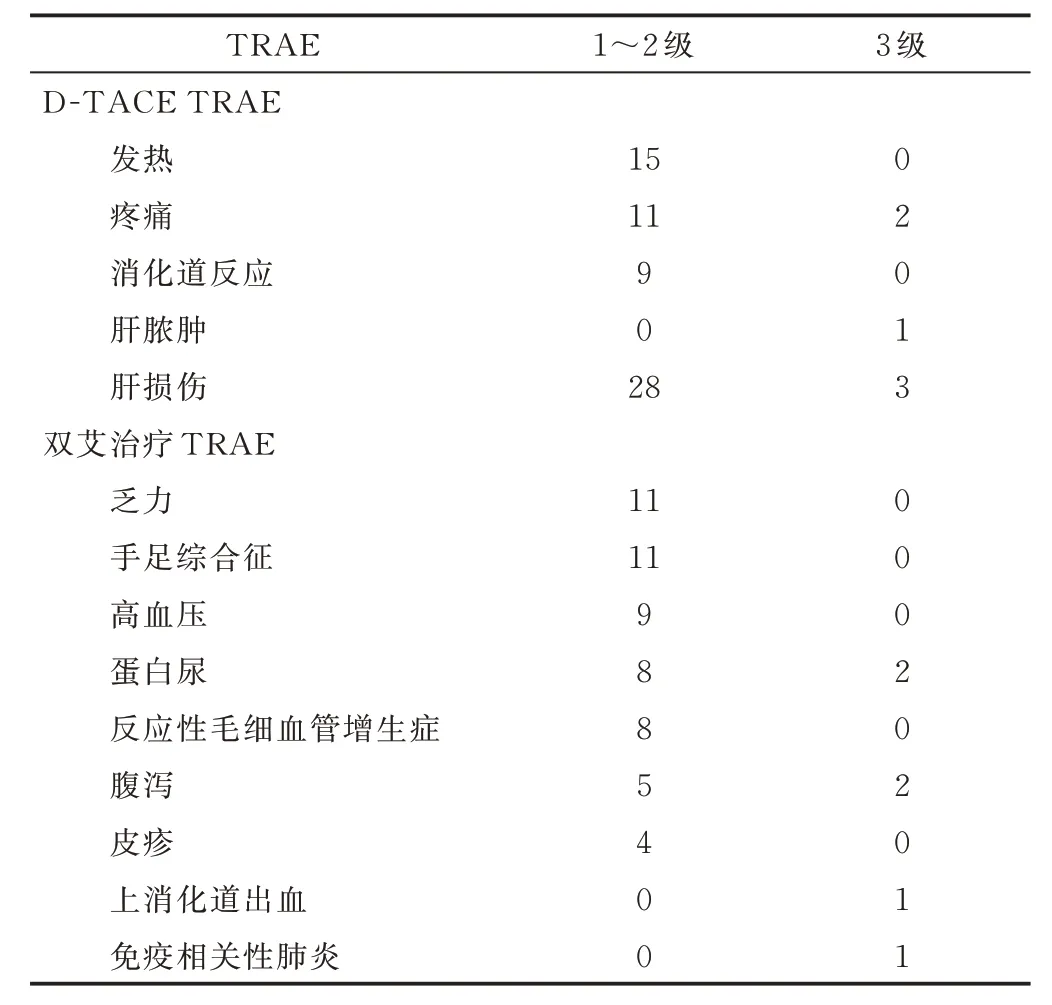
表3 D-TACE 联合双艾治疗巨块型HCC 的TRAE
经对症治疗/减少药物剂量/停药后,所有TRAE均得到有效控制,未出现治疗相关死亡事件。≥3 级双艾治疗TRAE 中,对1 例上消化道出血、2 例蛋白尿、2 例腹泻者将阿帕替尼剂量调整至两天1 片(250 mg),对1 例免疫相关性肺炎者停用卡瑞利珠单抗;症状改善后均逐渐恢复原方案。
3 讨论
巨块型HCC 早期一般无特殊临床表现,且常伴血管侵犯及肝内转移,预后较差;手术切除是最常用治疗方法,但术后复发率高,且可导致肝功能丧失等严重并发症。TACE 治疗巨块型HCC 安全、有效[5],但因巨块型HCC 肿瘤负荷较大,多次常规TACE(conventional-TACE, C-TACE)、反复使用大剂量化学治疗药物及碘化油不仅将加速肝硬化进程、加重肝功能损伤,还增加肝功能衰竭和门静脉高压合并上消化道出血风险;而D-TACE 可在靶器官内持续释放化学治疗药物,增加局部浓度、延长作用时间,具有更好的临床疗效[6]。DUAN 等[7]发现,相比C-TACE,DTACE 用于巨块型HCC 的临床反应、安全性及患者生存期更佳;但对晚期巨块型HCC,单一D-TACE 治疗不能有效延长患者生存期。阿帕替尼及PD-1 抑制剂卡瑞利珠单抗是我国自主研发的抗肿瘤药物,阿帕替尼有助于抑制TACE 后新生血管形成,与TACE 发挥协同增效作用[8];而TACE 可上调PD-1/细胞程序性死亡配体1(programmed cell death 1 ligand 1, PD-L1)表达,增强PD-1 抑制剂的免疫治疗效果[9]。既往研究[10]亦表明,D-TACE 联合双艾治疗可显著提高中晚期HCC 患者的生存获益。
LIU 等[11]采用D-TACE+阿帕替尼治疗巨块型HCC,其后1个月患者ORR 为64.7%、DCR 为82.4%;ZHANG 等[12]以D-TACE+卡瑞利珠单抗治疗巨块型HCC 后1 个月的ORR 为55.1%、DCR 为77.55%。本研究D-TACE 联合双艾治疗巨块型HCC 后1 个月的ORR 为65.71%,DCR 为88.57%,较上述研究均有所上升,提示D-TACE 同时联合上述2 种药物的疗效优于联合单一药物。一项单中心回顾性研究[13]采用D-TACE联合双艾治疗不可切除HCC,其PFS 和OS 分别为8.0 个月和25.0 个月。本研究截至随访末期的中位PFS 为8.09 个月,中位OS 为20.00 个月;PFS 与上述研究类似,但OS 较低,可能与本组大部分患者处于BCLC C 期、预后较差有关;同时,本组35 例中,治疗1、3、6 个月后CR 分别为6、10、12 例,主要原因在于巨块型HCC 血供丰富,抗血管生成靶向药物可在促进肿瘤血管正常化的同时改善肿瘤缺氧及免疫微环境,并逆转VEGF 介导的免疫抑制,促进肿瘤中的T 细胞浸润,从而增强抗PD-1 和抗PD-L1 效果[14];进一步联合D-TACE 可在短时间达到CR,减少TACE 次数。
本研究中TRAE主要为1~2级,且均经对症处理后改善,与既往研究[3]结果一致,表明双艾治疗的安全性与单药治疗相当。本组TRAE包括1例上消化道出血,可能与阿帕替尼引起血小板减少及血小板功能障碍有关[15]。
综上所述,D-TACE 联合双艾治疗巨块型HCC效果较佳且安全,不良反应可控。但本研究为小样本、单中心、回顾性观察,未设置对照组,且随访时间较短,有待后续进一步观察。
利益冲突:全体作者声明无利益冲突。
作者贡献:陈金威查阅文献、图像处理和分析、数据分析、撰写及修改文章;任建庄研究设计、修改及审阅文章;段旭华指导、研究设计;陈鹏飞研究实施、统计分析、经费支持;朱兴书研究实施、统计分析。
