CH4分子在外电场作用下的结构和解离特性研究
2024-01-24陈晓宇万文梓吴建光马建军
唐 臻,陈晓宇,万文梓,邹 勇,吴建光,马建军
(安徽工业大学,马鞍山安徽 243002)
甲烷(CH4)是大气中具有化学活性和辐射活性的气体,也是重要的温室气体.随着人类文明的发展,甲烷在空气中的总量在不断增加,到20 世纪90 年代浓度已达到1 714 ppbv.它通过吸收大气中的长波辐射,使得大气升温并改变大气层的净辐射通量.甲烷在平流层中与O2发生氧化反应生成水汽,在对流层中则与羟基反应生成臭氧.虽然CH4在大气中含量比CO2少,但是单位质量CH4全球变暖的潜力却是CO2的28 倍[1],因此减少CH4排放也是控制全球增温,实现碳中和目标的必要手段[2].甲烷是正四面体非极性分子,仅由非活性的C-H 键组成,常态下不易降解.近年来,采用高级氧化技术处理难降解有机物已成为研究的热点.Fenton 反应高级氧化工艺其高效、价廉、工艺装置相对简单,具有很大的实用价值[3].瓦斯是威胁煤矿安全生产的最大灾害源,瓦斯中甲烷含量一般大于80%,随着微生物技术的发展,甲烷氧化菌应用于瓦斯消除已初见成效.姜晓童等[4]探讨了在煤矿中用微生物降解甲烷的机理以及影响,结果表明在常压和足氧条件下通过甲烷氧化菌降解甲烷气体具有极大的可行性.刘栋等[5]研究了真空紫外光催化(TiO2/VUV)对低浓度甲烷的去除效果及影响因素,使光催化氧化技术在室内和密闭空间空气净化方面被寄予厚望.
近年来,关于分子外电场效应的研究得到了许多学者的密切关注.在电场作用下,分子可能会被激发到高激发态甚至电离解离、分子的电子结构发生变化、发生化学键的碎裂以及新自由基生成等一系列的化学变化.如张祥云等[6]采用密度泛函理论研究了CH3I 分子在外电场下的光谱和解离特性,结果表明,在沿着C-I 键方向施加外电场,随着电场强度增加,分子体系能量逐渐减小,偶极矩单调增加,能隙呈现先增加后减小趋势,C-I和C-H 键长逐渐增大,分子变得不稳定易于解离.李亚莎等[7]在研究CF3I分子在外电场作用下的特性时发现,随着外电场增加能隙逐渐减小,分子总能量增加,分子变得不稳定.吴永刚等[8]采用B3LYP/6-311++G(3df,3pd)方法和基组研究了CFCl3分子在外电场中的光谱和解离特性,发现电场对分子的结构、电偶极矩、能隙、红外和拉曼光谱性质都有影响,红外与拉曼光谱随外电场变化出现红移或蓝移现象.袁园等[9]采用B3LYP/6-311G(d,P)方法和基组研究了外电场下四氯甲烷光谱特性和解离特性.徐国亮等[10]采用密度泛函B3LYP和组态相互作用方法在6-311++G**水平上计算了甲烷在外场作用下的光激发特性.目前尚未见关于CH4分子在外电场中的光谱和解离特性的相关研究报道,本文选用B3LYP/6-311++G**方法和基组,对CH4分子在外电场下的光谱与解离特性进行理论研究,为利用外电降解该污染物提供理论依据.
1 理论和计算方法
外电场作用下分子体系的总哈密顿量可表示为[6-12]H=H0+Hint.其中H0为无外电场时的哈密顿量,在偶极近似下,电场与分子相互作用的附加哈密顿量Hint可表示为Hint=-μ·F.这里,μ为分子的电偶极矩,F为偶极电场.
本文利用高斯09程序软件包[11],采用B3LYP/6-311++G**密度泛函算法/基组沿着Z轴方向加不同强度的偶极场,探索外加电场对分子CH4的轨道能级、能隙、偶极矩、红外光谱和拉曼光谱的影响,最后探究外电场作用下CH4的解离特性.
2 结果与讨论
2.1 CH4分子的基态结构
CH4分子在没有外电场情况下的几何结构如图1所示,基于文献[10]所采用的算法和基组计算出的该分子结构参数的理论值和实验值比较吻合性.本文采用密度泛函理论B3LYP 方法在6-311++G**基组水平上,对CH4分子沿着Z 轴(1C-2H 键轴)方向依次添加不同的静电偶极电场(强度为-0.05,-0.04,-0.03,-0.02,-0.01 a.u.和0.01,0.02,0.03,0.04,0.05 a.u.)来研究该分子的红外和拉曼光谱特性,并计算外电场对1C-2H键的解离的影响.

图1 CH4分子的几何结构
2.2 外电场中分子的基本性质
为了探究电场对分子结构及光谱特性的影响,表1 显示通过计算得到的分子在不同外电场下的结构参数变化情况.表1的第2-5列表示不同外电场下分子中原子的电荷分布,从表1中可以看出,随着外电场强度从-0.05 a.u.到0.05 a.u.逐渐增加,C 原子所带的负电荷逐渐减少,沿着键轴上的2H 原子所带电荷由原来的正电荷逐渐变为负电荷,而其他H 原子所带正电荷逐渐增多.外电场的存在破坏了分子的对称性和电荷分布状况,导致分子的电偶极矩也随着电场的加入而增大.图2和图3分别显示了外电场下分子的电偶极矩以及分子总能量的变化情况.当沿着1C-2H 键轴的正向或反向增加电场时,2H 原子在外电场作用下向远离C 原子方向移动,分子的键长逐渐增大,表明因电场强度的增加而使得化学键变得脆弱,分子易发生解离,键长的变化与电场下电荷的转移有关[12-13],化学键两端的原子在引力与斥力组成的内应力作用下,在平衡位置处达到稳定状态.当有外电场存在时,电子由于受到电场力作用而沿着场强相反的方向运动,电荷发生转移,原子间的内应力也相应地发生变化,随着正向电场的增加,C 与2H 原子之间的作用逐渐由原来的吸引作用变为排斥相互作用,而且键长也随之增大,这就更容易发生解离.由图2 可看出,分子的电偶极矩随外加电场强度增加而增加.这是因为在外电场作用下,分子内电场与外电场相互作用[14-15],电负性相反的原子分别沿着电场的正反方向移动,分子被拉伸,分子的极性增大.由图3可知,分子的总能量随外加正向或反向电场的增加而减小.随着外电场场强大小从0 a.u.增加到0.050 a.u.时,电子的定向移动随电场强度的增大越明显,导致其分子内库仑引力增大,分子偶极矩也随之增大,哈密顿量中的势能绝对值增加,分子体系的总能量随之逐渐减小.
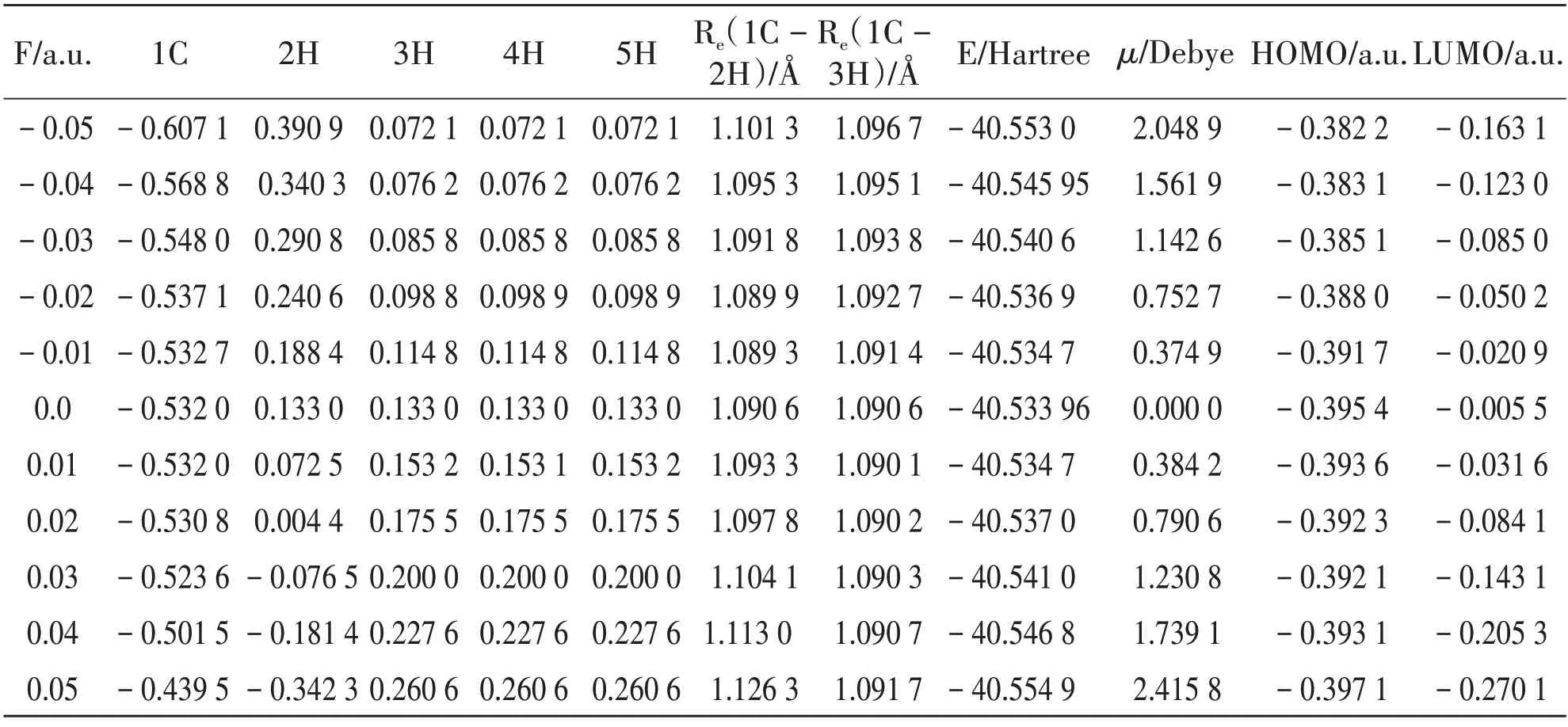
表1 不同电场下计算得到的CH4分子基态结构参数

图2 分子偶极矩随外电场的变化

图3 分子总能量随外电场的变化
2.3 外电场下分子的轨道能级分布
依照前线轨道理论[16-17],分子在参与化学反应时优先起作用的是最低占空分子轨道(the Lowest Unoccupied Molecular Orbital,LUMO)和最高占据分子轨道(the Highest Occupied Molecular Orbital,HOMO),LUMO 能级(数值上相当于分子的电子亲和势)越低,分子接受电子的能力越强,而HOMO 能级越高意味着分子就越容易失去电子.能隙Eg大小等于最低占空分子轨道能量EL与最高占据分子轨道能量EH之差,即Eg=EL-EH,它反映电子从LUMO 向HOMO 能级发生跃迁的能力,在一定程度上也代表分子参与化学反应的活性[18-19],分子的化学活性随着能隙的减小而增大,化学活性越大,则分子越不稳定.如图4 所示,分子的最高占据轨道能量几乎不随外电场变化,而最低占空分子轨道能量则随着电场强度绝对值大小增加而明显降低.随着正反向外电场强度的增加,能隙都逐渐减小.相比之下,正向电场比反向电场更容易减小能隙,其能隙急剧下降,占据轨道上的电子越容易被激发.总之,外电场的增强加剧了分子不稳定性.

图4 HOMO、LUMO 能级和能隙随电场变化
2.4 外电场下分子的红外光谱特性
采用B3LYP/6-311+G**方法和基组对该分子在不同外电场下的红外和拉曼光谱进行了计算,表2显示了不同电场下的红外、拉曼频率和强度变化情况,从表中可以看出,在无外电场情况下,V1≈V2≈V3≈1 339.5cm-1,该频率相对应于4 个H 原子与C 原子作反向运动,为三重简并振动;V4≈V5≈1 557.5cm-1,相应于分子相邻两对H 原子在与C 原子联线方向上,或在该联线垂直方向上同时作反向运动,为二重简并振动;V6=3 026.81cm-1相对于4个H原子沿着与C原子的连线上作对称伸缩振动,V4、V5、V6在无外电场下不显示红外活性;V7≈V8≈V9≈3 132.1cm-1相应于一对H原子作伸缩振动,另一对作压缩运动的反对称伸缩振动,也处于三重简并状态[20].无外电场时分子的红外和拉曼光谱如图5所示.随着外电场的引入,分子的各个振动频率和强度都发生了变化,为了清楚地描述外电场对红外光谱的影响,我们选取频率分别位于1 339.5 cm-1和3 132.1 cm-1的两条红外谱线的放大图,分别如图6和7所示.从图6(a)和(b)可以明显地看出,随着正向和反向电场的增加,这两条谱线的简并被部分解除,频谱位置随着电场强度增加向着低频方向偏移.随着电场的增强,两个分裂的谱线间隔越大.谱线强度随着正向电场强度增加而减弱,而在反向电场下谱线强度则是先减小后增加.外电场对不同谱线吸收谱强度的影响不同,图7 显示与图6 类似的变化趋势.
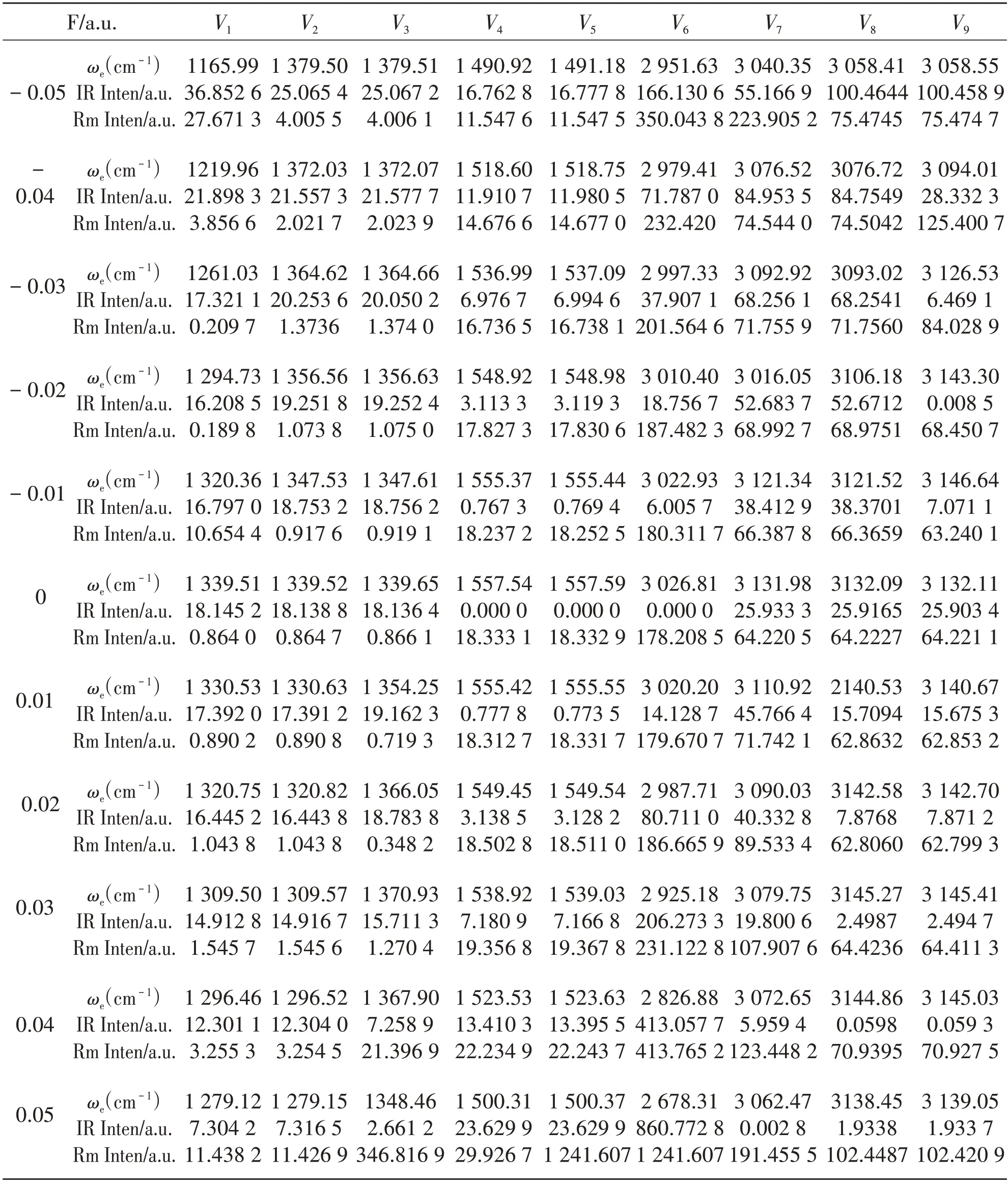
表2 不同外电场下CH4分子的谐振频率和红外、拉曼光谱强度
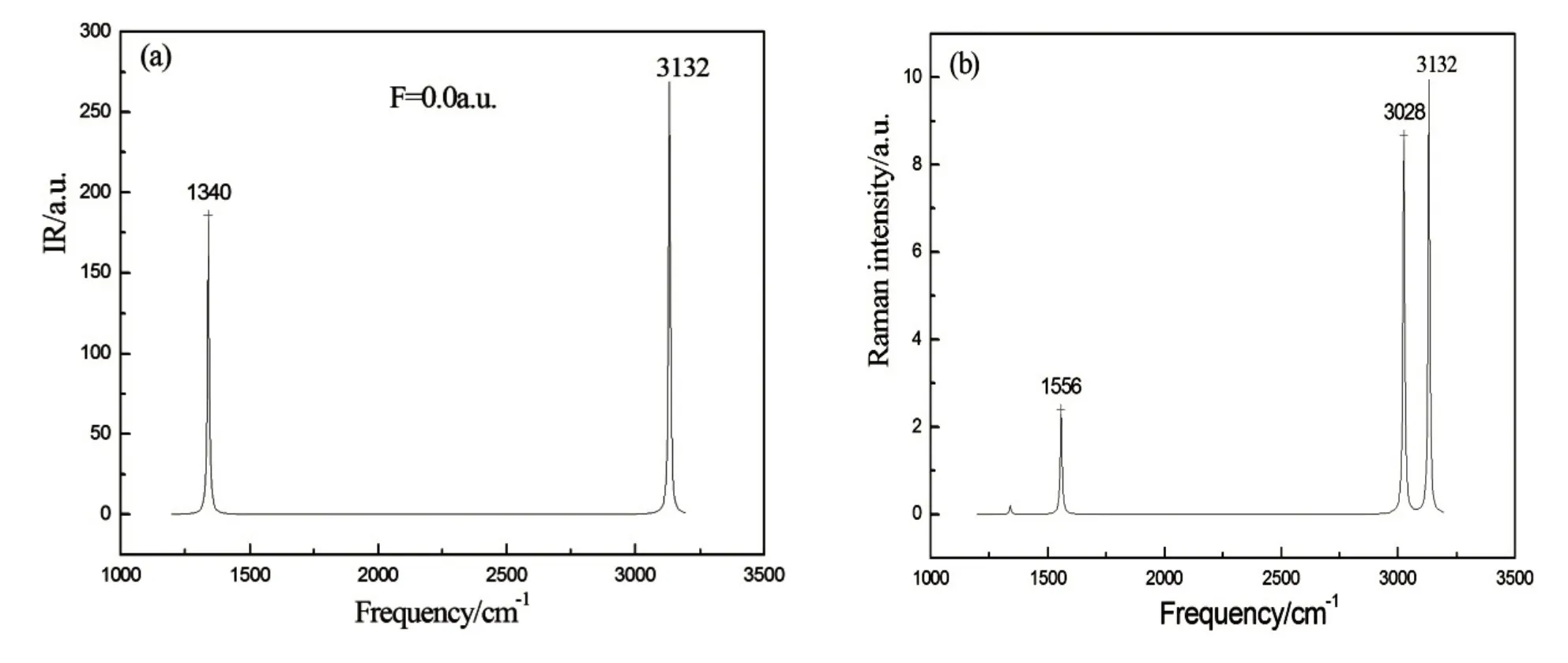
图5 在无外电场下的分子的红外和拉曼光谱:(a)红外光谱;(b)拉曼光谱

图6 红外谱线1 339.5 cm-1 随电场变化:(a)正向电场;(b)反向电场
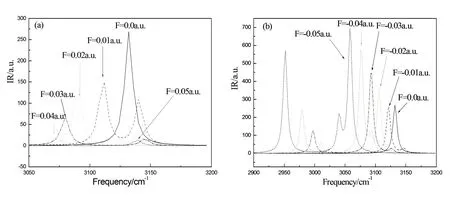
图7 红外谱线3 132.1 cm-1随电场的变化:(a)正向电场;(b)反向电场
图8和9分别显示无外电场时频率为1 557.5cm-1和3 132 cm-1的拉曼光谱在不同外电场下的放大图.从图8可以看出,频率为1 557.5cm-1的拉曼光谱随着外加电场强度大小的增加,频率向着低频方向移动,谱线没有发生分裂,正向电场的增加引起谱线强度增大,而反向电场的增加则引起谱线强度减弱.图9显示的频率为3 132 cm-1的拉曼光谱随着电场的变化趋势与红外光谱类似.
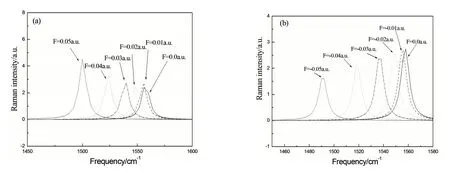
图8 拉曼谱线1557.5 cm-1随电场的变化:(a)正向电场;(b)反向电场
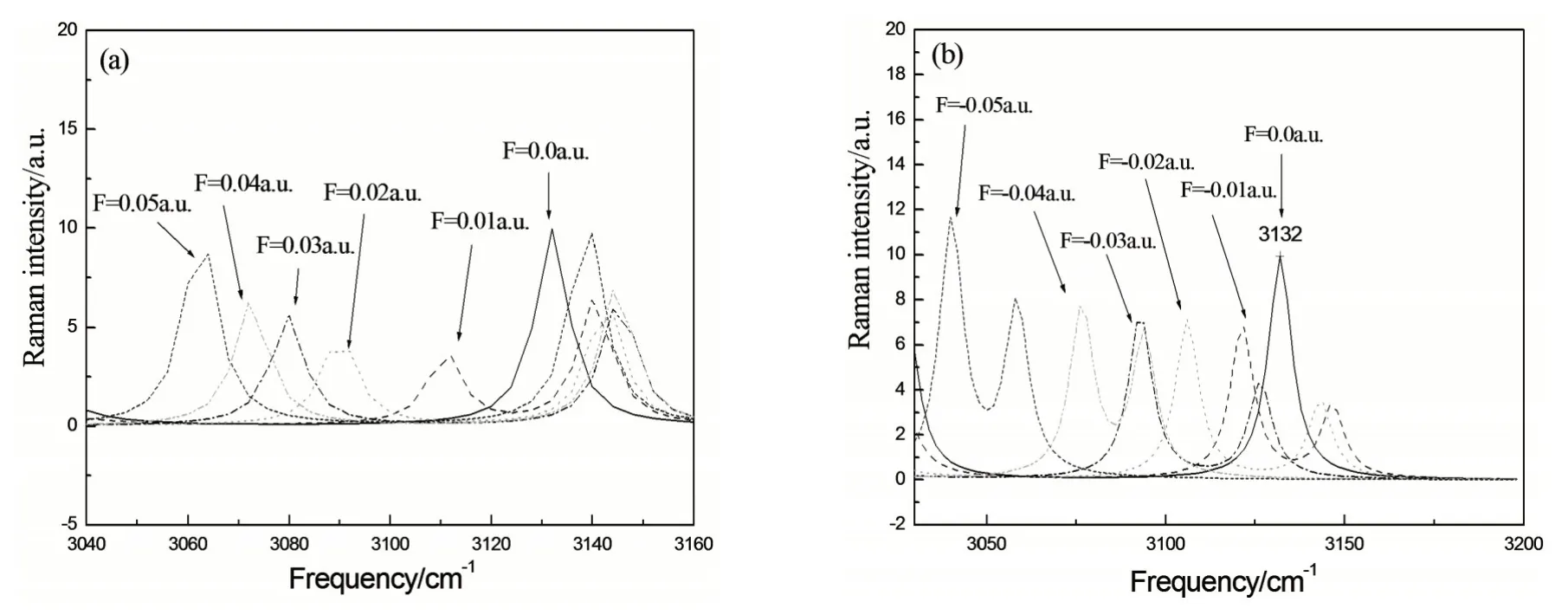
图9 拉曼谱线3 132.1 cm-1随电场的变化:(a)正向电场;(b)反向电场
这种在外电场作用下不同频谱发生相反方向的频移可能与在电场作用下的电荷布局以及核间距变化有关.由前面所述,随着电场强度从反向到正向逐渐增加,1C 原子所带的负电荷逐渐减少,2H 原子所带电荷由原来的正电荷逐渐变为负电荷,而3H,4H,5H 原子所带正电荷逐渐增多,1C-2H 之间的作用由原来的吸引变为排斥,而1C-3H(4H,5H)之间的相互作用则正好相反,1C-2H之间的核间距逐渐增大,1C-3H之间的核间距则随着反向电场增强而变大,随着正向场强增大先变小后增大,由于核间距的变化,导致分子的对称性遭到破坏,谱线发生分裂,核间距的增加引起化学键的强度减弱,谱线变弱.说明在此电场的作用下,内外电场的叠加影响分子的能级结构,综上所述,外加电场可以对分子或基团红外和拉曼光谱进行调控,也可用于分子或基团谱线分离,实现对分子或基团谱线信息的捕捉[8].
2.5 外电场下分子的解离特性
沿着1C-2H键轴方向分别施加不同的反向和正向外电场,采用之前的方法和基组对分子基态进行1C-2H 键方向的能量扫描,得到1C-2H 键的势能曲线(如图10).由图10 可知,1C-2H键的势能曲线随外电场强度大小的增加一直呈现降低趋势,势垒也逐渐减小,键的束缚能力逐渐减弱,说明外电场对CH4分子的解离势能曲线有重大影响.当正向电场强度增加到0.08 a.u.或者反向电场增加到0.09 a.u.时,势能曲线中势垒消失,分子中的1C-2H 键在电场作用下发生断裂,从而使得该分子发生降解.

图10 正向和反向电场下C-H键势能曲线
3 结论
使用高斯09程序软件包采用密度泛函理论,在B3LYP/6-311++G**水平上,对外电场下CH4分子的基态结构(包括键长、电偶极矩、能量)、红外和拉曼光谱以及C-H键的解离特征进行理论计算.结果表明:随着沿着键轴C-H 方向外加电场强度的增加,基态分子CH4中的C-H 键长和电偶极矩随之增加,分子体系的总能量随着外电场增加而减小.能隙随着外电场增加而减小,分子变得不稳定,易发生解离;随着外加电场强度大小的增加,分子的红外和拉曼光谱出现红移和谱线分裂现象,光谱强度也发生改变.电场可作为一种辅助手段将其谱线分离而获取各种分子信息.通过在外电场作用下对C-H键进行势能面扫描发现,当正向电场强度增加到0.08 a.u.或反向电场强度增加到0.09 a.u.时,能垒均消失,C-H键在正向和反向电场下都能发生解离,相比之下正向电场更容易使得CH4分子解离.该结果能够为CH4分子在电场作用下发生解离而降解提供理论依据.
