盐度对正戊烷在水溶液中扩散的影响
2024-01-22王靖茹刘月田柴汝宽宋来明毛钰鑫
王靖茹,刘月田,柴汝宽,宋来明,毛钰鑫
(1.中国石油大学(北京)油气资源与探测国家重点实验室,北京 102249; 2.中海油研究总院有限责任公司,北京 100028)
引言
随着石油开采、运输业的蓬勃发展,大量油污进入海洋,对水域造成污染,同时严重威胁人类和水生物的健康。石油是一种以烷烃为主的混合物,除了以油膜形式浮在水面,还会在水中扩散。与其他化学物质相比,烷烃由于碳键较为稳定而难以分解。烷烃属于非极性溶剂[1],不易溶于水等极性溶剂,因此研究以烷烃为例的有机质在水中的扩散有较大意义。Pokharel等[2]利用分子动力学模拟研究了气态短链烷烃在水中的自扩散系数,发现随着烷烃分子质量的增加,扩散系数逐渐减小。Pham等[3]研究烷烃在气-水界面的扩散,发现烷烃在气-水界面的扩散随着水相中离子浓度的增加而增加。Sakai等[4]研究油水环境中烷烃液滴的变化情况,发现随着烷烃碳数的增加,烷烃液滴尺寸的增长速率逐渐减小。陈聪等[5]研究了甘油在NaCl溶液中的扩散,发现随着甘油浓度的增加,体系中甘油的自扩散系数逐渐降低。目前关于有机质在水溶液中扩散的研究多集中于有机质在气-水界面的扩散[6-7],对于液态有机质在水相中的扩散研究相对较少,特别是水溶液盐度[8]对有机质扩散影响的研究更为少见。然而,海洋、地层水的盐度变化较大,研究盐度变化对有机质在水溶液扩散的影响对于环境保护工作意义重大。正戊烷作为碳数最低的液态烷烃,非极性较低,在水溶液中的扩散现象较为明显。研究正戊烷在水溶液中的扩散对正戊烷的溶解与分离有重要意义。
本研究首先采用动态悬滴体积分析方法(DPDVA)研究了正戊烷在MgCl2溶液中的扩散规律;而后利用分子动力学模拟研究正戊烷在MgCl2溶液中的扩散机理。本研究对分析在海水、地层水等多离子溶液中有机质分子扩散现象[9-10],进行海洋污染的治理[11]有指导作用。
1 实验及分子模拟方法
1.1 实验方法及步骤
采用动态悬滴体积方法[12-13]研究正戊烷在MgCl2溶液中的扩散规律。首先,在注射单元中吸入正戊烷,J型不锈钢注射器浸入装有不同盐度MgCl2溶液的石英样品池。而后,注射单元采用精度可达0.01 μL的高精度注射泵进液,由软件定量定速控制注射。向测量软件输入注射单元的水相与油相密度、温度数据后启动仪器。正戊烷液滴在注射器端口成型,静置,仪器每隔10 s测量一次油滴直径。正戊烷在水溶液中自动缓慢膨胀,测量直至端口不能束缚住液滴结束。CCD相机将液滴的实时形态传输给计算机,内置滴形分析软件实时读取并记录液滴直径的动态数据。
1.2 模拟方法
1.2.1 模型构建
建立MgCl2水溶液体系,模拟MgCl2在水溶液中的离子水化作用,分析离子水化对溶液中水分子产生的影响。采用Materials Studio软件中的Amorphous Cell模块构建模拟体系,体系内分子及离子组成见表1。

表1 水溶液体系组成
建立正戊烷-水溶液体系,模拟正戊烷在水溶液中的疏水作用,同时分析离子水化对正戊烷疏水作用产生的影响。表2为采用1 000个水分子,m个正戊烷分子(m=1,50),n对MgCl2(n=0,1,3,5,10)进行模块封装的模拟体系,采用Materials Studio软件中的Amorphous Cell模块构建模拟体系。图1为包含水分子、正戊烷分子、Mg2+和Cl-的模拟体系示意图。
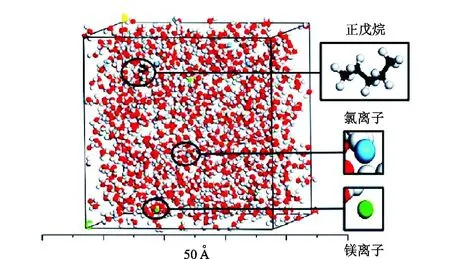
图1 模拟体系示意图

表2 正戊烷-水溶液体系组成
1.2.2 计算方法
通过Materials Studio软件中的Forcite模块中的Dynamics功能对溶液中的离子水化过程、正戊烷的疏水作用及正戊烷在水溶液中的扩散进行分子动力学模拟[14-16]。采用COMPASS力场计算原子间相互作用力;选用NPT系综,体系温度设置为298 K,体系压力设置为0.1 MPa,采用Nose恒温模式和Berendsen控温方法;选用Ewald加和法计算中长程静电作用力,Atom Based方法计算范德华相互作用力;模拟步长为1.0 fs,对模型进行300 ps的分子动力学模拟。
2 结果与分析
2.1 实验结果
图2为正戊烷液滴直径D的平方值随时间的变化图,表征了正戊烷液滴扩散面积的变化率。由图2可知:水溶液盐度对有机质的扩散有重要影响。实验初期正戊烷液滴在体系中扩散面积相近,随着时间的推移,正戊烷液滴在水相中不断扩张,且相较于纯水溶液,MgCl2水溶液中正戊烷液滴的扩散面积变化程度更为显著。同时随着盐度的增加,正戊烷液滴扩散面积的变化程度逐渐降低。对正戊烷液滴扩散面积随时间变化的散点图进行线性拟合,得到不同盐度下正戊烷液滴直径平方-时间曲线的斜率,即为正戊烷液滴扩散面积变化率。溶液盐度在0.5‰时正戊烷液滴扩散面积变化率最大,为2.75×10-9m2/s。1.0‰、4.0‰、5.0‰时正戊烷液滴扩散面积变化率相近,分别为2.12×10-9m2/s、2.56×10-9m2/s、2.04×10-9m2/s。溶液盐度进一步增加达到10.0‰与20.0‰时,正戊烷液滴扩散面积变化率持续降低,分别为1.83×10-9m2/s与1.53×10-9m2/s。而在纯水溶液中正戊烷液滴扩散面积变化率低于MgCl2溶液中的扩散面积变化率,仅为1.08×10-9m2/s。实验结果表明,MgCl2水溶液-正戊烷系统中存在转折盐度(0.5‰),使正戊烷液滴扩散面积变化率最大,正戊烷扩散程度最强。
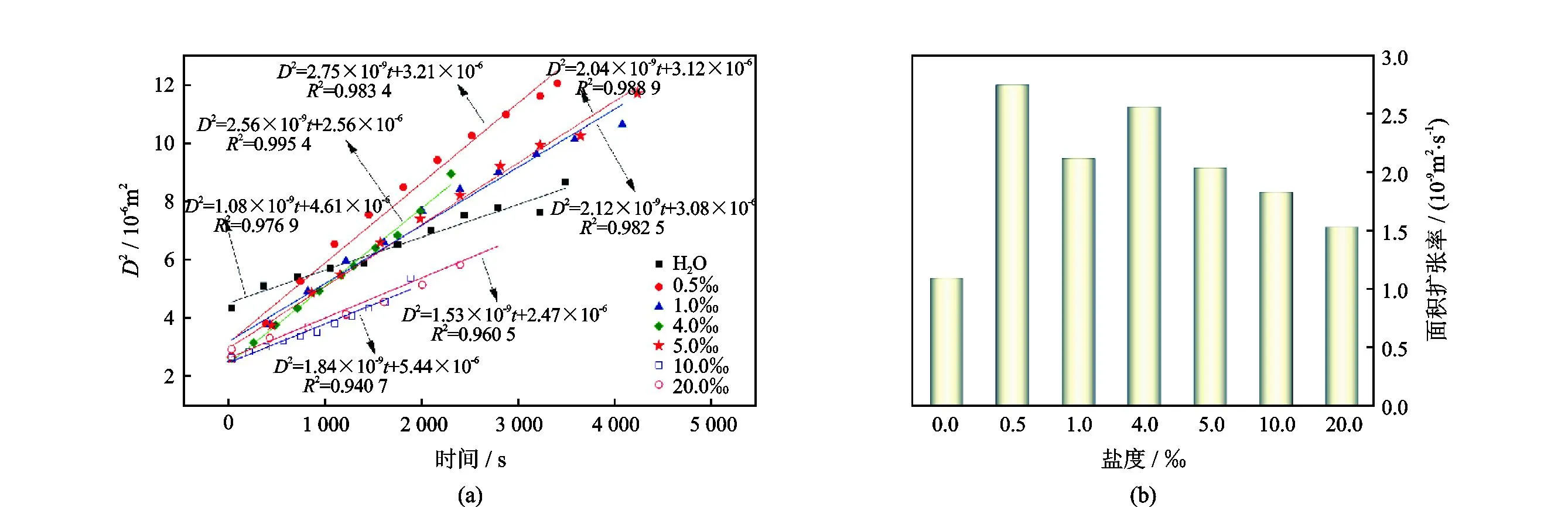
图2 正戊烷扩散面积变化率随盐度变化规律
2.2 分子模拟结果
2.2.1 离子水化模拟结果
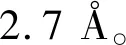
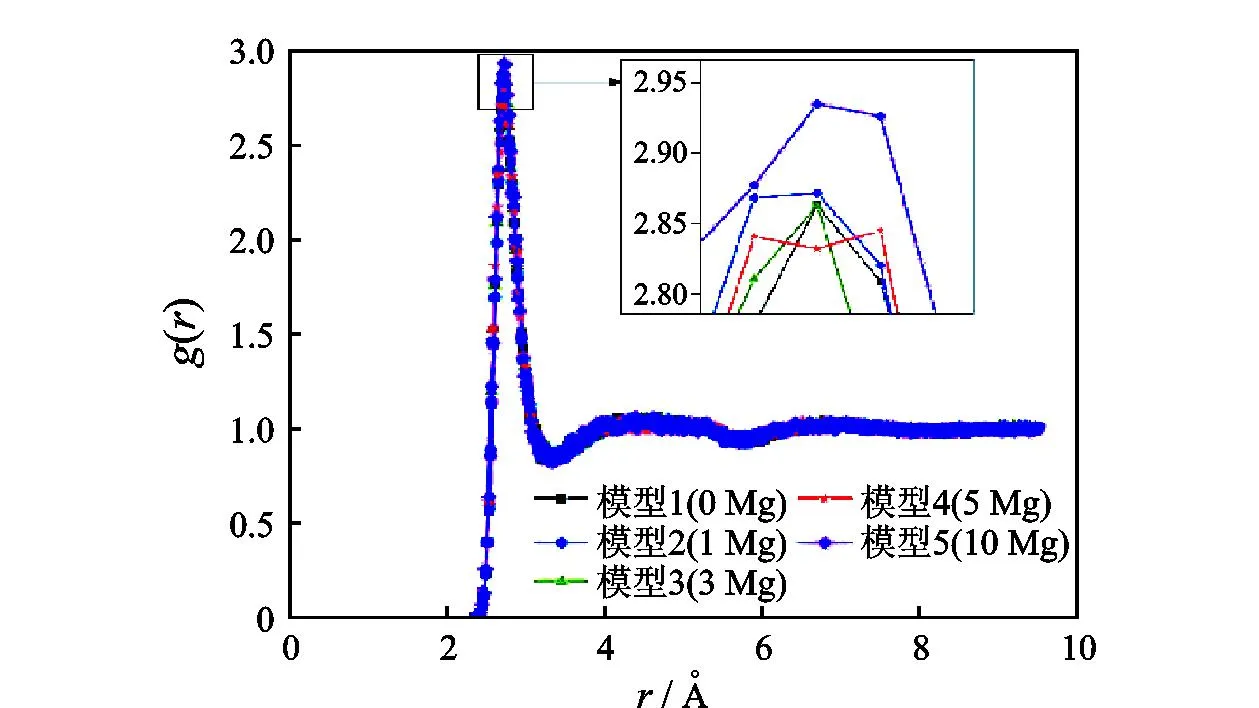
图3 不同盐度下O-O径向分布函数
2.2.2 正戊烷疏水作用模拟结果
图4为非极性分子在体系中疏水作用的模拟结果。图4(a)为模拟初期,水分子与正戊烷分子在体系中任意分布。图4(b)为体系进行分子动力学模拟后,正戊烷分子在体系中聚集产生的疏水作用。由图4可知:为了使体相水的吉布斯自由能最大化,溶质-正戊烷倾向于在水中聚集,使界面水的吉布斯自由能最小化。这种界面水与体相水之间的竞争产生疏水作用力,主要受体相水驱动[18]。

图4 非极性分子疏水作用


图5 不同正戊烷分子数体系的O-O径向分布函数
2.2.3 离子水化对正戊烷疏水作用的影响
图6(a)为模型6~10中不同盐度体系下的O-C径向分布函数,代表着水分子与正戊烷分子之间的分布情况。随着体系盐度的增加,O-C径向分布函数的第一个峰值先升高再降低。在模型9中,O-C径向分布函数达到最高值1.45。距离大于第一峰峰位时,无论盐度如何改变,O-C径向分布函数值都趋近于1。这说明在特定分子分布范围内,体系中粒子趋向于定向排布,脱离了这个距离范围,体系中粒子排布更具随机性。表现为水分子在正戊烷分子周围定向排布,建立出正戊烷分子的疏水单元。模型O-C径向分布函数值越高, 说明在该体系盐度下疏水作用越强。在模型9中O-C径向分布函数值最高,正戊烷分子疏水作用达到最强。图6(b)为模型6~10中不同盐度体系下水分子中H原子与正戊烷分子中H原子的径向分布函数。图6(b)中可观察到与图6(a)相似的结果,模型9中H(H2O)-H(C5H12)径向分布函数的第一峰峰值最高,达到1.15。然而H(H2O)-H(C5H12)径向分布函数峰值均低于O-C径向分布函数的峰值。说明相较于C、O原子,H原子在体系中的分布更具随机性,局部结构更不明显,溶液盐度对氢原子的分布影响较小。
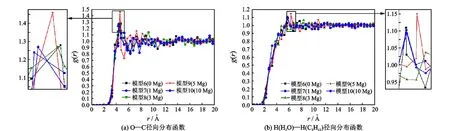
图6 径向分布函数分析
相较于模型6~10,模型11~15更贴近于实际情况。虽然也存在非极性分子--正戊烷分子扩散进入极性分子--水分子间的情况,但是极性分子间的相互作用力远远强于极性分子与非极性分子间作用力,会对非极性分子产生排斥作用,致使非极性分子即正戊烷分子聚集。图7为模型11~15中正戊烷分子自身的径向分布函数,存在2个明显峰值。由于正戊烷极性较弱,与极性分子水分子之间既存在吸引力又存在排斥力。图7中,随着溶液盐度的增加,正戊烷分子的径向分布函数第一峰峰值先增加后降低,在模型14中第一峰峰值达到最高62.1。说明在正戊烷-水溶液体系中,正戊烷分子构成的疏水单元不与水形成氢键,水在疏水单元周围重组且不牺牲氢键[16]。而体系中离子的加入,束缚了水的自由移动,限制了疏水单元周围水分子的重组进程。同时由于离子水化对水分子的定向束缚,导致体系中出现可以使正戊烷分子在水溶液中扩散的空腔,增加正戊烷分子的扩散强度。
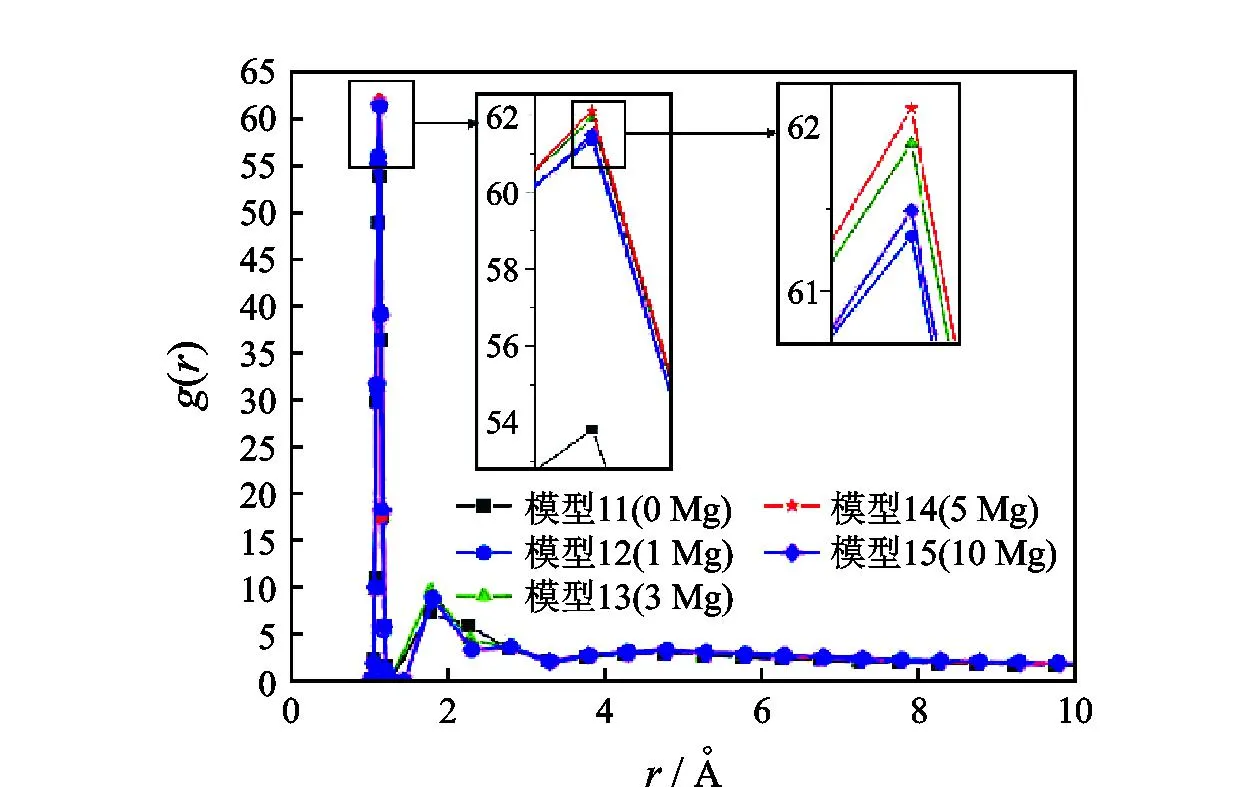
图7 正戊烷分子径向分布函数
图8为模型11~15中不同盐度体系下水分子之间的径向分布函数。图8显示的水分子径向分布函数存在2个明显峰值。随着溶液盐度的增加,水分子径向分布函数的第一峰值先增大后减小,而第二峰值与第一峰值相比变化较小,且两个峰值均高于纯水中水分子的径向分布函数值。说明随着溶液中盐度的增加,离子水化程度增加,水分子高度定向排列;当盐度增加到一定程度后,离子争抢水分子反而导致水分子的定向排列程度减弱。离子水化作用随盐度的变化,影响了水分子的排布,从而影响非极性组分的疏水作用。
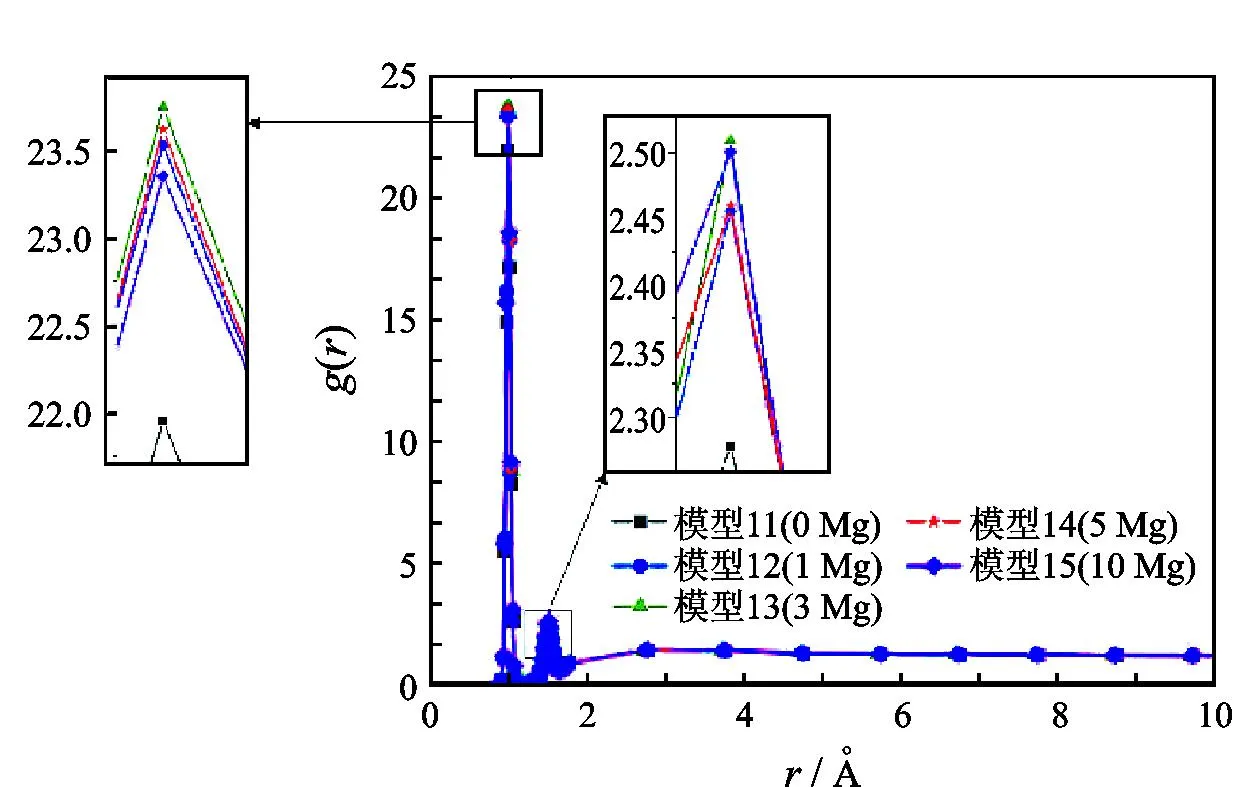
图8 水分子径向分布函数
3 机理分析
正戊烷属于非极性物质,水溶液为典型的极性溶液。非极性溶质在极性溶剂中因为疏水作用倾向于在水中聚集,形成疏水单元,使非极性分子存在一定的扩散空间。电解质离子的加入使得水分子在离子周围定向排布,水分子中的O原子倾向于向阳离子靠近,H原子倾向于向阴离子靠近。水分子受电解质离子的影响在离子周围聚集,这种聚集现象使水分子愈发远离非极性分子,造成非极性分子疏水单元的膨胀。非极性分子在体系中扩散空间的增加,使其在体系中扩散程度随之增加。随着体系中盐度进一步增加,体系中电解质离子数量大幅提升,离子水化效应使得电解质离子之间争抢水分子。水分子难以在离子周围稳定地定向排布,部分水分子在体系中重新回到游离状态。一方面,水分子脱离电解质离子的定向束缚,重新游离在体系中,压缩了非极性分子的扩散空间;另一方面,增加的电解质离子携带一部分所束缚的水分子,挤占了非极性分子的扩散空间,造成非极性分子扩散程度的降低。图9所示为盐度对正戊烷在水溶液中扩散的影响机理。图9(a)为正戊烷在纯水溶液中产生的疏水单元;图9(b)为低盐度溶液中,水分子在电解质离子周围定向聚集导致的疏水单元扩张;图9(c)为高浓度溶液中,体系中无序的水分子与携带水分子的电解质离子对疏水单元的压缩。
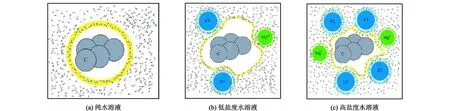
图9 盐度对正戊烷在水溶液中扩散影响机理
4 结 论
(1)通过分析MgCl2溶液中正戊烷的扩散情况,发现随着溶液盐度的增加,正戊烷液滴的面积扩张率呈现先增加后降低的趋势。说明正戊烷在水溶液中的扩散情况受溶液盐度的影响, 且存在转折盐度(0.5‰)使得扩散最强。
(2)使用分子动力学模拟常温常压下不同盐度MgCl2溶液中正戊烷的扩散情况,分析了不同分子间的径向分布函数的变化情况。盐度增加时,离子水化导致离子周围的水分子定向排布,影响正戊烷分子的疏水作用,使正戊烷分子组成的疏水单元周围出现可扩散的空腔,造成正戊烷分子扩散程度的增加。盐度进一步增加时,离子之间互相争夺水分子,水分子定向排布被打乱,可供正戊烷分子扩散的空腔缩小,减弱了正戊烷分子的扩散强度。
