基于FAERS数据库的丙酚替诺福韦和富马酸替诺福韦二吡呋酯不良事件信号挖掘与分析
2024-01-22李姜楠田雅兰
李姜楠,王 宇,宁 红,田雅兰
0 引言
目前,乙型肝炎病毒(Hepatitis B virus,HBV)在全球引发的公共卫生问题仍广泛存在,是肝脏肿瘤(Hepatocellular carcinoma,HCC)发展的重要危险因素[1]。世界卫生组织(WHO)估计每年新增HBV感染人数约150万,约82万人死于HBV感染并发症HCC或肝硬化[2-3]。目前,核苷(酸)类药物(NAs)是乙型肝炎抗病毒药物治疗的首要选择[4],其中,富马酸替诺福韦二吡呋酯(Tenofovir disoproxil fumarate,TDF)和丙酚替诺福韦(Tenofovir alafenamide fumarate,TAF)具有较强的抗病毒活性和较低的耐药率。《世界卫生组织(WHO)慢性乙型肝炎感染预防、关护和治疗指南》[5]、《中国慢性乙型肝炎防治指南(2019年版)》[6]、《美国肝病学会(AASLD)关于乙型肝炎指南》[7]均将上述两药列为抗HBV首选用药。TDF最早由Gilead Sciences(吉利德)公司研制,于2012年1月在美国获批上市,因其较好的抗病毒活性,在HBV的治疗中获得广泛应用[8]。TAF由Gilead Sciences公司于2016年推出,血浆稳定性较高,肝脏及淋巴细胞靶向性较强,有效降低给药后替诺福韦(Tenofovir,TFV)在全血中的平均暴露量,具有病毒抑制率高、病毒耐药率低、安全性好等特点。近年来,其临床使用率逐渐增加[9]。本研究应用数据挖掘技术对真实世界数据进行分析,研究两药不良事件特点,对其上市后的安全性进行初步评价,为临床合理用药提供参考。
1 资料与方法
1.1 资料来源 收集美国食品和药品监督管理局不良事件上报系统(FDA adverse event reporting system,FAERS)2017年第1季度至2022年第4季度共24个季度的数据。
1.2 数据处理 数据提取后剔除重复报告,筛选出药物名称为“tenofovir disoproxil fumarate”“VIREAD”“tenofovir alafenamide fumarate”“VEMLIDY”且为“首要怀疑(Primary suspect drug,PS)”的药物报告,并提取报告中患者年龄、性别、上报人职业、上报国家等信息。
1.3 信号挖掘方法 比例失衡法是药品不良事件信号挖掘主要方法之一,包括报告比值比法(Reporting odds ratio,ROR)与比例报告比值比法(Proportional reporting ratio,PRR)[10],本方法以比例失衡法四格表(表1)为基础。ROR法和PRR法具有计算简单、能估计相对危险度、计算结果一致性好等特点,但这两种方法的灵敏度较高,容易出现假阳性信号[11]。同时采用ROR与PRR两种方法可减少由于对照组的选择所带来的偏倚[12],因此,本研究同时采用这两种计算方法。两种方法的公式及阈值见表2[13]。

表1 比例失衡四格表
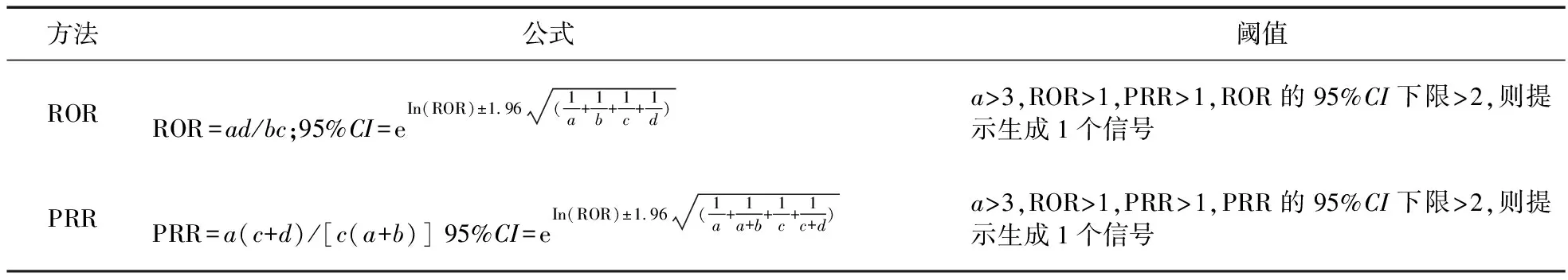
表2 ROR法及PRR法公式及阈值
1.4 信号分类方法 监管活动医学词典(Medical Dictionary for Regulatory Activities,MedDRA)由系统器官分类(System organ class,SOC)、高位组语、高位语、首选语、低位语5个层级构成,基本单位是首选术语PT(Preferred term,PT),用于对医疗事件进行划分和检索。本研究采用系统器官分类对挖掘出的药品不良事件进行整理。
2 结果
2.1 ADE上报情况 提取2017年第1季度至2022年第4季度药品不良事件(Adverse drug event,ADE)共27 770 559份报告,其中以TDF为首要怀疑药物的ADE报告175 960份,TAF为首要怀疑药物的ADE报告2 936份,具体见表3。
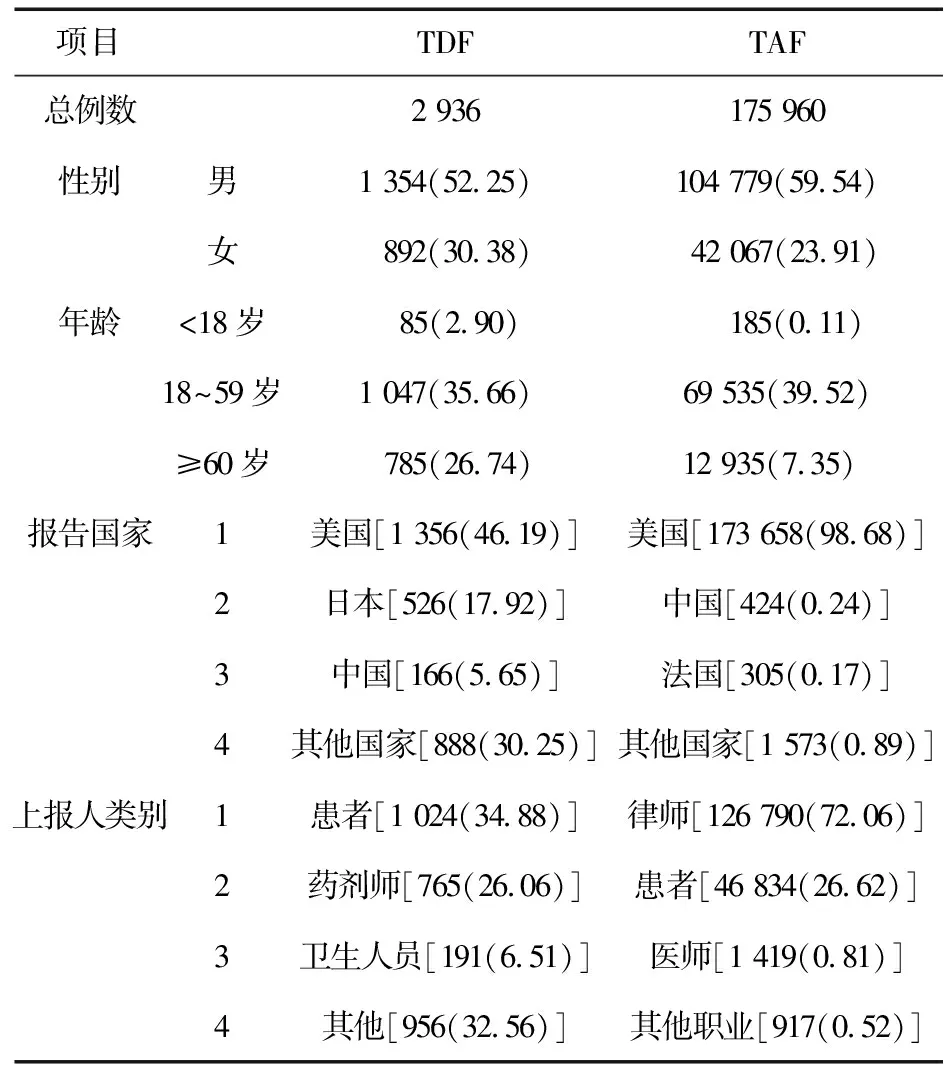
表3 TAF和TDF不良事件报告基本信息[例(%)]
2.2 ADE信号及说明书未收录的信号 将挖掘TAF、TDF的ADE信号按照报告信号响应强度值(PRR、ROR值)进行降序排列,获得报告信号响应强度值排名前25的ADE信号,见表4。对说明书未收录的TAF、TDF的较典型ADE信号,采用GraphPad Prism9.5.1绘制ROR值及其95%CI分布森林图,见图1。
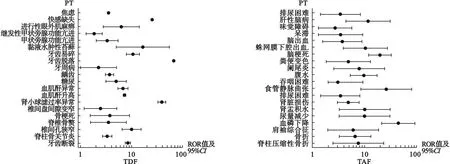
图1 两药说明书未收录信号分布森林图
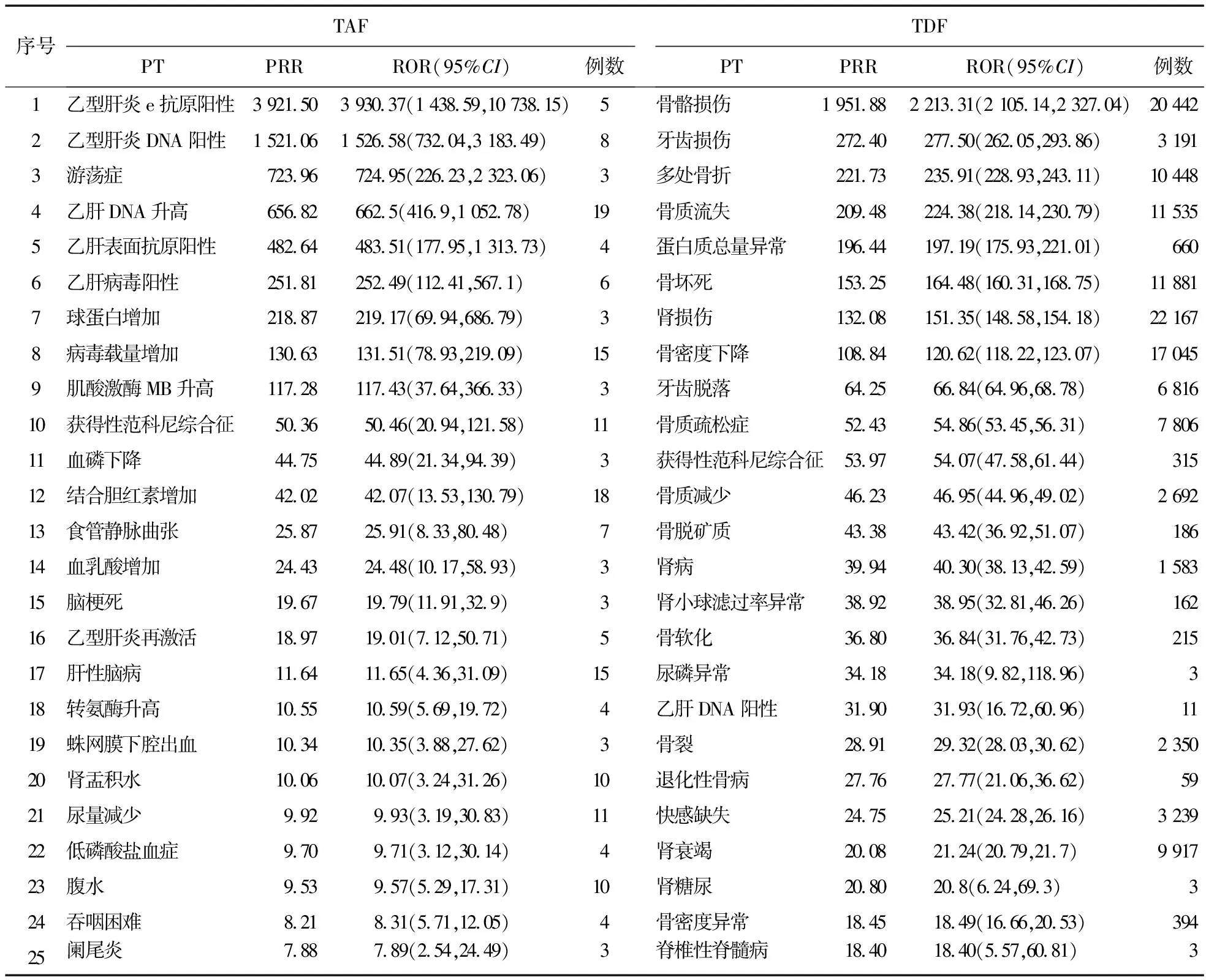
表4 TAF和TDF ADE信号强度前25位
2.3 TAF、TDF ADE信号主要SOC及重点系统可视图对比情况 采用MedDRA对两药不良事件信号进行主器官系统分类,其中,TDF关联12个主SOC,TAF关联15个主SOC,具体ADE信号主SOC占比情况见图2。对TDF和TAF的重点系统之间进行可视化对比,纳入标准:存在两药共同SOC分类,PT种类>3,PT总数>20。研究将两药符合纳入标准的SOC纳入ROR法中,计算得到两药重合系统各自ROR及95%CI,其中可视化对比两药在重点系统之间的差异,结果见图3。
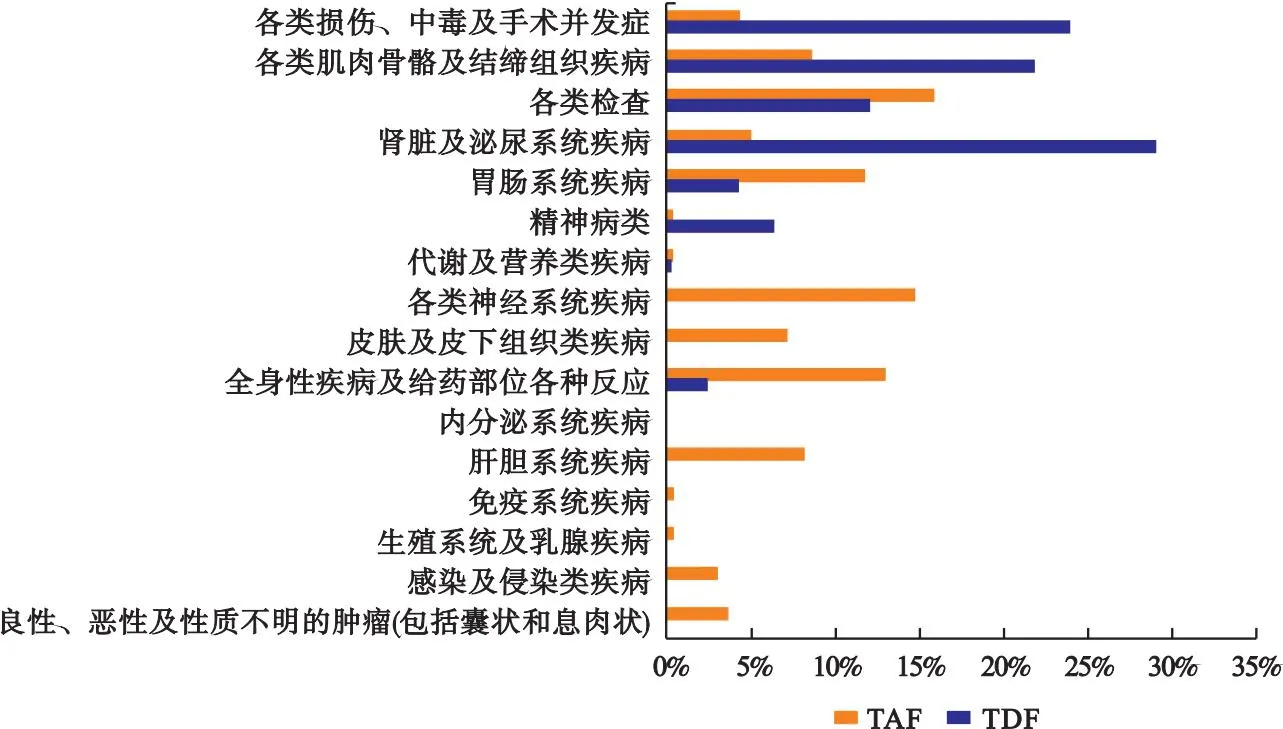
图2 TAF和TDF的ADE报告对应系统器官分类
3 讨论
3.1 两药各主系统间不良事件对比 肾脏系统ADE为TDF说明书中较常见的ADE,其中较严重的ADE为肾脏损伤、肾衰竭、终末期肾病等。本研究检测出TDF和TAF的肾脏系统ADE,但TDF在肾脏系统ADE数量占比(28.95%vs.4.94%)及SOC信号强度均高于TAF。TDF和TAF属于NAs类药物(由戊糖、碱基和磷酸构成),分子量较大,其在肾脏滤过速度较核苷类药物慢,容易在肾小管蓄积,具有一定肾脏毒性[14]。TAF的肾脏风险较TDF大幅降低,原因可能是TAF结构上增加酰胺键,降低了其降解物质在血浆中的浓度,增加肝脏靶向性,从而显著减少经由循环进入肾小管的药物含量[15]。尽管有研究显示,TAF的肾脏风险较TDF大幅下降,但在CrCl低于60 ml/min的患者中,其降解产物TFV的暴露风险明显增加[16-17]。同时,TAF药品说明书中提及,肌酐清除率(Creatinine Clearance,CrCl)≥15 ml/min但<30 ml/min的患者以及 CrCl<15 ml/min且正在接受血液透析的患者中,正常剂量富马酸丙酚替诺福韦片的药代学和药效学数据有限,结合本研究中两药均有肾脏系统ADE检出,提示对于重度肾功能不全患者,可能需要调整TAF剂量,且患者在使用TDF和TAF前后需密切监测肾功能,一旦出现问题,应及时停药并对症处理。
骨骼系统疾病是TDF上报数量最多、信号强度最强的ADE,其中较严重的为各种类型骨折、骨梗死、骨骼畸形等,可能对患者机体产生较为严重的不良影响,提示临床使用TDF时,需对患者做好用药交代,并密切监测骨骼相关检查指标。目前,TDF和TAF导致骨骼系统损伤的相关文献较少,其主要机制可能为肾小管损害继发的低磷血症引起骨骼形成减少和骨质破坏[18]。此外,两药均有血磷异常相关ADE检出。从图3可见,TAF在各类肌肉骨骼及结缔组织疾病的信号强度低于TDF,这与两药在肾脏损伤方面的风险相对应,与Fabbriciani等[19]研究结果一致,即TAF在骨骼和肾脏系统方面有较好的安全性,提示TDF患者在长期服药期间需要定期检测血磷水平和骨密度,对于本身存在骨骼系统疾病的患者,可优先选择对骨骼损伤风险更低的TAF。
两药的各类检查ADE中,有乙肝DNA阳性或乙肝DNA载量增加检出,其原因可能是NAs抗病毒作用机制是竞争性抑制HBV DNA复制,但无法有效抑制环状DNA分子(Covalently closed circular DNA,ccc DNA),或者由于HBV病毒出现耐药等因素影响[20],单一应用NAs抗病毒可能无法使全部患者达到病毒学应答,随着原发疾病进展或停药治疗后可能出现乙型肝炎急性恶化[21-22]。因此,HBV感染患者在服药过程中应当密切监测肝功能,在单一药物作用下治疗效果不佳的患者可考虑调整用药方案。
3.2 与药品说明书对比 两药中英文药品说明书中提及的不良反应与本研究检测获得的TAF和TDF的ADE信号基本一致,其中大部分安全信号与说明书不良反应相同,其与药物的药理毒性作用相关,体现了本次研究的可信度。TDF现有说明书未涉及内分泌系统疾病、各类神经系统疾病、新陈代谢和营养失调、精神病类、胃肠系统疾病等5个大系统分类。TAF现有说明书未涉及精神病类、生殖系统和乳腺疾病、新陈代谢和营养失调相关问题和良性、恶性及性质不明的肿瘤(包括囊状和息肉状)等5个大系统分类。上述药品说明书未涉及的系统器官安全信号提示临床观察到此类ADE时需警惕其与药品的相关性,对相关信号要及早发现,及时处理。同时,TDF说明书中皮肤及皮下组织类疾病和胃肠道疾病属于较为常见的不良反应,但本次研究未检测到相关安全信号,提示此类ADE还需更多的临床观察,并及时上报。从上述结果可见,两药现有的中英文说明书中涉及两药不良反应均不全面,故在临床用药过程中需密切关注可能的不良反应。
3.3 药品说明书未涉及的ADE信号分析 将本研究检测到的TDF和TAF相关ADE信号与两药说明书中提及的不良反应进行对比,获得TDF新的ADE信号41个,其中较为典型的有牙齿断裂、椎间孔狭窄、焦虑、甲状旁腺功能亢进、黏液水肿性苔藓;TAF新的ADE信号31个,包括乏力、横纹肌溶解、脑梗死、蛛网膜下腔出血、痴呆等,见图1。通过ROR法检测到信号强度较强的ADE信号,如TDF引发的牙齿脱落、椎间孔狭窄、快感缺失等,目前已有Jianfei等[23]观察到TDF致牙齿脱落1例;TAF引发的横纹肌溶解、脑梗死、蛛网膜下腔出血等,临床实际用药应密切关注上述相关症状。两药部分新的ADE信号与说明书中不良反应存在相关性,如TDF的椎间孔狭窄、牙齿断裂可能与药物相关骨质受损有关;另外,疾病自身进展也可能影响患者临床症状变化,导致错误上报药品不良事件,如TAF使用过程中出现的肝硬化、肝细胞癌等。
4 结论
研究显示,TDF的ADE发生较为集中,前4个SOC占比86.64%,提示TDF的ADE出现较为集中,临床可重点关注相关系统不良事件。TAF涉及的主要SOC为各类检查、各类神经系统疾病、全身性疾病及给药部位各种反应,前4个SOC系统占比55.05%,除了两药共有的SOC有信号外,在肝胆系统疾病、生殖系统和乳腺疾病、感染侵扰及良性、恶性和未特指的肿瘤也有ADE信号发现。提示TAF的ADE累及系统更广,尽管其他部位的信号强度不高,实际应用也不能忽视其重要性,因为随着时间推移,对信号强度的持续记录观察及ADE事件数量的积累,可能会发生药品不良反应事件显示为强烈信号的情况[24],临床使用中应注意偶见或罕见的ADE。研究显示,TAF克服了TDF部分缺点,在肾脏系统、骨骼系统显示出较好的安全性,且有研究表明,TAF和TDF在疗效方面作用相当[25],使用TAF进行抗HBV治疗,能够使更多的慢性乙型肝炎患者从抗病毒治疗中获益。
临床病例对照、队列研究等因受限于患者自身、研究方法或伦理等原因,导致研究样本量少,难以获取药品完整的安全性信息[25]。药品不良事件自发上报系统是对药品上市后临床用药的安全监测,可充分了解各药品不良事件[26]。本研究通过对FAERS数据库进行信号挖掘,获得了TAF、TDF药品不良事件在各个器官的分布,探索性地对比分析并评价两药SOC不良事件的差异,为临床合理选用两药提供了依据。本研究未考虑疾病本身及联合用药对安全信号的影响,FAERS中药品不良事件上报质量及信息完整性也会对研究结果产生影响。因此,药物与不良事件之间是否存在生物学联系,还需要进一步的研究和评估加以确定。
