临床药师参与IgA肾病合并糖尿病患者1例药学监护实践
2024-01-15金依依朱素燕徐萍
金依依,朱素燕,徐萍
IgA肾病是一种在肾小球系膜区以IgA或IgA为主的免疫复合物沉积,以肾小球系膜增生为基本组织学改变的肾小球性疾病。IgA沉积可损伤肾小球,引起炎性反应,导致肾脏内的血和蛋白质漏入尿液。随着时间的延长,损伤的肾小球可出现肾脏纤维化,最终导致终末期肾病,需进行肾脏移植或透析等肾脏替代治疗,给家庭和社会带来沉重的医疗负担。全球疾病负担报告提示,2017年因IgA肾病导致的终末期肾病患者人数10年增长22.7%。IgA肾病是1968年由法国学者Berger和Hinglais首先描述的,被认为是目前世界范围内最常见的原发性肾小球疾病[1]。流行病学调查显示,成人IgA肾病的发病率至少为2.5/100 000人每年,远高于其他类型的原发性肾小球肾炎[2]。IgA肾病也是我国最常见的肾小球疾病,调查显示,在亚洲人群中IgA肾病占原发性肾小球肾炎的45%[3-4]。IgA肾病的临床表现多样,其中20%的成年IgA肾病患者有高血压表现,约23%的IgA肾病可临床缓解,30%患者可存在不同程度的肾功能下降,若无有效干预,患病10~20年后,20%~40%的患者将进展至终末期肾病[5-6]。目前,研究人员尚未发现治疗IgA肾病的特异性治疗手段,现阶段以减少尿蛋白、对症降压及延缓疾病进展为进行综合支持治疗,但IgA肾病一旦出现肾脏纤维化,则难以修复。因此,IgA肾病治疗的最终目标是预防或延缓终末期肾病进展。本研究回顾临床药师参与1例IgA肾病伴糖尿病患者的诊疗过程,重点就降低尿蛋白、控制血压和血糖、控制免疫系统等治疗方案的安全性及有效性进行讨论分析,以期对IgA肾病伴糖尿病患者的药物治疗及药学监护提供参考,总结报道如下。
1 病例资料
患者女性,45岁,体质量74.7 kg,身高167 cm,主因“蛋白尿10个月,下肢水肿10 d”于2019年6月25日就诊于宁波大学附属第一医院泌尿内科。患者10个月前于当地医院体检时查尿常规提示“尿蛋白3+”,血生化提示“血肌酐91 μmol/L,尿酸494 μmol/L”,当时无泡沫尿,无血尿,无尿频尿急尿痛,无双下肢浮肿等不适,未予重视。10 d前无明显诱因下出现双下肢水肿,伴泡沫尿,前往当地医院就诊,查尿常规提示“尿蛋白3+,尿潜血3+”,血生化提示“血肌酐106 μmol/L,尿酸543 μmol/L,白蛋白34.8 g/L”,未予特殊治疗。患者为求进一步诊治,2019年6月24日于我院就诊,查尿常规提示“尿蛋白3+,潜血2+”,门诊以“肾炎综合征”收入院。
患者既往体健,否认肝炎病史与肺结核病史,否认“高血压、糖尿病、心脏病、脑血管病、肺病、肾病”史,否认药物过敏史,对虾过敏,反应为全身皮疹伴瘙痒,否认其他食物过敏史,否认手术、外伤、输血史,否认疫区、疫情、疫水接触史,否认中毒史,否认药物成瘾史,否认吸烟、饮酒史,否认传染病史,预防接种史不详。
入科查体:T 36.7 ℃,BP 145/100 mmHg,R 18 次/min。意识清楚,慢性病容,颜面部轻度水肿,双侧下肢轻度水肿,无皮疹、皮下出血、皮下结节、瘢痕。甲状腺未触及肿大,全身浅表淋巴结无肿大。颈软,颈动脉搏动正常,颈静脉无怒张,双肺呼吸音清晰,未闻及干湿性啰音。心率103 次/min,律齐,未闻及病理性杂音。腹平坦,腹部柔软,无压痛、反跳痛,腹部未及包块。肝脾肾未触及。肝浊音界存在,肾区无叩击痛。移动性浊音阴性。四肢肌力V级,双侧Babinski征阴性。
2 治疗经过
入院第1天(6月25日),患者入院诊断为:(1)慢性肾炎综合征;(2)高尿酸血症。尿常规提示:尿潜血3+,尿蛋白3+;血生化提示血肌酐98 μmol/L,经计算内生肌酐清除率为75.31 ml/min,尿酸547.9 μmol/L,两次24 h尿蛋白定量分别为2 134.6 mg/24 h和1 510.6 mg/24 h。患者血压127/90 mmHg,医嘱给予依那普利叶酸片5 mg口服,每天1次降尿蛋白治疗,同时给予非布司他片20 mg口服,每天1次降尿酸治疗,并行超声引导下经皮肾组织穿刺活检术。入院第5天(6月29日),患者肾功能复查结果提示血肌酐125 μmol/L,经计算内生肌酐清除率为59.04 ml/min。考虑患者住院期间血肌酐较前有所升高,故临床药师建议医师加强肾功能监测。医师采纳临床药师建议复查该患者肾功能水平。
入院第9天(7月3日),再次复查患者肾功能提示血肌酐156 μmol/L,经计算内生肌酐清除率为47.31 ml/min。临床药师考虑该患者应用依那普利叶酸片5 mg口服,每天1次治疗后血肌酐较基础值升高>30%,故建议医师减量应用依那普利叶酸片或停药。医师采纳临床药师建议停用该药。患者肾组织穿刺活检病理结果提示IgA肾病,轻、中度增生伴少数肾小球球性。医师修正诊断为IgA肾病,慢性肾脏病3期,同时加用糖皮质激素泼尼松片40 mg口服,每晨1次行免疫治疗。临床药师考虑该患者使用糖皮质激素且胃镜检查结果提示慢性萎缩性胃炎伴糜烂,故建议医师加用口服质子泵抑制剂治疗。医师采纳建议,给予泮托拉唑胶囊40 mg口服,每天1次。
入院第10天(7月4日),查血糖结果示:糖化血红蛋白6.7%,空腹葡萄糖6.27 mmol/L,餐后1 h血糖15.19 mmol/L,餐后2 h血糖11.47 mmol/L,餐后3 h血糖6.23 mmol/L。患者糖耐量试验显示符合糖尿病诊断标准,医嘱予二甲双胍片500 mg口服,每天2次联合阿卡波糖片50 mg口服,每天3次控制血糖。临床药师考虑患者目前诊断慢性肾脏病3期,且内生肌酐清除率为47.31 ml/min,二甲双胍的药品说明书记载中度(3 b级)和严重肾衰竭或肾功能不全(肌酐清除率<45 ml/min或肾小球滤过率<45 ml·min-1·1.73 m-2)者禁用二甲双胍,故建议医师停用二甲双胍,可继续使用阿卡波糖控制血糖。医师采纳临床药师建议,停用二甲双胍,继续服用阿卡波糖。
入院第11天(7月5日),患者出院,临床药师针对患者的出院带药做用药交代,并给予生活方式宣教,告知患者定期门诊随诊调整用药方案。患者住院期间药物治疗方案及出院带药情况,见表1。患者住院期间血肌酐情况,见表2。出院2周后(7月14日),患者在我院门诊随访复查肾功能,提示血肌酐116 μmol/L,较前好转。

表1 患者药物治疗方案
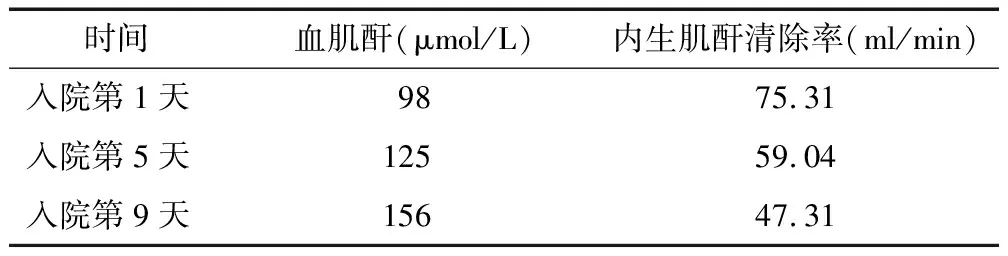
表2 患者血清肌酐水平
3 分析与讨论
3.1 非免疫抑制性治疗 原发性IgA肾病的病理机制还未完全阐明,目前被广泛接受的理论认为,IgA肾病是多种机制共同导致的,而非单一机制,被称为“多重打击假说”。IgA肾病的病变类型包括局灶节段性病变、毛细血管内增生性病变、系膜增生性病变、新月体病变及硬化性病变等。IgA肾病的临床表现形式较多,30%~40%的患者仅表现为尿检异常,可为无症状性蛋白尿和(或)镜下血尿,部分可伴有水肿和高血压;40%~50%的患者表现为肉眼血尿可伴有或不伴有咽炎、腹痛、腰痛、肌肉痛或低热,其中肉眼血尿合并咽炎是典型的临床综合征;10%以下的患者表现为肾病综合征或急进性肾炎综合征;罕见情况下,患者会发生急性肾损伤,这部分患者病理组织检测通常提示为新月体型IgA肾病[7]。肾活检显示显性或共显性系膜IgA染色是明确IgA肾病诊断的必要条件。光学显微镜下可显示出多种组织形态学改变,包括系膜基质扩张、系膜或毛细血管内细胞增生、纤维或纤维细胞新月体。
蛋白尿的定量和分型是IgA肾病病情判断、估计预后的关键因素。目前针对IgA肾病的治疗主要是对症支持治疗和免疫抑制治疗。其中肾素—血管紧张素系统的激活在慢性肾脏病的进展中起着重要作用,特别是肾脏局部肾素—血管紧张素系统活性的增强对IgA肾病的进展具有重要影响[8]。2021KDIGO临床指南指出,推荐对伴有蛋白尿(>1 g/d)的IgA肾病患者长期使用肾素—血管紧张素系统(RAS)阻断剂[血管紧张素转换酶抑制剂(ACEI)或血管紧张素Ⅱ受体拮抗剂(ARB)]治疗,目标血压为120/75 mmHg,蛋白尿<0.5g/d[9]。但大型Meta分析表明两者联合有较高的急性肾损伤和高钾血症风险。因此,不推荐IgA肾病患者联合使用ACEI和ARB。ACEI或ARB类药物用于控制血压和减缓肾病进展,其抗蛋白尿作用由降低肾小球内压及改善肾小球毛细血管壁的大小选择性介导[10]。该患者入院后尿常规提示:尿潜血3+,尿蛋白3+;两次24 h尿蛋白定量分别为2 134.6 mg/24 h和1 510.6 mg/24 h,考虑患者血压127/90 mmHg,故医嘱给予依那普利叶酸片5 mg(半片)口服,每天1次。使用ACEI类药物依那普利叶酸片降尿蛋白治疗时,患者血肌酐进行性升高。根据《中国高血压防治指南(2018年版)》推荐,血肌酐较基础值升高<30%时仍可谨慎使用,超过30%时可考虑减量或停药[11]。大量国内外文献和我国ACEI在肾病正确应用共识建议:用药初始2个月左右血肌酐可轻度上升(升幅<30%)者无需停药,但如用药过程中血肌酐升幅30%~50%甚至以上,提示肾缺血,应停用ACEI,若肾缺血被纠正且血肌酐恢复至用药前水平,才可再用ACEI[12]。入院第5天,患者肾功能复查结果提示血肌酐125 μmol/L,经计算内生肌酐清除率为59.04 ml/min。血肌酐较前有所升高,临床药师建议医师加强肾功能监测。入院第9天,再次复查患者肾功能提示血肌酐156 μmol/L,经计算内生肌酐清除率为47.31 ml/min。临床药师考虑该患者应用依那普利叶酸片5 mg口服,每天1次治疗后血肌酐较基础值升高>30%,故建议医师减量应用依那普利叶酸片或停药。患者出院后2周在我院门诊随访复查肾功能,提示血肌酐116 μmol/L,较前好转。
3.2 免疫抑制治疗 对于临床表现及病理类型均无特殊的IgA肾病,目前公认的治疗模式仍然是支持治疗模式,包括强化降压、RAS受体阻滞剂的治疗等[13]。对于经过上述治疗仍然出现持续性蛋白尿或肾功能进展的患者,考虑糖皮质激素治疗。2021KDIGO临床指南建议,对采用3~6个月合理的支持疗法(包括ACEI或ARB和控制血压)后蛋白尿仍持续≥1 g/d的患者给予6个月的皮质激素治疗[9]。
糖皮质激素可刺激胃酸分泌、导致骨质疏松、升高血压、引起糖耐量减低或血糖升高[11,14],故服用激素期间,监护患者血压、血糖变化情况,患者口服泼尼松片40 mg,每天1次,同时胃镜提示患者慢性萎缩性胃炎伴糜烂,考虑患者合并危险因素,故临床药师提醒医师给予质子泵抑制剂预防胃黏膜损伤,并密切关注患者有无胃肠道出血症状出现。
3.3 降糖治疗 《中国2型糖尿病防治指南(2020年版)》[14]指出,生活方式干预和二甲双胍应作为一线的治疗。在对患者进行生活方式干预的前提下给予降糖药物治疗,若无禁忌证,二甲双胍应一直保留在糖尿病的治疗方案中(A类推荐)。在一线治疗的基础上糖化血红蛋白仍>7%,可使用促泌剂、糖苷酶抑制剂、DPP4抑制剂、噻唑烷二酮(TZD)、SGLT2抑制剂等降糖药物。患者入院后查糖化血红蛋白6.7%,空腹葡萄糖6.27 mmol/L,餐后1 h血糖15.19 mmol/L,餐后2 h血糖11.47 mmol/L,餐后3 h血糖6.23 mmol/L。患者糖耐量试验显示符合糖尿病诊断标准,医嘱予二甲双胍片500 mg口服,每天2次联合阿卡波糖片50 mg口服,每天3次控制血糖。临床药师考虑患者慢性肾脏病3期,且内生肌酐清除率为47.31 ml/min,根据二甲双胍说明书,中度(3 b级)和严重肾衰竭或肾功能不全(肌酐清除率<45 ml/min或肾小球滤过率<45 ml·min-1·1.73 m-2)者禁用二甲双胍,建议停用二甲双胍,可继续使用阿卡波糖。
3.4 依那普利叶酸致肾功能损害的判断与评价 根据说明书,依那普利叶酸片有引起血清肌酐升高的不良发应,而该患者在使用上述药物后出现了血肌酐进行性升高,为判断药物与不良反应的相关性,临床药师采用诺氏评估量表来判断。诺氏评估量表是用于评估药物与不良反应因果关系的常用方法,通常用于评价和确定药物使用与不良反应之间的相关性,有利于确认和发现药物不良反应[15-16]。根据诺氏评估量表的评价结果[17],可将药物与不良反应之间的因果关系明确划分为“确定的”“很可能的”“可能的”“可疑的”4个类别。本病例中,临床药师通过诺氏评估量表评分为7分,根据评分,总分≥9分,表明该药物与不良反应的因果关系为肯定的,即具体客观证据及定量检测数据证实;总分5~8分为很可能有关,即具有客观证据或定量检测结果支持;总分1~4分为可能相关,即属于既不能够被充分证实,又不能够被完全否定的情况;总分≤0分为可疑的,即属于偶然或基本无关联的情况[18]。本例患者采用诺氏评估量表得出的总分值为7分,可判定为该不良反应与相关药物很可能有关,说明该患者血肌酐升高与依那普利叶酸相关。因此,临床药师及时建议医师停用可疑药物,并加强肾功能监测。最后,患者门诊随访时复查肾功能提示血肌酐较前有所下降。
4 药学监护
本例患者应用ACEI类药物依那普利叶酸进行非免疫抑制性治疗,治疗过程中,临床药师密切关注其用药的安全性。2021版的《KDIGO临床实践指南:慢性肾脏病患者的血压管理》指出,合并高血压的血压控制目标是收缩压<120 mmHg,强化降压治疗能够带来额外的心脏保护、生存和认知获益[9]。对于高血压合并慢性肾脏病患者降压药首选RAS阻断剂,包括ACEI、ARB,其不仅可以降压,还可以延缓某些肾脏病的进展和心脏病的发生。但在应用过程中可能会引起不良反应,包括高血钾和急性肾损伤,文献报道,应用ACEI时部分患者由于肾功能不全可出现快速、大幅度的血压下降或急性肾衰竭[12]。这可能超过了心血管和肾脏获益。使用RAS阻断剂后需要评估血压、血肌酐及血钾的变化。文献指出,应用ACEI血肌酐升高<35%(基线血肌酐值≤3 mg/dl)或绝对增高值<1mg/dl者可不改变治疗[12],如肌酐明显升高,就应停药或减量。但对双侧肾狭窄者应绝对禁用ACEI[12]。因此在该患者使用依那普利叶酸的过程中,临床药师密切监护患者血压、血钾水平和肾功能变化,同时监测患者是否发生咳嗽、血管性水肿等不良反应,同时告知患者在饮食上要限制钠盐摄入,每天盐摄入量保持在6 g以下,出院后需进行家庭血压监测。
患者使用糖皮质激素泼尼松进行免疫抑制治疗。糖皮质激素可刺激胃酸分泌、导致骨质疏松、升高血压、引起糖耐量减低或血糖升高[11,14]。故服用激素期间,临床药师监护患者血压、血糖变化情况,密切监测电解质防止出现低钾血症,并密切关注患者是否有胃肠道出血症状。该患者合并糖尿病,需每天监测空腹、餐后及睡前血糖,及时根据血糖监测结果调整降糖药物方案。告知该患者泼尼松片应每天清晨服用,餐后服用可以减少对胃黏膜的刺激。钙剂需于餐前1~2 h服用,以提高钙剂生物利用度。同时交代患者长期大剂量应用糖皮质激素会升高血浆胆固醇,激活四肢皮下脂酶,出现向心性肥胖,随着药量减少会逐渐改善。糖皮质激素在抑制炎性反应、减轻症状的同时,降低了机体防御功能,故长期应用会诱发或加重感染,必要时应给予有效、足量、敏感的抗菌药物。此外应注意使用糖皮质激素可能产生欣快感、激动情绪、食欲增加、失眠等表现,甚至出现精神和行为的改变。
患者应用阿卡波糖控制血糖,需每天监测空腹、餐后及睡前血糖,同时密切监测患者肾功能变化,及时根据血糖监测结果及肾功能调整降糖药物。
5 小 结
IgA肾病是一类慢性、进展性疾病,其临床表现、病理表现多样,预后差异性大,目前临床上尚缺乏有效的治疗方法。因此,考虑到IgA肾病的临床病程存在较大差异,决定治疗方法前,对患者疾病进展风险进行个体化评估显得至关重要。本病例中,临床药师积极参与患者的临床药物治疗,包括协助医师制订治疗方案,制订用药监护计划并进行每天药学查房,密切关注患者的病情变化和检查结果等。在该患者治疗过程中,药师重点关注患者IgA肾病治疗方案的制定,并运用药学专业知识,结合循证医学证据,积极参与临床治疗,协助临床医师选择安全、有效的治疗药物,发挥了临床药师在合理用药中的作用。用药期间,根据疾病及药物特点尤其关注患者血压、血糖、电解质及肾功能水平。该患者在使用ACEI类药物进行降尿蛋白时,血肌酐较基础值升高>30%,临床药师结合患者病情,权衡利弊建议停用依那普利叶酸。同时根据患者肾功能水平建议医师及时停用二甲双胍。患者出院时,临床药师对患者的出院带药进行了用药交代,并结合疾病进行了生活方式的宣教。本病例中,临床药师利用药学专业知识,参与临床诊疗,观察药物治疗的安全性及有效性,积极发挥临床药师的作用,为医师、患者服务,为临床合理用药提供参考。
利益冲突:所有作者声明无利益冲突。
