颈动脉超声造影联合高分辨核磁血管壁成像对缺血性脑卒中的预测诊断
2024-01-12李姝娜许晓华通信作者
王 燕,李 健,李姝娜,许晓华(通信作者)
(1 香港大学深圳医院超声医学科 广东 深圳 518053)
(2 香港大学深圳医院放射诊断科 广东 深圳 518053)
颈动脉粥样硬化斑块是缺血性脑卒中(cerebral ischemic stroke, CIS)的独立危险因素,除引起管腔狭窄外,不同性质的斑块对于CIS 发病的作用也不尽相同,易损斑块是指在颈动脉粥样硬化的基础上,具有破裂倾向、易发生血栓,迅速发展为责任病变的斑块,与缺血性脑血管病密切相关。随着诊断模式的不断更新,各种评估策略对不稳定斑块的正确识别变得至关重要。普通二维超声能对斑块进行适当的形态学评价,粗略地评估其稳定性,但是准确度和风险预测效力都有限。超声造影(contrast-enhanced ultrasound, CEUS)通过对斑块新生血管评价能够更准确地评估斑块稳定性,而且具有安全无辐射、实时评估、副作用少等优势[1]。高分辨核磁血管壁成像(high-resolution magnetic resonance vessel wall imaging, HRMR-VWI)可以清晰观察到血管壁的结构特点和斑块的具体组成成分等详细信息,计算标准化血管壁指数[2]。因此,本研究拟通过联合传统颈动脉超声、CEUS 及HRMRI-VWI 三项技术的诸多检测参数来进一步分析评估其对前循环CIS 发病的具体诊断效力。
1 资料与方法
1.1 一般资料
回顾性选取2021 年1 月—2023 年4 月在香港大学深圳医院就诊的由颈动脉粥样硬化斑块导致中、重度颈动脉狭窄患者42 例,其中男34 例、女8 例。所有患者均行颈动脉CEUS 及HRMRI-VWI 检测,同时收集患者的高血压、高血脂、高血糖、冠心病、吸烟等脑卒中相关危险因素。根据患者有无发生CIS 分成两组,脑卒中组28 例,以及非脑卒中组14 例。两组一般资料比较,差异无统计学意义(P>0.05),见表1。

表1 脑卒中组与非脑卒中组一般资料比较单位:例
纳入标准:①所有患者的颈动脉狭窄程度诊断均遵循《头颈部血管超声若干问题的专家共识(颈动脉部分)》标准[3];②急性CIS 诊断标准则遵循《中国急性缺血性脑卒中诊治指南2018》[4];③均签署知情同意书。排除标准:①颈动脉轻度狭窄及闭塞的患者;②对超声造影剂过敏以及不耐受磁共振检查患者;③心源性脑栓塞及其他非动脉粥样硬化性脑梗死患者。
1.2 方法
1.2.1 设备 超声检查采用飞利浦EPIQ 7 彩色多普勒超声诊断仪,采用高频探头[频率在(3 ~12)MHz]检查颈动脉。HRMR-VWI 检查采用西门子3.0T MRI 扫描仪,应用32 通道头颈联合线圈及优化的3D 可变翻转角度快速自旋回波T1 加权序列进行平扫和增强扫描成像。
1.2.2 颈动脉超声及造影检测 选取责任斑块并记录斑块位置、大小、回声、形状及血流等情况,经肘前静脉团注造影剂(六氟化硫微泡)2.0 mL,造影同时打开计时器,观察目标区域情况及增强变化过程2 ~3 min。
1.2.3 颈动脉高分辨率磁共振管壁成像检测 经肘部静脉注射钆特酸葡胺对比剂,剂量0.2 mmol/kg,注入完成后采用10 mL 0.9%氯化钠注射液对管道进行冲洗,随后进行扫描。
1.3 观察指标及评定标准
(1)比较两组血管结构参数,包括年龄、狭窄峰值流速(peak systolic velocity, PSV)、斑块处管腔原始内径(A)、颈内动脉相对正常内径(B)、颈动脉重构指数(carotid artery remodeling index, CRI)、血管外壁总面积(out wall area maximal lumen narrowing, OWAMLN)、管腔面积(lumen area maximal lumen narrowing, LAMLN)、病变层面管壁面积(wall area maximal lumen narrowing,WAMLN)、标准化管壁指数(normal wall index, NWI)等;比较两组超声造影分级;采用受试者工作特征(ROC)曲线分析CRI、颈动脉超声造影分级、NWI 对颈动脉中重度狭窄发生临床缺血症状的预测价值。
(2)重构指数(CRI)的测量:即颈动脉狭窄段最大原始管径与狭窄段以远无动脉粥样硬化累及的颈内动脉最大管径的比值。见图1。

图1 颈动脉重构指数测量方法
(3)超声造影分级:据中国颈动脉超声造影指南,颈动脉超声造影分级为,0 级:斑块无增强;Ⅰ级:斑块内有点状增强;Ⅱ级:造影后3 ~4 处点状增强,或1 ~2 条短线样增强;Ⅲ级:斑块内可见2 条以上线状增强,可贯穿或大部分贯穿斑块,或有血液流动征。见图2。
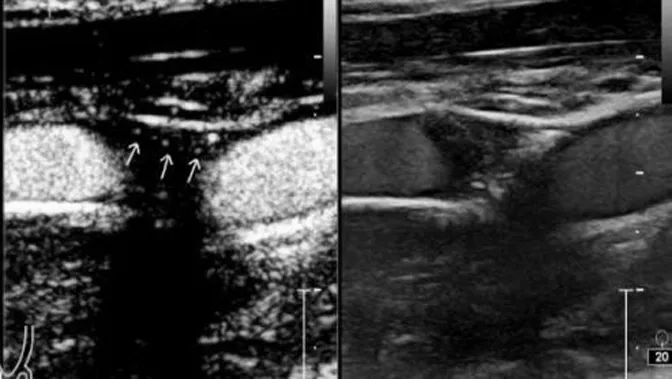
图2 颈动脉斑块造影显示斑块内可见多个造影微泡增强
(4)标准化血管壁指数(NWI)的测量:测量血管外壁总面积、管腔面积、病变层面管壁面积等数值,公式:NWI=病变层面管壁面积/血管外壁总面积。见图3。

图3 高分辨核磁显示责任斑块及血管管腔
1.4 统计学方法
采用SPSS 26.0 统计软件处理数据,符合正态分布的计量资料以均数±标准差(± s)表示,采用t检验;计数资料以频数(n)、百分率(%)表示,采用χ2检验,等级资料采用秩和检验。最后通过ROC 曲线分析确定各参数诊断急性缺血性脑卒中的效力以及最佳界值点,并绘制ROC 曲线图。以P<0.05 代表差异有统计学意义。
2 结果
2.1 两组血管结构定量资料的比较
两组年龄、PSV、B、LAMLN 比较差异不显著(P>0.05);两组A、CRI、OWAMLN、WAMLN、NWI 比较,差异有统计学意义(P<0.05),见表2。
表2 两组血管结构定量资料比较(± s)

表2 两组血管结构定量资料比较(± s)
组别 例数 年龄/岁 PSV/(cm·s-1) A/mm脑卒中组 28 71.07±4.01 247.00±108.01 8.14±0.87非脑卒中组 14 75.57±4.50 221.00±88.92 6.65±0.71 t 0.351 0.777 5.585 P 0.727 0.442 <0.001组别 例数 B/mm CRI OWAMLN/mm2脑卒中组 28 4.69±0.55 1.75±0.13 68.36±14.31非脑卒中组 14 4.48±0.46 1.54±0.12 45.53±9.57 t 1.217 4.966 5.383 P 0.231 <0.001 <0.001组别 例数 LAMLN/mm2 WAMLN/mm2 NWI脑卒中组 28 11.69±5.36 56.67±10.93 83.24±6.12非脑卒中组 14 15.18±6.02 31.65±9.60 65.46±5.54 t 1.911 7.269 9.148 P 0.063 <0.001 <0.001
2.2 两组造影分级的比较
两组超声造影分级比较,差异有统计学意义(P<0.05),见表3。
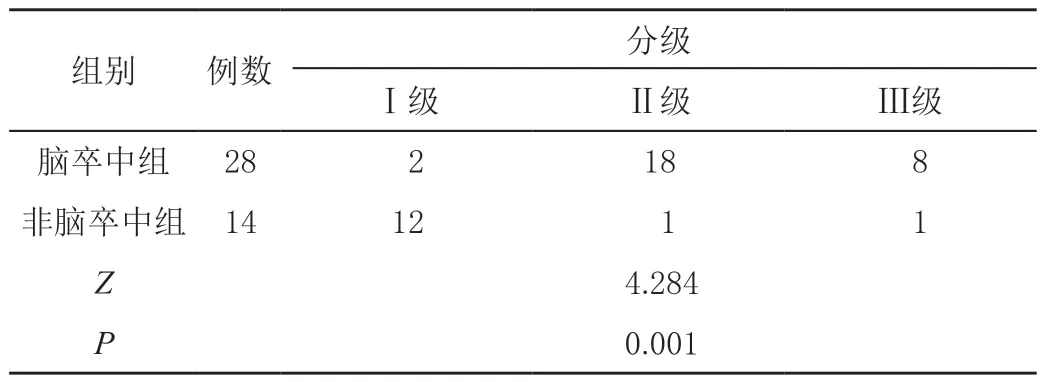
表3 超声造影分级情况比较 单位:例
2.3 ROC 曲线分析
ROC 曲线分析CRI、颈动脉超声造影分级、NWI 对颈动脉中重度狭窄发生临床缺血症状的预测价值见表4、图4 所示。

图4 ROC 曲线分析
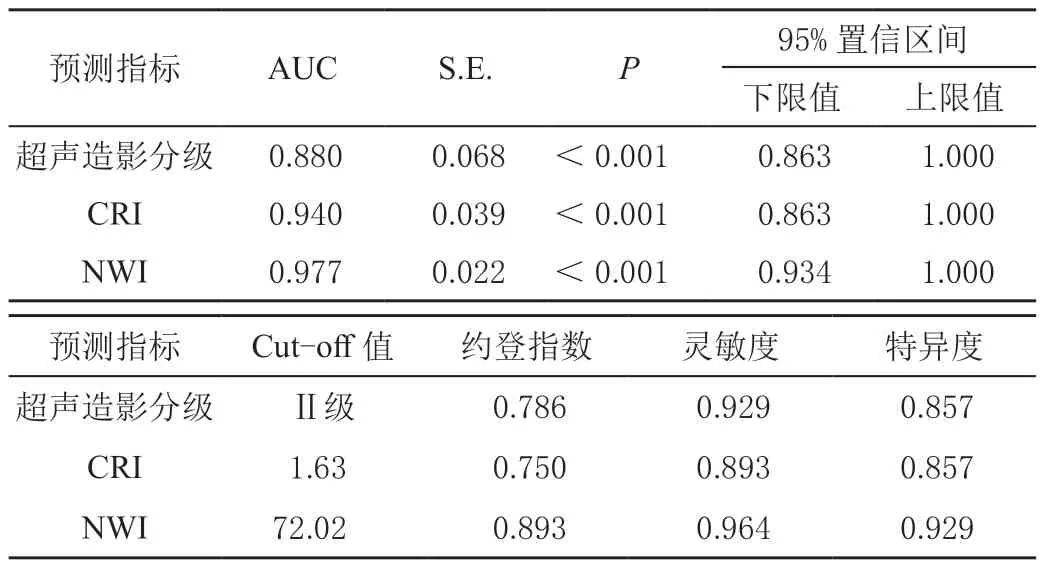
表4 超声造影分级、颈动脉重构指数、管壁标准化指数预测缺血性脑卒中的效力对比
3 讨论
颈动脉粥样硬化斑块引起的临床缺血事件不仅取决于狭窄程度,更取决于斑块的易损性。活动性炎症、薄纤维帽与大脂质核心、斑块破裂血栓形成、斑块内出血、血管壁正性重构等构成了易损斑块的高危特征,最终导致脑缺血终末事件的发生。
在动脉粥样硬化早期,血管可通过正性重构以维持动脉远段的供血,血管重构与斑块易损性密切相关。在本研究中颈动脉重构指数最佳界值为1.63,与先前研究(最佳界值为1.74)相比较数值偏小[5],考虑与病例数偏少有关,本次研究其诊断灵敏度和特异度都达到80%以上,CRI 可尝试预测颈动脉中重度狭窄患者临床缺血事件的发生。相比颈动脉超声造影和高分辨核磁,CIR的诊断效力稍弱,无论是特异度还是灵敏度都不如其他两种检测技术,这也正说明了传统超声诊断技术的临床局限性。
斑块内新生血管(intraplaque neovascularization,IPN)的存在是斑块不稳定的重要标志,而CEUS 斑块增强分级则是评估斑块内新生血管的关键指标。先前研究已经发现:CIS 患者的斑块造影增强强度明显高于非CIS 患者,且强化程度越高,CIS 发生风险越高[6]。王洁等[7]应用CEUS 评价脑梗死患者颈动脉硬化斑块内的新生血管分级情况发现:分级越高,患者NIHSS(美国国立卫生研究院卒中量表)评分越高。因此,斑块内的新生血管分级情况可作为脑梗死患者的病情危重程度及预后的重要预测指标。新近研究也证实:IPN 是近期缺血性卒中和颈动脉粥样硬化患者卒中复发的独立预测因子,而且IPN 可能是比颈动脉狭窄更早的预测指标,并有助于脑卒中复发的风险分层[8]。本研究也发现:超声造影分级是一项评估预测急性CIS 发病风险的有效参数(AUC = 0.880),而且超声造影分级Ⅱ级为其最佳诊断分界,诊断灵敏度高达92.9%,但缺点是特异度(85.7%)相对较低。这说明造影分级可作为一项足够敏感的早期评估指标来指导脑卒中的预防,但其对CIS 疾病结局特征的评估效力较弱。
先前研究应用三维对比HRMR-VWI 测量颈动脉管腔面积、管壁面积、管壁NWI 和信号强度等形态学参数预测诊断脑卒中患病风险的实际价值,并指出参数的联合应用其诊断效力更高[9]。本文研究更发现NWI 是一项综合效力最佳(AUC = 0.977)的诊断参数。尤其是在针对CIS 的诊断灵敏度、特异度分别达到96.4%、92.9%,可作为CIS 疾病预测的生物学特征指标。最近,研究者利用MR-VWI 分析发现双侧颈动脉斑块的生长和进展存在显著不对称性:与右侧颈动脉相比,左侧颈动脉斑块有更大的斑块负担、更高的脂质坏死核心和更大的斑块内出血体积,左侧颈动脉管壁NWI 更大,这些参数都将有助于大脑半球缺血性卒中偏侧化风险的预测评估[10]。
综上所述,本文研究初步证实了二维超声、CEUS及HRMR-VWI 的主要评估指标对于CIS 发病风险预测的有效性,以及各参数应用价值的具体差异。NWI灵敏度、特异度很高,可作为CIS 的特征性评估指标,值得临床应用。目前这方面的研究仍处于探索阶段,本文的研究病例数偏少,有选择偏倚,存在一定的不足,仍需要未来更大样本量的前瞻性研究来进一步地验证相关结论的真正意义。
