黄毛耳草总黄酮的提取工艺优化及有效成分的含量测定
2024-01-10金贤武何亚芬
金贤武,何亚芬
上饶市检验检测认证院药品检测分院,江西 上饶 334000
黄毛耳草(Hedyotis chrysotricha)又名敷地两耳草、地坎风、石打穿等,系茜草科耳草属植物金毛耳草Hedyotis chrysotricha(Palib.)Merr.的全草[1],收录于浙江、福建、江苏等地方中药材标准,主要分布于我国的浙江、江西、安徽、江苏、福建、湖南等地,是国药准字中药成方制剂肠炎宁片、伤湿丸的主要组方药材[2]。黄毛耳草味苦,性凉,归肝、胆、膀胱、大肠经,具有清热除湿、解毒消肿、活血舒筋的功效,临床上主要用于肾炎、肠炎、急性肝炎、跌打肿痛等疾病的治疗[3]。研究[4]显示,黄毛耳草主要含有黄酮、三萜、环烯醚萜苷、生物碱、甾醇等成分,具有防衰老、抗炎、抗菌、抗氧化、抗病毒、抗肿瘤等多种活性[5],是一味民间常用、价值较高的全草入药中药。
化学成分是中药发挥药效作用的物质基础。据报道,芦丁、烟花苷等黄酮类成分广泛存在耳草属植物中,具有较强的抗炎、镇痛、保肝及保护心脑血管等作用[6-7],可能是耳草作用于黄疸型病毒性肝炎、急慢性肾炎及肿瘤等疾病治疗的主要活性成分。目前,对于黄毛耳草黄酮类成分的提取工艺研究还相对较少,仅有学者通过正交法研究其提取与纯化工艺[8],还未有响应面法优化黄毛耳草总黄酮提取工艺及HPLC 法同时测定多个黄酮类成分的相关研究报道。本试验以黄毛耳草为研究对象,应用Box-Behnken 响应面法对黄毛耳草中总黄酮的提取工艺进行优化,采用HPLC 法测定黄毛耳草中芦丁、烟花苷的含量,以期为黄毛耳草资源的深入开发利用奠定基础。
1 仪器与试药
1.1 仪器
UV5500 紫外光度计(上海元析仪器有限公司);Agilent1260 高效液相色谱仪(Agilent 公司);Sartorius BS-124S 电子天平(德国赛多利斯公司);FW100 高速万能粉碎机(泰斯特仪器有限公司);优普超纯水仪(四川优普超纯科技有限公司)。
1.2 试药
对照品芦丁(批号111081-201202,纯度>98%),烟花苷(批号111683-200401,纯度>98%)购自中国食品药品检定研究院。乙腈为色谱纯,其余试剂均为分析纯。黄毛耳草购自溪福草药铺,经上饶市检验检测认证院药品检测分院彭任辉副主任药师鉴定为黄毛耳草的全草。
2 方法与结果
2.1 黄毛耳草总黄酮提取工艺优化
2.1.1 标准曲线的绘制 精密称取芦丁对照品12.68 mg,置100 mL 量瓶中,加入70%乙醇并定容至刻度,制得质量浓度为126.8 μg/mL 的对照品溶液。参照文献[9]方法,绘制芦丁的标准曲线,得芦丁回归方程为A=0.136 2C-0.002 4(r=0.999 7),表明芦丁在0~63.4 μg/mL 的质量浓度内与吸光度呈良好线性关系。
2.1.2 样品含量的测定 精密称取干燥粉碎后的黄毛耳草粉末1.0 g,置100 mL 具塞锥形瓶中,精密加入提取溶液,称定重量后超声提取,放冷,再称定重量,用提取溶液补足减失的重量,滤过,得供试品溶液。取1.0 mL 供试品溶液按“2.1.1”项下方法测定吸光度并计算总黄酮得率。总黄酮得率(%)=(A+0.002 4)×V×100/(0.136 2×m×1 000)。式中:A为吸光度值;V为提取液体积;m为样品质量。
2.1.3 响应面设计 在文献[9]报道的研究基础上,选择乙醇浓度、提取时间、液料比3 个因素为设计因素,设计黄毛耳草总黄酮提取条件,设计方案和所得的结果见表1 和表2。

表1 Box-Behnken试验设计因素与水平表

表2 响应面设计与结果
2.1.4 方差分析 Box-Behnken 响应面法所得的方差分析结果见表3。结果显示,黄毛耳草总黄酮得率对乙醇浓度、提取时间、液料比3 个因素的回归方程为:Y=12.53+0.11A+0.33B+0.28C-0.078AB+0.042AC+0.027BC-1.26A2-1.27B2-0.70C2。本试验所建立的模型得P值为0.005 9(P<0.001),差异有统计学意义;失拟项P值为0.119 7(P>0.05),差异无统计学意义,所建立的模型拟合程度良好,回归可靠。此外,二次项中A2、B2、C2的P值均小于0.000 1,均差异有统计学意义
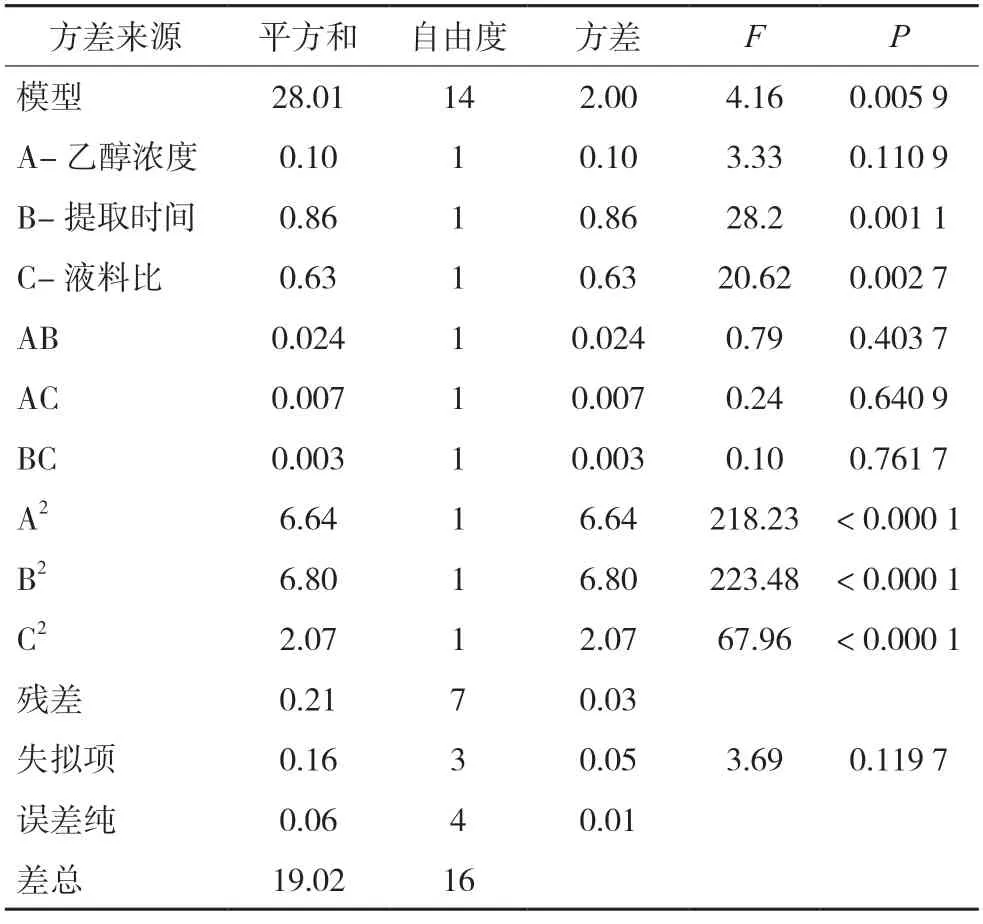
表3 方差分析结果
2.1.5 响应面分析 通过Design-Expert 9.0.4 软件绘制考察指标黄毛耳草总黄酮得率与自变量乙醇浓度、提取时间、液料比之间的等高线图,具体结果见图1。结果显示,黄毛耳草总黄酮的最佳提取工艺为:乙醇浓度70.44%、超声时间46.95 min、料液比12.41∶1,总黄酮预测得率12.59%。

图1 不同因素间的响应曲面图
2.1.6 验证试验 为便于操作,修正预测条件为:乙醇浓度70%、超声时间47 min、料液比12.5∶1,以此条件平行3 次提取黄毛耳草总黄酮,结果平均得率为12.62%,与预测得率12.59%无明显差异,表明拟合良好,所优化的工艺稳定可靠。
2.2 HPLC 法测定芦丁和烟花苷含量
2.2.1 对照品溶液的制备 精密称取芦丁和烟花苷对照品适量,置50 mL 量瓶中,加70%甲醇溶解,定容,摇匀,得浓度分别为352.6、68.4 μg/mL 的混合对照品溶液。
2.2.2 供试品的制备 取粉碎后的黄毛耳草药材1.0 g,置50 mL 具塞锥形瓶中,精密加入10 mL 的70%甲醇,称定重量,超声提取45 min,放冷,再称定重量,补足减失的重量,摇匀,滤过,即得。
2.2.3 专属性试验 采用Agilent Extend C18 色谱柱(4.6 mm×250 mm,5 μm);以甲醇(A)-0.5%甲酸溶液(B)为流动相进行梯度洗脱(0~20 min,35%→60%A;20~302 min,60%→68%A);检测波长为360 nm;流速为1.0 mL/min。分别取10 μL混合对照品溶液和供试品溶液进行分析,结果如图2 所示,各成分之间分离较好。
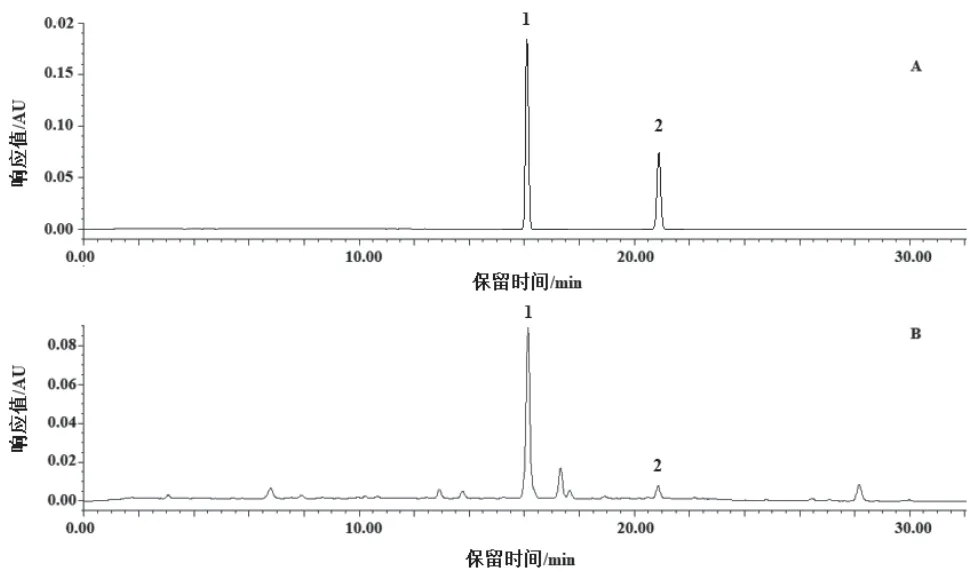
图2 HPLC色谱图:A.对照品;B.黄毛耳草
2.2.4 线性关系 精密吸取0.1、0.5、1.0、2.0、5.0、10.0 mL“2.2.1”项下的混合对照品溶液,置10 mL容量瓶中,加70%甲醇定容至刻度。按“2.2.3”项下色谱条件测定,以浓度X 对峰面积Y 进行回归计算,结果芦丁、烟花苷在质量浓度3.526~352.6、0.684~68.4 μg/mL 范围内与峰面积呈良好的线性关系,回归方程分别为Y=32 174X+332.6(r=0.999 7)和Y=10 211X+126.5(r=0.999 3)。
2.2.5 精密度试验 取干燥粉碎后的黄毛耳草药材1.0 g,按“2.2.2”项下方法制备供试品溶液,按“2.2.3”项下色谱条件测定,重复进样6 次。结果芦丁、烟花苷的峰面积RSD 分别为0.84%、1.25%,表明仪器精密度良好。
2.2.6 稳定性试验 取供试品溶液,按“2.2.3”项下色谱条件分别在0、2、4、8、12、24 h 进样分析。结果芦丁、烟花苷的峰面积RSD 分别为1.83%、1.02%,表明供试品溶液24 h 内稳定。
2.2.7 重复性试验 取干燥粉碎后的黄毛耳草药材6 份,各1.0 g,按“2.2.2”项下方法制成供试品溶液,按“2.2.3”项下色谱条件测定,计算峰面积RSD。结果芦丁、烟花苷的峰面积RSD 分别为1.29%、2.37%,表明重复性良好。
2.2.8 加样回收试验 取干燥粉碎后的黄毛耳草药材6 份,每份约0.5 g,精密称定,加入适量的芦丁、烟花苷对照品,再按“2.2.2”项下方法制备加样回收供试品溶液,测定其含量并计算回收率,结果见表4。

表4 加样回收率试验
2.2.9 含量测定 取干燥粉碎后的黄毛耳草药材,按“2.2.2”项下方法平行制备3 份供试品溶液,吸取10 μL 注入HPLC 测定芦丁和烟花苷的含量。结果测得黄毛耳草中芦丁的含量为0.74 mg/g,烟花苷的含量为0.058 mg/g。
3 讨论
正交试验法和响应面法是目前药物有效成分提取工艺优化的主要应用方法。有学者通过正交法对黄毛耳草的总黄酮提取工艺进行了优化,但相比于正交法只是试验所用水平的某一种组合,响应面法可通过多项拟合直观地分析出各个因素之间交互关系,结果更精密准确,因此,本试验选择采用响应面法优化黄毛耳草的总黄酮提取工艺。
黄毛耳草中主要含有黄酮、三萜、环烯醚萜苷、生物碱等类成分,其中黄酮类成分包括芦丁、烟花苷、槲皮素、水仙甙等,是黄毛耳草作用于黄疸型病毒性肝炎、急慢性肾炎及肿瘤等疾病治疗的主要活性成分[9]。对于其有效成分黄酮类的含量测定主要是测定芦丁或者槲皮素的含量[10]。本试验选择以芦丁和烟花苷为指标性成分,建立了其HPLC 含量测定方法。
本研究采用Box-Behnken响应面法试验设计法,首次对黄毛耳草的总黄酮提取工艺进行了优化,得到了操作简便、提取率高、预测性好的提取方法。同时,还建立了准确可靠、操作简便、重现性高、稳定性好、专属性强的黄酮类成分HPLC 含量测定方法,为黄毛耳草的质量控制标准提升完善提供了依据。
