阿那曲唑与他莫昔芬治疗肥胖的激素受体阳性绝经后乳腺癌的效果对比研究
2024-01-10高华谭艳红胡韶军
高华,谭艳红,胡韶军
苏州市第九人民医院药剂科,江苏苏州 215200
乳腺癌对妇女身心健康有重要危害,其发病风险与多种因素有关,包括绝经、乳头溢液、饮食重盐、家族史、长期不良情绪等[1-3]。因此,有必要加强绝经后乳腺癌患者的早期诊治,降低其死亡风险。内分泌治疗是雌激素受体( estrogen receptor,ER)阳性病例的有效治疗方法,可增加患者的生存率,但实际治疗过程仍需注意肥胖因素以及耐药问题等对预后产生的负面影响。他莫昔芬是乳腺癌患者手术治疗后常见辅助用药,可预防疾病复发,延缓肿瘤的转移,但有研究提示,单纯给予他莫昔芬治疗的作用有限[4]。阿那曲唑适用于绝经后病例的辅助治疗,可有效改善雌激素水平过高等问题,并抑制乳腺肿瘤的生长。本研究以回顾性分析方式,选取2022年6月—2023年1月苏州市第九人民医院收治的92例ER阳性绝经后乳腺癌患者为研究对象,对两种药品的应用效果进行比较,重点讨论其在伴有肥胖因素病例中的应用价值。现报道如下。
1 资料与方法
1.1 一般资料
回顾性分析本院收治的92 例ER 阳性绝经后乳腺癌患者的临床资料。根据用药方案进行分组,两组患者一般资料对比,差异无统计学意义(P>0.05),具有可比性。见表1。

表1 两组患者一般资料比较
1.2 纳入与排除标准
纳入标准:符合《中国抗癌协会乳腺癌诊治指南与规范(2021年版)》[5]相关诊断标准,且经病理诊断证实;停经时间>1年;合并肥胖,判断标准为体质指数(body mass index, BMI)≥25kg/m2;ER 阳性;给药前未使用托瑞米芬等药品;服药时间>6 个月;临床资料完整。
排除标准:合并其他恶性肿瘤者;伴严重器官实质性病变者;用药依从性差者。
1.3 方法
对照组口服他莫昔芬片(国药准字H32021472;规格:10 mg),10 mg/次,2 次/d。
观察组口服阿那曲唑片(国药准字H20050328;规格:1 mg),1 mg/次,1 次/d。
两组持续用药6 个月以上。
1.4 观察指标
比较两组疗效、性激素指标、血脂指标与不良反应。疗效参考实体瘤疗效评价标准(Response Evaluation Criteria in Solid Tumors 1.1,RECIST1.1)[6],病灶完全消失,则为完全缓解(complete response, CR);病灶缩小≥50%,且复查时无新病灶,则为部分缓解(partial response, PR);病灶缩小<50%,或增大<25%,且无新病灶,则为无变化(no change, NC);病灶增大>25%,或发现新病灶,则为疾病进展(progressive disease, PD)。总有效=PR率+CR 率。性激素指标包括雌二醇(estradiol, E2)、黄体生成素(luteinising hormone, LH),采集空腹静脉血8 mL,放射免疫法进行测定。血脂指标包括三酰甘油(triglyceride, TG)、总胆固醇(total cholesterol,TC),采血方法同上,采用比色法检测。不良反应类型包括头痛头晕、皮肤潮红等,计算总发生率。
1.5 统计方法
采用SPSS25.0 统计学软件处理数据,符合正态分布的计量资料以(±s)表示,行t检验;计数资料以例数(n)和率(%)表示,行χ2检验,P<0.05 为差异有统计学意义。
2 结果
2.1 两组患者疗效比较
观察组总有效率高于对照组,差异有统计学意义(P<0.05)。见表2。
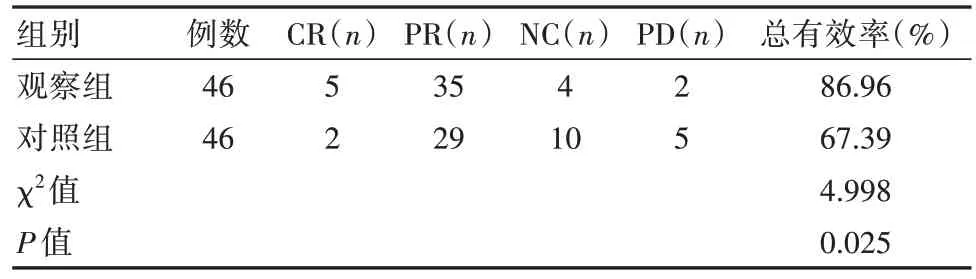
表2 两组患者疗效比较
2.2 两组患者性激素指标比较
治疗前两组E2、LH 水平比较,差异无统计学意义(P>0.05);治疗后观察组E2、LH 水平低于对照组,差异有统计学意义(P<0.05)。见表3。
表3 两组患者治疗前后性激素指标比较(±s)
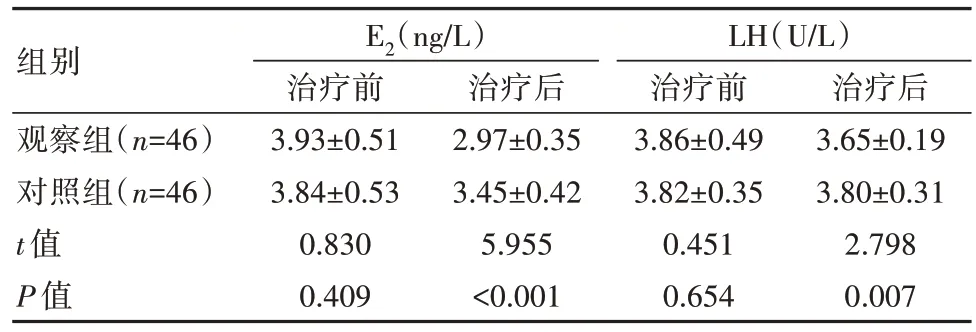
表3 两组患者治疗前后性激素指标比较(±s)
组别观察组(n=46)对照组(n=46)t 值P 值E2(ng/L)治疗前3.93±0.51 3.84±0.53 0.830 0.409治疗后2.97±0.35 3.45±0.42 5.955<0.001 LH(U/L)治疗前3.86±0.49 3.82±0.35 0.451 0.654治疗后3.65±0.19 3.80±0.31 2.798 0.007
2.3 两组患者血脂指标比较
治疗前,两组TG、TC 水平比较,差异无统计学意义(P>0.05);治疗后,观察组TC 水平高于对照组,差异有统计学意义(P<0.05)。见表4。
表4 两组患者治疗前后血脂指标比较[(±s),mmol/L]
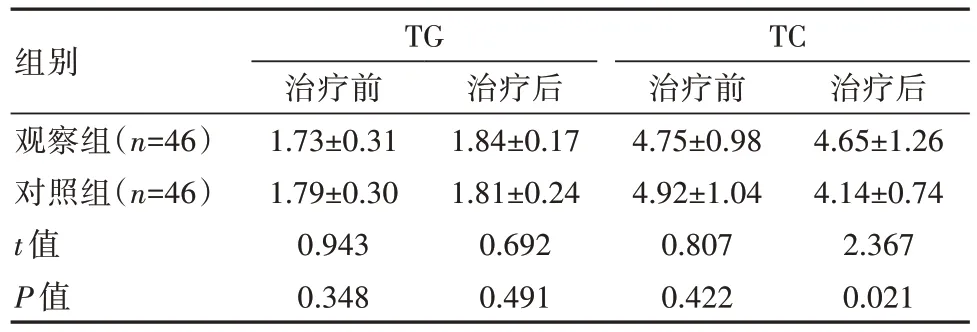
表4 两组患者治疗前后血脂指标比较[(±s),mmol/L]
组别观察组(n=46)对照组(n=46)t 值P 值TG治疗前1.73±0.31 1.79±0.30 0.943 0.348治疗后1.84±0.17 1.81±0.24 0.692 0.491 TC治疗前4.75±0.98 4.92±1.04 0.807 0.422治疗后4.65±1.26 4.14±0.74 2.367 0.021
2.4 两组患者不良反应发生率比较
两组不良反应发生率比较,差异无统计学意义(P>0.05)。见表5。
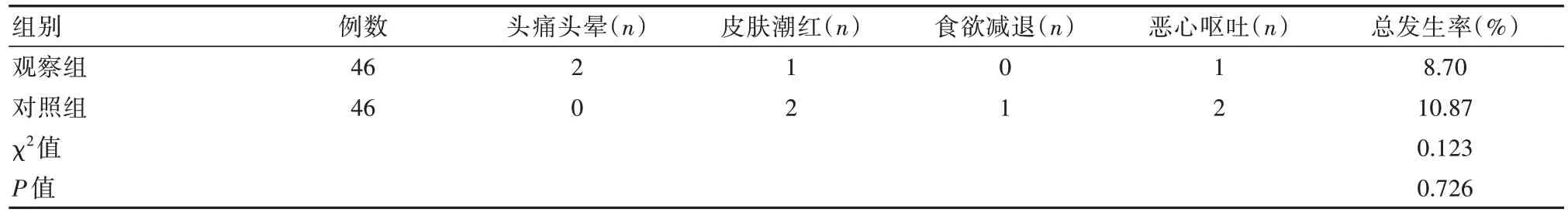
表5 两组患者不良反应发生率比较
3 讨论
积极开展乳腺癌早期诊治工作,根据筛查数据与临床诊断结论,尽早给予规范治疗,能够降低乳腺癌发病对妇女身心健康造成的危害,改善其生存质量。绝经后患者的年龄普遍较大,受慢性疾病、恶性肿瘤、生理功能减退等多种因素的影响,患者体质偏弱,对术后放化疗的耐受情况较差,故在确认ER 阳性后,多选择内分泌治疗作为辅助医疗方案,如应用他莫昔芬[7]、阿那曲唑[8-9]等药物。
本研究对两种常用药物在肥胖病例中的应用价值进行比较,根据RECIST 1.1 中的相关标准,对持续用药6 个月后的效果进行评价,结果显示,观察组达到CR、PR 标准的例数分别为5 例与35 例,总有效率为86.96%;与之相比,对照组达到CR、PR标准的例数仅2 例、29 例,总有效率为67.39%,观察组更高(P<0.05)。该结果表明,辅助应用阿那曲唑的效果优于他莫昔芬,对肥胖病例的病情控制有更加显著的作用。现阶段关于两类药品用于肥胖病例的报道较少,参考童刚领等[10]研究得出的结论,在ER 阳性转移性乳腺癌治疗中,阿那曲唑组的CR率、PR 率分别为73.08%、23.07%,他莫昔芬组的CR率、PR 率分别为33.33%、37.50%,前者的临床疗效更加显著,与本文结论一致。分析上述差异的原因,可能与两类药品作用机制的差异性有关。王帅兵等[11]指出,他莫昔芬对ER 阳性病例的疾病控制有重要价值,但其本身的抗肿瘤作用较弱,需要经过体内代谢发挥相应作用效果。激素水平改变与乳腺癌患者的病情有关,既往常将其作为疗效评估的参考指标[12]。本研究中,观察组E2、LH 水平分别为(2.97±0.35)ng/L、(3.65±0.19)U/L,明显低于对照组。王华龙等[13]指出,阿那曲唑组的E2水平为(2.86±0.37)ng/L,低于他莫昔芬组的(3.83±0.55)ng/L;阿那曲唑组的LH 水平为(3.68±0.26)ng/L,低于他莫昔芬组的(3.88±0.29)U/L,与本文结论一致。对肥胖病例,血脂指标的监测具有重要意义,尤其是TG、TC 等重要指标异常升高,可能提示患者存在血管病变风险。本研究中,两组治疗后TG 水平分别为(1.84±0.17)mmol/L、(1.81±0.24)mmol/L,与治疗前比较无明显变化,但观察组TC 水平高于对照组(P<0.05)。该结果提示,他莫昔芬在控制血脂指标方面具有优势。本研究中,两组病例涉及的不良反应主要为头晕头痛、皮肤潮红等,提示药品的安全性良好,与既往报道一致[14-15]。
综上所述,伴有肥胖病例的绝经后乳腺癌患者治疗难度较大,在确认ER 阳性并具备常规内分泌治疗条件的情况下,优先考虑应用阿那曲唑,有望取得较满意的治疗效果。
