增加骨密度鹿骨片保健食品的功能学和安全性评价
2024-01-08张悦李珊珊孙印石孙德水霍晓慧
张悦,李珊珊,孙印石,孙德水,霍晓慧
(中国农业科学院特产研究所,吉林 长春 130112)
鹿骨为梅花鹿(Cervus nipon)或马鹿(Cervus elaphus)等鹿科动物的骨头,是中国传统的动物药材之一。《本草纲目》记载鹿骨有“主内虚,续绝伤,补骨除风”等功效。《唐本草》中记载鹿骨可“主虚劳,可为酒。主风虚,补骨髓”。现代研究表明,鹿骨中含有骨胶原、蛋白质、软骨素、磷脂质和磷蛋白等成分,能够促进骨形成以及体内胶原蛋白和弹性蛋白的更新,抑制骨吸收,促进软骨内骨化[1]。李倩等[2]对鹿骨中的Ca、Na、Mg、K、Fe、Al 及Ag 等19 种元素进行了含量测定,结果表明鹿骨中的常量元素钙的含量较高,鹿骨可作为钙补充剂进行开发利用。
随着人类老龄化社会的到来,骨质疏松发病率呈逐年上升趋势,越来越多的人意识到补钙的重要性[3]。骨质疏松症是一种以骨量减少和骨结构钙破坏为特征,导致脆性骨折风险增加的一种疾病,在儿童、老年人和绝经后的妇女中最为常见[4]。Calvo 认为,美国绝经妇女患有骨质疏松疾病的原因是由于磷酸钙分解,血清中磷元素增加[5]。目前研究认为,成骨量少为主要因素,同时与体重、遗传和运动等因素也息息相关[6,7]。近几年FDA 批准了阿仑膦酸钠、激素替代疗法作为治疗骨质疏松症的主要策略,但其临床试验中心肌梗塞、中风和心血管死亡等风险增加,严重限制了其广泛应用。Mullard[8]和彭斯伟等[9]对单味中药的抗骨质疏松作用和机制进行了综合阐述,并在研究中逐渐发现中药是治疗骨质疏松症安全有效的药物。鹿骨作为传统的动物药材,含有较高的钙含量及营养成分,但在治疗骨质疏松症方面并未广泛应用。因此,本研究参考了《保健食品检验与评价技术规范》(2003 版)中的“增加骨密度功能检验方法”,建立了低钙动物模型,以碳酸钙干预作为阳性对照组[10],对本课题组自主研发的保健食品“鹿骨片”的功能学检测及安全性进行了评价,以期为该产品的进一步开发提供数据支持。
1 材料与方法
1.1 药品与试剂
鹿骨片为中国农业科学院特产研究所特种动植物加工团队研制。产品主要由鹿骨粉、维生素D3和辅料组成,规格为0.8 g/片,每次2 片,每日2 次。产品中鹿骨粉含量为62.5 g/100 g,钙含量为12.53 g/100 g,维生素D3含量为306.67g/100 g。普通饲料、低钙饲料由北京科奥协力饲料有限公司生产,其中普通饲料的钙离子含量为1.22%,低钙饲料配方,见表1。碳酸钙为食品级,其余试剂均为国产分析纯。
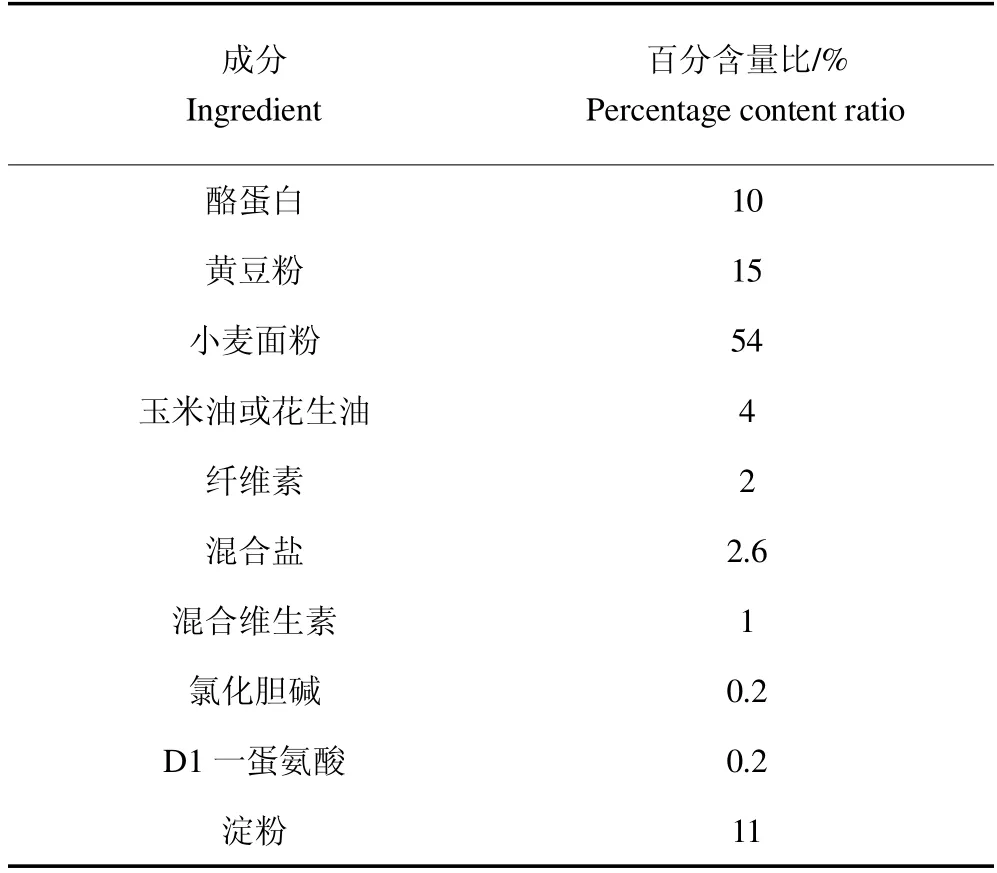
表1 低钙饲料配方Table 1 Low calcium feed formulation
1.2 试验动物
选用辽宁长生生物技术股份有限公司繁殖的清洁级Wistar 健康雄性大鼠48 只,体重为132~159 g,生产许可证SCXK(辽)2018-0001,试验动物在温度20~25 ℃、相对湿度为40%~70%的环境中饲养。
1.3 仪器
电子天平、722S 分光光度计、全自动生化分析仪(美国贝克曼BECKMAN COULTER AU680)、血乳酸分析仪(英国Analox EKF Lactate scout)、高速台式离心机(上海安亭TGL-16G)。
1.4 增加骨密度试验方法
1.4.1 试验动物分组及处理 将48 只Wistar 雄性大鼠随机分为6 组,每组8 只,分别为对照组、模型组、碳酸钙(250 mg/kg)组和给药剂量组。除对照组以普通饲料饲养外,其他5 组大鼠以低钙饲料饲养进行造模。按照人体推荐量的5 倍、10 倍及15 倍设置的鹿骨片低、中和高给药剂量(265 mg/kg、530 mg/kg和795 mg/kg)组。阳性组给予碳酸钙250 mg/kg,对照组和模型组给予等量生理盐水,各组均每天给药1次,连续给药90 d。
1.4.2 骨密度测定 试验大鼠每天测定体重,90 d 后将各组大鼠处死并迅速取出右侧股骨,去除附着的软组织,然后将骨组织置于4%多聚甲醛溶液中固定。取出另一侧股骨在105 ℃烘箱中烘干至恒重,置于样品瓶中消化后利用原子吸收分光光度计测定骨钙含量。另外将多聚甲醛固定的样本放入样品杯中并固定,利用micro CT,在相同条件(扫描电压70 kV,扫描电流200A,层距20.13m,平面分辨率300 ms,连续扫描约808 层)下扫描,测定骨密度。
1.5 小鼠急性毒性试验
选用清洁级ICR 健康成年小鼠20 只,雌、雄各10 只,在动物房内检疫室检疫饲养5d,体重为17.5~20.7g。试验前动物禁食16 h、不禁水,用最大耐受量进行小鼠急性毒性试验。受试样品直接灌胃,比重为1.1 g/kg,按最大灌胃量20 mL/(kg·bw)一次性给样,受试物给予剂量为22.0 g/(kg·bw)。连续观察14 d,记录中毒表现及死亡情况。
1.6 大鼠30 d喂养试验
选用清洁级SD 健康离乳大鼠80 只,在动物房内检疫室检疫3 d,按体重随机分为4 组,每组20 只,雌、雄各半。受试样品为干燥粉末,折合人体推荐剂量为3.2 g/人(以60 kg 体重计),按人体推荐量的50 倍、75倍和100 倍设鹿骨片低剂量组[每天2.66 g/(kg·bw),BL]、鹿骨片中剂量组[每天3.98 g/(kg·bw),BM]、鹿骨片高剂量组[每天5.31 g/(kg·bw),BH],另设一个溶剂对照组[每天0 g/(kg·bw),C]。样品均用无菌水配制,对照组以无菌水代替受试物,每天1 次灌胃,给药量为10 mL/(kg·bw)。大鼠连续30 d按剂量灌胃含受试样品饲料,自由进食饮水,每周称1 次体重,每天观察动物的一般情况,有无中毒表现和死亡。试验结束后,观察体重、血液学指标、血液生化指标、脏器指数和病理学检查。
2 结果与讨论
2.1 鹿骨片对大鼠体重的影响
以265 mg/kg、530 mg/kg、795 mg/kg 剂量经口给予大鼠鹿骨片90 d 后,由图1 可知,给予低钙饲料的模型组大鼠体重明显低于对照组(P <0.05),证明造模成功。各剂量组大鼠的体重持续增长且一般状态良好,试验期间无不适反应。模型组、给药组及碳酸钙组大鼠体重差异不显著(P >0.05)。
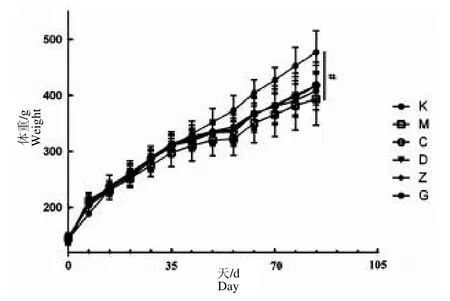
图1 大鼠体重变化Fig.1 Body weight changes of rats
2.2 鹿骨片对大鼠骨钙含量的影响
由图2 可知,给予低钙饲料的模型组大鼠骨钙含量明显低于正常对照组(P <0.05),给予鹿骨片90 d后,碳酸钙组及鹿骨片低、中剂量组的大鼠骨钙含量明显高于未给药的模型组(P <0.05),而鹿骨片高剂量组与模型组相比没有显著差异。因此,鹿骨片能够提高低钙大鼠骨钙的含量。
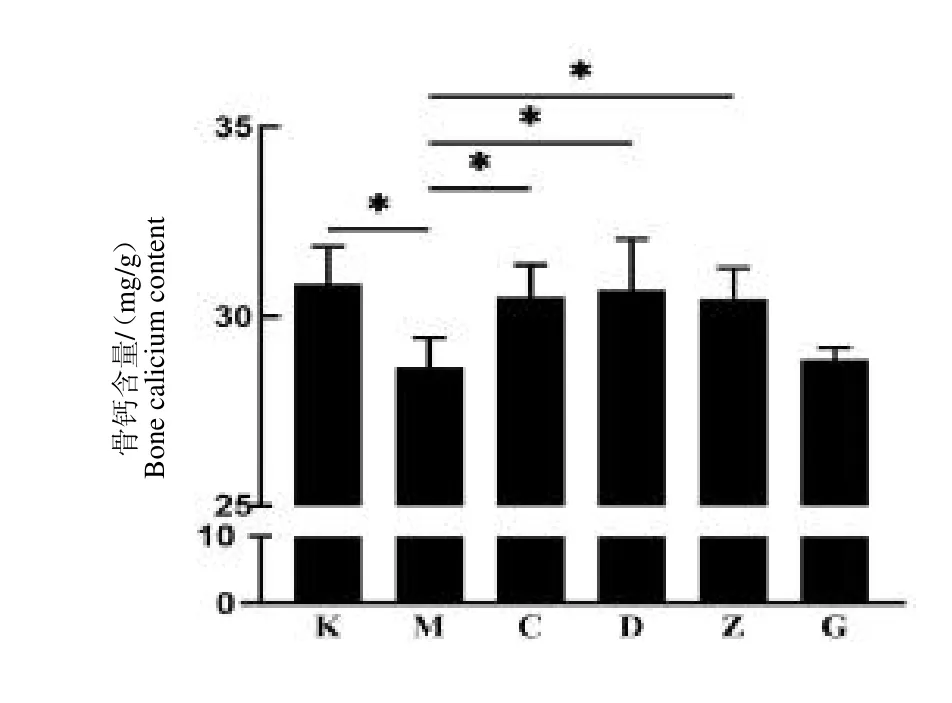
图2 大鼠左侧股骨骨钙含量变化Fig.2 Changes of calcium content in left femur of rats with increased bone mineral density
2.3 鹿骨片对大鼠骨密度的影响
由图3 和图4 可知,给予低钙饲料的模型组大鼠远心端骨密度及中心点骨密度均明显低于正常对照组(P<0.01)。给药后,碳酸钙组及鹿骨片低剂量组的大鼠远心端骨密度及中心点骨密度均高于模型组M(P<0.05),且鹿骨片补钙效果呈剂量依赖性,中、高剂量组远心端骨密度及中心点骨密度均显著高于模型组(P<0.01)。其中高剂量组基本可使大鼠骨密度恢复至正常程度。因此,鹿骨片具有增加缺钙大鼠骨密度的作用。
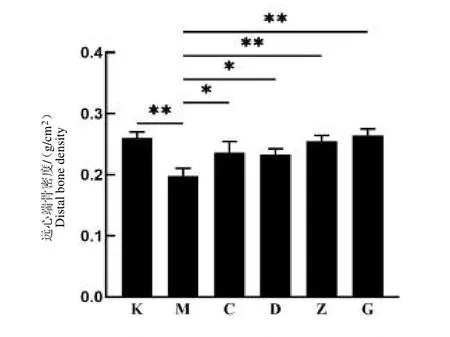
图3 给药期间大鼠右侧股骨远心端密度变化Fig.3 Changes in the density of the right distal femur in rats during the drug administration
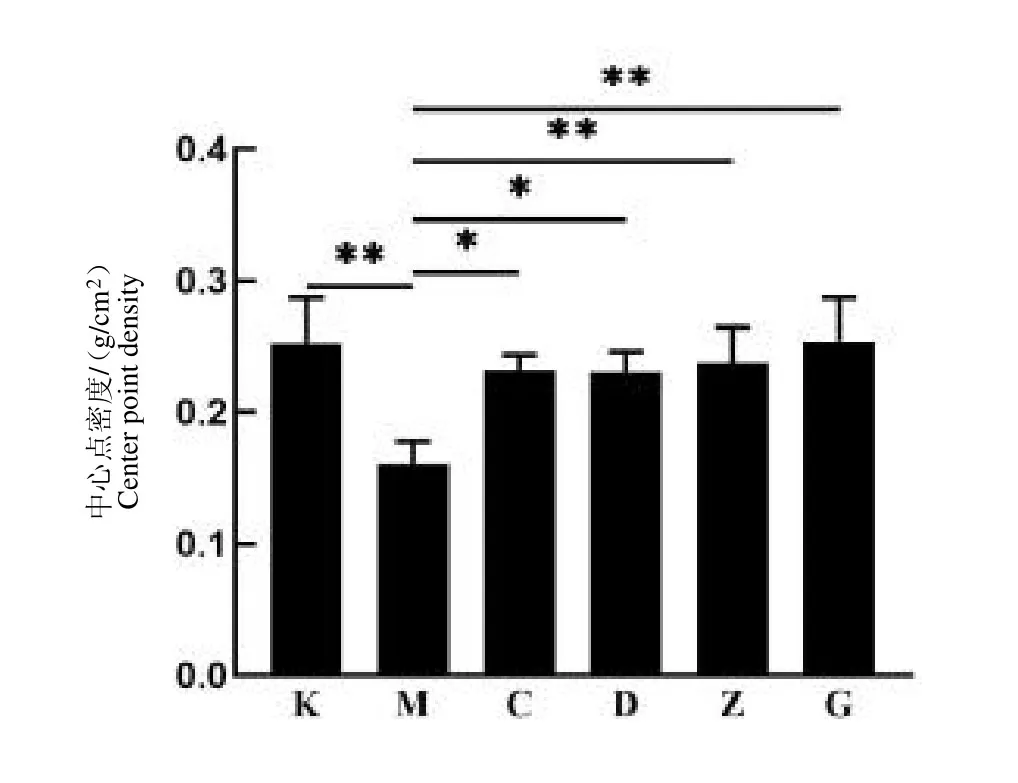
图4 给药期间大鼠右侧股骨中心点骨密度变化Fig.4 Changes in bone mineral density at the right femoral centroid in rats during drug administration
2.4 急性毒性试验
由表2 可见,急性毒性试验观察期间,鹿骨片对小鼠体重无影响。各组动物饮食和活动正常,生长良好,未见任何中毒表现,无死亡。鹿骨片的雌、雄性小鼠急性经口的最大耐受量(MTD)大于22.0 g/(kg·bw),按《保健食品检验与评价技术规范》(2003 版)规定,属于无毒级。
表2 鹿骨片小鼠急性毒性(±)Table 2 Acute oral toxicity of deer bone tablet in mice (±)
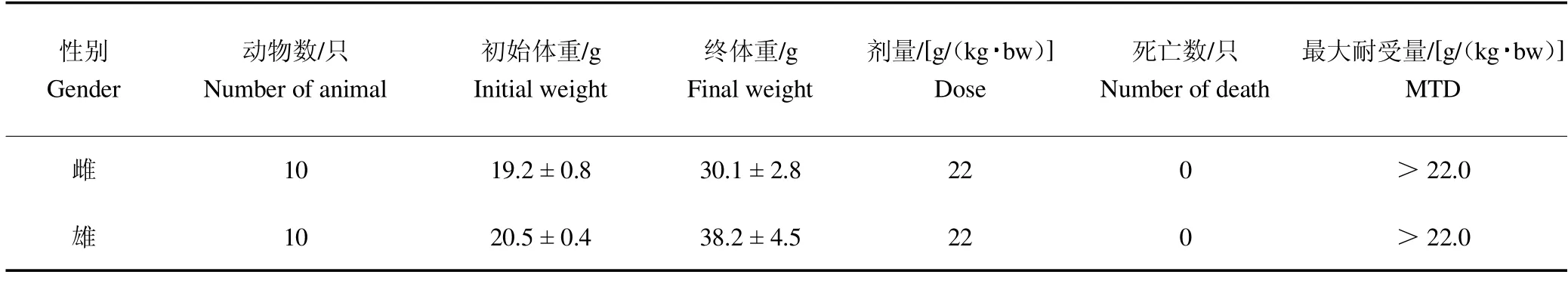
表2 鹿骨片小鼠急性毒性(±)Table 2 Acute oral toxicity of deer bone tablet in mice (±)
2.5 30 d 喂养试验
2.5.1 一般观察 试验期间,对照组和各剂量组大鼠经过一般观察,饮食和活动正常,生长良好,均未见异常症状和体征,未见任何中毒及死亡现象。
2.5.2 鹿骨片对大鼠体重的影响 各剂量组雌、雄大鼠的体重持续增长且状态良好,各组动物饮食和活动正常,试验期间无不适反应且未见异常症状和体征,鹿骨片低、中、高剂量组与对照组相比均无显著性差异(P>0.05),表明鹿骨片对大鼠体重无明显影响,结果见表3。
表3 鹿骨片对大鼠体重的影响(±,N=10)Table 3 Influence of deer bone tablet on body weight of rats (±,N=10)
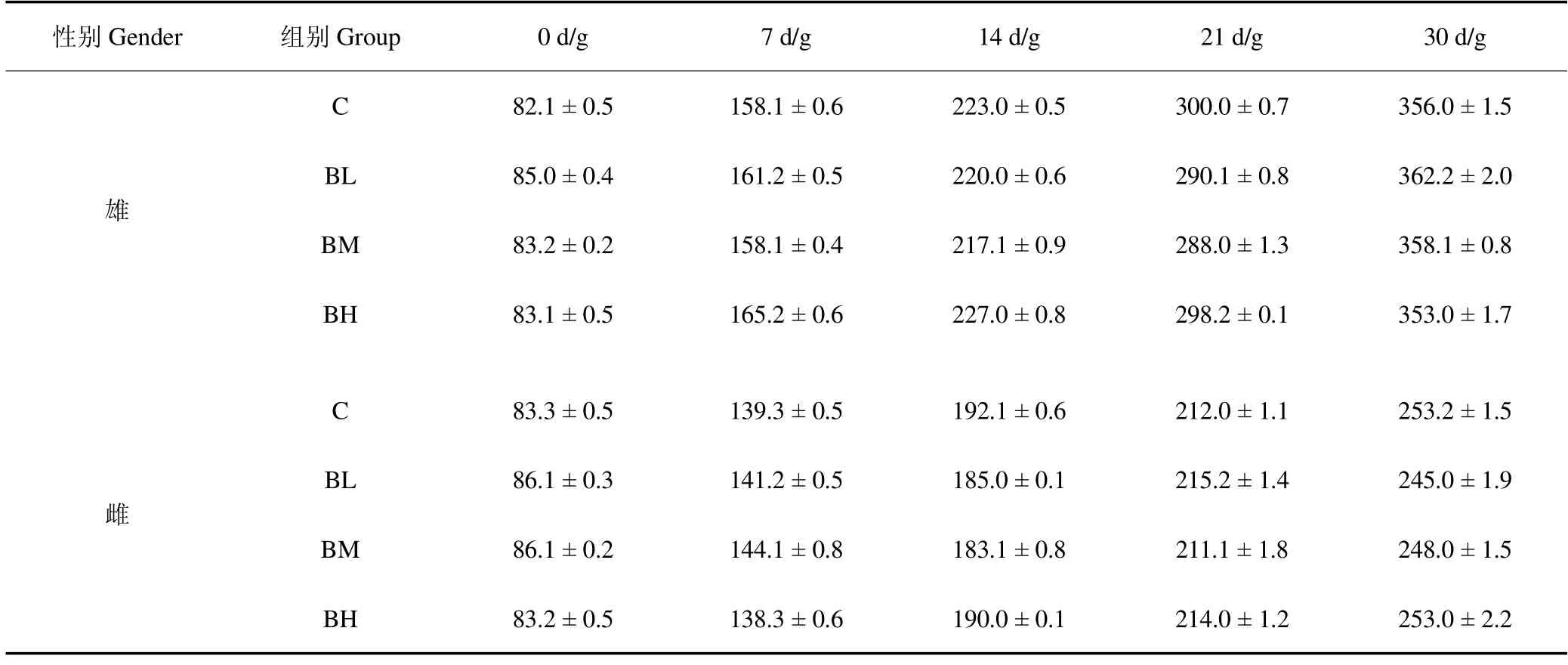
表3 鹿骨片对大鼠体重的影响(±,N=10)Table 3 Influence of deer bone tablet on body weight of rats (±,N=10)
2.5.3 鹿骨片对大鼠血液学指标的影响 由表4 结果可知,雌、雄大鼠对照组和各剂量组的红细胞计数、白细胞计数及其分类均在正常范围内,结果表明鹿骨片对大鼠血液学指标的差异无统计学意义(P>0.05)。
表4 鹿骨片对大鼠血液学指标的影响(±,N=10)Table 4 Influence of deer bone tablet on hematological indices of rats (±,N=10)
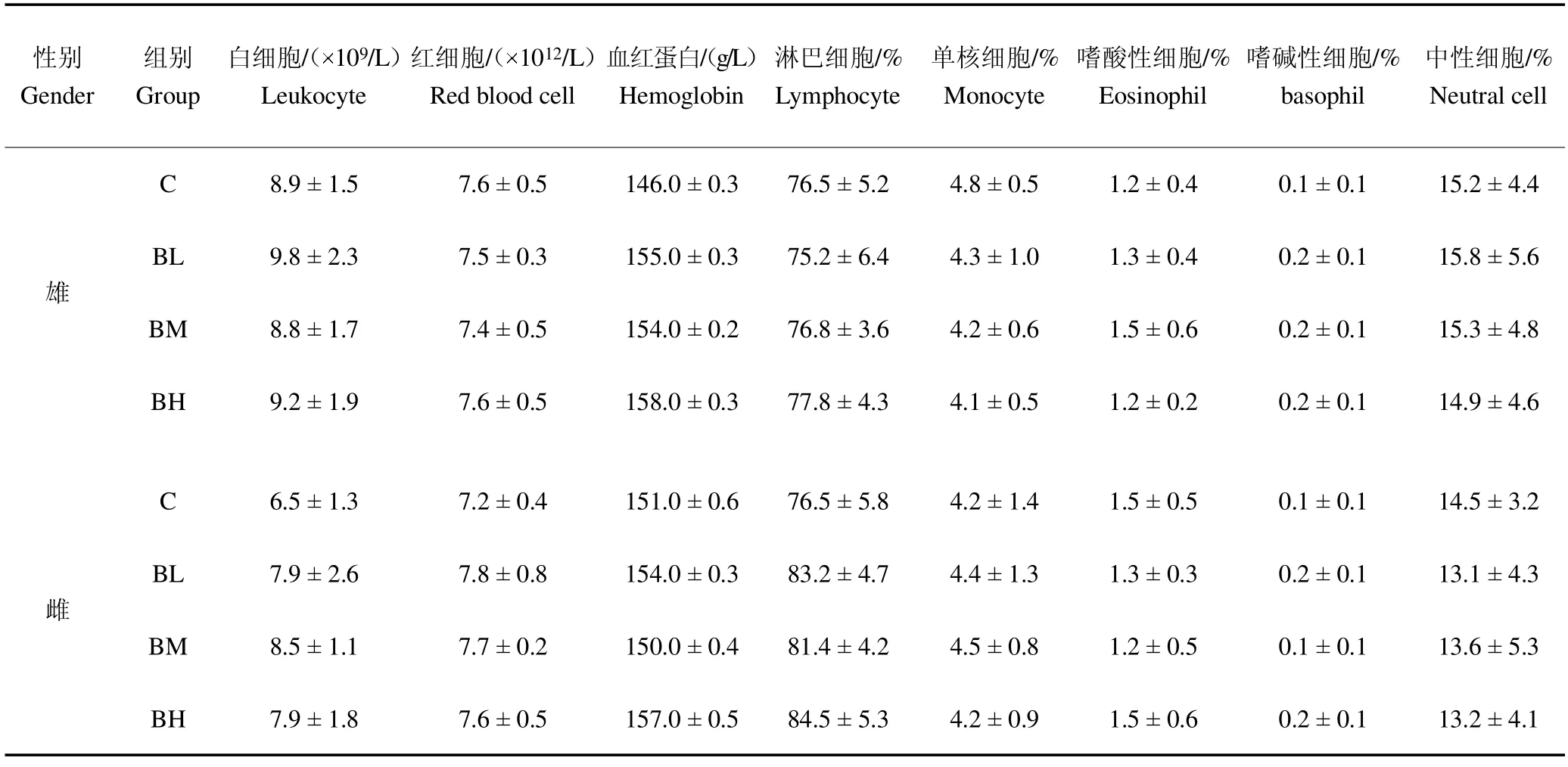
表4 鹿骨片对大鼠血液学指标的影响(±,N=10)Table 4 Influence of deer bone tablet on hematological indices of rats (±,N=10)
2.5.4 鹿骨片对大鼠血液部分生化指标的影响 由表5 可见,雌、雄大鼠对照组和鹿骨片各剂量组的血清谷丙转氨酶、谷草转氨酶、总蛋白、白蛋白、总胆固醇、甘油三酯、尿素氮、肌酐和血糖均在正常参考值范围内。表明鹿骨片对大鼠血液部分生化指标的差异无统计学意义(P >0.05)。
表5 鹿骨片对大鼠血液部分生化指标的影响(±,N=10)Table 5 Effects of deer bone tablet on some blood biochemical indexes of rats (±,N=10)
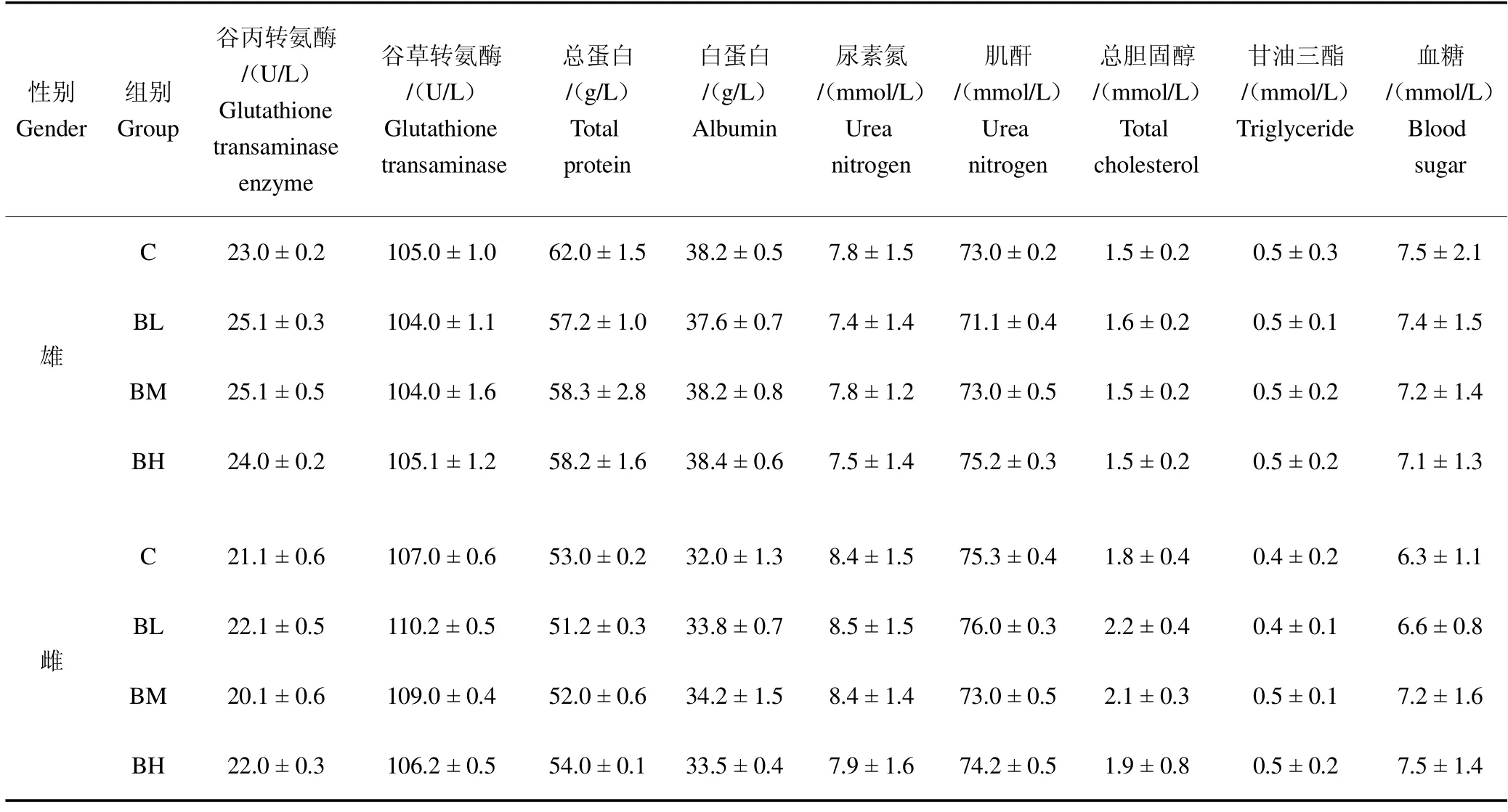
表5 鹿骨片对大鼠血液部分生化指标的影响(±,N=10)Table 5 Effects of deer bone tablet on some blood biochemical indexes of rats (±,N=10)
2.5.5 病理学及组织检查 由表6 可见,各剂量组肝脏、肾脏、脾脏、睾丸和卵巢绝对重量与对照组比较,差异不显著(P>0.05)。通过对大鼠解剖,未见由该受试物引起的肝、肾、脾、胃、十二指肠、睾丸和卵巢脏器毒性病理改变。
表6 鹿骨片对大鼠脏器绝对重量(±,N=10)Table 6 Effect of deer bone tablet on the absolute weight of rats'organs (±,N=10)
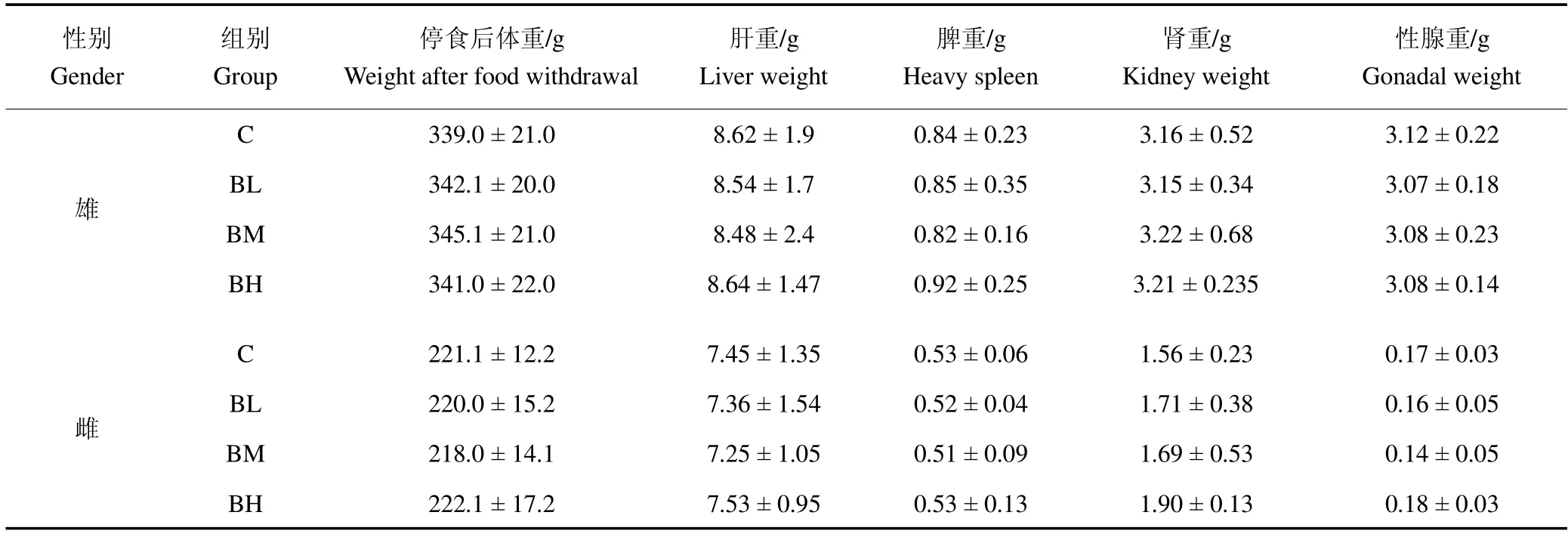
表6 鹿骨片对大鼠脏器绝对重量(±,N=10)Table 6 Effect of deer bone tablet on the absolute weight of rats'organs (±,N=10)
骨骼中的蛋白质90%为胶原蛋白、骨胶原及软骨素,具有促进皮层细胞代谢、防止人体老化的功能[11]。其中骨胶原和钙组成了独特的补钙途径,能够增加骨密度,强化骨骼韧性,达到预防和改善骨质疏松的作用[12]。鹿骨中含有较多的骨胶原[13],通过促进软骨内骨化及体内胶原蛋白及弹性蛋白的更新功能,起到增加成骨量的作用,又因含有较高的钙含量,钙、磷含量比为18.44: 9.92≈1.86: 1,接近人体吸收钙磷的最佳比例(钙:磷≈2:1)[13],在增加骨密度、骨钙含量方面具有一定优势,可作为钙补充剂开发利用[14]。鹿骨中含有的氨基酸总量为24.69%,必需氨基酸占氨基酸总量的16.65%,具有丰富的营养成分以及较高的经济价值[15]。
骨重建是存在于人类生命中的一个长期持续性的过程,骨重建是依靠甲状旁腺素和降钙素的水平调控,通过骨吸收和骨生成过程得以实现的平衡活动[16]。骨质疏松的根本原因就是新骨量的产生少于被吸收骨量,导致的骨重建平衡活动的失衡,骨量的丢失[17]。故骨密度测定被认定为是评价骨质疏松程度的客观量化指标及主要依据[18]。鹿骨作为传统动物药之一,虽具有着较高钙含量,但在预防骨质疏松症方面的研究较少。本研究以鹿骨片高、中和低3 个剂量组对缺钙模型大鼠进行灌胃90 d 后,大鼠的骨密度显著增加,骨钙含量显著高于低钙模型组大鼠,且与碳酸钙组大鼠无显著差异,且鹿骨片的雌、雄性小鼠急性经口MTD大于22.0 g/(kg·bw),属于无毒级,可以安全食用。本研究结果表明鹿骨片具有一定的预防骨质疏松症的作用,可为该产品的进一步开发提供数据支持。
3 结论
以鹿骨片高、中和低3 个剂量组(265 mg/kg、530 mg/kg、795 mg/kg)灌胃缺钙模型大鼠90 d 后,大鼠的骨密度显著增加,骨钙含量显著高于低钙模型组大鼠,且与碳酸钙组大鼠无显著差异。根据卫生部《保健食品检验与评价技术规范》(2003 版),可判定鹿骨片具有增加骨密度及骨钙含量的功能。小鼠急性毒性试验中,鹿骨片对小鼠体重无影响且各组动物饮食和活动正常,生长良好,未见任何中毒表现及死亡情况。鹿骨片的雌、雄性小鼠急性经口最大耐受量(MTD)大于22.0 g/(kg·bw),属于无毒级。每天给予大鼠低、中、高[2.66 g/(kg·bw)、3.98 g/(kg·bw)和5.31 g/(kg·bw)]3 个剂量30 d 后,大鼠一般情况良好,体重及脏器指标无显著异常,血液学指标及部分生化指标结果均在标准范围内,各脏器病理组织学检查未见异常病理改变。根据卫生部《保健食品检验与评价技术规范》(2003版)之30 d 喂养试验结果判定,鹿骨片最大剂量未观察到有害作用,属于无毒级。本研究结果表明,鹿骨片具有预防骨质疏松的作用且无害,且为拓展鹿骨在预防骨质疏松方面的应用提供理论依据。
