米格列醇+格列吡嗪治疗2型糖尿病患者的临床疗效及对血糖水平的影响
2024-01-06姚思丹
姚思丹
(福建省漳州市龙海区紫泥卫生院,福建 漳州 363100)
2型糖尿病(diabetes mellitus type 2,T2DM)占所有糖尿病患者90%以上,是临床多见的慢性代谢疾病,以高血糖为主要症状表现[1]。长期高血糖易导致眼、血管、神经、肾脏等重要器官受损甚至肾功能衰竭,将血糖稳定在合理范围内是控制疾病的关键[2-3]。胰岛素分泌不足、胰岛素利用障碍是导致糖代谢异常的重要因素,因此除了干预患者的饮食习惯,临床推荐应用降血糖药治疗[4]。格列吡嗪是第二代磺脲类降血糖药,可增强胰岛素作用,提升糖代谢效率[5]。但临床实践过程中发现单一药物的降糖效果欠佳,部分患者血糖控制效果不好,主要表现为餐后血糖异常升高,空腹血糖(fasting plasma glucose,FPG)、餐后2 h血糖(2 hour postprandial blood glucose,2 hPG)、糖化血红蛋白(glycosylated hemoglobin type A1c,HbA1c)等血糖指标波动过大。有研究提出[6],针对糖尿病患者餐后血糖升高的情况,可采用α-葡萄糖苷酶抑制剂治疗,通过抑制葡萄糖、单糖的吸收速度以保持血糖稳定,米格列醇是现阶段常用的α-葡萄糖苷酶抑制剂[7]。基于此,本研究将为我院2022年1月至2023年1月期间收治的T2DM患者100例分别应用格列吡嗪治疗和米格列醇+格列吡嗪治疗,对比二者的应用效果。
1 资料与方法
1.1 一般资料 研究方案符合医学伦理要求,经我院医学伦理委员会审批后,选择我院2022年1月至2023年1月期间收治的100例T2DM患者,采用计算机系统随机分为格列吡嗪组和联用组(米格列醇联合格列吡嗪治疗),每组各50例。两组患者基线资料均衡性良好(P>0.05)。
1.2 纳入与排除标准 纳入标准:①符合T2DM的诊断标准,在我院接受常规检查后确诊。②可耐受本研究所用治疗方法。③饮食、治疗依从性均较好。④患者或家属对研究知情同意并签署知情同意书。排除标准:①存在严重糖尿病并发症。②合并凝血、免疫功能异常与血液系统疾病患者。③存在急慢性感染的患者。
1.3 方法 格列吡嗪组予以格列吡嗪控释片(上海安必生制药技术有限公司,国药准字H20223472,规格:5 mg)口服,初始剂量为5 mg/d,随后根据血糖控制情况酌情增减,每次增减2.5~5 mg,最大给药剂量每次10 mg,每日2次。
联用组格列吡嗪控释片服用方法、剂量与格列吡嗪组相同,再此基础上给予米格列醇片(浙江医药股份有限公司,国药准字H20074195,规格:50 mg)口服,每次50 mg,每日3次。
两组患者均持续治疗12周,并配合完成各项观察指标评估。
1.4 观察指标 于治疗前、治疗12周后对比患者的血糖指标、胰岛功能指标,并计算两组血糖达标率,统计两组患者治疗期间的不良反应情况。①血糖指标:采集患者同一时刻外周静脉血4 mL,常规抗凝处理后采用全自动生化分析仪检测FPG、2 hPG、HbA1c。以FPG≤7.0 mmol/L、2 hPG≤10.0 mmol/L、HbA1c≤6.5%为达标。②胰岛功能指标:采集患者外周静脉血3 mL,以3000 r/min离心15 min后使用化学发光仪检测C肽(C-peptide,C-P)、空腹胰岛素(fasting insulin,FINS)。采用稳态模型胰岛素抵抗指数(homeostasis model assessment-insulin resistance,HOMA-IR)评估胰岛素抵抗水平,计算方法:HOMA-IR=FPG×FINS/22.5。③药物不良反应:叮嘱患者密切观察治疗期间身体状况,定期监测血糖,一旦出现头晕头痛、胃肠道反应、皮疹、低血糖等情况需及时报告。
1.5 统计学方法 本研究中的基线资料与观察指标所得数据均采用SPSS 19.0统计学软件分析,血糖、胰岛功能指标等计量资料经Shapiro正态性检验符合正态分布,使用t检验,以表示,血糖达标率、不良反应发生率等计数资料用χ2检验,以n(%)表示,检验结果P<0.05代表差异具有统计学意义。
2 结果
2.1 两组患者基线资料对比 两组患者基线资料对比,差异不具统计学意义(P>0.05)。见表1。

表1 两组患者基线资料对比
2.2 两组血糖达标率比较 治疗后,联用组共有45例患者血糖指标达标,5例不达标,达标率为90.00%,格列吡嗪组共有37例血糖指标达标,13例不达标,达标率为74.00%,联用组血糖达标率高于格列吡嗪组(χ2=4.336,P<0.037)。
2.3 两组患者血糖水平比较 治疗后,联用组的FPG、2 hPG、HbA1c均低于格列吡嗪组,差异有统计学意义(P<0.05)。见表2。
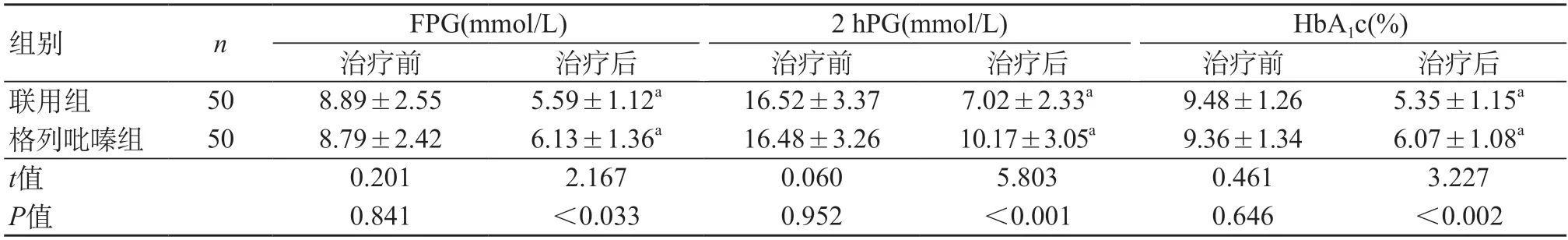
表2 两组患者血糖水平比较
2.4 两组患者胰岛功能指标比较 联用组的C-P、FINS高于格列吡嗪组,HOMA-IR低于格列吡嗪组(P<0.05)。见表3。

表3 两组患者胰岛功能指标比较
2.5 两组患者药物不良反应比较 联用组的不良反应发生率为10.00%(5/50),格列吡嗪组为6.00%(3/50),两组差异无统计学意义(P>0.05)。见表4。
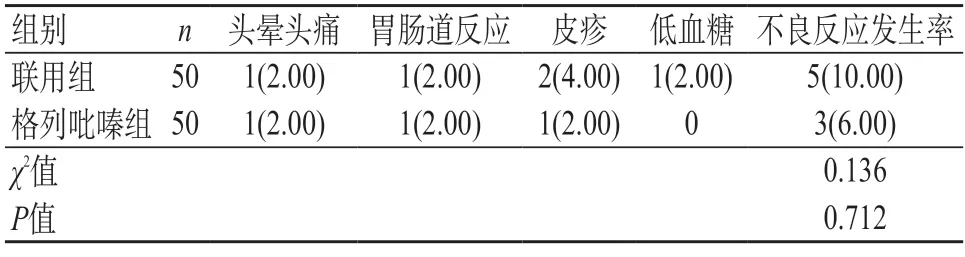
表4 两组患者药物不良反应比较[n(%)]
3 讨论
糖尿病是一种以高血糖为典型特征的代谢疾病,其中T2DM占所有糖尿病患者90%以上,是主要发病类型[8]。该病既往多见于中老年人群,近年来随着人们生活方式转变,发病呈现出年轻化趋势,已成为常见病和多发病。患者血糖指标长期偏高,易导致血管病变,并随着疾病进展,诱发心脏病变、脑血管疾病、视力下降或失明、肾功能衰竭以及下肢溃烂等严重并发症,大大增加了患者家庭与社会负担。该病目前无法完全治愈,治疗以控制血糖水平,降低并发症发生风险为目的,饮食、运动干预是该病的首要治疗措施,对于部分通过饮食、运动干预效果不佳的患者,临床将采取药物治疗方法。
T2DM主要因胰岛素分泌不足、胰岛素抵抗引起,减弱肝脏对机体外周组织葡萄糖摄取、存储和利用的能力[9]。格列吡嗪是临床常用降糖药,可直接影响葡萄糖的转运、利用,以增强葡萄糖的摄取能力,从而起到降低血糖的效果,但仅靠单一药物治疗效果有限,需采用联合用药措施进一步提升疗效[10]。α-葡萄糖苷酶是人体糖代谢过程中的重要成员,小肠绒毛中的α-葡萄糖苷酶可促使淀粉、蔗糖等物质生成葡萄糖和果糖等营养物质,从而被机体吸收。在α-葡萄糖苷酶高活性状态中,小肠吸收的速度较快,而胰岛素分泌不足或敏感性下降等因素可导致血糖在餐后短时间内迅速上升,且对胰腺造成刺激,不利于保护胰腺功能[11]。α-葡萄糖苷酶抑制剂主要作用为稳定血糖,并提升胰岛素敏感性[12]。本次研究为联用组患者应用米格列醇联合格列吡嗪治疗,取得较好效果,结果显示,该组患者治疗后各项血糖指标均低于格列吡嗪组,且血糖达标率显著较高,提示联用格列吡嗪与米格列醇可提升控糖效果。格列吡嗪是第二代磺脲类药物,具有较强的胰岛β细胞靶向作用,可与细胞膜的磺酰脲受体结合,关闭钾离子通道并开启钙离子通道,可提升细胞液中的钙离子含量,从而加速胰岛素分泌,对促进糖代谢有重要作用。米格列醇作为一种α-葡萄糖苷酶抑制剂,可局部在小肠中发挥作用,延缓淀粉、蔗糖等物质的分解,并且可增强小肠中下段的α-葡萄糖苷酶活性,促进碳水化合物分解为单个葡萄糖,从而促使餐后血糖峰值降低,血糖曲线更稳定[13]。联合使用格列吡嗪和米格列醇,可从不同路径提升糖代谢效率,增强对外周组织糖的摄取、存储能力,降糖效果更明显,二者联用可稳定患者餐后血糖变化曲线,避免短时间内血糖升高。
胰岛素由胰岛β细胞分泌,在正常状态中,胰岛β细胞会不断分泌胰岛素,使机体内胰岛素处于稳定的水平,以控制肝糖原输出,确保机体血糖稳定。C-P是胰岛β细胞分泌的产物,由胰岛素原分解形成。C-P指标具有较好的稳定性,不受外源性胰岛素影响,是观察胰岛β细胞功能的敏感指标。胰岛素抵抗指体内胰岛素转化葡萄糖的能力下降,HOMA-IR是用于判断胰岛素抵抗程度的数学模型[14]。在本研究中,联用组治疗后的C-P、FINS明显提升并高于格列吡嗪组,HOMA-IR明显降低并低于格列吡嗪组,说明联合治疗有助于提升胰岛β细胞分泌胰岛素能力,改善胰岛素抵抗。格列吡嗪主要通过直接降低血糖和胰岛外作用来降低胰岛素抵抗,血糖处于合理、稳定的水平有助于提升外周胰岛素靶组织的敏感性,促使HOMA-IR值降低,胰岛外作用包括提升葡萄糖激酶活性、提高胰岛素受体络氨酸激酶活性等,从而促进胰岛素稳态分泌。米格列醇则通过延缓二糖、多糖、复合糖水解减缓葡萄糖与其他单糖的吸收速度,从而稳定血糖指标,降低对胰腺的刺激,并提升外周组织胰岛素敏感性。两药联合起效可从多途径促进胰岛素稳态分泌,减小血糖波动来保护胰腺功能,降低胰岛素抵抗,提升胰岛素敏感性[15]。本次研究结果还显示,联用组与格列吡嗪组的头晕头痛、胃肠道反应、皮疹、低血糖等不良反应发生情况相当(P>0.05),且所有患者反应均较轻,提示联合用药不会显著增加不良反应发生风险,安全性有保障。
综上所述,米格列醇+格列吡嗪治疗T2DM具有较好疗效,降糖效果显著,并且可改善胰岛功能,改善胰岛素抵抗,安全性有保障,临床可应用。
