P,Nd双掺杂MoNiOx异质结电催化全解水性能研究
2024-01-04刁文涛周涛李其国许子圆龙鑫宋炬坤陆绍苑沈培康田植群
刁文涛, 周涛, 李其国, 许子圆, 龙鑫, 宋炬坤, 陆绍苑, 沈培康, 田植群*
(1.广西大学 双碳科学与技术研究院, 广西 南宁 530004;2.广西大学 物理科学与工程技术学院, 广西 南宁 530004)
0 引言
氢能作为一种清洁能源,是实现“双碳”目标的最为理想的替代能源。目前,氢气的制备大多采用化石燃料催化裂解的方式获取,这种方法尽管具有低成本的优势,但易造成大量二氧化碳的排放,现已不符合实现“双碳”目标的要求。随着可再生能源的广泛利用,制约电解水的电力成本已大为降低[1],电解水制氢成为了经济可行的技术方式[2],然而,电解水反应的动力学缓慢,特别是涉及多步质子耦合电子转移(proton coupled electron trasfer, PCET)的析氧反应(ocygen evolution reaction, OER),从而引起了较大的槽压,降低了电解水的效率[3]。其中,贵金属及其氧化物(如Pt、IrO2和RuO2等)虽然表现出极好的反应活性;但由于成本过高的原因未被广泛应用[4],因此,发展非贵金属催化剂是解决这一问题的关键。
近年来,人们聚焦于低成本的非贵金属异质结水电解催化剂发展,其中包括NiSe2/FeSe2p-p异质结[5]、核-双壳纳米γ-Fe2O3@FeS2@C[6]、CoSe2-MoS2多壳空心球(MSHSs)[7]、Ni2P-CoCH/CFP[8]、MoO2-Ni异质结[9],由于异质界面具有较大的功函数差,有利于引起电子转移,从而降低了反应中间体的吸附能,因此提升了材料的催化活性[10]。其中,低价Mo元素表现出了优良的促进水分解的催化活性,同时Ni的氧化物和羟基氧化物表现出良好的析氧活性,从而表现全解水双功能催化的性能。为了进一步优化MoO2-Ni异质结的性能,研究者们又相继发展出了P-Mo-Ni3S2@NF[11]、NiS2-MoS2空心球[12]、Ni/Mo2C纳米花[13]、Ni-NiMoO4/NiS2[14]等新结构催化剂,然而,进一步调变异质结构催化剂电子结构仍然是一个难点,从而影响了该类型催化剂性能的进一步地提升。
为此,本文中合成了一种P和Nd双掺杂MoNiOx异质结全解水催化剂PMoNiNd,通过场发射扫描电镜(SEM)、透射电镜(TEM)、X射线衍射仪(XRD)、X射线光电子能谱(XPS)、电化学工作站等表征方式揭示催化剂的微观结构、组分、电子结构和析氢析氧催化活性之间的关系。
1 实验部分
1.1 材料
实验用主要材料包括:泡沫镍(NF,厚度为1 cm,广胜佳金属材料有限公司)、浓盐酸(HCl,质量分数为36.5%,上海麦克林生化科技股份有限公司)、六水合氯化镍(NiCl2·6H2O,AR,上海阿拉丁生化科技股份有限公司)、氢氧化钾(KOH,AR,上海麦克林生化科技股份有限公司)、六水合氯化钕(NdCl3·6H2O,AR,上海麦克林生化科技股份有限公司)、磷钼酸水合物[H3P(Mo3O10)4·xH2O,AR,上海麦克林生化科技股份有限公司]、二水合钼酸铵[(NH3)2MoO4·2H2O,AR,上海麦克林生化科技股份有限公司]。
1.2 P和Nd掺杂MoNiOx异质结(P@MoNiOx-NdMo8O14)的制备
首先,将泡沫镍[20 mm×40 mm(长度×宽度)]浸入100 mL物质的量为0.1 mol/L HCl中,超声处理20 min,之后使用200 mL 混合溶液(去离子水与乙醇体积比为1∶1 )进行冲洗和超声处理20 min,使用无尘布去除表面吸附水即可得到预处理的泡沫镍。
PMoNiNd的制备过程如图1所示。在50 mL的PTFE内衬中加入30 mL去离子水作为溶剂,称取1.6 mmol(0.380 g)的六水合氯化镍(NiCl2·6H2O)和0.4 mmol(0.143 g)的六水合氯化钕(NdCl3·6H2O)溶于去离子水中,搅拌15 min得到溶液。然后再称取2.0 mmol(0.304 g)的磷钼酸水合物(H3P(Mo3O10)4·xH2O)溶于此溶液中,搅拌15 min。之后将预处理后的泡沫镍放入该溶液。
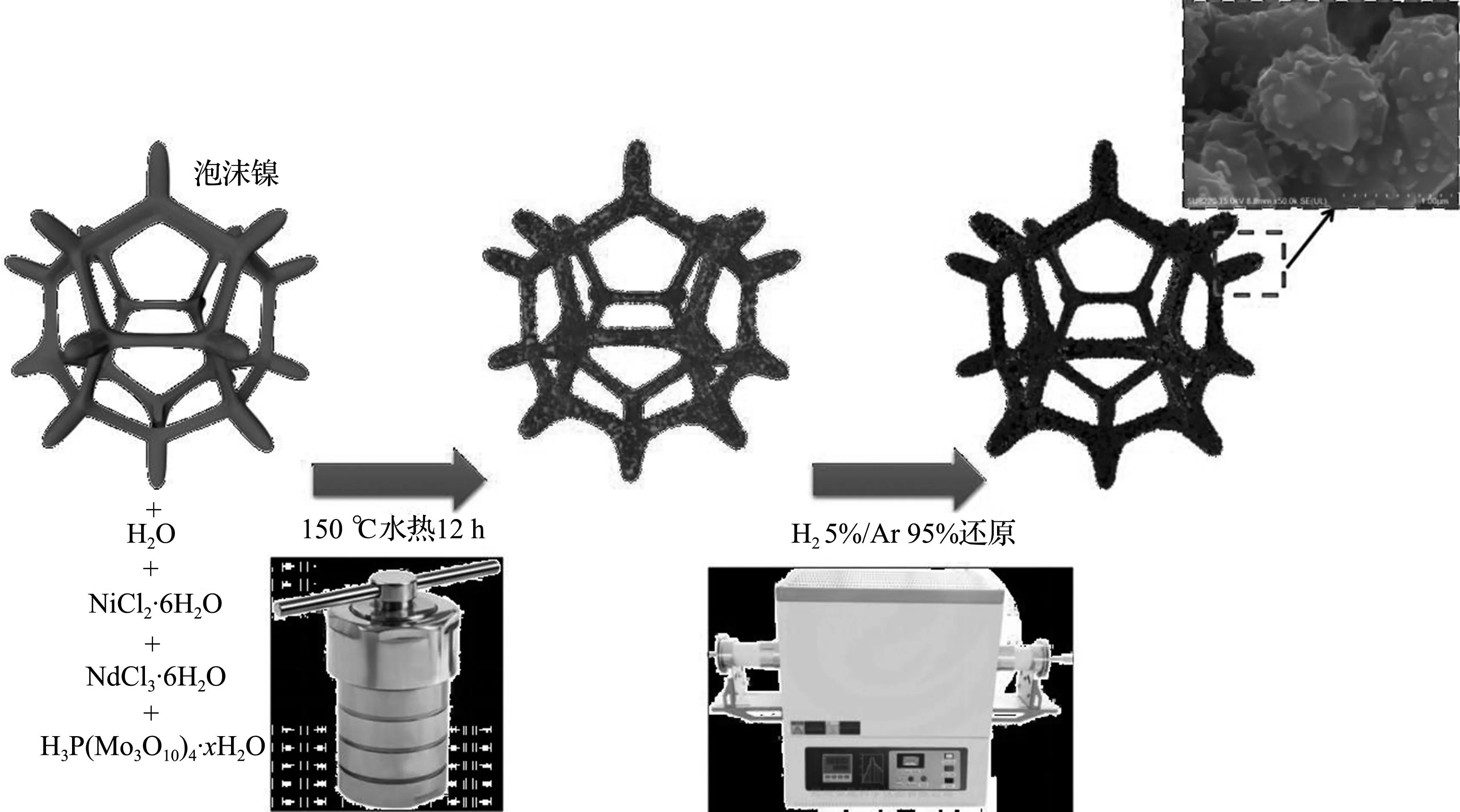
图1 PMoNiNd的制备过程Fig.1 Synthesis process of PMoNiNd
封盖后一起放进不锈钢高压釜中,在150 ℃进行12 h的水热反应,之后冷却至室温,取出反应后的泡沫镍,使用无水乙醇洗涤3次,然后在干燥箱中60 ℃保温12 h烘干,得到前驱体。将烘干的前驱体在H2与Ar的体积比为5∶95的气体环境中进行450 ℃的热还原处理,升温速率为5 ℃/min,保温2 h,待冷却至室温后得到样品P@MoNiOx-NdMo8O14(PMoNiNd)。
为了比较,我们又采用同样的方式制备了只掺杂Nd元素的Nd@MoOx-Ni(MoNiNd),只是在制备过程中将2.0 mmol(0.304 g)的H3P(Mo3O10)4·xH2O改为2 mmol的(NH3)2MoO4·2H2O;又在不使用NdCl3·6H2O的条件下制备得到只掺杂P的P@MoOx-Ni(PMoNi);以及在既改用2 mmol的(NH3)2MoO4·2H2O又不使用NdCl3·6H2O的条件下制备得到没有任何掺杂的MoO2-Ni(MoNi)。
1.3 材料表征
使用场发射扫描电子显微镜(Hitachi SU8220型,日本日立公司)观测材料的微观形貌和尺寸,结合能谱测试系统(EDX)对材料进行各项元素的含量分布表征。采用X射线衍射仪(SmartLab型, 日本理学公司)对材料进行物相分析,射线源为Cu Kα,波长为1.540 56 Å,测试电压为40 kV,电流为30 mA。扫描范围从10° 到90°,扫描速率为10(°)/min。使用环境球差校正透射电子显微镜(Titan ETEM G2 80-300 型,美国FEI公司)观察滴在微栅(70 μm)上面的材料的形貌和晶体结构。加速电压300 kV,点分辨率为0.23 nm。采用X射线光电子能谱仪(ESCALAB 250Xi型,Thermo Fisher Scientific公司)对材料进行元素组成和含量的分析,辐射源采用单色Al靶X射线源,光斑尺寸为200~900 μm,能量分辨率不大于0.45 eV,灵敏度为1×106s-1。
1.4 电化学测试
使用三电极体系进行电化学水分解测试,电解液为1 mol/L KOH溶液(25 ℃),可逆氢电极作为参比电极,石墨棒电极作为对电极,使用含有尺寸为10 mm×10 mm(长度×宽度)铂片的电极夹固定有效面积为10 mm×10 mm的泡沫镍基催化剂作为工作电极。循环伏安扫描(CV),电压范围为-0.5~0.1 V(析氢反应),1.1~1.5 V(OER),活化20圈。极化曲线(LSV)电压范围为-1.0~0.1V(析氢反应),1.1~2.2 V(析氧反应),经过电压矫正。电化学阻抗谱测试,频率范围为0.1~100 000 Hz,对结果进行等效电路拟合。使用恒电流法测试材料的稳定性,电流为±10 mA/cm2。所有的电化学测试均使用电化学工作站(DH7000型,江苏东华公司)完成。
2 结构和成分表征
PMoNiNd、MoNi、PMoNi和 MoNiNd的结构和成分分析如图2所示。从图2(a)可见,PMoNiNd材料的微观形貌为生长在泡沫镍表面的不规则多面体,P和Nd元素的掺杂使得催化剂的微观结构和成分发生明显变化。MoNi样品为纳米线结构如[图2(b)]所示,与已经报道的结果相同[15],由于前驱体NiMoO4在(H25%/Ar95%)还原过程中含氧量降低,Ni和MoO2发生偏析而形成。分别掺杂P和Nd元素后的样品分别为多面体和低密度的纳米线,如图2(c)、2(d)所示。使用扫描电镜的能谱仪(EDX)表征样品的元素分布,如图2(e),可观察到PMoNiNd样品表面Mo,Ni、P,O、Nd元素的均匀分布,表明P和Nd元素在MoNiOx中的成功引入。使用透射电子显微镜(TEM)分析PMoNiNd催化剂的晶体结构。高角环形暗场图像[图2(f)]展示了PMoNiNd多面体的表面结构。根据HRTEM图像[图2(g)]可知纳米颗粒晶体的晶面间距为0.21、0.25 nm,分别对应NdMo8O14的(221)、(211)晶面。使用X射线衍射仪对材料进行成分和结构表征,如图2(h)所示,样品MoNi、PMoNi和MoNiNd主要由MoO2和Ni组成,其XRD图谱与MoO2标准卡片的PDF(No.76-1807)、Ni(PDF No.70-0989)相符,但P和Nd元素的掺杂改变了MoO2或Ni的晶相,与MoNi样品相比,掺杂Nd元素后的MoNiNd在衍射角为43.8°、51.9°出现的Ni特征峰发生蓝移,这是由于更大原子半径的Nd原子引起晶格应变,造成Ni晶体的(111)、(200)晶面间距增大[16-17]。P和Nd的掺杂对MoO2和Ni的晶体结构的影响不同。与MoNi相比,PMoNi的峰强增加,峰宽变窄,表明晶体的结晶度提高,衍射角为25.8°位置的MoO2(110)晶面特征峰消失,表明掺杂P之后的MoOx物种为非晶态,未在还原过程中发生明显偏析,其峰位更符合NiO的标准卡片(PDF No.75-0197),表明形成了长程有序的NiO晶体。在同时掺杂P和Nd之后,PMoNiNd样品的特征峰与NdMo8O14的标准卡片(PDF No.80-0815 )和Ni的标准卡片(PDF No.70-0989)相符,表明其主要成分有NdMo8O14、Ni,其中Ni峰来自泡沫镍基底的信号,证明Nd元素的成功引入。

图2 PMoNiNd、MoNi、PMoNi和 MoNiNd的结构和成分分析Fig.2 Analysis of structures and compositions for PMoNiNd, MoNi, PMoNi, MoNiNd
使用X射线光电子能谱仪分析材料表面各元素的电子结构信息,X射线光电子能谱测试如图3所示,P和Nd元素的掺杂显著改变了Mo原子和Ni原子的配位环境,从而改变二者电子结构。MoNi的Mo 3d谱图表现出6个分裂峰,分别位于结合能228.43、229.53、231.43、231.54、232.63、234.54 eV,分别对应于Mo3+3d5/2、Mo4+3d5/2、Mo6+3d5/2、Mo3+3d3/2、Mo4+3d3/2、Mo6+3d3/2,与已经报道的MoO2-Ni异质结构测试结果相同[9,15],如图3(a)所示。在掺杂P、Nd元素之后,各Mo 3d物种的电子能级未发生明显变化,但比例出现明显差异,如图3(e)所示,MoNi的不同Mo物种比值为Mo6+∶Mo4+∶Mo3+=57.1∶24.5∶18.4,P元素掺杂后Mo6+3d下降至53.2%,Mo4+增加至32.8%,Nd元素掺杂后的催化剂MoNiNd表面Mo物种的电子能谱也发生相似的变化,但Mo6+比例显著降低至51.4%,Mo3+则增加至26.1%。 同时掺杂P和Nd元素后Mo6+∶Mo4+∶Mo3+=36.5∶27.8∶35.5,表现出最低比例的Mo6+和最高比例的Mo3+。由于协同效产生的电子转移使得Ni 2p电子能级变化与之相反,MoNi,PMoNi,MoNiNd和PMoNiNd的Ni2+2p3/2电子能级红移幅度逐渐增大,分别为854.98、856.03、856.02、856.43 eV。由此可知,伴随着P和Nd的引入,Mo6+3d比例发生不同程度的减少,Mo3+3d物种则明显增加,这表明Mo原子电子云密度提升了,高价氧化态物种比例降低了以及低价氧化态物种比例增加了,低价态的Mo物种(Mo4+/Mo3+/Mo2+)有利于调整析氢反应中间体的吸附能,提高析氢活性[9,15]。相反地,Ni2+2p3/2电子能级发生明显红移[图3(b)],表明Ni原子周围电子云密度降低,氧化态提升,高价Ni物种更有利于在反应过程中形成有利于析氧的NiOOH物种,提升材料的OER催化活性[18]。综上所述,P和Nd元素的掺杂能够调整MoNiOx异质结构的电子结构,推动电子转移过程,造成界面上的电子云分布不平衡,进一步提升低价Mo物种的比例,提高Ni物种的价态,这有助于降低活性物质转变的能垒,提升材料的电解水催化活性[15,17,19]。
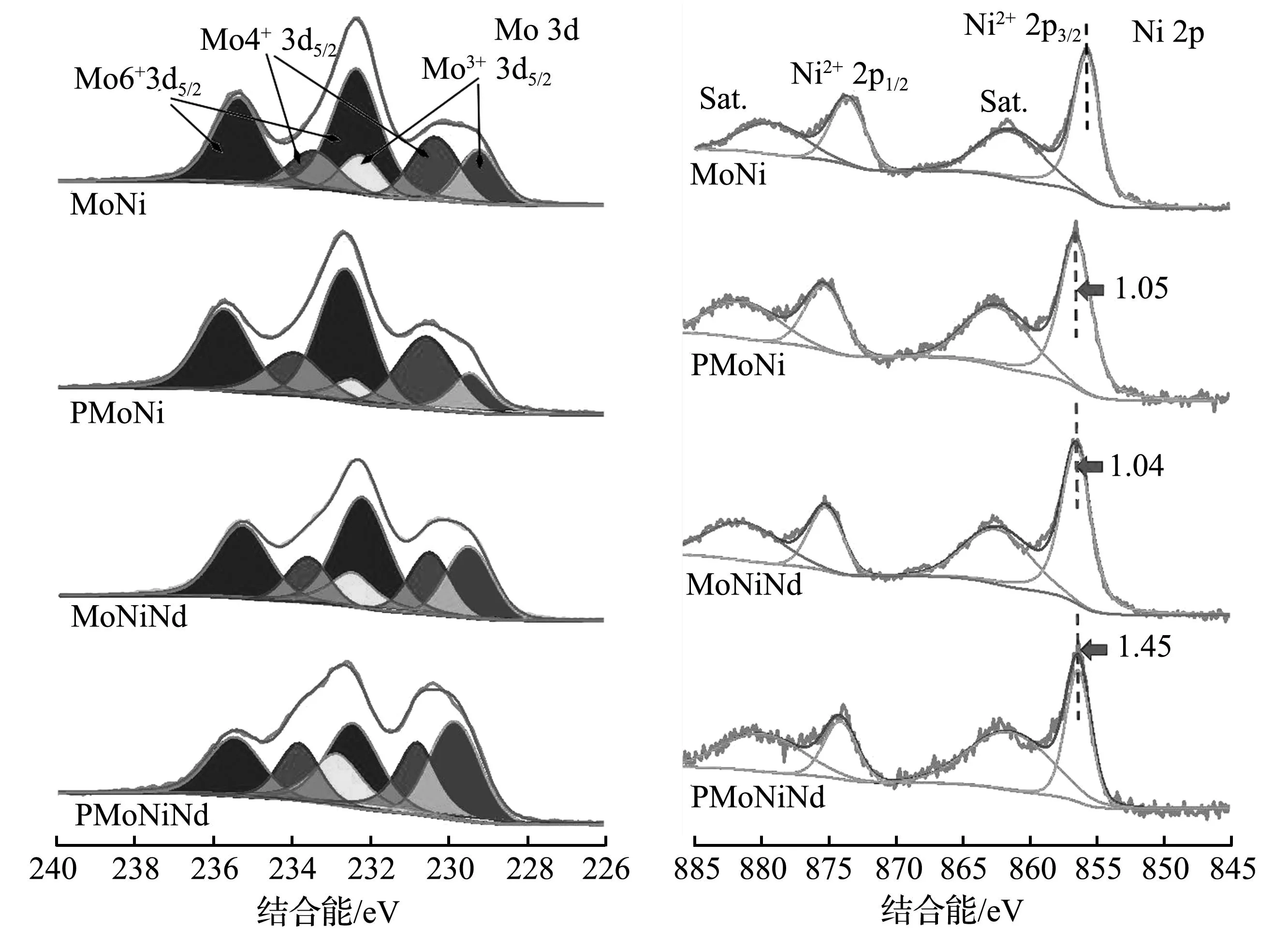
(a) Mo 3d的XPS谱图 (b) Ni 2p的XPS谱图
除此之外,通过对比MoNiNd和PMoNiNd的P 2p光电子谱图[图3(c)]发现,Nd元素的掺杂使得P 2p3/2的比例上升至58.5%,表明Nd元素的存在导致P原子的电子云密度增加。对比MoNiNd和PMoNiNd的Nd 3d光电子谱[图3(d)],结果显示只掺杂P元素的PMoNiNd出现了Nd4+3d物种,反映了P元素的掺杂可提高Nd原子的氧化态,降低其电子云密度。综上所述,高价的Mo物种比例的降低反映了电子云密度的提升,而Ni2+2p电子能级的增加和配位环境中的Nd4+3d5/2的出现,反映了电子云密度的降低,结果表明,P和Nd元素的引入改变了原本Mo物种和Ni物种之间的电子结构,导致PMoNiNd表现出最高比例的低价Mo 3d物种和最高氧化程度的Ni2+2p物种,已有结果证明二者的形成分别能够优化HER和OER反应中间体的吸附能[9,14-15],从而提升电化学析氢析氧的催化活性。
3 全解水性能
MoNi、PMoNi、MoNiNd和PMoNiNd的电化学测试结果如图4所示。从图4(a)可见样品MoNi、PMoNi、MoNiNd和PMoNiNd分别需要33.4、207.7 mV,37.6、199.8 mV,55.9、243.4 mV和12.9、182.1 mV 的过电位可以达到10、500 mA/cm2的电流密度,通过对比发现PMoNiNd表现出最好的析氢活性。从图4(b)可见,PMoNiNd较小的直径表现出电子转移阻抗较小,表明PMoNiNd催化剂表面具有最高的电子转移效率,这有利于电化学析氢反应过程中反应物与位点的电荷转移,提高反应速率和催化活性。从图4(c)可见,塔菲尔斜率反应了电化学反应过程中电流随电压变化的速度,PMoNiNd最小的Tafel斜率(91.70 mV/dec)不仅体现其较快的反应动力学[图4(c)],也表明其反应界面发生的反应过程决速步为Heyrovsky过程,即H2O+e-+Hads=H2+OH-[19-20]。
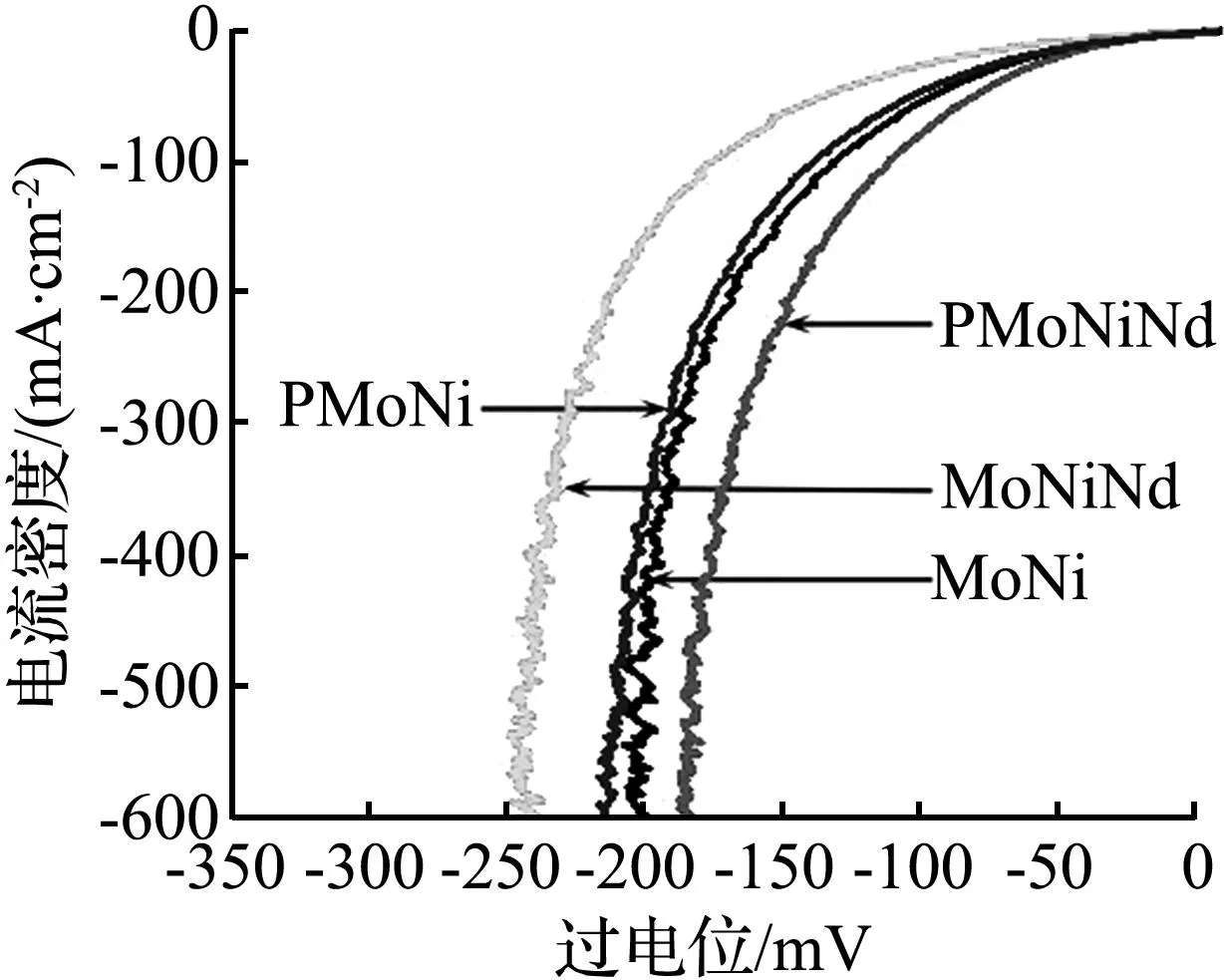
(a) 析氢极化曲线
在电化学析氧反应测试中(图4d),PMoNiNd表现出最高的催化活性,达到10、100 mA/cm2的电流密度分别需要282.5、328 mV的过电位,显著低于MoNi(322.3、410.1 mV ),PMoNi(318.9、418.1 mV )和MoNiNd(274.9、360.6 mV )。同时PMoNiNd具有最小的界面电荷转移电阻[图4(e)]和塔菲尔斜率(43.5 mV/dec)[图4(f)],表明催化剂反应界面存在高效的电子传输通道,反应过程决速步主要为H2O的解离(Heyrovsky过程),即H2O-e-=H++*OH。
使用恒电流法对PMoNiNd催化剂进行HER和OER稳定性测试,结果表明P和Nd元素的引入对电子结构的调控作用具有较强的稳定性,不会轻易在反应过程中失效。如图4(g)所示,PMoNiNd催化剂在±10 mA/cm2的电流密度下经过28 h的HER和OER稳定性测试,过电位没有发生明显增加。
微观结构形成的不同反应界面能够形成不同数量的活性位点,也是影响催化剂催化活性的重要因素之一。双电层电容Cdl与材料的电化学活性面积成正比,因此通过测量MoNi、PMoNi、MoNiNd和PMoNiNd的双电层电容可以定量分析其电化学活性面积。使用循环伏安法测得材料的Cdl,如图4(h)、4(i)所示,MoNi具有最高的双电层电容34.17 mF/cm2,可能是因为其微观形貌为高比表面积的纳米线,表明其具有最大的电化学活性面积,在反应过程中能够暴露更多的活性位点,但在HER和OER活性测试结果中[图4(a)、4(d)],MoNi样品的活性都不是最高的,反而双电层电容值最低的PMoNiNd活性最高,进一步表明PMoNiNd电极表面表现出的高反应活性与电化学活性面积无关,而主要受被强化的协同作用影响。
图5(a)、5(b)总结了近几年发表的一部分全解水催化剂的催化性能[21-30],通过对比可知,PMoNiNd表现出最小的塔菲尔斜率,并且析氢析氧活性都具有一定的优势。
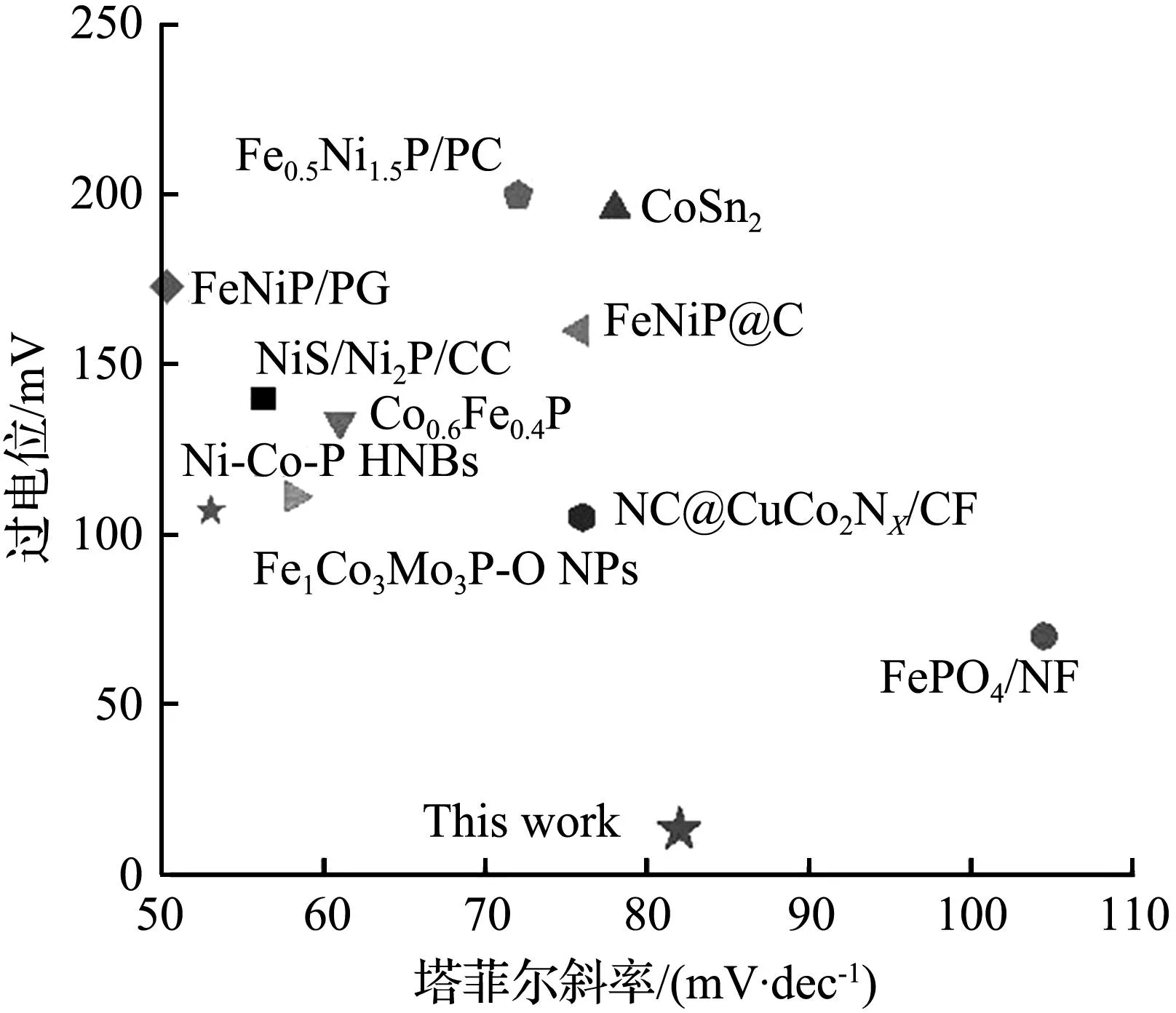
(a) 析氢活性对比
通过全解水测试模拟本研究得到的催化剂在电化学水分解过程中的催化活性。在1 mol/L KOH溶液中,使用PMoNiNd同时作为阴极和阳极进行双电极体系的电化学全解水测试(图6)。达到10 mA/cm2的电流密度仅需1.58 V的槽压,经过25 h的稳定性测试[图6(a)],电位没有发生明显增加,稳定性测试前后的极化曲线(LSV)基本重合[图6(b)],表明本研究报道的PMoNiNd具有良好的全解水催化活性和稳定性。
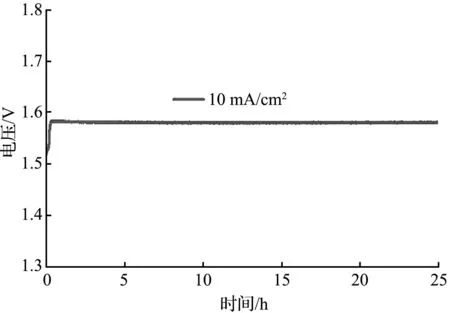
(a) 稳定性测试
4 结论
本研究使用水热法和氢气还原法成功制备了P、Nd修饰的MoNiOx异质结构全解水催化剂,其中P、Nd的引入进一步降低了Mo元素的Mo4+3d物种的结合能,增加了Ni元素的Ni2+2p物种的结合能,降低了其在反应过程中向活性物种NiOOH转变的能垒,表现出比P、Nd元素各自掺杂更高的电解水催化活性。在HER和OER测试中达到100 mA/cm2的电流密度分别仅需 107.7、328 mV的过电位。将其同时作为阴极和阳极进行全解水测试时,仅需1.58 V的槽压就能达到10 mA/cm2的电流密度。本研究使用的双元素优化MoNiOx异质结催化性能的策略为有效提升催化剂析氢析氧催化性能提供了新思路。
