肺癌化疗患者发生肺部感染危险因素的Meta分析
2024-01-04谢双燕李思瑾李泽云马阿敏余咏兰谢独
谢双燕,李思瑾,李泽云,马阿敏,余咏兰,谢独
1.广州中医药大学第一附属医院放射治疗科 广东省中医临床研究院,广东广州 510405;2.广州中医药大学第一附属医院妇儿中心,广东广州 510405;3.广州中医药大学第一临床医学院,广东广州 510006
肺癌是全球发病率和死亡率均较高的恶性肿瘤之一[1]。2020年,中国肺癌发病率及死亡率分别为17.9%和23.8%,均呈上升趋势[2]。化疗是目前治疗肺癌的重要手段,但肺癌化疗患者常伴有肺部感染,尤以革兰阴性菌为主,可导致治疗难度增加,如若得不到及时有效的治疗,严重者会转为重症肺炎,甚至危及生命[3-5]。因此,全面掌握肺癌化疗患者发生肺部感染的危险因素,及时识别高危人群,对提高患者的预后和生活质量具有重要意义。基于此,本研究采用循证方法,对肺癌化疗后肺部感染发病危险因素的研究文献进行系统分析,旨在筛选出导致肺部感染的相关危险因素,为预防肺癌化疗患者发生肺部感染提供依据。
1 资料与方法
1.1 纳入和排除标准
纳入标准:①纳入人群为已确诊为肺癌且行化疗的患者;②与肺癌患者化疗后肺部感染可能有关的个人因素、既往史、肿瘤因素、化疗前因素、化疗因素和化疗后因素,各危险因素定义基本相似;③化疗后发生肺部感染,且有明确的肺部感染诊断标准;④研究设计包括病例对照研究和队列研究。排除标准:①合并其他部位感染(如泌尿系感染、手术切口感染、消化道感染等);②非中、英文文献;③纽卡斯尔-渥太华量表(Newcastle-Ottawa scale,NOS)总分≤4分的文献;④无法提取数据的文献。
1.2 文献检索策略
计算机检索中国知网、万方、维普、PubMed、Embase和the Cochrane Library数据库,搜集从建库至2022年10月公开发表的肺癌患者化疗后发生肺部感染的危险因素的相关研究。检索采取主题词和自由词相结合的方式。英文检索词包括:lung cancer、chemotherapy、pulmonary infection、lung infection、pneumonia、healthcare-associated pneumonia、risk factors、related factors、influence factor、relevant factors、factors、predictors等;中文检索词包括:肺癌、肺恶性肿瘤、化疗、肺部感染、肺炎、危险因素、影响因素、相关性、原因、预测因素等。
1.3 文献筛选与资料提取
2名研究者独立筛选文献、提取资料并交叉核对。如有争议,咨询第三方进行协助判断。提取文献内容包括作者、发表时间、研究地区、研究涉及类型、样本量、研究因素(仅纳入有≥2篇文献报道的)及相关数据等。
1.4 纳入研究的质量评价
2名研究者独立采用NOS对纳入研究进行文献质量评价并交叉核对[6]。若评分结果不一致时,请第三方参与决定。NOS共8个条目,总分9分,≤4分为低质量,5~6分为中等质量,≥7分为高质量。
1.5 统计学方法
应用Rev Man 5.3和Stata 15.0软件进行统计分析。采用Meta分析合并比值比(odds ratio,OR)及95%置信区间(confidence interval,CI)。根据研究间的异质性采用固定/随机效应模型。本研究通过改变数据分析模型进行敏感度分析。采用Begg’s检验和Egger’s检验对纳入文献数量最多的暴露因素进行发表偏倚分析。
2 结果
2.1 文献检索结果
共检索得到1005篇文献,剔除重复文献,阅读摘要、原文并根据纳入排除标准逐层筛选,最终纳入15篇文献[7-21]进行Meta分析。
2.2 纳入文献的基本特征和质量评价
共纳入15篇文献,其中14篇[7-14,16-21]为病例对照研究,1篇[15]为队列研究,包括3960例肺癌化疗患者,化疗后肺部感染患者893例,共涉及21项相关因素,见表1。14篇病例对照研究的质量评分为6~8分,1篇队列研究的质量评分为9分。

表1 纳入文献的基本特征
2.3 Meta分析结果
2.3.1 个人因素 纳入研究涉及的患者个人因素包括年龄、性别、吸烟史和饮酒史。结果显示,年龄≥60岁、吸烟史、饮酒史均增加肺癌患者化疗后并发肺部感染的风险(P<0.05);性别与肺癌患者化疗后发生肺部感染无相关性(P>0.05),见表2。

表2 肺癌患者化疗后肺部感染影响因素的Meta分析结果
2.3.2 既往史 纳入研究涉及的既往史包括高血压、糖尿病、冠心病、肺不张和低蛋白血症。结果显示,糖尿病、高血压、肺不张、低蛋白血症均增加肺癌患者化疗后并发肺部感染的风险(P<0.05);冠心病与肺癌患者化疗后发生肺部感染无相关性(P>0.05),见表2。
2.3.3 肿瘤因素 纳入研究涉及的肿瘤因素包括肿瘤位置、TNM分期、病理分型(小细胞肺癌/非小细胞肺癌)和病理类型(腺癌/鳞癌)。结果显示,TNM分期为Ⅲ~Ⅳ期、中央型肺癌、小细胞肺癌患者化疗后并发肺部感染的风险增加(P<0.05);病理类型与肺癌患者化疗后发生肺部感染无相关性(P>0.05),见表2。
2.3.4 化疗前因素 纳入研究涉及的化疗前因素包括侵入性操作、应用抗菌药物和化疗前卡氏功能状态(Karnofsky performance status,KPS)评分。结果显示,侵入性操作、化疗前KPS评分<80分均增加肺癌患者化疗后并发肺部感染的风险(P<0.05);应用抗菌药物与肺癌患者化疗后发生肺部感染无相关性(P>0.05),见表2。
2.3.5 化疗因素 纳入研究涉及的化疗因素包括化疗药物和化疗时间。结果显示,联合使用化疗药物、化疗时间>2周增加肺癌患者化疗后并发肺部感染的风险(P<0.05),见表2。
2.3.6 化疗后因素 纳入研究涉及的化疗后因素包括化疗后白细胞计数、化疗后白蛋白水平和住院天数。结果显示,化疗后白细胞计数≤3.0×109/L、化疗后白蛋白<30g/L、住院天数>20d均增加肺癌患者化疗后并发肺部感染的风险(P<0.05),见表2。
2.4 敏感度分析
本研究通过转换数据分析模型进行敏感度分析,分别在固定/随机效应模型下计算21项暴露因素的合并OR值及其95%CI。结果显示,除吸烟史外,其余20项暴露因素的结果均无实质性改变,表明本研究得到的结果较为稳定且可信度较高,见表3。
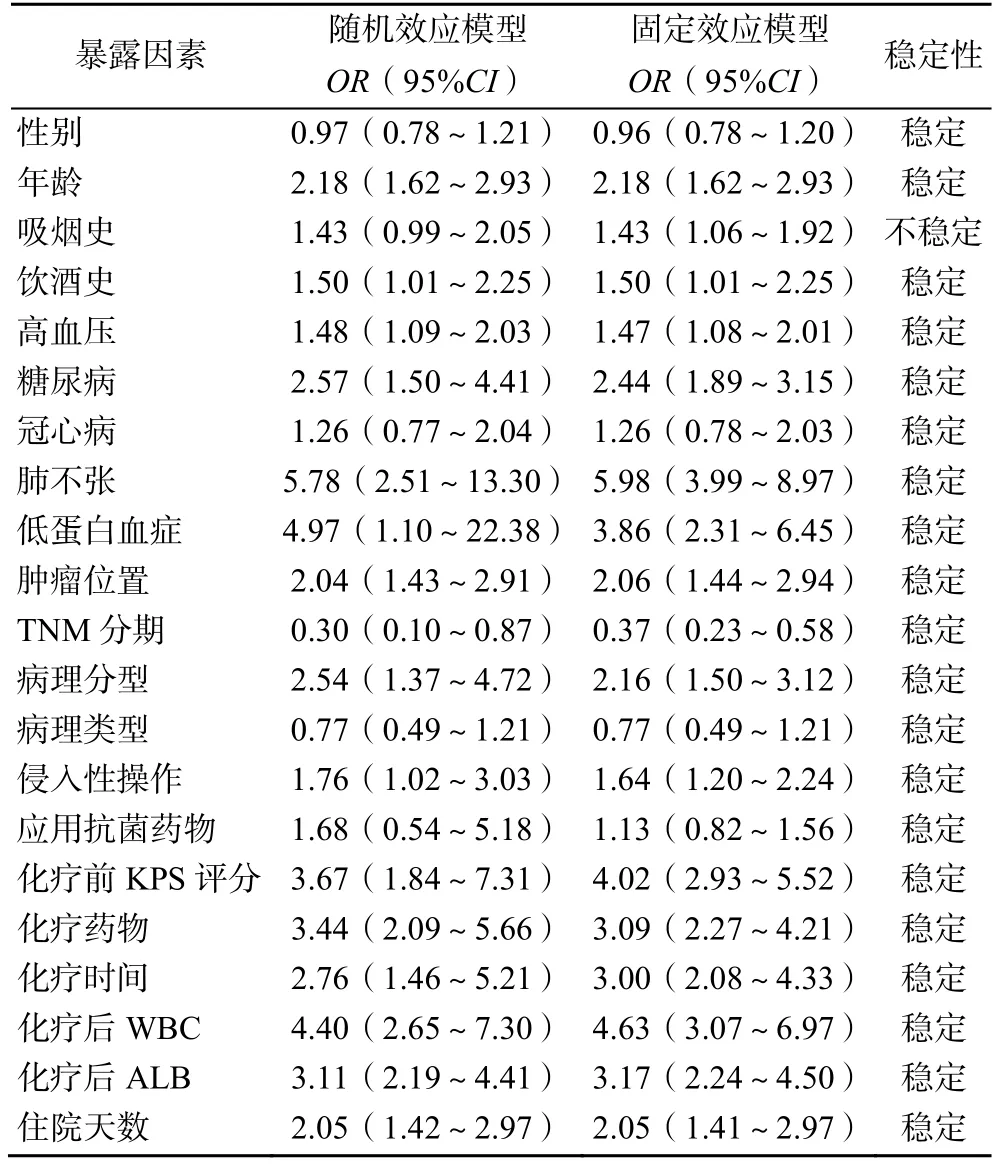
表3 暴露因素的敏感度分析结果
2.5 发表偏倚
以纳入文献数量最多(12篇)的暴露因素性别为指标,采用Begg’s检验和Egger’s检验进行发表偏倚分析。结果显示,Begg’s检验的P=0.193,Egger’s检验的P=0.247,均表明本研究未发现明显的发表偏倚,见图1、图2。

图1 性别的Begg’s分析图

图2 性别的Egger’s分析图
3 讨论
本研究共纳入15篇文献进行Meta分析,共涉及21项相关因素。纳入的研究病例来源于不同地区和医院,其流行病学、医疗条件和检测技术均存在一定的差异,可能是导致部分危险因素的相关文献之间产生异质性的原因。
个人因素中,年龄≥60岁、有吸烟和饮酒史均是肺癌化疗后肺部感染的危险因素。因此,应鼓励肺癌患者(尤其是高龄患者)戒烟、戒酒,养成良好的生活习惯,尽可能减少危险因素,预防化疗后肺部感染的发生。既往史的研究表明,合并高血压、糖尿病、肺不张或低蛋白血症的肺癌患者更容易发生肺部感染。因此,肺癌患者化疗前后要动态监测血压、血糖,从饮食、运动、药物等入手,严格控制血压、血糖水平。对肺癌伴有肺不张患者,及时对症处理缓解肺不张状况,以利于气道分泌物排出及淋巴回流,减少细菌停留繁殖,从而降低肺部感染的概率。在肺癌患者化疗期间,积极纠正患者的低白蛋白血症,提高免疫力,降低肺部感染的发病率。肿瘤因素中,TNM分期Ⅲ~Ⅳ期、中央型、小细胞肺癌是肺癌化疗后肺部感染的高危因素。临床医生应根据TNM分期、肿瘤位置和病理分型等为肺癌患者制定精准有效的个体化治疗方案,尤其是抗肿瘤方案选择和抗生素的使用,让患者的治疗达到最优化,提高患者的生存率及生存质量[22]。侵入性操作是肺癌化疗后肺部感染的高危因素,临床上应尽量避免不必要的侵入性操作,对救治过程需要采取多种有创诊疗措施的患者应加强医疗操作时的院感防控,同时密切监测相关症状,不需要时应尽早拔除[23]。本研究还发现,化疗前KPS评分<80分是肺癌化疗后肺部感染的高危因素。此类患者应保持呼吸道通畅,必要时给予雾化、吸痰等处理,预防肺部感染,减少并发症。化疗因素中,联合使用化疗药物、化疗时间>2周是肺癌化疗后肺部感染的高危因素。故而在肺癌患者化疗过程中应进行全面评估,充分认识可能导致肺部感染的危险因素,防范于未然,避免肺部感染发生。此外,化疗后白细胞计数≤3.0×109/L、白蛋白<30g/L和住院天数>20d也是肺癌患者肺部感染的危险因素。在肺癌患者化疗过程中及化疗后,应密切监测血象和血清白蛋白水平,及时给予升白等处理,同时指导患者合理饮食,补充足量的蛋白质。尽量缩短住院时间,避免院内交叉感染和重复感染,加强营养,必要时在化疗开始前预防性使用升白针,以降低肺部感染的发病率。
本研究的局限性:①纳入研究的文献各自分析的因素不完全相同,导致部分因素无法纳入合并,在结果分析上存在局限性;②纳入研究数量有限,且危险因素的分层不同,不能进行更细致的分层研究;③受研究设计类型限制,选择性和信息偏倚无法避免。
综上,影响肺癌化疗患者并发肺部感染的危险因素较多,临床上可参考本研究结果,有针对性地对危险因素进行有效预防和治疗,从而减少肺部感染的发生,以改善患者的预后和生活质量。
