高载量钴离子掺杂MnO2 用于高性能锌离子混合电容器
2024-01-03徐子明刘恒翰吴凤楠李生娟
姚 远,徐子明,刘恒翰,吴凤楠,李生娟
(上海理工大学 材料与化学学院,上海 200093)
随着“双碳”战略目标的提出和对新型能源的需求不断增加,电化学储能器件的研究引起人们的关注。电池(锂离子电池、锌离子电池等)具有较高的能量密度,但功率密度和循环寿命有待提高[1-3]。超级电容器具有快速充放电的速率、高的功率密度和超长的使用寿命,但因能量密度低而限制了其大规模应用[4-5]。以电容器型电极为阳极、电池型电极为阴极的混合电容器因兼具电池和超级电容器的优点而被广泛研究。
混合电容器的概念源于锂离子电池领域,但受制于金属锂的资源有限和有机电解质的安全问题,使其无法在生活中广泛应用[6]。基于其他一价和多价金属阳离子的混合电容器,如Na+[7]、K+[8]、Zn2+[9]、Ca2+[10]和Al3+[11],活性金属离子(Na+和K+)有安全风险,多价金属离子(Ca2+和Al3+)存在相对迟缓的扩散和反应动力学等缺点[12]。锌离子混合电容器(zinc ion hybrid capacitors,Zn-HCs)资源丰富、环境友好且安全性高,故成为新一代储能器件中最有前途的候选电容器之一。Ma 等[13]首次提出了MnO2用作阴极材料来构建Zn-HCs,证实了γ-MnO2和活性炭(active carbon,AC)构造的锌离子混合电容器具有与Zn-MnO2电池相当的能量密度,但其具有更大的功率密度。然而,其在充/放电过程中存在结构不稳定的问题,且当MnO2的负载量高时,MnO2缓慢的电子传输同样影响电极材料的电化学性能。为了解决这个问题,研究[14-16]发现,钴离子在电极材料的改性中可起到提高电导率、扩大电压窗口、提高循环稳定性等重要作用。在电化学领域,为了获得满意的电化学性能,锰基氧化物电极通常需要较小的活性材料负载量(通常小于0.5 mg/cm2)或采用薄膜结构[17-18]。事实上,低质量负载材料的总电容和储能都很小,这限制了它们在高能量体系中的实际应用。如何在提高负载量的同时又能使电极材料具有优异的稳定性成为一个亟待解决的问题。目前开发价格低廉、安全环保、导电性高、性能优异的电极材料还需要研究者们不断地探索研究,相信在不久的将来会有所突破,使得锌离子混合电容器得到有效的利用,以填补电池和电容器之间的空缺。钴离子掺杂MnO2(Co-MnO2)在Zn-HCs 领域还鲜有报道,可以同时改善高负载量MnO2电极的电导率和结构稳定性的有效策略尚未被证实。
本研究通过恒流电沉积法在碳布(carbon cloth,CC)上制备了高负载量的Co-MnO2作为Zn-HCs 的阴极材料。钴离子的掺杂提高了MnO2的电导率,促进了Zn-HCs 在充/放电过程中的电子传输。同时,钴离子的掺杂增大了MnO2的层间距,有利于Zn2+在充放电过程中的迁移扩散,且起到稳定层间结构的作用。组装成Zn-HCs 后,在2 mA/cm2的电流密度下具有5 883.0 mF/cm2的超高面积比电容,还可提供3 154.9 μWh/cm2的最大面积能量密度,和13.2 mW/cm2的峰值功率密度。此外,组装成准固态Zn-HCs 具有较好的机械柔韧性的同时具有较高的功率密度和能量密度。该Zn-HCs 已经达到了部分电池的水平,具有实际应用的潜力。
1 试验
1.1 Co-MnO2 和MnO2 阴极的制备
首先,用硝酸在140 ℃下对CC 进行2 h 酸化处理以增强其亲水性,以乙醇和去离子水反复洗涤几次后干燥备用。电沉积在三电极电解槽中进行,以1 cm×1 cm 的CC 为工作电极,铂片电极作为对电极(counter electrode,CE),饱和甘汞电极(saturated calomel electrode,SCE)作为参比电极。将10 mmol Mn(CH3COO)2·4H2O、10 mmol Na2SO4和0.5 mmol Co(CH3COO)2·4H2O 溶解在90 mL 去离子水中以形成均匀溶液。室温下,在10 mA/cm2的恒定电流下进行电沉积,电沉积时间为40 min。电沉积结束后,使用乙醇和去离子水反复清洗3 次,然后在90 ℃下干燥12 h。通过沉积前后质量差测得活性物质的负载量为13.8 mg/cm2。同时制备不掺杂钴离子的MnO2,制备方法同上,其中MnO2的负载量为11.9 mg/cm2。
1.2 AC 阳极的制备
将AC、聚偏氟乙烯(polyvinylidene fluoride,PVDF)和导电炭黑按照质量比为7∶2∶1 的比例混合并分散在N-甲基吡咯烷酮中,形成均匀油墨状的浆液。随后将油墨状的浆液涂敷在裁好的CC 上,90 ℃下干燥12 h。
1.3 Co-MnO2//AC 锌离子水系和准固态混合电容器的组装
以Co-MnO2(大小为1 cm×1 cm)为阴极,AC(大小为1 cm×1 cm)为阳极,两电极的质量比为1.0∶2.5,电解质为2.0 mol/L ZnSO4+0.2 mol/L MnSO4。当组装准固态锌离子混合电容器时,电极保持不变,电解质使用聚乙烯醇(polyvinyl alcohol,PVA)/ZnCl2-MnSO4凝胶。其中PVA 凝胶电解质的制备过程为:将1.00 g PVA、2.72 g ZnCl2和0.30 g MnSO4溶于10 mL 去离子水中,然后在90 ℃下剧烈搅拌加热3 h。
1.4 材料表征
使用Bruker D8-Advance X 射线衍射仪(X-ray diffractometer,XRD)分析样品的晶体结构和物相。用Quanta FEG450 场发射扫描电镜(scanning electron microscope,SEM)对其形貌进行表征。用JEOL-2010 能量色散X 射线光谱(energy disperse spectroscopy,EDS)研究元素组成和分布。采用X 射线光电子能谱(X-ray photoelectron spectrometer,XPS)在10-7Pa 的真空中分析样品中组成元素的化学组成和价态。
1.5 电化学测试
电化学性能用电化学工作站(CHI 760E,上海辰华仪器有限公司)进行测量。在双电极体系中,分别在水系电解质和凝胶电解质中研究了水系和准固态Co-MnO2//AC 锌离子混合电容器的电化学性能。通过公式[19]:
可以计算出电极材料的面积比电容Cs。式中:Cs为面积比电容;I为放电电流;Δt为放电时间;ΔV为去除电压降损失后的放电电压窗口,S为电极材料的几何面积。
根据公式[19]:
计算得到Zn-HCs 的能量密度E和功率密度P。
2 结果与讨论
2.1 基础表征
Co-MnO2和MnO2样品的XRD 谱图如图1 所示。MnO2的XRD 谱图在37.1°、42.4°、56.0°和66.8°处分别对应层状MnO2(ε-MnO2,PDF#30-0820)的(100)、(101)、(102)和(110)晶面,因为10 mA/cm2的电流密度较大,形核较多,所以MnO2晶核主要沿着(100)晶面二维生长[20]。而Co-MnO2的(100)晶面对应的特征峰(37.0°处)略微减小。根据布拉格方程判断,这是由于离子半径较大的钴离子取代了锰离子的位置导致的局部晶格间距变大,从而导致了晶面间距减大。这也表明了钴离子成功的掺杂到MnO2的晶格中。
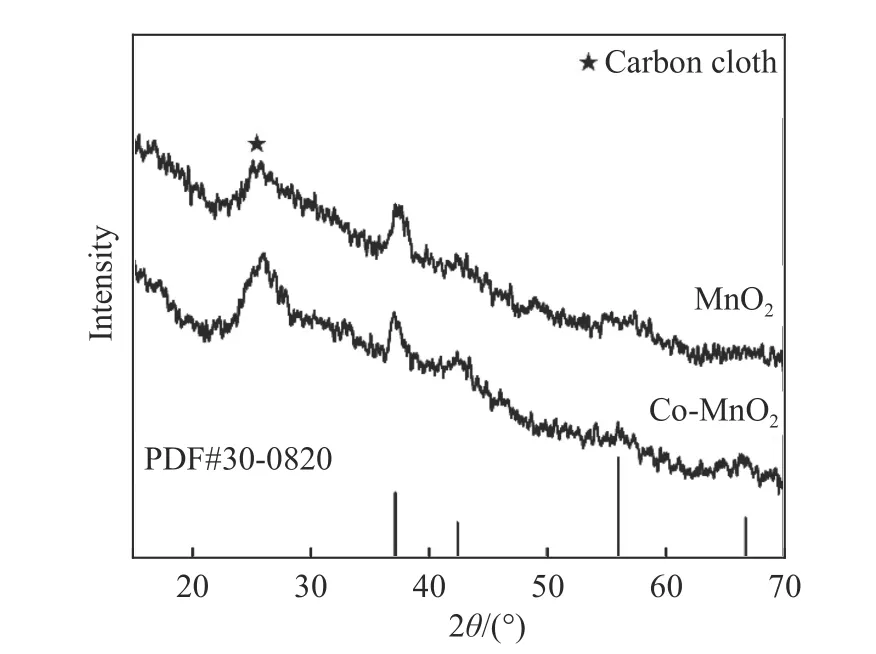
图1 MnO2 和Co-MnO2 的XRD 谱图Fig.1 XRD patterns of MnO2 and Co-MnO2
为了进一步确定钴离子掺杂的价态,对MnO2和Co-MnO2进行了XPS 分析,通过观察制备的MnO2和Co-MnO2的XPS 光谱图的全谱图,见图2(a)。可以看出XPS 检测到了Co、Mn、O 和C 等元素,证明恒电流电沉积制备的钴离子掺杂的MnO2已制备成功,其中C 元素属于CC 基底。如图2(b)所示的为MnO2的Mn 2p 轨道拟合了位于641.5 eV 和653.2 eV 处的高分辨自旋轨道峰,其中Mn 2p3/2范围内的3 个峰分别对应着Mn3+(640.8 eV)和Mn4+(642.2 eV 和643.2 eV),Mn 2p1/2范围内的峰对应着Mn4+(653.2 eV)[21]。图2(c)为MnO2的O 1s 光谱,其中529.7 eV 处的峰归属于Mn-O-Mn 键的结合能,531.1 eV 的峰归属于Mn-OH 键的结合能,532.5 eV 处的峰归属于表面吸附的OH-和结合水的结合能[22]。在图2(d)中,Co 2p 的两个高分辨自旋轨道峰(779.6 eV 和796.4 eV)归属于Co2+。值得注意的是,Co-MnO2的Mn 2p 轨道(见图2e)与MnO2的Mn 2p 轨道不同的是Mn3+的强度显著增强,表明Co-MnO2中有Co2+、Mn3+和Mn4+结合的产物[23]。如图2(f)所示,Co-MnO2的O 1s 轨道的分峰在M-O、表面吸附的OH-和结合水处没有明显变化,而是由于Co 的掺杂,使得M-O-H(M=Mn和Co)的结合能变为了531.5 eV。根据上述结果,可以确定在恒电流沉积过程中,钴离子主要以+2 价的形式掺杂到MnO2的晶体结构中,并在掺杂过程中使得Mn3+的含量有所增加。有研究表明,Mn3+比Mn4+表现出更强的氧化还原活性和导电性,因此,钴离子的掺杂对能量存储有着积极的作用[24]。

图2 MnO2 和Co-MnO2 的XPS 谱图Fig.2 XPS patterns of MnO2 and Co-MnO2
通过SEM 对材料的形貌进行表征,Co-MnO2和MnO2样品的SEM 图如图3 所示。从图3(a)可以看出钴离子掺杂前后MnO2的形貌没有发生改变,在CC 表面均匀覆盖,没有显现出堆积团聚的现象。从图3(b)可以看出MnO2和Co-MnO2纳米片尺寸相近,交错分布且彼此之间存在一些空间且牢牢地附着在CC 纤维的表面,没有出现活性材料脱落的现象,其疏松的结构有利于电解质离子的传输扩散,未造成活性物质的浪费,从而具有利于电化学性能的提升。

图3 MnO2 和Co-MnO2 的SEM 图Fig.3 SEM images of MnO2 and Co-MnO2
2.2 电化学表征
在组装Zn-HCs 前,对AC 和Co-MnO2单电极进行了电化学测试。图4(a)为AC 和Co-MnO2分别作为工作电极在三电极体系下进行的循环伏安(cyclic voltammetry,CV)曲线,其中AC 阳极的类矩形曲线显示了其吸附/脱附的过程,Co-MnO2的CV 曲线在0.76 V(vs.SCE)处的氧化峰和在0.24 V(vs.SCE)处的还原峰显示了Zn2+在Co-MnO2阴极的嵌入/脱嵌过程。为了进一步测试Co-MnO2阴极的电化学性能,将涂敷AC 的CC 作为阳极,在液态电解质(2.0 mol/L ZnSO4+0.2 mol/L MnSO4)中组装的Co-MnO2//AC Zn-HCs 与MnO2//AC Zn-HCs 进行比较。图4(b)展示了两种Zn-HCs 在2 mA/cm2的电流密度下的恒电流充放电(galvanostatic chargedischarge,GCD)曲线。该曲线没有充放电平台且具有较好的对称性,证明Co-MnO2组成的Zn-HC 仍保持着电容器的特性,证实了钴离子的掺入可以提高MnO2的电化学性能。图4(c)展示了Co-MnO2//AC Zn-HCs 在10~80 mV/s 不同扫描速率下的CV 曲线。随着扫描速度的增加,CV 曲线的形状没有发生显著的变化,表明其具有良好的电流响应能力。基于图4(d)和图4(e)的GCD 曲线,根据公式(1)计算得出不同电流密度下Co-MnO2//AC Zn-HCs 和MnO2//AC Zn-HCs 的面积比电容如图4(f)所示。Co-MnO2//AC Zn-HCs 在2 mA/cm2的电流密度下具有5 883.0 mF/cm2的优异的面积比电容,在20 mA/cm2的电流密度下,还保持着1 797.3 mF/cm2的面积比电容。MnO2//AC Zn-HCs 在2 mA/cm2的电流密度下具有3 388.0 mF/cm2的面积比电容,在20 mA/cm2的电流密度下,仅仅产生1 065.5 mF/cm2的面积比电容。这主要归功于钴离子的掺杂使得材料发生晶格畸变,提高了材料的电导率,有利于电子的传输[15,25]。如图4(g)所示,为了进一步研究电极材料的界面动力学行为,对Co-MnO2和MnO2进行了电化学阻抗谱(electrochemical impedance spectroscopy,EIS)的研究,Co-MnO2表相比于比MnO2的曲线与实轴的交点横坐标值最小,其中二者与实轴的交点值分别为7.7 Ω 和8.5 Ω,在高频区的半圆直径最小以及低频直线的斜率最大,表明Co-MnO2内阻和离子扩散电阻较低,具有良好的导电性和较高的离子扩散速率。进一步证实了钴离子的掺杂提高了MnO2的电子电导率和Zn2+的扩散速率,电化学储能得到了提高。如图4(i)所示,Co-MnO2//AC Zn-HCs 在20 mA/cm2的电流密度下循环5 000 次后,初始容量保持率为65.1%,优于MnO2//AC Zn-HCs 在循环2 000 次后,仅55.2%的初始容量保持率,表明Co-MnO2在循环过程中具有较好的循环性能。
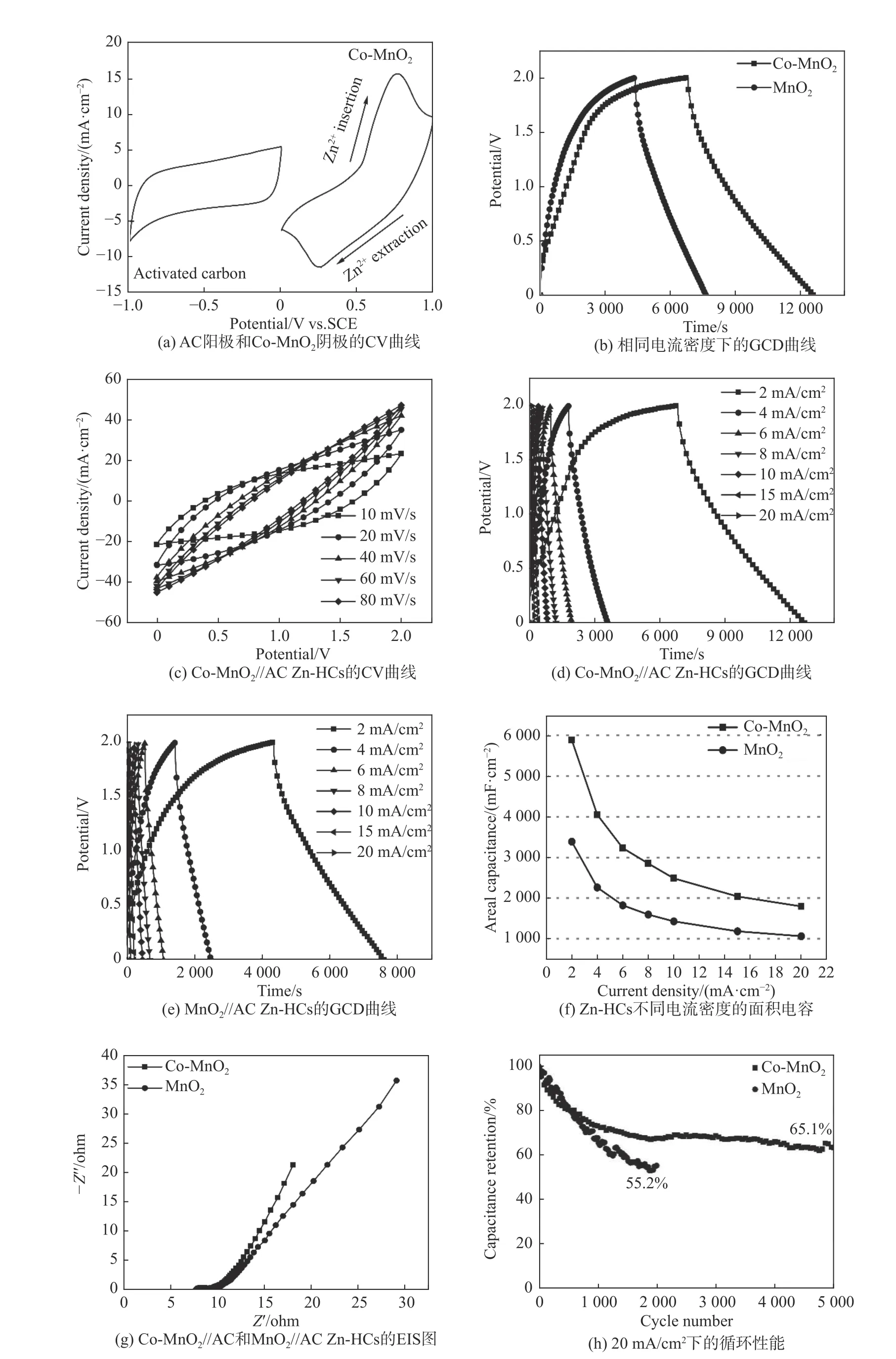
图4 Co-MnO2//AC 和MnO2//AC Zn-HCs 的电化学性能Fig.4 Electrochemical properties of Co-MnO2//AC and MnO2//AC Zn-HCs.
为了证明Co-MnO2//AC Zn-HCs 的实用性,还进行了柔性准固态Zn-HCs 的电化学测试,组装成的柔性准固态Zn-HCs 其结构示意图如图5(a)所示。Co-MnO2//AC 准固态Zn-HCs 在10~80 mV/s的扫描速率范围内的CV 曲线如图5(b)所示。随着扫描速度的增加,CV 曲线的形状没有发生显著的变化,表明其在凝胶电解质下同样具有良好的电流响应能力。图5(c)所示的GCD 曲线显示出较大的面积比电容,具有良好的电化学性能,在电流密度为1 mA/cm2时,面积比电容达到2 506.7 mF/cm2。如图5(d)所示,当将准固态Co-MnO2//AC 锌离子混合电容器弯曲成各种角度时,其CV 曲线基本保持不变,显示出其具有良好的柔性。图5(e)展示了水系和准固态Co-MnO2//AC Zn-HCs 的面积功率密度和能量密度,其中水系Co-MnO2//AC Zn-HCs 的最大面积功率密度为3 154.9 μWh/cm2,最大面积能量密度为13.2 mW/cm2。准固态Co-MnO2//AC Zn-HCs 的最大面积功率密度为1 351.1 μWh/cm2,最大面积能量密度为8.61 mW/cm2。所制备的Zn-HCs的面积能量密度及功率密度高于已报道的水系和准固态Zn-HCs[9,26-29]。此外,如表1 所示,该电极材料组装的Zn-HCs 的面积能量密度已经达到了许多已报道的水系和准固态锌离子电池的水平。

表1 Co-MnO2//AC Zn-HCs 的面积能量密度与报道的锌离子电池进行了比较Tab.1 Area energy density of Co-MnO2//AC Zn-HCs compared with the reported zinc ion cells
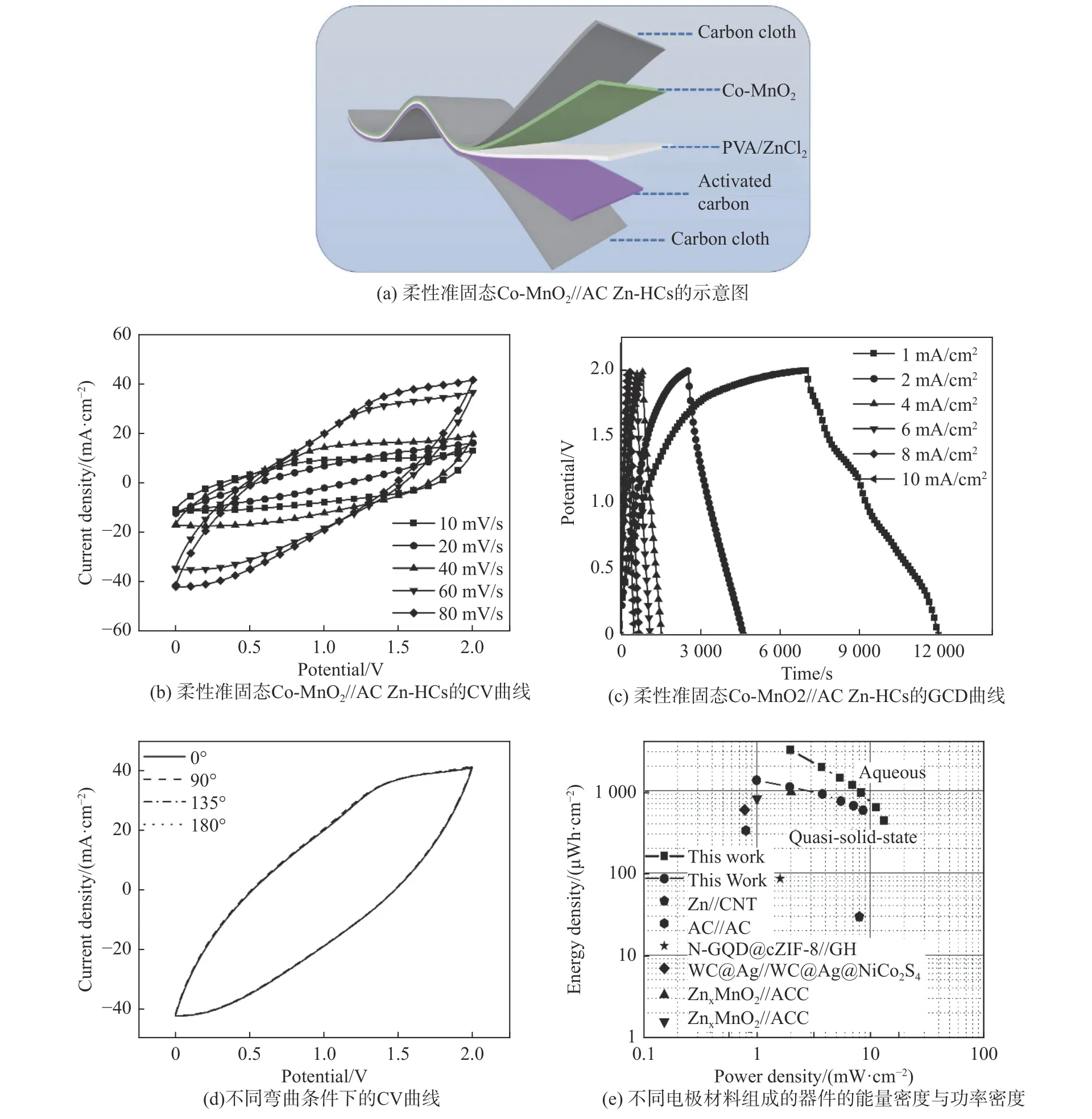
图5 柔性准固态Co-MnO2//AC Zn-HCs 的电化学性能Fig.5 Electrochemical properties of flexible quasi-solid Co-MnO2//AC Zn-HCs
2.3 扩散动力学表征
此外,通过循环伏安法研究了Co-MnO2电极上的电荷储存动力学。图6(a)显示了电极在1、2、5 和10 mV/s 的不同扫描速率下的CV 曲线。CV 曲线中的一对氧化还原峰对应于Zn2+的嵌入/脱嵌过程。随着扫描速率的增加,CV 曲线保持了良好的形状,表明了良好的倍率性能。接下来,通过CV 曲线分析了电极的赝电容的贡献,以解释该电极的优良性能。电极的电化学反应可以由公式:

图6 Co-MnO2 电极的扩散动力学Fig.6 Diffusion kinetics of Co-MnO2 electrode
确定。式中:i为电流;a和b都是常数;v为扫描速率。当b的值接近0.5 时,反应过程依赖于离子扩散控制,当b的值接近1.0 时,反应过程由电容来控制[36]。图6(b)绘制了扫描速率和峰值电位之间的线性关系,峰值1、2 分别对应于b值为0.51 和0.60,这意味着电荷储存过程主要由离子扩散控制,这提供了良好的Zn2+扩散动力学。电极的电容贡献率通过公式:
计算得出。图6(c)展示了在1~10 mV/s 的扫描速率下电容和扩散贡献的柱状图。随着扫描速率从1 mV/s 增加到10 mV/s,电容贡献从33.1%增加到91.3%。较高的电容贡献代表了该电极在水系电解质中的快速反应动力学和优异的倍率性能[37]。
3 结论
本文通过简单的恒流电沉积法,在CC 上生长钴离子掺杂的MnO2,并可以在高负载量(13.8 mg/cm2)的条件下表现出令人满意的面积比电容。以Co-MnO2为阴极组装的水系Zn-HCs 在2 mA/cm2的电流密度下具有5 883.0 mF/cm2的超高面积比电容,面积能量密度为3 154.9 μWh/cm2,以及在20 mA/cm2的电流密度下经过5 000 次完全充放电后,容量保持率达到65.1%。准固态Zn-HCs 同样具有优异的电化学性能。Co-MnO2//AC Zn-HCs 具有优异性能的原因可归结于以下几点:(1)钴离子的的掺杂提高了MnO2的电导率促进了Zn-HCs 在充/放电过程中的电子传输。(2)钴离子的掺杂增大了MnO2的层间距,有利于Zn2+在充放电过程中的迁移扩散。(3)钴离子的掺杂引起了MnO2的晶体结构发生畸变,且钴离子在层间稳定结构,从而有利于在循环中的稳定性。这些原因使得电极材料在高负载量下具有优异的电化学性能。较高的能量密度可与部分已报道的锌离子电池媲美,加上良好的机韧性,有望用作新一代的储能器件,使同时具备高的能量密度和功率密度的储能器件成为可能。
