不同厂家二丁颗粒微生物限度检查方法建立及结果分析评价
2023-12-30李昀铮
李昀铮
松原市食品药品检验所,吉林 松原 138000
二丁颗粒具有清热解毒、利湿退黄的功效,临床上多用于热疖痈毒、咽喉肿痛、风热火眼等相关疾病的治疗[1-2]。其主要药材如紫花地丁、蒲公英以及板蓝根等都具有一定的抑菌效果,因此在对其进行微生物限度检查时,原则上必须遵照《中国药典》要求的方法,先开展供试液抑菌活性的消除工作,之后再推进下一步的检查。
本研究通过对5 个相关生产企业中的15 批次二丁颗粒进行检测,利用方法学验证来找出合适的微生物限度检验方式,进而对选中的5 个生产企业中15 批次的二丁颗粒进行微生物限度检验,然后对检验结果进行分析和探讨,以期为众多二丁颗粒生产企业提供一定的参考。
1 仪器与材料
1.1 仪器
BSC-1304IIA2 苏净安泰生物安全柜、BHC-1300IIA2 苏州安泰生物安全柜、BXP-280S 智能微生物培养箱(上海博讯实业有限公司),SPX-150 生化培养箱(扬州慧科电子有限公司),BPX-272 型电热恒温培养箱(上海博讯实业有限公司),BAXSystem Q7 全自动病原微生物快速检测系统(美国-杜邦),SHZ-82A 水浴恒温振荡器(金坛市白塔金昌实验仪器厂),移液器(德国VITLAB),YXQ-LS-100SII 立式压力蒸汽灭菌器(上海博讯实业有限公司),BXM-30R 立式压力蒸汽灭菌器(上海博讯实业有限公司)。
1.2 样品
本次实验所用到的二丁颗粒是5 家公司共15个批次的产品,见表1。
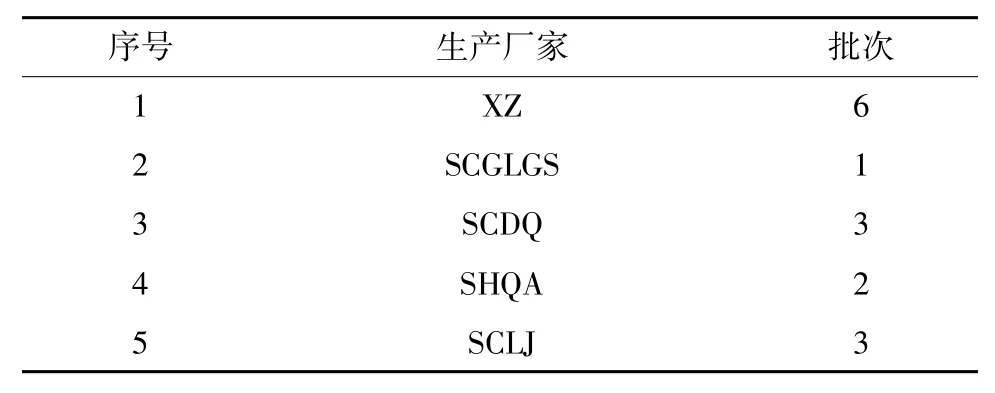
表1 二丁颗粒生产厂家及批次
1.2.1 培养基
胰酪大豆胨琼脂培养基(TSA,批号:220426);胰酪大豆胨液体培养基(9S-CD,批号:220519);沙氏葡萄糖琼脂培养基(SDA,批号:220616);麦康凯液体培养基(批号:220426);麦康凯琼脂培养基(批号:220505)。上述培养基均已通过培养基适用性检查。
1.2.2 稀释液
pH 为7.0 的无菌氯化钠-蛋白胨缓冲液(批号:220118),0.05%(V/V)聚山梨酯80 稀释液,pH 为7.0的无菌氯化钠-蛋白胨缓冲液和稀释液均购于北京路桥技术股份有限公司。0.9%氯化钠,购于天津市科密欧化学试剂有限公司(批号:20200916)。
1.2.3 菌种(传代次数,来源)
金黄色葡萄球菌ATCC6538:第1 代;铜绿假芽孢杆菌ATCC9027:第1 代;枯草芽孢杆菌ATCC6633:第1 代;白色念珠菌ATCC10234:第1 代;黑曲霉菌ATCC16404:第1 代;大肠埃希菌ATCC25922:第1代。来源:美国菌种保藏中心。
2 方法与结果
2.1 菌液的制备
遵照《中国药典》2020 版四部通则1108 的规定进行配制[3]。
2.2 供试液的制备
取供试品10 g,加入100 mL pH 为7.0 的无菌氯化钠-蛋白胨缓冲液中,置于40 ℃恒温水浴并振荡直至其完全溶解,即得到1∶10 的供试液A。利用逐级稀释法,再得到1∶100 的稀释液样品b 和1∶1 000 的稀释液样品c。
2.3 需氧菌总数、霉菌和酵母菌总数计数方法适用性试验
阳性菌组:从“2.1”选项中提前准备好的稀释级菌液中,取出0.1 mL 制备好的菌液(菌量不大于10 000 CFU/mL),将其加入9.9 mL pH 为7.0 的无菌氯化钠-蛋白胨缓冲液中,根据规定量和方法注入平皿和规定的培养基中,将按照规定时间和温度进行培养后测得的菌数记作a;试验组对照组:取5 份10 mL 供试液A 分别和5 种含有0.1 mL 试验菌的菌液置于无菌管中,混匀,并按照上述方法测得菌数b;供试液对照组:取10 mL 供试液A 和0.1 mL pH为7.0 的无菌氯化钠-蛋白胨缓冲液置于无菌管中,按上述方法测得菌数c;计数结果按照如下公式进行计算:回收率:R=(b-c)/a×100%,当R 值在0.5~2范围内对,可认为此法能够用于该样本细菌数量的统计[4-5]。
基于二丁颗粒的抑菌作用,采用供试液按照1:10 培养基稀释法(5 倍稀释法即在5 个平皿中,每个皿中都含有供试液0.2 mL,各加入15~20 mL 胰酪大豆胨琼脂培养基)作为需氧菌总数进行计算,按照规定量和方法注入平皿与规定的培养基中,并按规定时间和温度进行培养后测得回收率的结果。实验表明,以上5 种菌株的回收率范围均在0.5~2 之间。
2.4 大肠埃希菌检验方法适应性检验
试验组:将10 mL 供试液A 接种到100 mL 胰酪大豆胨液体培养基中,并将其与大肠杆菌的菌悬液(不大于100 CFU)混合。阳性对照组:将1 mL 大肠埃希菌菌悬液加入100 mL 胰酪大豆胨液体培养基中。供试液对照组:用供试品代替试验组液体进行试验。阴性对照组:同批灭菌配制、完成灭菌的胰酪大豆胨液体培养基。以上试验组、阳性对照组、供试液组及阴性对照组均按《中国药典》2020年版的四部要求进行试验。
测试结果显示,在15 批次的检验样本中,在测试的对照和阳性对照样本中,大肠埃希菌都是在测试样本(加菌)生长的,供试组(未加菌)以及阴性对照组中均没有生长表现。由此可以得出,此方法适用于本品的控制菌检查。
2.5 此次微生物限度检验结果
根据此次的检验结果,本次试验二丁颗粒的微生物限度标准如下:需氧菌总数不可以超过103CFU/g;霉菌和酵母菌法的总数不可以超过102CFU/g;不可以检出大肠埃希菌。
此次微生物限度检验结果如下:此次试验中15批次的二丁颗粒需氧菌总数,霉菌和酵母菌总数合格率为100%,都没有检出大肠埃希菌。
3 分析
二丁颗粒中的紫花地丁、蒲公英、板蓝根等药材均具有抑菌性。其中紫花地丁提取物的抑菌活性按照大小顺序依次为:停乳链球菌>金黄色葡萄球菌>大肠杆菌>无乳链球菌>乳房链球菌>沙门氏菌[6]。其中蒲公英的多项成分如总黄酮、多糖绿原酸分别对大肠杆菌、沙门氏菌、金黄色葡萄球菌、痢疾杆菌、枯草芽草杆菌等有抑制作用[7];板蓝根能有效抑制金黄色葡萄球菌和枯草芽孢杆菌,具有光谱抗菌作用[8]。通过试验发现不同药厂经过工艺提取后的二丁颗粒对金黄色葡萄球菌、枯草芽孢杆菌和铜绿假单胞菌的抗菌效果各不相同,这可能是因为每个厂家的工艺不同,受工艺影响,其抑菌强度也会有所变化。相信随着技术水平的提高与工艺的完善,中药口服制剂受到的污染因素会有所减少,使微生物限度检查指标提升,药品质量控制进一步发挥作用。
4 结论
本文通过对15 批次二丁颗粒微生物限度的方法学检验,得出如下结果:需氧细菌总数的测定可以使用培养基稀释法,霉菌、酵母菌、大肠埃希菌的测定可以使用常规法。最终研究结果表明,来自5 个生产企业的15 个批次二丁颗粒的微生物限度检查结果都符合规定。
