鸡蛋黄中4种生物活性成分联合提取工艺
2023-12-08郭晓徐刘恒洋尹玉鑫宋绍奇刘美玉
郭晓徐,刘恒洋,尹玉鑫,宋绍奇,刘美玉*
(1.河北工程大学生命科学与食品工程学院,河北 邯郸 056038;2.邯郸市天然产物与功能性食品开发重点实验室,河北 邯郸 056038)
鸡蛋黄约占鸡蛋质量的50%,蛋黄中生物活性成分很多,其中重要成分有卵黄免疫球蛋白(immunoglobulin of yolk,IgY)、卵黄高磷蛋白(phosvitin,PV)、蛋黄油和卵磷脂(phospholipids,PL)[1-2]。IgY 是蛋黄中唯一的免疫蛋白,主要存在于浆液中,约占蛋黄总蛋白的10%[3]。IgY 具有较强的抗菌免疫活性,且安全无毒,同时还具有增强机体的免疫功能的能力[4-5],广泛应用于抗病毒、抗细菌感染、抗肿瘤以及免疫学诊断等领域[6-8],在动物疾病控制中也被广泛应用[9];PV 是一种富含磷酸丝氨酰残基的天然活性蛋白质[10],具抗氧化性[11]、热稳定性和乳化性能,常用于化妆品、营养品、医药制造等领域[12],还可作为钙强化的辅助剂,应用前景广阔[13-14]。蛋黄油药食两用,其味甘、性平,不仅能清热解毒,而且具有杀菌、消炎、止痛和修复表皮细胞的功能[15-16]。PL 在促进神经信号传导、提高大脑活力、延缓机体衰老、防止血管硬化和抗血栓等方面均有显著作用[17],还具有良好的乳化、润湿、分散等作用,广泛应用于食品、医药、化妆品等行业[18-19]。本文采用水稀释法[20]、盐析法[21]、有机溶剂提取法从蛋黄中提取分离卵黄免疫球蛋白、卵黄高磷蛋白、蛋黄油和卵磷脂,探究鸡蛋黄综合利用最大化、提高鸡蛋价值且适合工业化生产的工艺条件,以期为鸡蛋精深加工提供技术依据。
1 材料与方法
1.1 试验材料与试剂
新鲜鸡蛋:邯郸市复兴区标准化养鸡场。
酶联免疫试剂盒:上海研尊生物科技有限公司;考马斯亮蓝(G250、R250):上海康朗生物科技有限公司;牛血清白蛋白(1 mg/mL):合肥博美生物科技有限责任公司;硫酸铵、95%乙醇、正己烷、氯化钠(均为分析纯):天津欧博凯化工有限公司;0.1 mol/L HCl、0.01 mol/L 磷酸盐缓冲液(phosphate buf-fered saline,PBS)(pH7.2):河北工程大学农产品深加工实验室自制。
1.2 仪器与设备
酶标仪(EL311s):赛默飞世尔科技有限公司;冷冻干燥机(SCIENTZ-10ND):宁波新芝生物科技股份有限公司;台式高速冷冻离心机(TG16):湖南湘仪实验室仪器开发有限公司;紫外可见分光光度计(UV-2700):日本岛津仪器有限公司;消化炉(HYP-1040):上海巴玖实业有限公司;多通道磁力搅拌器(SP200-2T):杭州米欧仪器有限公司;台式酸度计(PB-10):赛多利斯公司;生物安全柜(HR40-11A2):青岛海尔生物医疗股份有限公司;电子天平(PX22ZH):奥豪斯仪器有限公司;高温鼓风干燥箱(BPG-9100BH):上海一恒科技有限公司;恒温水浴槽(WT100-18):杭州米欧仪器有限公司。
1.3 试验方法
1.3.1 制备流程
卵黄免疫球蛋白、卵黄高磷蛋白、蛋黄油和卵磷脂4 种活性物质联合提取工艺流程见图1。
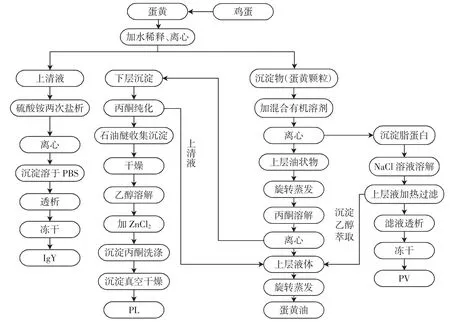
图1 提取工艺流程Fig.1 Scheme of extraction process
1.3.2 IgY 提取的单因素设计
准确称取5 份蛋黄液,每份5 g,分别添加蛋黄液2、4、6、8、10 倍体积的蒸馏水稀释,并用0.1 mol/L 的HCl 调至不同pH 值(4.0、4.5、5.0、5.5、6.0),搅拌均匀,于-20 ℃下冷冻12 h,4 ℃解冻。分别在4 500×g离心(15、25、35、45、55 min)后得到上清液水溶性组分(water soluble fraction,WSF)和沉淀物(脂蛋白)。在上清液中(WSF)加入不同用量的4 ℃饱和硫酸铵,使硫酸铵浓度达到30%、40%、50%、60%、70%,4 ℃下静置12 h,进行第1 次盐析,4 500×g离心25 min 后取沉淀,溶于适量pH7.2 的磷酸盐缓冲液,加入上清液(WSF)体积2/3 的4 ℃蒸馏水和1/3 的4 ℃饱和硫酸铵,进行第2 次盐析,静置4 h,3 000×g离心20 min,取沉淀溶于适量PBS,置于10 kDa 透析袋中,透析脱盐20 h,期间换水6~7 次,冷冻干燥,得IgY 成品。
1.3.3 IgY 提取的正交试验设计
根据IgY 提取的单因素试验结果,选取稀释倍数、pH 值、离心时间、硫酸铵浓度4 个因素,以IgY 含量为判断标准,进行正交试验设计,正交因素与水平见表1。

表1 正交因素与水平Table 1 Factors and levels of orthogonal experiments
1.3.4 PV 提取的单因素设计
将脂蛋白在常温下风干2 h,准确称取5 份,每份3 g。加入不同体积比(1∶0、1∶1、1∶2、1∶3、1∶4)的混合有机溶剂(95%乙醇∶正己烷)。溶剂使用量为脂蛋白的不同倍数(2、4、6、8、10 倍),磁力搅拌30 min,静置8 h,3 000×g离心20 min,取下层胶状物,烘干,用玻璃棒碾碎,溶于不同浓度(1.65、1.70、1.75、1.80、1.85 mol/L)氯化钠溶液中。氯化钠溶液使用量设计为5、10、15、20、25 mL,混合均匀,静置6 h,3 000×g离心20 min,取上清液于不同温度(50、60、70、80、90 ℃)的水浴锅中加热30 min,过滤,收集滤液,置于8~10 kDa透析袋中透析脱盐20 h,冷冻干燥后即为PV 成品。
1.3.5 PV 提取的响应面试验设计
在单因素试验基础上,采用Design-Expert 10.0.8软件,进行Box-Behnken 三因素三水平响应面设计,以混合有机溶剂体积比、溶剂使用量、氯化钠浓度为自变量,以提取的PV 含量为响应值进行优化。其响应面试验设计的因素和水平见表2。

表2 响应面试验因素与水平Table 2 Response surface test factors and levels
1.3.6 蛋黄油和卵磷脂提取
上层油状物是溶解在混合有机溶剂中的蛋黄油、卵磷脂等,提取蛋黄油、卵磷脂首先要去除混合有机溶剂。在45 ℃、50 r/min 的条件下,对上层油状物旋转蒸发,以去除有机溶剂,所得产物加入丙酮溶解,静置5 h,3 000×g离心20 min。取上层液体进行旋转蒸发,直至无液体蒸馏出,得到蛋黄油。下层沉淀用适量无水乙醇溶解,加入丙酮反复碾洗,至丙酮颜色澄清透明,取沉淀,用蒸馏水清洗干净,真空干燥,得淡黄色胶条状卵磷脂(PL)。
1.3.7 指标测定
总蛋白质含量的测定:采用考马斯亮蓝法测定总蛋白质含量[22]。
IgY 含量的测定:使用紫外可见分光光度计分别测定提取液在260 nm 和280 nm 处的吸光值,并以生理盐水作为对照,根据下列公式来计算IgY 含量[23]。
Q=1.50A280-0.75A260
式中:Q为IgY 含量,mg/mL;A280和A260为IgY 在280 nm 和260 nm 处的吸光值。
PV 含量的测定:磷的含量用微量定磷法来检测,由于卵黄高磷蛋白含有约10%的磷,所以有机磷含量的10 倍就是卵黄高磷蛋白的含量[24],计算公式如下。
M=10M1
式中:M为PV 含量,mg/mL;M1为有机磷含量,mg/mL。
PV 回收率的计算公式如下。
R=M1/M2×100
式中:R为PV 回收率,%;M1为PV 含量,mg/mL;M2为回收物中总蛋白质的含量,mg/mL。
IgY 活性的测定:采用酶联免疫试剂盒进行测定。
1.4 数据统计及分析
使用IBM SPSS Statistics 软件对IgY 提取正交试验进行数据统计分析。使用Design-Expert 10.0.8 软件对PV 提取响应面试验进行数据统计分析。
2 结果与分析
2.1 IgY 提取试验结果分析
2.1.1 稀释倍数对IgY 含量的影响
稀释倍数对IgY 含量的影响见图2。
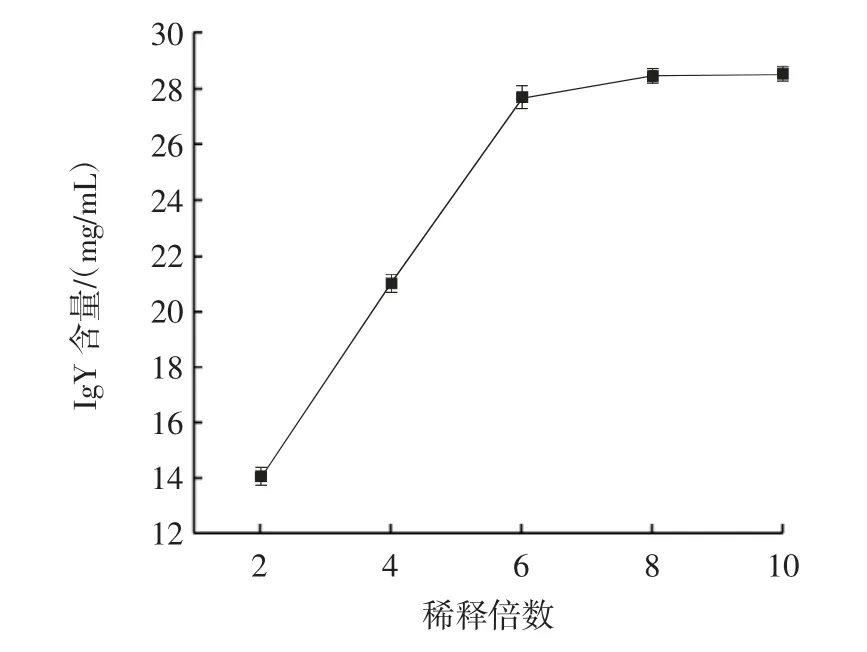
图2 稀释倍数对IgY 含量的影响Fig.2 Effect of dilution fold on IgY content
由图2 看出,随着稀释倍数的增加,IgY 含量呈上升趋势,在稀释6 倍后,上升趋势趋于平缓。根据上清液颜色变化发现稀释4 倍时,上清液颜色浑浊;6 倍时上清液有轻微的淡黄色,稀释8、10 倍后上清液为澄清透明。上清液颜色变化与图2 结合可推断稀释4 倍时,脂蛋白未完全分离,IgY 含量在20 mg/mL 左右。稀释6、8 倍IgY 含量均在28 mg/mL 左右,6 倍为一个转折点。结合实际生产的成本和蛋白质含量,综合考虑稀释倍数选4、6、8 倍较为合适。
2.1.2 pH 值对IgY 含量的影响
pH 值对IgY 含量的影响见图3。

图3 pH 值变化对IgY 含量的影响Fig.3 Effect of pH change on IgY content
由图3 可知,IgY 含量随pH 值的增加呈先升高后降低的趋势。在pH5.0 时IgY 含量为最高值,此时的上清液透明,说明脂蛋白和水溶性蛋白已经分离完全。卵黄免疫球蛋白在pH4~11 时蛋白活性保持稳定,因此,pH 值选择4.5、5.0、5.5 较为合适。
2.1.3 离心时间对IgY 含量的影响
离心时间对IgY 含量的影响见图4。
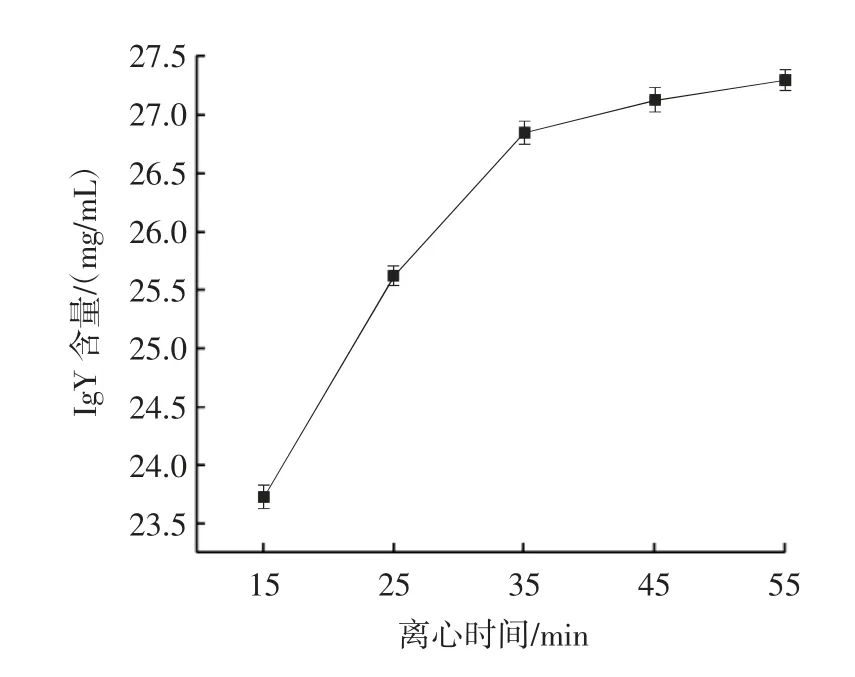
图4 离心时间对IgY 含量的影响Fig.4 Effect of centrifugation time on IgY content
由图4 得出,IgY 含量随离心时间的延长而增加,在离心时间为35 min 后IgY 含量上升缓慢,说明此时溶液中的蛋白均已形成沉淀。从实际生产角度出发,离心时间的延长必然会导致生产成本和机器损耗加大。因此,离心时间选择25、35、45 min 较为合适。
2.1.4 硫酸铵浓度对IgY 含量的影响
硫酸铵浓度对IgY 含量的影响结果见图5。

图5 硫酸铵浓度对IgY 含量的影响Fig.5 Effect of ammonium sulfate concentration on IgY content
由图5 可知,随着硫酸铵浓度的增加,IgY 含量整体呈现上升趋势,硫酸铵浓度为60%时,IgY 含量最高,随后含量下降。高浓度的盐离子在蛋白质溶液中会与蛋白质竞争水分子,使蛋白质从溶液中沉淀出来,但是过高的盐浓度会增加后期的脱盐工作量,也会导致脱盐不彻底,降低IgY 蛋白含量和纯度。因此硫酸铵浓度选择50%、60%、70%较为合适。
2.1.5 IgY 提取的正交试验结果分析
IgY 提取的正交试验结果见表3。
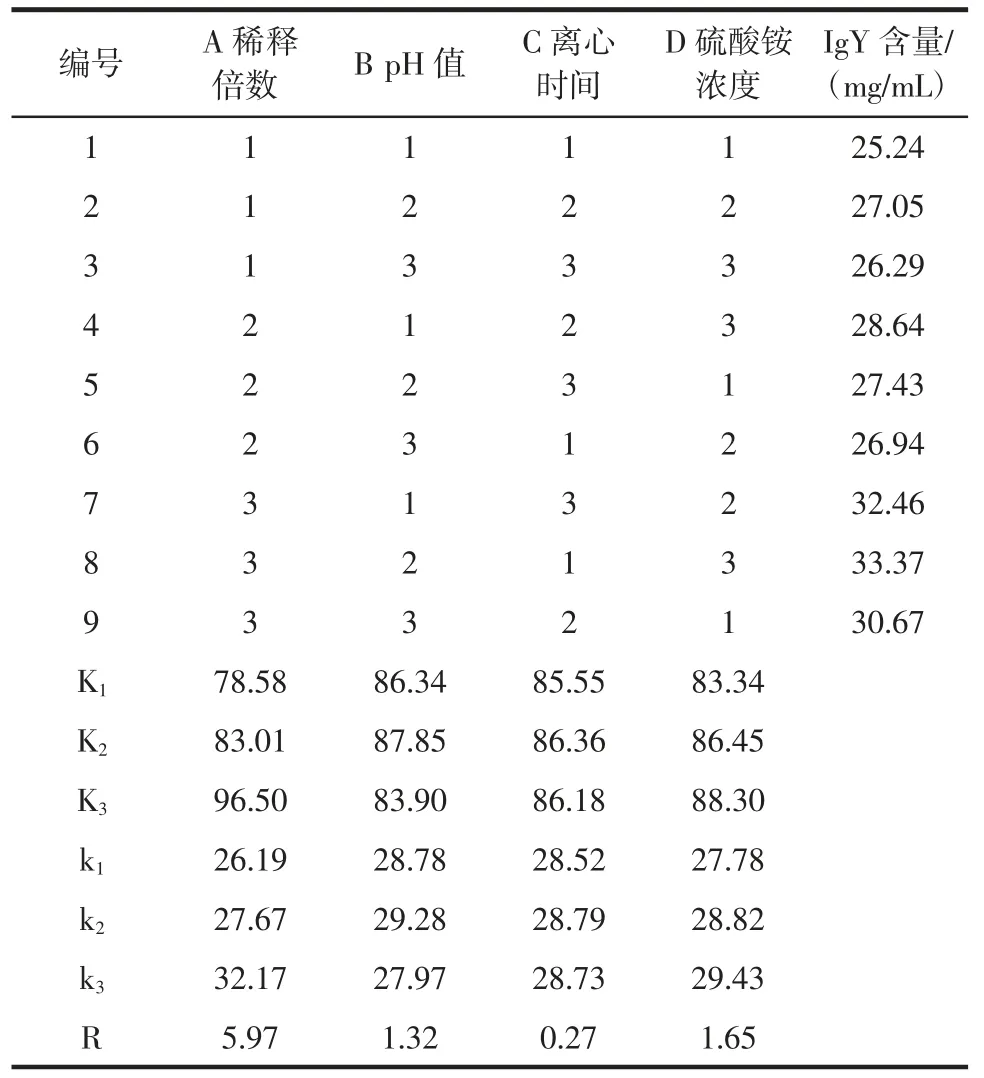
表3 IgY 提取的正交试验结果Table 3 Orthogonal experimental results of IgY extraction
由表3 可知,各因素对IgY 含量影响顺序为稀释倍数>硫酸铵浓度>pH 值>离心时间。IgY 含量最高的正交试验组为第8 组,5 g 蛋黄液可提取出33.37 mg卵黄免疫球蛋白。直观分析最优组合为A3B2C1D3,然而均值的最优组合为A3B2C2D3。其差别在于离心时间的选择,考虑到实际生活中大规模的生产和成本,离心时间的选择越小越好,故最优组合为A3B2C1D3。
对最优组合进行验证试验,其平均值为33.22mg/mL。与试验结果33.37 mg/mL 非常接近,试验重复性很高。
IgY 提取方差分析结果见表4。

表4 IgY 提取方差分析Table 4 Analysis of variance of IgY extraction
由表4 可知,各因素对结果的影响大小为稀释倍数>硫酸铵浓度>pH 值>离心时间,与直观分析结果一致。其中稀释倍数、硫酸铵浓度、pH 值对结果影响极显著(P<0.01),离心时间对IgY 含量影响不显著(P>0.05)。进一步说明试验稳定性良好。
2.2 PV 提取试验结果
2.2.1 不同混合有机溶剂体积比对PV 含量的影响
不同混合有机溶剂体积比对PV 含量的影响见图6。
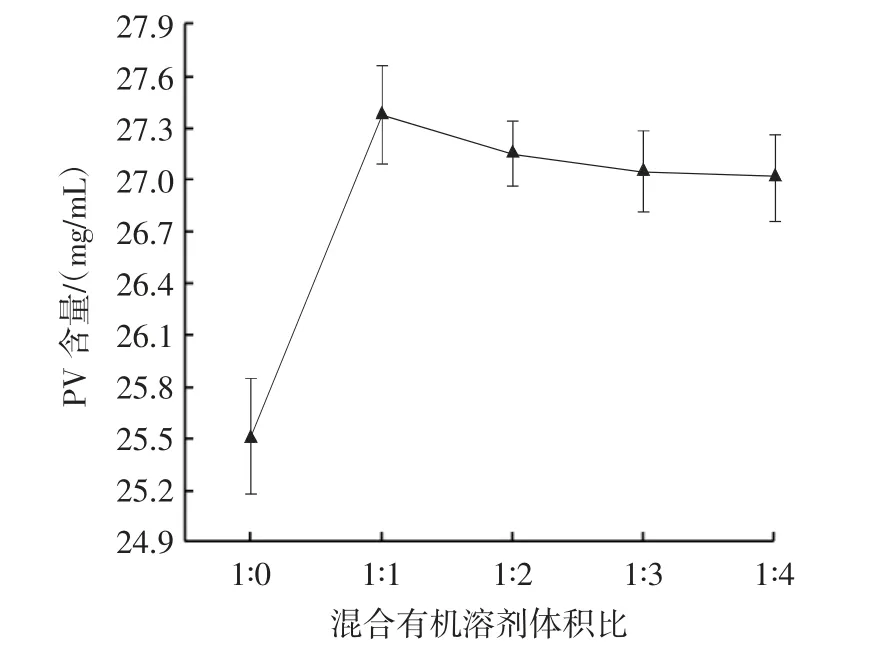
图6 混合有机溶剂体积比对PV 含量的影响Fig.6 Effect of volume ratio of mixed organic solvent on PV content
由图6 可知,卵黄高磷蛋白的含量随着混合有机溶剂中正己烷的增加先升高后降低。正己烷的存在能够加强脂类和蛋白质的分离效果,随着正己烷的增加,在收集卵黄高磷蛋白时,附着在烧杯壁上的蛋白也随之增加,收集不彻底可能是导致蛋白含量降低的原因。如用混合有机溶剂收集附着在烧杯壁上的蛋白会造成溶剂使用量的变化,影响结果。从生产成本和蛋白含量的角度出发,选用混合有机溶剂体积比为1∶0、1∶1、1∶2 较为合适。
2.2.2 不同溶剂使用量对PV 含量的影响
不同溶剂使用量对PV 含量的影响见图7。

图7 溶剂使用量对PV 含量的影响Fig.7 Effect of solvent usage on PV content
由图7 可知,PV 含量随有机溶剂使用量的增加而增加,在使用量为6 倍混合有机溶剂时蛋白含量没有大的变化,说明此时有机溶剂的作用已可以做到蛋白质和脂类分离效果的最大化。此后溶剂使用量的增加不会增加生产效益,还会使生产成本加大,环境污染加大。综合考虑选用6 倍溶剂使用量进行后续试验。
2.2.3 不同氯化钠浓度对PV 含量的影响
不同氯化钠浓度对PV 含量的影响见图8。
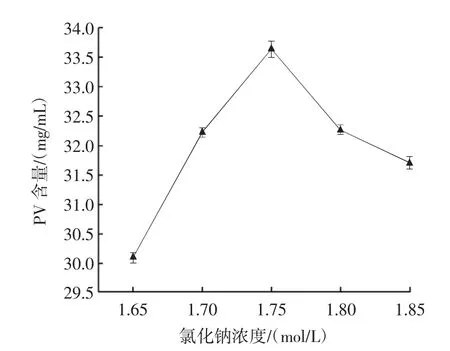
图8 氯化钠浓度对PV 含量的影响Fig.8 Effect of NaCl concentration on PV content
由图8 可知,卵黄高磷蛋白在一定浓度的NaCl 溶液中有较好的溶解性,卵黄高磷蛋白在1.65~1.85 mol/L NaCl 溶液中蛋白溶解性先增加后下降,1.75 mol/L 的NaCl 溶液中溶解性最好,提取蛋白含量最高。实际生产中NaCl 浓度增加会加大成本。综合考虑,NaCl 溶液浓度选择1.70、1.75、1.80 mol/L 较为合适。
2.2.4 不同氯化钠用量对PV 含量的影响
不同氯化钠用量对PV 含量的影响见图9。

图9 氯化钠用量对PV 含量的影响Fig.9 Effect of sodium chloride dosage on PV content
由图9 可知,NaCl 溶液作为卵黄高磷蛋白的溶解剂对结果而言是比较稳定的,PV 含量在NaCl 用量15 mL 和25 mL 处有较高值,随着用量的增加对结果的影响幅度在0.2 mg 以内。用量的增加必然会加大后续的脱盐流程的工作量,从成本和蛋白含量两方面考虑,选用15 mL 作为NaCl 的用量。
2.2.5 不同温度对PV 含量的影响不同温度对PV 含量的影响见图10。
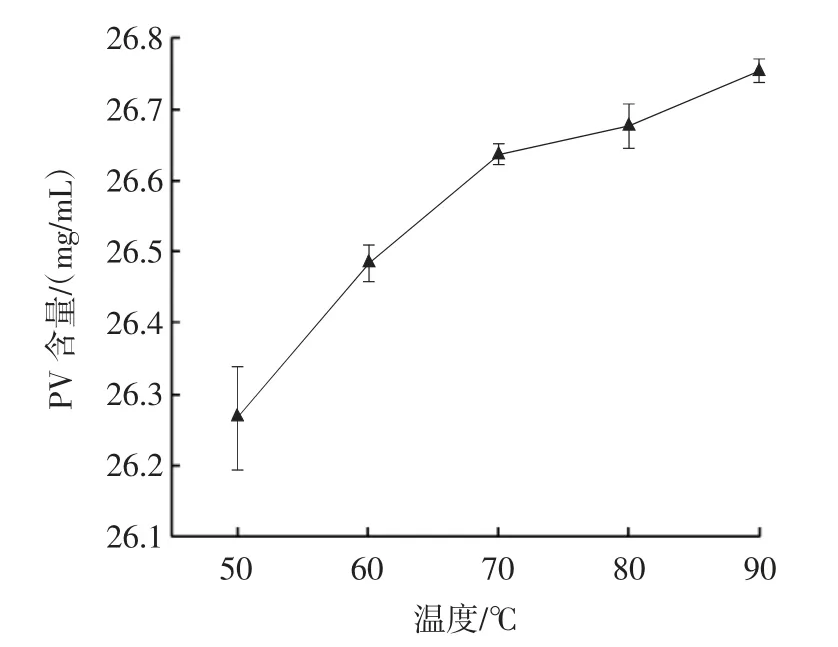
图10 温度对PV 含量的影响Fig.10 Effect of temperature on PV content
由图10 可知,随着温度的升高,卵黄高磷蛋白的含量也会随之增加,在50~90 ℃范围内,蛋白含量增幅在0.5 mg 以内。卵黄高磷蛋白具有较好的热稳定性,温度的升高会使其它的蛋白变性从而沉淀下来,起到一定的纯化效果。从纯度和含量等方面考虑,以90 ℃作为温度最佳选择。
2.2.6 PV 响应面试验结果分析
对PV 提取的工艺以单因素试验确定的水平因素,结合卵黄高磷蛋白含量,根据表2 进行响应面提取优化,结果如表5、表6所示。

表5 响应面设计试验结果Table 5 Experimental results of response surface design

表6 模型方差分析Table 6 Analysis of variance
PV 含量的二次回归拟合方程:PV 含量/(mg/mL)=33.35+0.747 5A+0.581 3B-0.316 3C+0.305 0AB+0.425 0AC-0.647 5BC-4.95A2-1.91B2-3.54C2。
通过表6 的模型方差分析可以得出,A、B对PV含量显著影响(P<0.05),A2、B2、C2均为极显著(P<0.01),C影响不显著(P>0.05),且各因素之间的交互作用不显著,并且对响应值卵黄高磷蛋白含量的影响顺序为A>B>C。
根据回归方程得出各因素之间交互作用对PV 含量影响的响应面和等高线,见图11。

图11 各因素交互作用的响应面与等高线Fig.11 Response surface and contour map of interaction of various factors
根据二次回归方程得到响应面图均为凸起开口向下的曲面,表示PV 含量存在最大值,响应曲面的坡度越陡说明变化越快,对试验结果影响越显著;等高线呈椭圆形、越密集,交互作用越强,等高线呈圆形、越稀疏则相反。
由图11 可知,A、B、C三者间的两两交互作用对PV 含量影响不显著,该结论与方差分析结果一致。
2.2.7 结果验证
根据回归模型,利用Box-Behnken 对试验结果进行分析处理,得到提取卵黄高磷蛋白的最佳条件为混合有机溶剂体积比为1∶1.078、有机溶剂使用量为6.34 倍、氯化钠浓度为1.747 mol/L,测得卵黄高磷蛋白含量为33.437 mg/mL。
为检验响应面优化结果的可靠性,综合考虑实际操作的局限性,取混合有机溶剂体积比为1∶1.08、有机溶剂使用量为6.35 倍、氯化钠浓度为1.75 mol/L。在此最优条件下进行5 次验证试验,卵黄高磷蛋白含量为33.30 mg/mL,与理论值比较,相对误差较小,重复性好,因此该优化提取工艺参数模型准确可靠。此方法为取3 g 沉淀物(脂蛋白),而5 g 蛋黄液可得到4.5 g沉淀物(脂蛋白),5 g 蛋黄液可得到49.95 mg PV,即1 g蛋黄液可得9.99 mgPV。
2.3 蛋黄油和卵磷脂分离结果分析
上层液体旋转蒸发后得蛋黄油,下层沉淀经丙酮纯化、真空干燥后得卵磷脂,实测值与理论值见表7。

表7 试验实测值与理论值比较Table 7 Comparison between measured value and theoretical value
从表7 看出,蛋黄油提取含量偏低,其原因为采用溶剂萃取法提取蛋黄油,参考文献[25]出油率仅60%左右,此方法提取率偏低。提取过程中多次离心分离,也可能导致脂类附着于离心管上,造成含量偏低。
卵磷脂提取量与理论值相接近,提取产品颜色为淡黄色。高纯度的卵磷脂颜色为淡黄乳白色,这说明本方法提取的卵磷脂纯度较高。
3 结论
本文探索了以鸡蛋黄为原料,制备卵黄免疫球蛋白、卵黄高磷蛋白、蛋黄油、蛋黄卵磷脂的工艺流程。新鲜蛋黄预处理后的蛋黄液在一定条件下应用不同的提取方法,通过单因素试验选取因素、以正交试验或响应面试验对工艺进行优化,结果表明,正交试验优化IgY 提取的最优工艺条件为5 g 蛋黄稀释8 倍、调pH 值到5.0、离心时间为35 min、硫酸铵浓度为70%;响应面优化PV 提取的最佳提取工艺条件为混合有机溶剂体积比(95%乙醇∶正己烷)1∶1.08、有机溶剂使用量为6.35 倍、氯化钠浓度为1.75 mol/L。在此条件下5 g 蛋黄可得33.30 mg IgY、49.95 mg PV、0.97 g 蛋黄油、0.53 g PL,换算得1 g 蛋黄得6.66 mg IgY、9.99 mg PV、194 mg 蛋黄油、106 mg PL。该方法成本低、无污染、便捷、高效,可为功能食品提供功能基料,极大提高鸡蛋附加值,保障蛋鸡业健康可持续发展。
