基于美国FAERS的伊沙佐米风险信号挖掘Δ
2023-12-01赵新才张剑萍上海交通大学医学院附属第六人民医院药剂科上海200233
杨 莉,赵新才,徐 嵘,张剑萍 (上海交通大学医学院附属第六人民医院药剂科,上海 200233)
多发性骨髓瘤(multiple myeloma,MM)是克隆浆细胞异常增殖的血液系统恶性肿瘤,多发于老年人,常见症状包括骨髓瘤相关器官功能损伤,如血钙增高、肾功能损害、贫血、骨病、继发淀粉样变性等[1]。目前,该病相关治疗方案的显著进展是引入了蛋白酶体抑制剂(proteasome inhibitor,PI)、免疫调节剂、针对骨髓瘤细胞表面抗原的单克隆抗体和自体造血干细胞移植[2]。
伊沙佐米是全球首个口服PI,主要通过抑制蛋白酶体的生物功能来发挥杀伤肿瘤细胞的作用,现多与来那度胺和地塞米松联合(即“IRd 方案”),用于既往接受至少1种药物治疗的MM成人患者[3]。该药于2015年在美国获批上市,于2018年在我国上市并于同年进入国家医保目录,使得我国MM患者的用药可及性大大提高。然而在临床广泛应用的同时,该药的安全性也备受重视。研究指出,伊沙佐米会增加患者3级以上血小板减少、腹泻、皮疹、周围神经病变的发生率;除此之外,该药还可引起恶心、呕吐、便秘、周围水肿和背痛等常见的不良反应[4―5]。上述安全信息虽已被药品说明书收录,但为更好、更全面地了解和评估伊沙佐米的安全性,本研究拟对美国FDA 不良事件报告系统(FDA adverse event reporting system,FAERS)数据库收录的相关药品不良事件(adverse drug event,ADE)报告进行提取和分析,进一步为临床规范、合理使用该药提供参考。
1 资料与方法
1.1 数据来源
本研究的原始数据来源于FAERS 数据库,利用Open Vigil 2.1 在线工具(http://h2876314.stratoserver.net:8080/OV2/search/)进行相关数据查询、清洗及提取。FAERS 数据库是自发呈报数据库,由美国FDA 每季度更新1 次[6]。Open Vigil 2.1 是一种公开且免费的、可在线使用以解析FAERS数据库数据的药物警戒分析工具,会自动剔除信息不完整和重复的报告,可一定程度地提高纳入报告的整体质量[7]。
本研究数据提取起始时间为伊沙佐米在美国获批上市的时间(2015年11月20日),截止时间为Open Vigil网站最近更新的时间(2023年3月31日)。目标药物的检索通用名限定为“ixazomib”,同时将“role of drug”限定为“首要怀疑药物(primary subject)”。
对于从网站中提取到的原始数据,以1例“个人安全报告(individual safety reports,ISR)”作为1 例ADE 来进行统计。
1.2 信号挖掘与分析
本研究基于比例失衡法的2×2列表(表1),采用报告比值比(proportional reporting ratio,PRR)法和贝叶斯置信区间递进神经网络(Bayesian confidence propagation neural nework,BCPNN)法对伊沙佐米的风险信号进行挖掘[8]。PRR 法阳性信号的判定标准为:在目标药物ADE 发生数(DE)≥3 的情况下,若PRR≥2 且χ2≥4,则记作1个阳性信号;PRR值越大,阳性信号则越强,即伊沙佐米与该ADE 之间的相关性越强[9]。BCPNN 法阳性信号的判定标准为:计算信息成分(information component,IC)值及其下限(IC-2SD),0<IC-2SD≤1.5为弱信号,1.5<IC-2SD≤3 为中信号,IC-2SD>3 为强信号[10―11]。数据分析采用WPS表格(2023版)软件。同时,原始数据采用国际人用药品注册技术协调会编制的国际医学用语词典(Medical Dictionary for Regulatory Activities,MedDRA)25.1 版对信号的系统器官分类(system organ class,SOC)和首选术语(preferred term,PT)进行标准化编码。
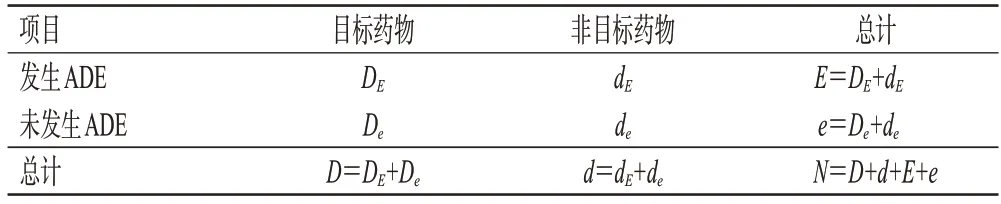
表1 比例失衡法的2×2列表
2 结果
2.1 伊沙佐米相关ADE报告的基本情况
本次研究共提取到13 841份以“伊沙佐米”为“首要怀疑药物”的ADE报告。其中,男性占比(49.53%)略高于女性(45.52%);在排除年龄缺失的数据(6 221例)后,65 岁及以上患者居多(72.48%);报告分别来自57 个国家/地区,上报最多的是美国(52.90%),随后依次是加拿大(14.11%)、日本(9.15%)、英国(6.57%)、法国(5.12%)、中国(3.53%)等。结果见表2。
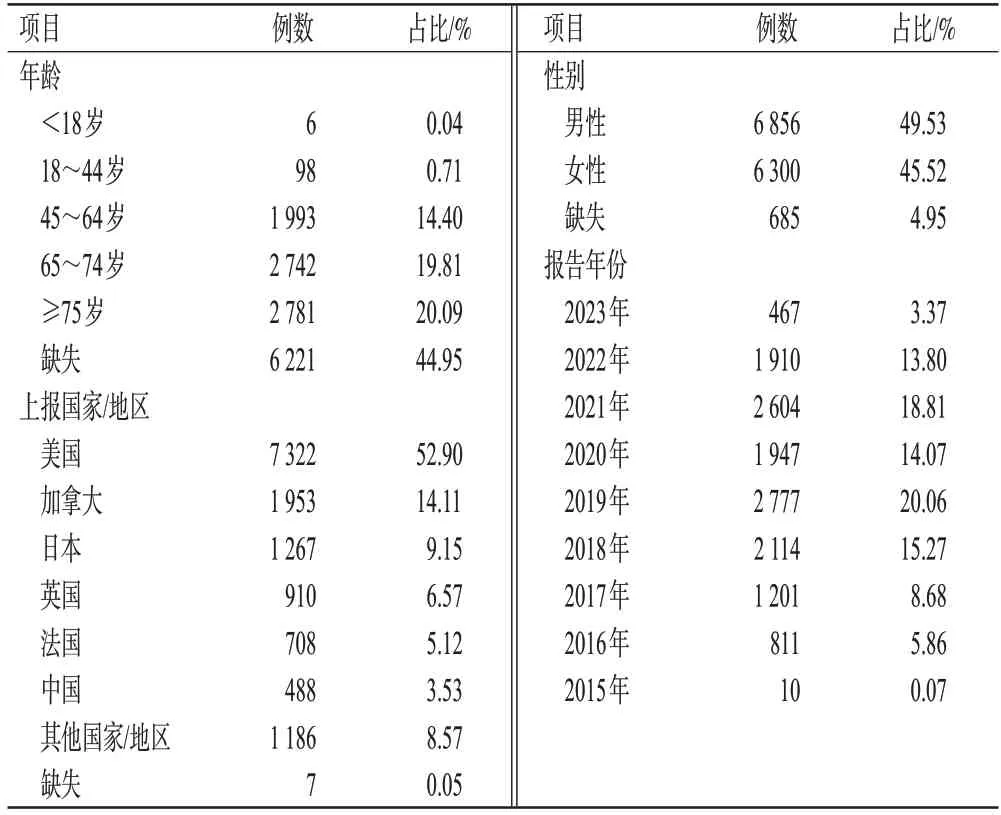
表2 伊沙佐米相关ADE报告的基本情况(n=13 841)
2.2 伊沙佐米阳性信号分析结果
排除适应证相关和完全不相关的PT 后,本研究共获得以伊沙佐米为“首要怀疑药物”且经PRR、BCPNN法判定均为阳性的信号共186 个,涉及患者13 538 例。其中,周围神经病、血小板计数降低、血小板减少症、血细胞减少症、神经病学症状的发生频次和PRR信号强度均排在前50位,具体见表3。
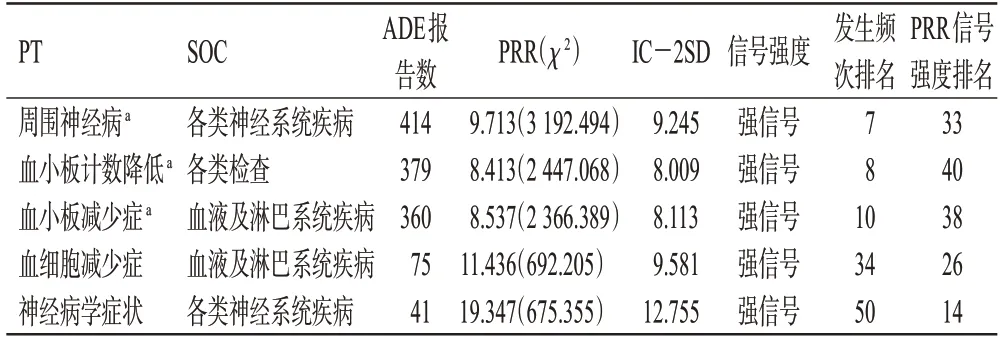
表3 伊沙佐米ADE 发生频次和PRR 信号强度均排前50位的阳性信号
伊沙佐米186个阳性信号PT中,包含强信号51个、中信号99 个、弱信号36 个,累及SOC 共19 个。其阳性信号主要集中在全身性疾病及给药部位各种反应(2 687例)、胃肠系统疾病(2 588例)、感染及侵染类疾病(1 705例)等。结果见表4。

表4 伊沙佐米信号累及SOC情况和对应PT信号强度等级划分
3 讨论
3.1 伊沙佐米阳性信号分析
本研究发现,伊沙佐米在周围神经病(414 例,PRR=9.713,强信号)、血小板计数降低(379 例,PRR=8.413,强信号)、血小板减少症(360 例,PRR=8.537,强信号)、血细胞减少症(75 例,PRR=11.436,强信号)、神经病学症状(41 例,PRR=19.347,强信号)这5 个PT 的发生频次和信号强度均排在前50 位内,主要累及SOC为各类神经系统疾病、各类检查、血液及淋巴系统疾病,与目前各项真实世界研究中常见的不良反应基本相符[12―13]。此外,上述各类神经系统疾病和血液及淋巴系统疾病2 个SOC 还包含一些未被药品说明书记载但呈中/强度的阳性信号PT,如痴呆、共济失调、肌阵挛、舞蹈病、脊髓压迫、异常感觉、感觉减退、认知障碍、味觉障碍、多发神经病、发热性骨髓再生障碍、贫血,对于这些相关症状,临床应予以关注。
3.1.1 累及胃肠系统疾病的阳性信号分析
伊沙佐米相关ADE 发生频次最多的是全身性疾病及给药部位各种反应(2 687 例),但强信号死亡和ADE的定义过于宽泛,讨论意义不大。排除这2 个PT 后,伊沙佐米致ADE 发生频次最多的是胃肠系统疾病(2 588例)。其中,发生频次较多的有腹泻(1 077例,强信号)、恶心(737 例,中信号)、呕吐(459 例,中信号)、便秘(275例,中信号),上述信号均已被药品说明书收录。值得注意的是,肠梗阻(机能性)(12 例,中信号)可能是伊沙佐米的重度胃肠道安全事件,也可能是其新的潜在不良反应。
3.1.2 累及感染及侵染类疾病的阳性信号分析
感染及侵染类疾病阳性信号包含的PT 较多且大多尚未被药品说明书收录。其中,强信号PT 有12 个(1 030例)、中信号PT有30个(627例),主要涉及肺部感染、上呼吸道感染、胃肠道感染、脓毒症、带状疱疹等。国内一项多中心真实世界研究报道了多例伊沙佐米引起肺部感染、上呼吸道感染和肠道感染的病例[14];另一项多中心临床Ⅱ期研究也提及,肺炎是伊沙佐米使用者常见的严重ADE[15],这些报道与本次研究结果基本相符。可见,在使用伊沙佐米时,临床应重点关注该药致感染的相关ADE,尤其是肺部感染的发生。
3.1.3 累及心脏器官疾病的阳性信号分析
MM患者通常年龄较大,且携带心血管毒性累积的危险因素,增加了PI的心脏毒性负荷[16]。在本研究收集到的心脏器官疾病中/强度阳性信号中,心脏淀粉样变性(7例,强信号)和急性冠脉综合征(14例,强信号)均未在中文药品说明书中被提及,临床需予以重视。
虽然伊沙佐米作为可逆性PI,其心血管毒性事件并不常见,但国外学者曾报道过1例患者在接受伊沙佐米治疗后出现急性失代偿性心力衰竭,且停药后左心室功能未能恢复正常[16];国内的一项真实世界研究也报道了2 例患者接受IRd 方案治疗后,因出现3~4 级心力衰竭且并发心脏淀粉样变性而停药[14]。可见,上述2 个心脏器官疾病强信号可能是伊沙佐米新的潜在不良反应,有必要进一步评价其实际临床意义。
3.1.4 累及肾脏及泌尿系统疾病和其他的阳性信号分析
本研究收集到肾脏及泌尿系统中/强度阳性信号只有1个,即肾功能损害(91例,中信号),在各类检查中还收集到了51例血肌酐升高(中信号)的病例报告。肾功能损害本身是MM 的并发症之一,根据相关研究,伊沙佐米的肾清除率较低,当复发/难治性MM 患者的肌酐清除率低于30 mL/min 时,需选择较低的起始剂量(3 mg)[17]。2017、2018年相关研究分别报道了2 例与伊沙佐米相关的药物致血栓性微血管病的病例,这2例患者均表现出了急性肾损伤症状[18―19],可能与PI免疫介导和剂量依赖性毒性等因素所致的内皮细胞损伤及微血管病变有关[20]。国内一项回顾性研究也报道了1例接受伊沙佐米方案治疗后出现短暂肌酐升高,予保肾治疗后回落的病例[13]。可见,伊沙佐米有导致MM患者肾功能损害的可能,但两者的关联还需更多临床研究予以证实。
另外值得一提的是,超说明书使用(1 306 例)在伊沙佐米相关ADE发生频次中排第2位,临床需进一步关注该药的实际应用情况,保证其应用的合理性、规范性。
3.2 数据挖掘的局限性
数据挖掘作为一种广泛应用于药物不良反应监测的方法,可在数据量庞大的ADE报告中检测风险信号,有利于药物潜在不良反应的发现。但由于FAERS 数据库中的信息是自发上报的,且参与上报的人员并非全是医务人员,上报质量也参差不齐,故常存在上报数据缺失、漏报,患者实际临床信息缺失,难以排除其他风险因素等不足[21]。Open Vigil 在线工具虽已对不完整的上报数据进行了筛选,但也一定程度地导致了样本脱落,这些因素最终都会不可避免地对数据挖掘结果产生不利影响。另外,本研究以PRR 法和BCPNN 法所挖掘出的阳性信号仅能说明药物与ADE信号之间存在统计学关联,但其明确的临床意义还需真实世界研究予以验证。
综上所述,基于FAERS数据库挖掘的伊沙佐米风险信号中,上报频次较多的ADE基本与药品说明书记载相符,也与目前各真实世界研究的常见不良反应相符,主要涉及胃肠系统疾病、各类神经系统疾病和血液及淋巴系统疾病;感染及侵染类疾病中出现中/强度阳性信号PT最多,且多数未被药品说明书记载,主要表现在肺部感染、上呼吸道感染、胃肠道感染、脓毒症、带状疱疹等方面;心脏器官疾病中的强信号急性冠脉综合征、心脏淀粉样变性可能是该药新的潜在不良反应;肾功能损害与伊沙佐米ADE的关系还需进一步讨论。可见,除需常规关注的伊沙佐米相关胃肠系统疾病、各类神经系统疾病、血液及淋巴系统疾病等常见ADE外,临床还需关注患者在治疗期间可能出现的各种感染,密切监测其心血管毒性和肾功能损害的发生,保证患者用药的安全、有效。
