基于柠檬酸的氮掺杂碳量子点对Fe3+的检测
2023-11-09阮丽琴徐仕玲
阮丽琴, 徐仕玲, 朱 航
( 莆田学院 药学与医学技术学院, 福建 莆田 351100 )
0 引言
碳量子点作为一种新型纳米材料,因特有的光学与化学性质、良好的生物相容性[1-3]、制作成本低廉等而获得了科学界和工业界的广泛关注,并且成功应用于荧光探针、药物传递、生物成像及传感器等多个领域[4]。 相较于传统半导体量子点而言,碳量子点的合成更加简便、环保,且碳量子点具有生物毒性低、水溶性好、光学性质稳定等优点,是科研材料的首选。 碳量子点的制备方法可以分为两个大类:自上而下法和自下而上法[4]。 在早期,为提高碳点的荧光效率,通常需要在碳点合成过程中加入强酸或强碱[5-6]。 而现在,制备碳量子点多采用一些价格低廉且具有良好生物相容性的材料,包括L-谷氨酸、烟丝、香菇、柠檬酸、大豆和芝麻等[7-9],但大部分合成出来的碳量子点荧光量子产率依旧相对较低。 为了提高碳量子点的荧光性能,人们尝试了不同的办法,包括对碳量子点进行表面钝化、官能团的修饰、杂元素掺杂等。 其中,在碳量子点合成过程中掺杂N、S 等元素能够显著提高荧光量子产率[10-11]。
铁是生物体内不可缺少的金属元素之一[12-13],多以Fe2+、Fe3+的形式存在于人体内。 研究表明,高浓度的Fe3+会激增部分癌症的发病率以及对部分器官(心脏、肝脏等) 功能的损害[14-15]。 铁污染是指铁对生活环境以及生活用水的污染。 铁毒性小,但水体中铁化合物浓度为0.1~0.3 mg·L-1时,会影响水的色、嗅、味等性状,当水中Fe3+浓度增大时,会引起水质污染并且对生活环境造成破环,严重影响居民的生活用水与生存条件,从而危害人体健康。 因此,如何快速准确地检测环境中Fe3+的含量有着十分重要的意义。 本文使用简单快捷的熔融法合成了具有良好荧光性能的氮掺杂碳量子点(N-CQDs), 其荧光猝灭程度与Fe3+浓度呈正相关关系, 可用于建立快速检测溶液中Fe3+浓度的方法。
1 材料与方法
1.1 实验仪器与试剂
实验仪器: F-7000 荧光分光光度计(日立科学仪器(北京)有限公司), TU-1950 双光束紫外-可见分光光度计(北京普析通用仪器有限责任公司), Nicolet iS20 傅里叶变换红外光谱仪(赛默飞科技公司)。 实验试剂: PBS 缓冲溶液(上海阿拉丁生化科技股份有限公司), 一水合柠檬酸、 氯化镍(NiCl2)、 氯化铬(CrCl3)、 硫酸铜(CuSO4)、 硫酸镁(MgSO4)、 氯化钴(CoCl2)、氯化钙(CaCl2)、 氯化铝(AlCl3)、 氯化铁(FeCl3)、 氯化亚铁(FeCl2)、 氢氧化钠(NaOH)等均为分析纯(国药集团化学试剂有限公司),四乙烯五胺(上海麦克林生化科技有限公司)。
1.2 N-CQDs 的合成
取5.0 g 一水合柠檬酸置于50 mL 的圆底烧瓶中, 放入油浴锅中加热到150 ℃, 使其熔融,并在熔融状态下搅拌10 min, 用移液器逐滴加入1.0 mL 四乙烯五胺, 搅拌1h。 在这1h 内, 液体充分混合反应产生少量白烟, 由无色液相逐渐变为黑褐色稠状物, 取出后冷却至室温, 稠状物变硬形成类似糖块的物体。 将糖块状物加入10 mL 去离子水充分溶解并移至离心管中, 得到的N-CQDs 母液, 将其放置于避光处, 4℃冷藏备用。
1.3 N-CQDs 稳定性的考察
取适量的N-CQDs 母液用去离子水稀释104倍, 记录其初始荧光强度值, 然后等量分装三管,体积均为10 mL。 其中两管用于探究N-CQDs 溶液的时间稳定性, 分别标记实验起始日期, 一管常温保存, 一管4 ℃冷藏保存, 不定期检测溶液的荧光强度。 观察不同温度保存条件下, N-CQDs溶液荧光强度的变化情况。 另外一管用于探究N-CQDs 溶液的光稳定性, 记录N-CQDs 溶液的初始荧光强度后, 将溶液放置于354 nm 紫外灯光下连续照射10 h, 每间隔2 h 测一次荧光强度。
1.4 pH 值对N-CQDs 荧光强度的影响
取适量的N-CQDs 母液, 使用pH 值为4.0~10.0 的PBS 缓冲溶液稀释104倍, 同时也使用去离子水稀释N-CQDs 母液至相同的浓度作为对照, 记录它们的荧光强度值进行比较。
1.5 金属离子对N-CQDs 荧光强度的影响
取适量的N-CQDs 母液用去离子水稀释104倍, 记录下其初始荧光强度值, 备用。 配制浓度均为1 mmol·L-1的Ni2+、 Cr3+、 Cu2+、 Mg2+、Co2+、 Ca2+、 Al3+、 Fe3+、 Fe2+溶液, 各取1 mL 分别置于9 个试管内, 然后分别加入9 mL 稀释后的N-CQDs 溶液, 均匀混合, 混合溶液的金属离子浓度均为0.1 mmol·L-1, 静置1 h, 再测各混合溶液的荧光强度F。 另取一试管, 加入1 mL去离子水和9 mL 稀释后的N-CQDs 溶液, 混匀后, 测其荧光强度F0, 作为空白对照。
1.6 N-CQDs 对Fe3+的检测
取足量的N-CQDs 母液用去离子水稀释104倍, 记录下其初始荧光强度值, 备用。 精密称取适量的FeCl3, 用去离子水溶解并配制成浓度为0.1 mol·L-1的Fe3+母液。 将Fe3+母液分别用去离子水稀释至100、 500、 1 000、 1 500、 2 000、 2500、3 000、 3 500、 4 000、 4 500、 5 000、 6000、 7 000、8000、 9 000、 10 000 μmol·L-1。 在16 个试管内分别加入上述各浓度的Fe3+溶液1mL, 同时加入9 mL 稀释后的N-CQDs 溶液, 使得各试管中的溶液N-CQDs 浓度相同, 而Fe3+的终浓度分别为10、 50、 100、 150、 200、 250、 300、 350、 400、450、 500、 600、 700、 800、 900、 1 000 μmol·L-1。摇匀混合溶液, 静置1 h 后, 分别测其荧光强度F。 另取一试管, 加入1 mL去离子水和9 mL 稀释后的N-CQDs 溶液, 混匀后, 记录其荧光强度F0, 作为空白对照。
2 结果与讨论
2.1 N-CQDs 的荧光性能
从N-CQDs 的傅里叶红外光谱(图1)可见,3 448 cm-1处的吸收峰归因于伸缩振动。1 654和1 554 cm-1处的典型吸收带可分别认为是和的伸缩振动。 1 400 cm-1处对应的伸缩振动峰[16], 表明反应原料之间酰胺键的成功形成和N 的掺杂。 951 cm-1处的特征吸收峰是和的伸缩振动引起。以上结果表明, N-CQDs 表面含有大量的羟基、 羧基和氨基等基团, 从而保证了其良好的水溶性。
利用紫外-可见分光光度计在200 ~800 nm波长范围内对所合成的N-CQDs 的吸光度进行测定, 发现N-CQDs 在340nm 左右有最大吸收。 利用荧光分光光度计在激发和发射狭缝均为5 nm条件下测定了所合成的N-CQDs 在不同激发波长下的荧光发射光谱(图2), 结果发现: 当激发波长由300 nm 增加到350 nm 时, 荧光强度值逐渐升高; 但是当激发波长继续增加到370nm, 荧光强度值却逐渐降低。 由此可见, 所合成的NCQDs 的最佳激发波长为350 nm, 这和紫外可见分光光度计的测试分析结果相符合。 量子点的尺寸越小, 有效能级的禁带宽度越大, 则其激发所需要的能量就会越大, 发射出的光的波长越短;反之, 发射出的光的波长越长[17]。 由图2 可见,当激发波长由300 nm 增加到350 nm 时, 伴随着红移出现, 这可能是N-CQDs 的尺寸效应造成的; 当激发波长在350 ~370 nm 范围内时, 发射波长的红移范围较小, 这可从侧面印证了所制备的N-CQDs 尺寸大小较为均一。
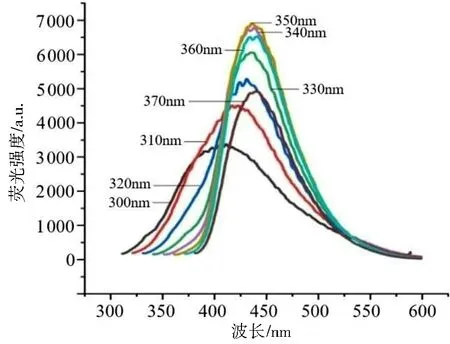
图2 N-CQDs 在不同激发波长下的荧光发射光谱
2.2 N-CQDs 的稳定性
不同保存条件下N-CQDs 溶液的荧光强度与初始荧光强度比值F/F0变化情况如图3 所示。结果表明: 常温下保存15 d 的N-CQDs 溶液的荧光强度变化不大(图3(a)); 在4℃低温保存45 d的N-CQDs 溶液的荧光强度保持稳定, 未发生明显变化(图3(b))。 可见所合成的N-CQDs 在常温和低温下保存都具有较好的稳定性。 在354nm的紫外灯光持续照射下, N-CQDs 溶液的荧光强度10 d 内并未发生明显变化(图3(c)), 由此可得出所合成的N-CQDs 具有良好的抗光漂白性。
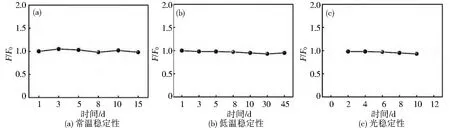
图3 N-CQDs 的稳定性
2.3 pH 值对N-CQDs 荧光强度的影响
用pH 值为4.0~10.0 的PBS 缓冲溶液对NCQDs 溶液进行稀释, 同时使用去离子水稀释NCQDs 溶液(pH 值为4.0 左右)作为对照, 使用荧光分光光度计检测荧光强度, 测得相关溶液的荧光强度值如图4 所示。 N-CQDs 在去离子水中和pH 值为4.0 的缓冲溶液中的荧光强度值最大, 随着pH 值的升高, 荧光强度值逐渐减小,当pH 值增大到10.0 后, 荧光强度值出现大幅度降低, pH 值为10.0 时N-CQDs 溶液荧光强度约为pH 值为4.0 时的81%。 由此推断, 溶液的酸性越强, N-CQDs 溶液荧光强度越强, 这可能是因为所合成的N-CQDs 中的碱性物质会干扰荧光强度。
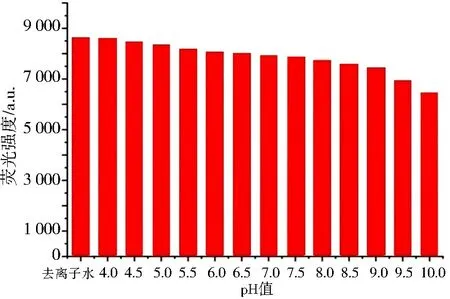
图4 pH 值对N-CQDs 溶液荧光强度的影响
2.4 N-CQDs 对Fe3+的检测
混合金属离子后的N-CQDs 溶液与未混合金属离子的N-CQDs 溶液(空白对照)的荧光强度比值F/F0如图5 所示, 在混合的金属离子中, NCQDs 对Fe3+具有良好的选择性, 由此可建立基于N-CQDs 荧光猝灭的检测Fe3+方法。 而Ni2+、Cr3+、 Mg2+、 Ca2+、 Fe2+等对N-CQDs 溶液荧光强度影响不大, Al3+的加入反而使N-CQDs 溶液的荧光强度增大。
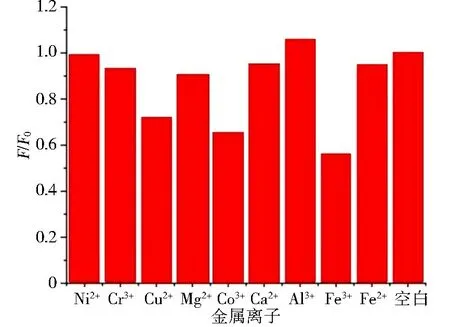
图5 金属离子对N-CQDs 荧光强度的影响
基于Fe3+对N-CQDs 溶液的荧光猝灭效应,通过优化条件, 建立更进一步的检测Fe3+的分析方法。 图6 为不同Fe3+浓度条件下N-CQDs 溶液的荧光猝灭结果, 可以看出, 随着Fe3+浓度不断增大, 对N-CQDs 溶液的荧光猝灭效应也越来越强。 以Fe3+浓度为横坐标、 以初始荧光强度值与混合Fe3+后的荧光强度的比值F0/F为纵坐标作图, 如图7 所示。 由图7 可见, Fe3+浓度在0 ~1 000μmol·L-1的范围内与N-CQDs 溶液的荧光猝灭程度呈良好的线性关系, 所得的标准曲线方程为:F0/F=0.1080c(Fe3+)+0.8553, 线性相关系数R2= 0.99931, 检出限为9.16μmol·L-1。
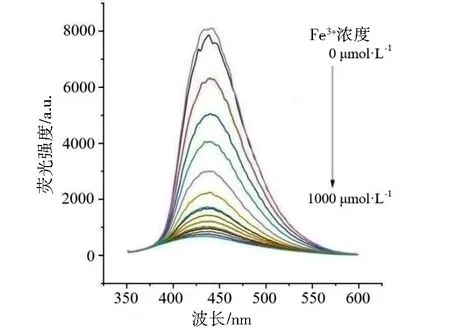
图6 不同浓度Fe3+对N-CQDs 荧光强度的影响
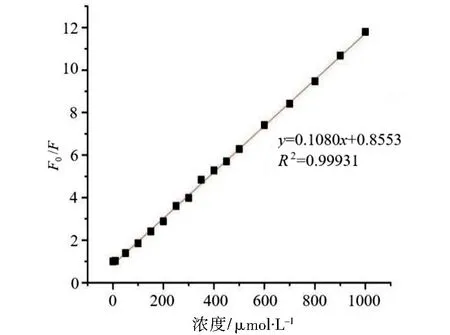
图7 N-CQDs 荧光淬灭程度与Fe3+浓度的关系
3 结论
本实验以一水合柠檬酸和四乙烯五胺作为原料, 采用熔融法合成了N-CQDs, 制备简单便捷,获得的N-CQDs 拥有丰富的官能团和良好的水溶性。 N-CQDs 水溶液在紫外光的照射下可发出强烈的蓝色荧光, 其紫外最大吸收波长为340 nm,荧光最佳激发波长为350nm, 具有优良的发光性能。 N-CQDs 溶液的最佳保存条件为低温、 酸性, 同时N-CQDs 具有良好的抗光漂白性。 与其他金属离子相比, Fe3+对N-CQDs 的荧光猝灭效应最强, 而且Fe3+在0 ~1 000 μmol·L-1的浓度范围内与N-CQDs 的荧光猝灭程度呈线性关系,R2=0.999 31, 检出限为9.16 μmol·L-1。 由此可见, 所合成的N-CQDs 可用于建立快速检测Fe3+浓度的方法, 可广泛应用于检测工业废水、生活用水、 食品与药品中的Fe3+。
