CdS-MoS2复合光催化剂的制备与可见光产氢性能研究
2023-11-09王丽萍张雯珺林海峰黎艳艳
王丽萍,张雯珺,林海峰,黎艳艳
(青岛科技大学 化学与分子工程学院,山东 青岛 266042)
近年来,现代工业对石油、煤和天然气等化石资源的严重依赖已造成了严重的能源短缺和环境污染问题。为了人类社会的可持续发展,新型可再生能源的开发势在必行[1]。氢能具有能量密度高、易于存储以及燃烧产物无污染等特点,是替换化石燃料的最理想能源之一[2]。在生产氢气的各种方法中,半导体光催化技术能够利用可再生的太阳能将水分解为氢气,因此受到了人们的广泛关注[3]。众所周知,太阳光谱中可见光占据了约43%的比例,而紫外光的占比仅为4%左右[4],因此可见光响应型光催化剂的研制具有重要意义。过渡金属硫化物半导体(CdS,MoS2,ZnIn2S4等)由于具有较强的可见光吸收能力和合适的质子还原导带电势,目前已成为光解水产氢反应研究的热门材料[5]。然而,过渡金属硫化物半导体较高的光生电荷复合速率和光腐蚀等问题严重削弱了光催化活性[6]。针对过渡金属硫化物半导体的这些缺陷,科学家通过金属/非金属元素掺杂、异质结构筑和助催化剂修饰等策略来促进载流子分离和增强光稳定性,并取得了许多重要的研究进展[7]。其中,助催化剂修饰提高过渡金属硫化物光催化性能的原因主要来源于以下三个方面:首先,助催化剂为光吸收体提供了大量的催化活性位点,因此有效降低了反应的能垒促进反应的动力学;其次,助催化剂与光吸收体之间形成的内建电场能够引导光生电子和空穴往界面的相反方向移动,从而显著抑制了载流子的复合过程;此外,助催化剂可以通过提取光生空穴来克服因空穴氧化所造成的光稳定性问题[8]。因此,合理设计具有助催化剂修饰的过渡金属硫化物半导体光催化剂有望实现高效的光解水产氢反应。
1 仪器与材料
1.1 材料
乙醇(C2H5OH)、乙酸镉(Cd(CH3COO)·2H2O)、硫代乙酰胺(TAA)、四硫代钼酸铵((NH4)2MoS4)、N,N-二甲基甲酰胺(DMF)、N-甲基吡咯烷酮(NMP)、聚四氟乙烯(PTFE)、乳酸(C3H6O3)、抗坏血酸(C6H8O6)、三乙醇胺(TEOA)、硫化钠(Na2S·9H2O)、亚硫酸钠(Na2SO3)等分析纯化学药品购买自中国上海国药化学试剂有限公司,实验中所用水为去离子水。
1.2 分析测试仪器
光催化反应仪器,Labsolar-6A型,北京泊菲莱科技有限公司;氙灯光源,Microsolar-300A型,北京泊菲莱科技有限公司;气相色谱仪,GC7900型,上海天美科学仪器有限公司;光电反应装置,PEC2000型,北京泊菲莱科技有限公司;电化学工作站,CHI 660D型,上海辰华仪器有限公司;透射电子显微镜,Tecnai G2 F20型,美国 FEI 公司;紫外-可见漫反射光谱仪,Shimadzu UV 3600型,日本岛津公司;X-射线光电子能谱仪,ESCALAB 250 Xi型,美国赛默飞世尔科技公司;X-射线粉末衍射仪,D/max 2500 PC型,日本理学株式会社。
1.3 CdS纳米颗粒的制备
本实验通过油浴反应的方法制备CdS纳米颗粒。用量筒量取50 mL乙醇倒入150 mL圆底烧瓶中,然后使用电子分析天平称取0.184 5 g乙酸镉粉末加入烧瓶中,二者充分混合,超声10 min至药品完全溶解。然后将盛放药品的圆底烧瓶置于油浴中80 ℃加热10 min之后,加入0.052 1 g硫代乙酰胺搅拌溶解并继续加热1 h。待产物冷却至室温后,分别用乙醇和水对产物进行离心洗涤(两次水、一次乙醇),随后于60 ℃真空干燥箱中干燥过夜得到CdS纳米颗粒。
1.4 CdS-MoS2的制备
本实验通过N,N-二甲基甲酰胺溶剂热法制备了不同MoS2负载量的CdS-MoS2-x%复合光催化剂,其中x%表示复合物中MoS2的质量分数。以CdS-MoS2-3%为例:取两个小离心管分别盛放2.514 5 mg四硫代钼酸铵和50 mg CdS,在两个离心管中分别加入5 mLN,N-二甲基甲酰胺进行超声溶解和分散。随后将两个离心管中的混合物转移至同一个50 mL反应釜中,再加入10 mLN,N-二甲基甲酰胺,搅拌至混合均匀。最后,将反应釜放入烘箱中,在200 ℃下静置12 h。反应结束且冷却至室温后,将反应的产物分别用乙醇和水离心洗涤(两次水、一次乙醇),然后置于60 ℃真空干燥箱中干燥过夜得到CdS-MoS2复合物。
1.5 MoS2纳米片的制备
本实验通过N,N-二甲基甲酰胺溶剂热法制备了MoS2纳米片。将0.157 7 g四硫代钼酸铵加入20 mLN,N-二甲基甲酰胺中进行超声溶解,搅拌分散至混合均匀。随后,将反应釜放入烘箱中,在200 ℃下静置12 h。反应结束且冷却至室温后,将反应的产物分别用乙醇和水离心洗涤(两次水、一次乙醇),然后置于60 ℃真空干燥箱中干燥过夜得到MoS2纳米片。
1.6 光催化产氢活性测试
样品的光催化产氢活性采用与GC7900型气相色谱仪相连的Labsolar-6A型在线光催化设备进行测试。使用配备400 nm截止滤光片的300 W氙灯提供所需要的可见光辐照。使用循环水泵将反应温度控制为10 ℃。每次实验前,将10 mg样品超声分散于100 mL含体积分数10%乳酸的水溶液中,得到均匀的悬浮液用于催化反应。然后,将反应悬浮液转移到反应器中并用真空泵抽走溶解的空气。在辐照条件下,每隔30 min由气相色谱仪的热导率检测器(TCD)监测释放的氢气。此外,还采用0.375 mol/L抗坏血酸、体积分数10% TEOA和0.35 mol/L Na2S/0.25 mol/L Na2SO3溶液进行测试,以研究不同牺牲剂对样品光催化活性的影响。
1.7 光电化学测试
光电化学性质采用三电极结构的CHI 660E电化学工作站进行测试。Ag/AgCl和Pt片分别为参比电极和对电极。工作电极的制备步骤如下:首先将样品粉末与NMP和PTFE混合并通过研磨得到均匀的浆液。随后,将浆液均匀地涂覆在掺氟的氧化锡(FTO)玻璃(1 × 2 cm2)的导电面上,接着经过自然干燥之后于流动N2气氛下450 ℃焙烧1 h得到工作电极。采用0.5 V偏压,在体积分数10%乳酸水溶液中测试样品的光电流响应曲线。
2 实验结果与讨论
2.1 材料表征
图1为实验制备的CdS,MoS2和CdS-MoS2-5%的X-射线衍射(XRD)图谱。从图1中可以看出, CdS产物的XRD衍射峰与纤锌矿CdS(JCPDS No.01-0780)的相一致。与体相六方结构的MoS2(JCPDS No.77-1716)相比,合成MoS2的(002)和(004)衍射峰向低角度方向移动,这可归因于MoS2层间距变大造成的结果。层间距增大的MoS2纳米片有助于暴露出更多活性的边缘S原子,从而提高光催化产氢的活性。此外,CdS-MoS2-5%复合物显示出了对应于纤锌矿CdS(JCPDS No.01-0780)的衍射信号,然而与MoS2相关的衍射峰没有被观察到,这可能与MoS2较低的负载量有关。
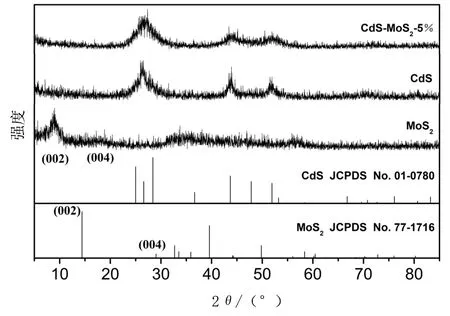
图1 CdS,MoS2和CdS-MoS2-5%的XRD图谱
利用紫外-可见漫反射(UV-vis DRS)光谱测试研究了所合成CdS,MoS2和CdS-MoS2-5%对光的响应能力。如图2a所示,CdS的光学吸收边位于546.3 nm,而MoS2则显示出了从紫外到可见光区的强光吸收能力。因此,与纯CdS相比,负载有MoS2的CdS-MoS2-5%复合物的光学吸收边明显往长波长方向移动,这表明其光俘获能力得到了增强。此外,进一步确定了CdS和MoS2的禁带宽度,根据的是Kubelka-Munk方程:(Ahν)n=K(hν-Eg) (A:吸光度,hν:光子能量,K:常数,Eg:禁带宽度,n:0.5和2分别对应于间接跃迁半导体和直接跃迁半导体)[9]。从图2b所示的Tauc图可以看出,CdS的Eg值为2.40 eV,而MoS2的Eg值则显著减小到了1.34 eV。
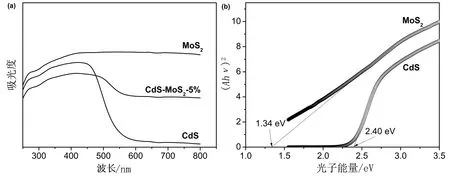
图2 (a) CdS,MoS2和CdS-MoS2-5%的紫外-可见吸收光谱;(b) CdS和MoS2的禁带宽度
通过透射电子显微镜(TEM)和高分辨TEM(HRTEM)对CdS-MoS2-5%复合物的微观结构进行了分析。图3a的TEM图像表明,CdS-MoS2-5%复合物含有很多尺寸均一的纳米颗粒。而且,从图3b的HRTEM图可以看出,MoS2纳米片通过紧密地包覆于CdS纳米颗粒表面形成了CdS-MoS2复合材料。根据条纹间距的分析结果,0.31和0.35 nm间距的晶格条纹分别与纤锌矿CdS(JCPDS No.65-3414)的(101)和(100)晶面相符,而间距为0.78 nm的晶格条纹则可归属于六方结构MoS2膨胀的(002)晶面。因此,上述TEM和HRTEM测试结果表明了CdS-MoS2-5%复合物中同时存在CdS和MoS2两种组分,而且这两种组分通过结合形成了紧密的耦合界面。

图3 CdS-MoS2-5%的(a) TEM和(b) HRTEM图像
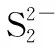
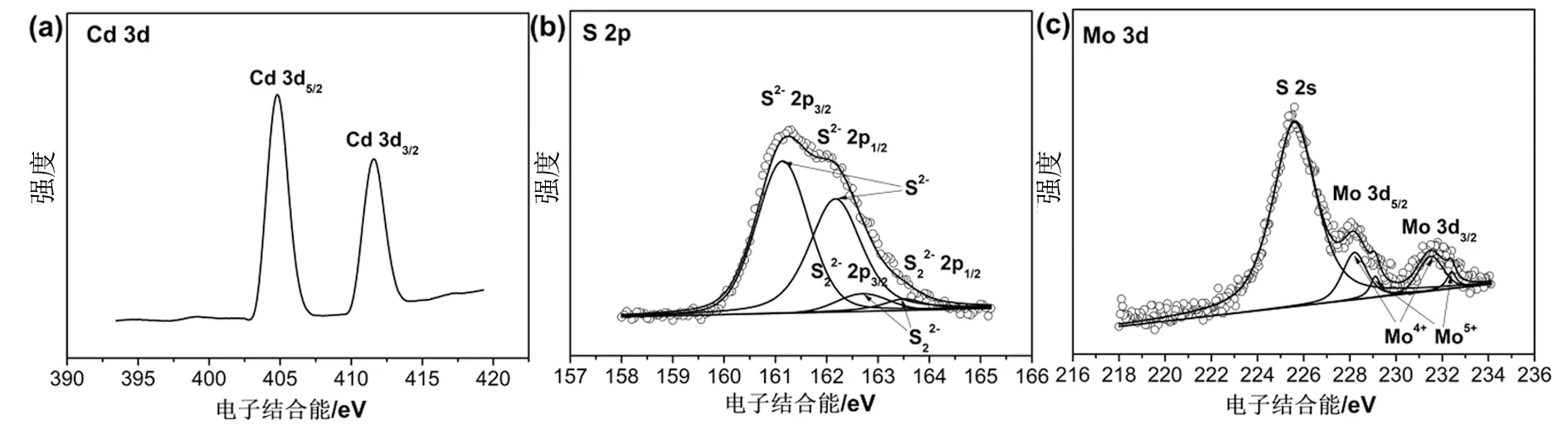
图4 CdS-MoS2-5%复合物的(a) Cd 3d,(b) S 2p和(c) Mo 3d XPS能谱
2.2 材料性能研究
在可见光(λ>400 nm)辐照下,测试了不同样品在乳酸牺牲剂条件下的光解水产氢性能。图5a,b分别为不同样品的产氢活性和相应的产氢速率,其中MoS2没有产氢活性,而CdS则由于较高的电荷复合速率表现出了低的产氢活性(1.98 mmol·g-1·h-1)。与CdS相比,不同MoS2负载量的CdS-MoS2复合物展示出了显著提高的产氢活性。随着MoS2负载量的增加,CdS-MoS2复合物的产氢活性逐渐提高并在质量分数5% MoS2负载量时(CdS-MoS2-5%)获得了最佳的产氢活性29.62 mmol·g-1·h-1,为纯CdS的14.9倍之多。然而,当MoS2的负载量超过5%时,CdS/ZnS复合物的活性则开始下降,这可能是由于过多的MoS2负载遮蔽了CdS对光的吸收,从而减少了可用于将质子还原为氢气反应的光生电子数量。CdS-MoS2-5%的光解水产氢活性显著高于Pt负载的CdS以及大部分文献中的CdS复合光催化剂[14-18]。
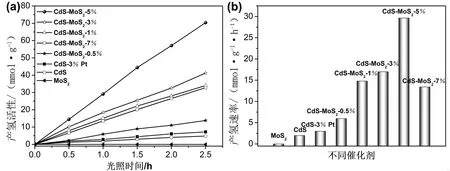
图5 不同样品的光催化产氢(a)活性和(b)平均速率
另一方面,测试了CdS-MoS2-5%在不同空穴清除剂溶液中的产氢活性。从图6的平均产氢速率图可以看出,CdS-MoS2-5%在乳酸溶液中的产氢活性最高,其次是三乙醇胺(TEOA)、Na2S/Na2SO3和抗坏血酸溶液。上面的结果表明,对于CdS-MoS2光催化体系,乳酸为最佳的产氢反应牺牲剂。
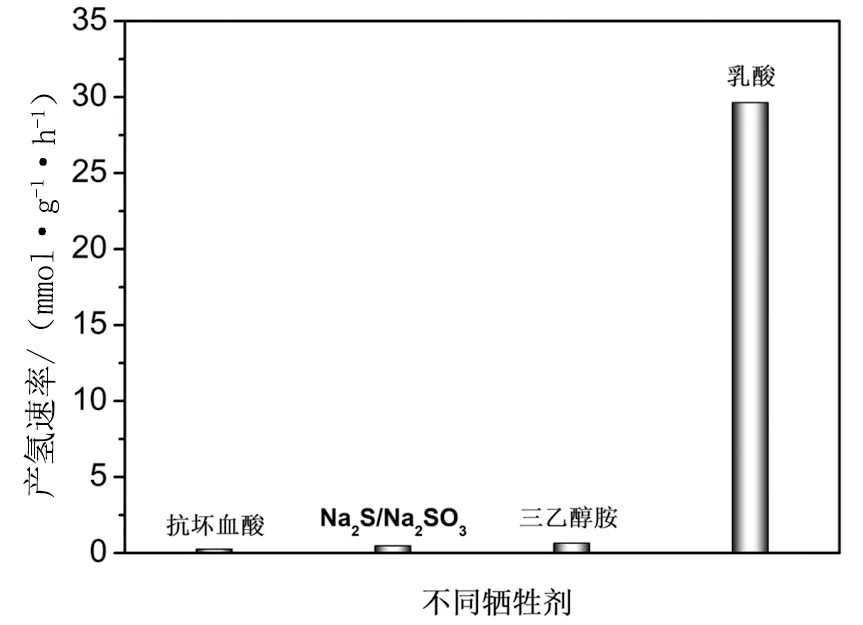
图6 CdS-MoS2-5%在不同空穴清除剂溶液中的平均产氢速率
众所周知,光催化反应中,光催化剂的载流子分离能力是影响其光催化活性的最主要因素之一。为了探究CdS-MoS2-5%复合物优良光催化活性的来源,通过光电流响应测试对其光生电荷分离能力进行了研究,并使用CdS和MoS2作为对比样品。如图7所示,CdS,MoS2和CdS-MoS2-5%三种催化剂在可见光辐照下均表现出了快速的光电流响应[19]。与CdS和MoS2相比,CdS-MoS2-5%表现出了更高的光电流密度,这表明后者具有更强的抑制光生电荷复合过程的能力[20]。CdS-MoS2-5%出色的光生电荷分离能力能够促进载流子的充分利用,因此有效提高了光解水产氢的活性。
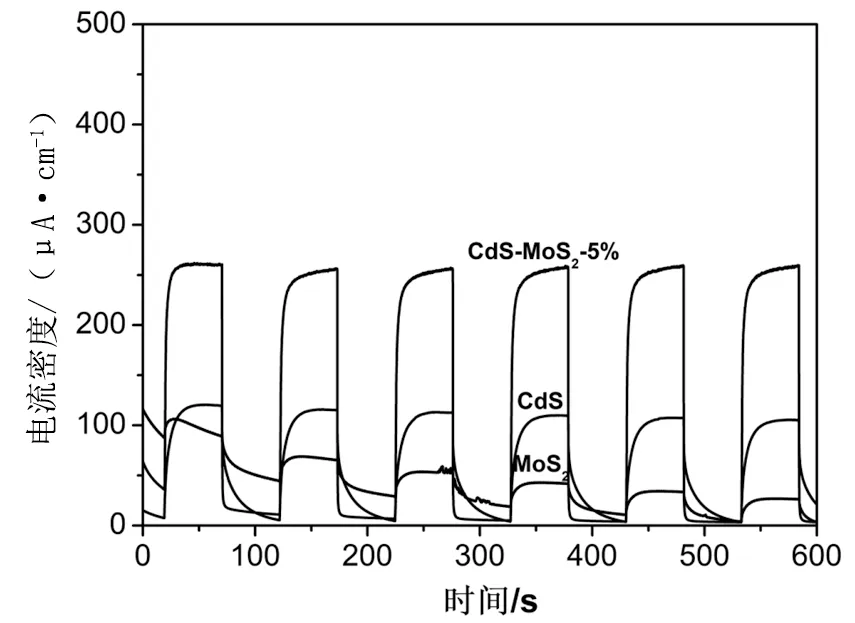
图7 CdS,MoS2和CdS-MoS2-5%的瞬态光电流响应
3 结论