含氟均三嗪类化合物的合成及生物活性
2023-11-09姜硕张如松朱宝玉光明甲孙鉴昕许良忠王明慧
姜硕,张如松,朱宝玉,光明甲,孙鉴昕,许良忠,王明慧
(青岛科技大学 化学与分子工程学院,山东 青岛 266042)
均三嗪类化合物是一种几丁质合成抑制剂,其对双翅目幼虫有着特殊活性,可使双翅目幼虫发生畸变,作用效果相当于激素调节剂[1]。目前三嗪类化合物已经商品化的有灭蝇胺[2]、莠去津[3]等。根据王梅祥等[4]报道,化合物1和2对在质量浓度为20 mg/L时,对红蜘蛛的杀虫活性高达100%。
图1均三嗪类化合物是以三聚氯氰为原料,与不同的小分子胺进行反应生成最终化合物,根据巨修练[5]报道了以三聚氯氰和对三氟甲基苯胺为原料合成的均三嗪化合物3和4对黏虫的LD50分别为0.53 μg/cm-2和0.47 μg/cm-2。6号位上与胺反应生成的化合物杀虫活性明显高于与醇反应生成的化合物。且根据灭蝇胺与莠去津等已报道的高活性化合物结构可分析,大多数高活性的化合物皆为对称结构(图2),可以推断对称结构有助于提高杀虫活性。氰氟虫腙[6]是一种已报道的高效杀虫剂,其活性中间体4-三氟甲氧基苯胺具有良好的杀虫活性,氟原子的可大大提高化合物的亲脂性,甲氧基可增加内吸性,将4-三氟甲氧基苯胺引入均三嗪中,有助于提高均三嗪化合物的杀虫活性。

图1 均三嗪类化合物

图2 含氟三嗪类杀虫剂结构式
所以,以灭蝇胺为先导化合物,通过中间体衍生化法,对三聚氯氰的2位、4位和6位进行改造,将4-三氟甲氧基苯胺基团接入均三嗪结构中,再引入苄胺或小分子的胺和醇,合成一系列含氟三嗪类化合物,从而获得高效绿色而且经济的新型均三嗪类杀虫剂(图3)。
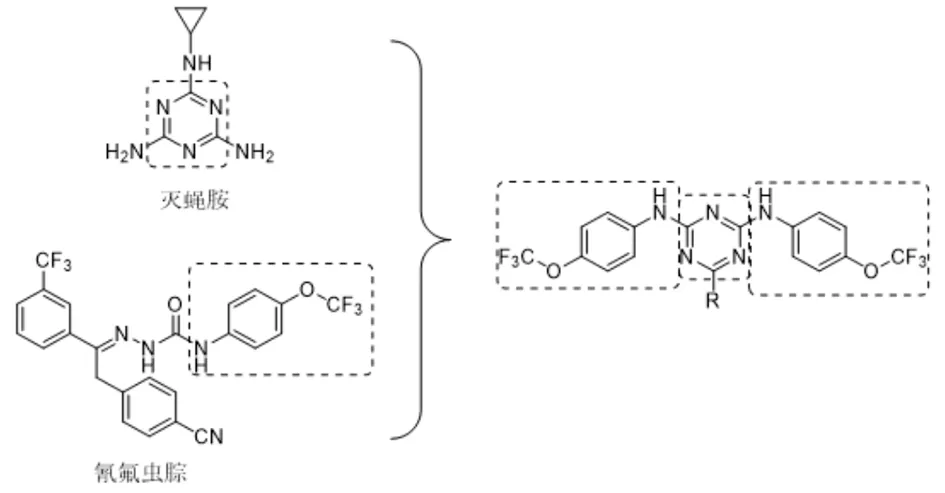
图3 目标化合物的设计路线
1 实验部分
1.1 实验仪器与试剂
所有实验药品均来自于上海毕得医药科技股份有限公司,所用溶剂均来自于烟台双双化工,且均为分析纯,所用仪器见表1。

表1 实验仪器
1.2 合成路线及方法
设计路线见图4,图5为活性拼接基团。
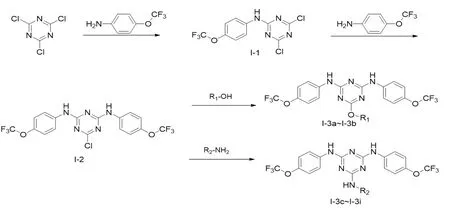
图4 含氟均三嗪类化合物的合成路线图
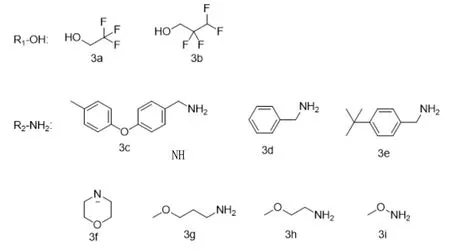
图5 活性拼接基团
根据合成过程来看,该系列含氟均三嗪类化合物本质上来说是进行了三次亲核取代,以三聚氯氰为起始原料首先与一分子对三氟甲氧基苯胺在2号位上发生取代反应,进而再与一分子对三氟甲氧基苯胺在4号位上发生取代反应,最后一步再与烷基胺或者烷基醇在6号位上发生取代反应。
1.2.1 中间体6-氯-N2,N4-双(4-三氟甲氧基苯基)-1,3,5-三嗪-2,4-二胺(Ⅰ-2)的合成
取1.84 g(0.01 mol)三聚氯氰置于250 mL三口瓶中,加入1,4-二氧六环20 mL,再加入3.036 g(0.022 mol)无水K2CO3,冰水浴下搅拌15 min,用滴液漏斗缓慢滴加1.77 g(0.01 mol)对三氟甲氧基苯胺,滴罢,继续搅拌30 min,溶液由澄清变为乳白色浑浊液,TLC监测反应完毕后,此时生成中间体Ⅰ-1。不进行处理直接进行下一步,将反应液移至室温,继续滴加1.77 g(0.01 mol)对三氟甲氧基苯胺。继续室温下反应15 h,溶液由乳白色变为黄色,TLC监测反应完毕,得到该中间体Ⅰ-2溶液,不作处理直接进行下一步反应。
1.2.2 目标化合物目标化合物Ⅰ-3a~Ⅰ-3b的合成
向上述Ⅰ-2中间体0.01 mol反应溶液中室温加入1.5 g(0.012 mol)无水K2CO3,继续加入0.012 mol烷基醇,100 ℃下反应15 h,TLC监测反应完毕,加入30 mL水与20 mL乙酸乙酯萃取,分液,有机相用无水硫酸钠进行干燥,旋蒸出溶剂,柱层析得到最终产物Ⅰ-3a与Ⅰ-3b。
1.2.3 目标化合物目标化合物Ⅰ-3c~Ⅰ-3i的合成
向上述Ⅱ中间体0.01 mol反应溶液中室温加入1.5 g(0.012 mol)无水K2CO3,继续加入0.012 moL烷基胺,40 ℃下反应3 h,TLC监测反应完毕,加入水与乙酸乙酯萃取,无水硫酸钠进行干燥,旋蒸出溶剂,柱层析得到最终产物Ⅰ-3c~Ⅰ-3i。
1.2.4 化合物Ⅰ-3a~Ⅰ-3i的结构表征数据如下:
Ⅰ-3a:6-(2,2,2-三氟乙氧基)-N2,N4-双(4-三氟甲氧基苯基)-1,3,5-三嗪-2,4-二胺,白色固体,收率93.6%;m.p.141.2~143.8 ℃;1H NMR (400 MHz,DMSO-d6) δ 10.09 (s,2H),7.81 (d,J=18.3 Hz,4H),7.33 (d,J=8.6 Hz,4H),5.04 (q,J=9.1 Hz,2H).13C NMR (101 MHz,DMSO-d6) δ 169.63,143.98,138.63,128.27,125.50,124.46,122.75,121.92,121.79,119.99,119.38,116.84,62.30。HRMS(ESI):理论值:C19H13F9N5O3[M+H]+:530.087 5,实测值:530.086 9。
Ⅰ-3b:6-(2,2,3,3-四氟丙氧基)-N2,N4-双(4-三氟甲氧基苯基)-1,3,5-三嗪-2,4-二胺,白色固体,收率92.1%;m.p.145.9~146.5 ℃;1H NMR (400 MHz,DMSO-d6) δ 10.07 (s,2H),7.82 (s,4H),7.33 (d,J=8.6 Hz,4H),6.68 (m,J=51.9,5.1 Hz,1H),4.93 (t,J=14.2 Hz,2H).13C NMR (101 MHz,DMSO-d6) δ 169.85,165.58,143.97,138.67,124.46,122.43,121.92,121.81,119.38,117.71,116.84,115.49,115.23,114.96,112.31,110.18,109.84,109.51,107.72,107.38,107.05,62.39,62.13,61.87。HRMS(ESI):理论值:C20H13F10N5O3[M+H]+:562.093 7,实测值:562.086 1。
Ⅰ-3c:N2-(4-对甲苯基)苄基-N4,N6-双(4-三氟甲氧基)苯基-1,3,5-三嗪-2,4,6-三胺,白色固体,收率95.2%;m.p.245.9~247.2 ℃;1H NMR (500 MHz,Chloroform-d) δ 8.42 (s,2H),7.62 (t,J=9.4 Hz,4H),7.36 (d,J=8.2 Hz,2H),7.28 (d,J=8.4 Hz,2H),7.22 (s,4H),7.09 (dd,J=13.2,8.0 Hz,4H),6.71 (d,J=8.5 Hz,1H),4.70 (s,2H),2.48 (s,3H).13C NMR (125 MHz,Chloroform-d) δ 166.47,159.95,155.53,155.44,155.42,155.36,149.95,144.28,136.34,132.64,132.58,130.02,130.01,130.00,129.99,129.98,129.97,122.34,122.32,122.30,122.29,122.26,121.77,121.76,121.75,121.74,121.74,121.71,121.69,121.66,121.63,121.61,120.63,120.62,120.60,120.60,119.56,116.15,116.12,116.10,116.07,20.57,20.54,20.50。HRMS(ESI):理论值:C31H25F6N6O3[M+H]+:643.189 2,实测值:643.180 9。
Ⅰ-3d:N2-苄基-N4,N6-双(4-三氟甲氧基)苯基-1,3,5-三嗪-2,4,6-三胺,白色固体,收率90.2%;m.p.202.6~209.3 ℃;1H NMR (400 MHz,DMSO-d6) δ 9.37 (d,J=14.7 Hz,2H),7.94 (d,J=8.6 Hz,2H),7.82 (d,J=8.7 Hz,2H),7.40~7.32 (m,4H),7.31~7.22 (m,4H),7.22 - 7.19 (m,1H),4.58 (d,J=6.3 Hz,2H).13C NMR (101 MHz,DMSO-d6) δ 166.33,164.57,164.49,143.03,140.69,140.04,139.88,128.65,127.39,127.02,121.99,121.60,121.53,119.45,44.00。HRMS(ESI):理论值:C24H19F6N6O2[M+H]+:537.147 4,实测值:537.145 3。
Ⅰ-3e:N2-(4-叔丁基)苄基-N4,N6-双(4-三氟甲氧基)苯基-1,3,5-三嗪-2,4,6-三胺,白色固体,收率90.6%;m.p.235.4~238.2 ℃;1H NMR (500 MHz,DMSO-d6) δ 9.35 (s,1H),9.31 (s,1H),7.93 (d,J=8.8 Hz,2H),7.76 (d,J=28.0 Hz,2H),7.35 (d,J=8.1 Hz,2H),7.29 (d,J=7.9 Hz,2H),7.26 (d,J=8.6 Hz,2H),7.20 (d,J=8.6 Hz,2H),4.53 (d,J=6.1 Hz,2H),1.26 (s,9H).13C NMR (101 MHz,DMSO-d6) δ 166.27,164.54,164.45,149.41,142.98,140.06,139.88,137.59,127.18,125.36,121.98,121.59,121.52,119.44,43.73,34.52,31.54.HRMS(ESI):理论值:C28H27F6N6O2[M+H]+:593.210 0,实测值:593.301 6。
Ⅰ-3f:6-吗啉基-N2,N4-双(4-三氟甲氧基)苯基-1,3,5-三嗪-2,4-二胺,白色固体,收率94.6%;m.p.214.3~215.3 ℃;1H NMR (500 MHz,DMSO-d6) δ 9.44 (s,2H),7.83 (d,J=8.5 Hz,4H),7.29 (d,J=8.6 Hz,4H),3.76 (t,J=4.8 Hz,4H),3.68 (t,J=4.8 Hz,4H).13C NMR (101 MHz,DMSO-d6) δ 165.14,164.44,143.12,139.77,121.95,121.75,119.42,66.45,43.95.HRMS(ESI):理论值:C21H19F6N6O3[M+H]+:517.142 3,实测值:217.150 1。
Ⅰ-3g:N2-(3-甲氧基丙基)-N4,N6-双(4-三氟甲氧基)苯基-1,3,5-三嗪-2,4,6-三胺,白色固体,收率92.9%;m.p.172.4~173.2 ℃;1H NMR (500 MHz,Chloroform-d) δ 8.47~8.43 (m,1H),7.61 (d,J=8.5 Hz,2H),7.51 (d,J=8.5 Hz,2H),7.16 (d,J=9.0 Hz,2H),7.10 (s,2H),6.36 (s,1H),3.59 (q,J=6.4 Hz,2H),3.52 (t,J=5.8 Hz,2H),3.34 (s,3H),1.91 (m,J=6.2 Hz,2H).13C NMR (126 MHz,DMSO-d6) δ 166.14,164.57,164.34,142.98,140.04,121.72,121.53,119.69,70.32,58.34,38.12,29.80.HRMS(ESI):理论值:C21H21F6N6O3[M+H]+:519.157 9,实测值:519.306 5。
Ⅰ-3h:N2-(3-甲氧基乙基)-N4,N6-双(4-三氟甲氧基)苯基-1,3,5-三嗪-2,4,6-三胺,白色固体,收率91.6%;m.p.154.5~156.0 ℃;1H NMR (400 MHz,DMSO-d6) δ 9.40 (s,1H),9.30 (s,1H),7.91 (d,J=8.6 Hz,4H),7.27 (d,J=8.5 Hz,4H),7.21 (s,1H),3.52 (t,J=2.3 Hz,2H),3.51 (q,2H),3.30 (s,3H).13C NMR (101 MHz,DMSO-d6) δ 166.18,164.54,164.36,143.01,140.01,121.97,121.59,119.44,71.07,58.35,39.45.HRMS(ESI):理论值:C20H19F6N6O3[M+H]+:505.1423,实测值:505.302 1。
Ⅰ-3i:N2-(3-甲氧基)-N4,N6-双(4-三氟甲氧基)苯基-1,3,5-三嗪-2,4,6-三胺,白色固体,收率75.0%;m.p.132.3~134.0 ℃;1H NMR (500 MHz,DMSO-d6)δ10.28 (s,1H),9.63 (s,2H),7.94~7.79 (m,4H),7.28 (d,J=8.6 Hz,4H),3.72 (s,3H).13C NMR (101 MHz,DMSO-d6) δ 168.31,164.53,143.28,139.65,121.95,121.68,119.41,63.65.HRMS(ESI):理论值:C18H15F6N6O3[M+H]+:477.111 0,实测值:477.201 2。
1.3 生物活性测试
1.3.1 杀棉蚜活性测试
本试验参照NY/T 1154.6—2006《农药室内生物测定试验准则杀虫剂》第6部分:浸虫法,具体方法如下:取长势一致的两叶一心棉苗,每株棉苗上接100头棉蚜幼虫,置于养虫室培养24 h后,将棉苗倒置入系列浓度药剂中浸10 s,水分挥发后立即检查原始虫数,并放入养虫室培养。每个浓度3次重复,以0.1 %吐温-80水溶液处理为对照。置于(26±1)℃、相对湿度70%~80%、光照16 h∶8 h(L∶D)条件下正常饲养。药前记录总虫数,药后24,48,72 h 记录残留蚜虫数,计算死亡率和校正死亡率。
1.3.2 杀红蜘蛛活性测试
本试验参照 NY/T 1154.14—2008《农药室内生物测定试验准则杀虫剂》第14部分:浸叶法进行,具体方法如下:按照试验设计将药剂配制成为系列浓度的稀释液,以0.1%吐温-80水为对照;选取新鲜的茭白,切成厚度 0.5 cm 的薄片,在对应药剂中浸渍10 s后取出,自然晾干。将滤纸剪成合适大小平铺于直径6 cm带盖塑料杯底部,放入大小一致的红蜘蛛幼虫,饥饿处理2 h后放入带毒茭白;置于(26±1)℃、光照 16 h∶8 h(L∶D)条件下,处理24,48,72 h 后,以毛笔碰触刺激不能活动者为死亡,记录死虫数,计算各处理死亡率和校正死亡率。
2 实验结果与讨论
2.1 杀棉蚜活性测试结果
通过表2杀棉蚜活性数据,所合成的新型三嗪类化合物大多数表现为高活性,在试验质量浓度为5 mg/L时Ⅰ-3c杀棉蚜率能够达到95%,Ⅰ-3d也能达到85%,而Ⅰ-3a与Ⅰ-3b在50 mg/L时活性在25%以下,从构效关系来看,6号位取代基为胺时比取代基为醇时活性要好,且取代基为苄胺时活性最好。
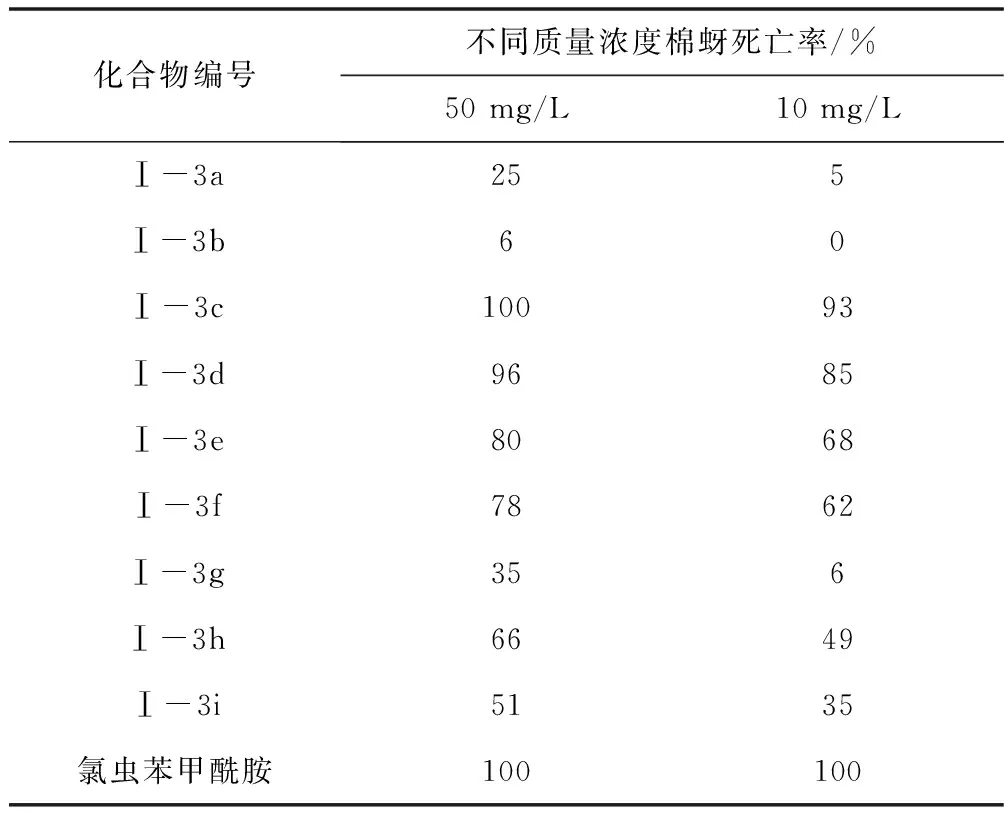
表2 目标化合物Ⅰ-3a~Ⅰ-3i的杀棉蚜活性测试数据

表3 目标化合物Ⅰ-3a~Ⅰ-3i的杀红蜘蛛活性测试数据
2.2 杀红蜘蛛活性测试结果
通过杀红蜘蛛活性数据,在试验质量浓度为50 mg/L时Ⅰ-3c、Ⅰ-3d、Ⅰ-3e红蜘蛛死亡率能够达到100%,质量浓度降低为10 mg/L时,Ⅰ-3c、Ⅰ-3d也能达到95%以上,而Ⅰ-3b与Ⅰ-3h在50 mg/L时活性也仅有15%左右,与杀棉蚜活性基本一致,6号位取代基为胺时比取代基为醇时活性要好,且取代基为苄胺时活性最好。所以推测吸电子强的基团能提高化合物的活性,苄胺的吸电子能力强于醇的吸电子能力,甲氧胺的活性最低,因为甲氧胺本身存在p-p共轭结构,降低了氮原子的电子云,导致杀虫活性减弱,对于苄胺来说,对位取代基团为吸电子基团时活性强,Ⅰ-3c的6号位取代基为4-对甲苯氧基苄胺,该苄胺的对位为对甲苯氧基,起到吸电子能力,而Ⅰ-3e的6号取代位为叔丁基,是供电子基团,而且对叔丁基本身的空间位阻较大,对苄胺的胺基上的电子云密度同样起到降低作用,所以活性方面Ⅰ-3c>Ⅰ-3d>Ⅰ-3e。
2.3 合成条件影响
由于三聚氯氰的特殊结构,其本身的三个氯原子均能与吸电子基团发生取代反应,但是每取代一个氯原子之后,下一个氯原子的会变得艰难,所以取代第一个氯原子时最佳环境为冰水浴条件下反应,在低温下活泼的三聚氯氰选择取代一个氯的能力强,且由于三聚氯氰非常活泼,所以不存在反应缓慢的情况若在第一步就在室温反应,则溶液迅速变为黄色,而不是冰水浴下的乳白色这是由于产生二取代化合物导致。第一个氯原子取代后生成中间体Ⅰ-1,Ⅰ-1本身取代能力降低,发生取代反应时可以将反应移至室温,室温下继续反应,二取代的选择性较高,基本没有杂质的产生低温会影响反应速度,高温会产生大量杂质,生成三取代化合物,导致产率大大下降。二取代结束后生成的中间体Ⅰ-2活性继续降低,这时进行三取代时必须升温,升温情况根据另一种反应物的取代基而定。总体而言,由于该化合物的反应为三步取代反应,可以“一锅法”进行,不需要每一步都拿到固体,符合简单、绿色、经济化学。
3 结论
本章合成了Ⅰ-3a~Ⅰ-3i共8个未报道的新型含氟均三嗪类化合物和1个已知的含氟均三嗪类化合物,从合成方法看,以灭蝇胺为先导化合物,通过衍生化法将杀虫活性强且经济的对三氟甲氧基苯胺代替胺基,再与苄胺等反应合成一系列含氟三嗪类化合物,并对所合成的目标化合物进行1H NMR、13C NMR、HRMS分析,确定了所有目标化合物的结构。
此外,通过多次实验,对合成该系列目标化合物的合成条件,如温度、加料方式、比例等都做了的优化,对比发现,“一锅法”所得到产物的收率远高于分步反应得到产物的收率,并且“一锅法”反应简单、所需溶剂少,更加绿色。该“一锅法”注意的是,在合成中间体Ⅰ-1时,温度不能高于10 ℃,否则反应体系变黄。在合成中间体Ⅱ-2时,温度不能高于40 ℃,否则生成过多杂质导致收率降低。
在生物活性测试方面,该系列化合物的杀虫活性明显强于喹唑啉类杀虫剂,大多数化合物在50 mg/L下都具有良好的杀虫效果,部分化合物,如Ⅰ-3c、Ⅰ-3d、Ⅰ-3e在5 mg/L下对红蜘蛛的杀虫活性能够达到85%以上。同时在5 mg/L下,Ⅰ-3c和Ⅰ-3d对棉蚜的杀虫活性也能够达到85%以上,已经达到高活性的标准。根据构效结果,不难看出活性最好的三个化合物Ⅰ-3c、Ⅰ-3d、Ⅰ-3e,6号取代位上均为苄胺,推测含有苄胺结构片段可能是之事杀虫活性较高的结构单元,但是由于作用机制尚不明确,具体活性判断还需进一步探索。
