14例儿童色素减退型蕈样肉芽肿诊疗分析
2023-10-24蒋芮理陈柳青
夏 云 胡 枫 姜 倩 蒋芮理 陈柳青
武汉市第一医院皮肤科,湖北武汉,430022
蕈样肉芽肿(mycosis fungoides,MF)是结外非霍奇金淋巴瘤中最常见的一种亚型,起源于皮肤,低度恶性,约占原发性皮肤T细胞淋巴瘤的60%[1]。目前病因和发病机制仍然不清,早期表现缺乏特异性,不易早期诊断。色素减退型蕈样肉芽肿(hypopigmented MF,HMF)是儿童MF中较常见的一种类型。1973年被Ryan等首次报道,与经典型MF好发于中老年男性不同,HMF好发于儿童及青少年,约占此年龄段MF病例的53%~79%,尤其亚洲人群及深色人种易受累,但没有明显的性别差异[2]。由于本病呈慢性进展,常被误诊及漏诊。光疗在HMF应用较为成熟,补骨脂素联用长波紫外线(PUVA)或窄谱中波紫外线(NB-UVB)推荐为一线疗法,与PUVA相比,NB-UVB避免了因服用补骨脂素导致的胃肠道反应、光敏感、肝功能损害、潜在的白内障风险,被认为是一种安全有效便捷的治疗方法[3]。目前国内外关于HMF诊疗方面的报道较少,儿童HMF报道更少,故本研究对2015年7月至2020年7月我院皮肤科门诊收治的14例HMF患儿的临床资料,总结该病的临床、影像、病理表现、治疗、预后及随访情况。
1 临床资料
1.1 研究对象 收集2015年7月至2020年7月武汉市第一医院皮肤科确诊的14例HMF患儿临床资料,诊断标准参见文献。男性患儿5例,女性患儿9例。诊断年龄4~13岁,平均(8.2±3.8)岁;发病年龄3~12岁,平均(6.2±3.2)岁;病程9个月至7年,平均(3.1±1.8)年。除了一例患儿有I型糖尿病病史,其余患儿均既往体健。所有患儿均无化学性、放射性及有毒性物质接触史,无长期暴晒史,无系统性疾病、肿瘤病史及过敏史。家族中均无类似疾病患者。
1.2 研究方法 回顾性分析2015年7月至2020年7月在武汉市第一医院皮肤科确诊的14例HMF患儿临床资料,包括人口学资料、临床表现、实验室及辅助检查、皮肤影像、皮肤组织病理表现、治疗及随访情况。完全消退:100%清除;部分消退:50%~99%清除;疾病稳定:皮损增加<25%,消退<50%;疾病进展:皮损增加>50%[4]。
2 结果
2.1 临床资料 14例HMF患儿一般情况均可,无发热及体重减轻。心肺部听诊正常,未扪及肝、脾及浅表淋巴结肿大,其余各系统检查未见明显异常。14例患儿中,4例临床分期为T1N0M0/IA期,10例为T2N0M0/IB期。有3例皮损位于躯干,6例分布于躯干和四肢,5例累及面部、颈部、躯干及四肢。所有患儿皮损均表现为色素减退斑,甲盖至患儿手掌大小,呈不规则形或类圆形,边界欠清晰,局部皮损融合,其中4例色素减退斑上见细小鳞屑,5例表皮轻微皱缩,未见浸润性红斑、丘疹及斑块,无明显自觉症状(图1a,1b)。14例HMF患儿有6例首诊诊断HMF,其余8例在确诊前,有4例次曾疑诊副银屑病,3例次疑诊白色糠疹,2例次疑诊特应性皮炎,2例次疑诊白癜风,2例次疑诊炎症后色素减退。部分患儿曾外用地奈德乳膏、0.03%他克莫司软膏、吡美莫司乳膏,皮损无明显好转。

1a,1b:治疗前临床照片:背部及下肢屈侧见大小不等、不规则形或类圆形,边界欠清晰的色素减退斑,局部融合;1c,1d:经NB-UVB照射治疗后大部分皮疹消退;1e,1f:皮肤镜下见色素减退呈波点状模式,血管呈点状、短细线状模式;1g,1h:RCM镜下示表皮各层及真表皮交界处可见高折光细胞,基底层色素环折光减弱
2.2 实验室情况 14例患儿血常规、肝肾功能、红细胞沉降率、C反应蛋白、自身免疫抗体、淋巴细胞亚群及体液免疫功能均未见明显异常。外周血涂片检测均未见异常淋巴细胞。胸部正侧位X射线检查和彩超(肝脏、胆囊、胰腺、脾脏、肾脏、浅表淋巴结)均正常。
2.3 皮肤影像检查 14例患儿皮损处皮肤镜下皮纹明显,可见白色糠样鳞屑及橙黄色片状区域,色素减退模式呈现波点状色素减退8例、斑马样色素减退3例、网格状色素减退3例,血管模式呈点状、精子样、短细线状和星状血管结构。反射式共聚焦显微镜(RCM)下显示,棘层紊乱,可见数个圆形或类圆形高折光细胞,色素减退斑均表现为基底层色素轻度减退,未见明显色素缺失,真表皮交界处及真皮浅层可见较多高折光异形细胞,2例患者见少数低折光的圆形至椭圆形细胞聚集形成的囊泡样结构(图1e~1h)。
2.4 皮肤病理学检查 见图2。皮损组织病理检查示棘层轻度肥厚,棘层下部和基底层可见异形淋巴细胞浸润,核深染,部分扭曲呈脑回状,部分聚集呈Pautrier微脓疡,表真皮交界处及血管周围有带状和苔藓样浸润的淋巴细胞。免疫组化:CD3均阳性,CD20均阴性,4例仅CD8阳性,10例CD8、CD4均阳性。
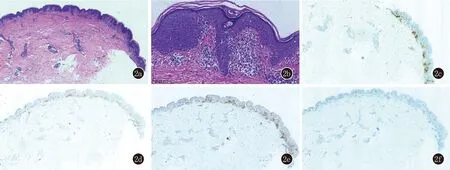
2a,2b:表皮内可见淋巴细胞移入,局部形成Pautrier微脓肿(2a:HE,×40;2b:HE,×200);2c,2d,2e,2f:CD3+,CD4+,CD8+,CD20-(免疫组化,×100)
2.5 治疗和随访 14例HMF患儿除2例,其余12例均给予窄谱中波紫外线(NB-UVB)治疗,初始剂量0.3~0.5 J/cm2,每周2~3次,每次增加原照射剂量的10%~20%,直至照射部位出现淡红斑后予维持治疗,10例患儿照射后出现皮肤干燥,给予润肤处理后改善,2例出现轻度光敏反应,调整剂量后好转,无严重红斑及水疱等不良反应,8例患儿皮疹完全清除,4例部分清除,有3例复发,复发后再次给予NB-UVB治疗,皮损全部消退。见图1c、1d,见表1。另外2例患儿,1例外用糠酸莫米松乳膏治疗,每日1次,3个月后改为隔日1次,随访6个月,治疗后皮损消退面积>80%,未出现不良反应,1例外用0.03%他克莫司软膏治疗,每日2次,3个月后改为每日1次,随访8个月,治疗后皮损消退面积>80%,未出现不良反应。
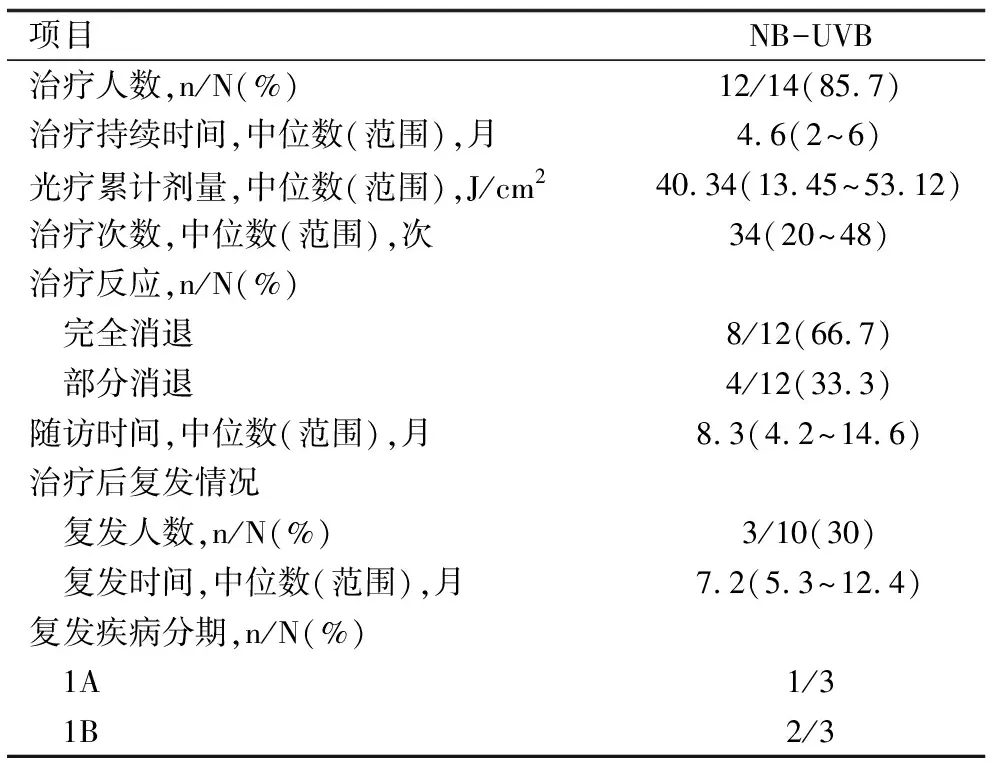
表1 12例儿童HMF光疗反应
3 讨论
HMF是MF中较为罕见的亚型,多累及儿童,病程进展缓慢。Castano等通过统计分析认为儿童MF中色素减退型占72.5%,成年人仅为0.9%[5]。对于HMF的发病机理,Ryan提出了“表皮起源”的假说,认为皮损内异常淋巴细胞在表皮内增殖,先引起表皮内炎症反应,之后再引起基底细胞病变,此假说解释了早期MF患者色素减退或脱失的原因[6]。
HMF的临床表现为大小不一的类圆形或不规则的色素减退斑,边界不清,表面可有少许鳞屑,罕见表皮萎缩,主要分布于躯干及四肢,大多无自觉症状,部分患者可有轻度瘙痒。皮损可持续数年甚至数十年,通常不伴淋巴结和内脏等系统受累。HMF早期临床表现和病理变化都缺乏特异性。王涛等[7]总结T细胞受体(TCR)基因重排并不是诊断HMF的必要指标,HMF的诊断主要依靠典型的临床和组织病理表现,需与特应性皮炎、白色糠疹、花斑癣、慢性痘疮样苔藓样糠疹、白癜风、无色素性色素失禁症、炎症后色素减退等疾病相鉴别。疾病越后期特征愈明显,患者常需要多点多次取病理才能明确诊断。
Rodney等统计HMF从发病到诊断的时间间隔为7个月至24年,平均5.3年[8]。本研究14例患儿病程为9个月至7年,平均3.1年,提示HMF的早期诊断可能是临床医师最大的挑战,对疑诊患者需进一步检查和长期随访。根据T细胞淋巴瘤的TNM分期法,HMF多处于IA和IB期,较少超过IIA期。本研究14例HMF中有4例IA期,10例为IB期,仅有色素减退的皮肤表现,属于HMF早期病变。未发现淋巴结其他系统受累证据,与文献报道结果一致,提示HMF为惰性疾病,需长期随访。
皮肤镜下表现对HMF诊断有一定辅助价值,其特征表现为橙黄色片状区域,波点状、网格状或斑马样色素减退的无结构区域模式,点状、短细线状血管以及由其构成的精子样或星状模式,这些皮肤镜表现在组织病理中与异形淋巴细胞、亲表皮性和苔藓样浸润相对应[9]。本组14例患儿皮损皮肤镜下表现和既往报道一致,治疗后上述特征结构减少。Lallas等[10]报告早期MF皮损皮肤镜下短细线状血管和橙黄色斑片状区域敏感度分别为93.7%和90.6%,特异度分别为97.1%和99.7%。提示皮肤镜对于指导活检必要性和活检部位的选择有一定价值,对于判断疗效及预后也可能有一定辅助指导意义,但仍需多中心和大样本的进一步研究来验证。RCM下HMF皮损表现为表皮各层及真表皮交界处较多高折光细胞,部分病例可见少数低折光的圆形至椭圆形细胞聚集形成的囊泡样结构,基底层色素环折光减弱,色素环外较多高折光细胞分布,本文的报道的病例RCM表现与此结论一致。
HMF皮损符合典型的MF组织病理,Khopkar等通过分析15例HMF的组织病理,发现真表皮淋巴细胞浸润是本病特征性组织病理表现,其次为表皮内可见大的异形淋巴细胞。有40%可见Pautrier微脓疡[11]。本研究中14例患儿HMF均符合MF的组织病理改变,其中有2例可见Pautrier微脓疡。余12例未见Pautrier微脓疡,推测可能与疾病早期有关[12]。
HMF细胞表型符合T细胞表型,但与经典MF以CD4+T细胞浸润为主不同,HMF患者多以CD8+T细胞浸润为主。本研究中有4例CD8阳性,10例CD8、CD4均阳性。HMF发生色素减退可能与CD8+T细胞的细胞毒效应有关,细胞毒作用破坏黑素细胞,以及CD117不稳定和表达降低,最终导致黑素细胞数量减少并出现功能紊乱[13]。HMF预后较经典型好可能也与CD8+T细胞表型相关,经典型MF早期以Th1型免疫反应为主,当疾病进展时Th1反应向Th2反应转变;HMF中CD8+T细胞参与Th1免疫反应,可能阻止了疾病向下一阶段进展[14]。
与经典型MF相比,HMF预后良好。HMF目前尚无推荐指南或标准治疗方案。常用的治疗包括外用氮芥和糖皮质激素,光化学疗法包括补骨脂素长波紫外线(PUVA)、窄谱中波紫外线(NB-UVB)。光化学疗法在HMF的治疗中较为成熟,由于简便而有效,常推荐使用。对于早期HMF患者,PUVA在治疗斑块期MF中占优势[15],但长期PUVA治疗可能增加患皮肤癌风险。而NB-UVB是早期HMF治疗的首选,其优势在于避免了因服用光敏剂导致的不良反应,长期治疗安全性较高。
早期HMF患者采用NB-UVB为主的治疗方法安全且有效。王超等[16]报道HMF患者使用NB-UVB治疗,2次/周,治疗3个月后,色素减退斑基本恢复到正常肤色。Kanokrungsee等报道11例HMF经NB-UVB治疗均有效,完全消退7例,之后3例在随访中复发,中位复发时间10个月,复发后重启NB-UVB治疗再次达临床痊愈[17]。笔者考虑到本研究中12例患儿HMF的皮损均为色素减退斑,无丘疹及斑块,属于早期HMF,故均采用NB-UVB治疗,经不同疗程NB-UVB治疗后,达到8例完全缓解,4例部分缓解,之后有3例出现复发,2例出现轻度光敏反应,调整剂量后好转,无严重红斑及水疱等不良反应。笔者对14例患儿电话随访,随访时间最长约7年。随访发现,3例在痊愈后5.3、7.2、12.4个月复发,重新进行NB-UVB治疗,皮损消退。截止至发稿时间,全部患儿尚未出现病情进展。HMF自然病程可达20~30年,Furlan等报道20例MF患者中,HMF在20年时的疾病相关存活率为98%,疾病进展风险率为9%,预后显著好于经典型MF[18]。尽管如此,即使对患者进行治疗,仍有HMF进展至肿瘤期,甚至死亡的相关报道。Amorim等[19]报道了1例HMF患者采用PUVA治疗,患者大部分皮损治疗后好转,但在随访2年时临床分期由IA期进展至IIB期,之后患者因骨髓浸润引起全血细胞减少,最终并发感染导致死亡。因此,HMF应始终被视为恶性肿瘤性疾病,需长期随访,有必要定期对患者进行全面的临床评估,包括外周血和外周淋巴结检查,以及行影像学检查明确脏器受累情况及TCR基因重排检测。
综上所述,HMF是一种少见的低度恶性的皮肤T细胞淋巴瘤,好发于有色人种,在儿童及青少年中常见。病程呈慢性进展性。由于早期皮损缺乏特异性,易漏诊误诊,皮肤影像有一定辅助诊断价值,对于反复发作、常规治疗无效时要排除本病,尽早行组织病理及免疫组化检查以明确诊断。局部外用糖皮质激素及光疗有效,可以作为一线治疗方案。对于进展期及肿瘤期患者,应行全身系统检查以评估病情。
